一种吲哚化合物及制备方法与应用与流程
1.本发明属于医药领域,具体涉及一种吲哚化合物及制备方法与应用。
背景技术:
2.褪黑素(melatonin,mt)是由脑松果体分泌的激素之一。褪黑素属于吲哚杂环类化合物,其化学名是n-乙酰基-5甲氧基色胺,又称为松果体素、褪黑激素、褪黑色素。褪黑素合成后,储存在松果体内,交感神经兴奋支配松果体细胞释放褪黑素。褪黑素的分泌具有明显的昼夜节律,白天分泌受抑制,晚上分泌活跃。褪黑素可抑制下丘脑-垂体-性腺轴,使促性腺激素释放激素、促性腺激素、黄体生成素以及卵泡雌激素的含量均减低,并可直接作用于性腺,降低雄激素、雌激素及孕激素的含量。另外, mt有强大的神经内分泌免疫调节活性和清除自由基抗氧化能力,可能会成为新的抗病毒治疗的方法和途径。mt最终在肝脏中代谢,肝细胞的损伤可影响体内mt的水平。
3.大量临床和实验研究显示,褪黑素作为内源性神经内分泌激素,对中枢神经系统有直接和间接地生理调节作用,对睡眠障碍、抑郁症和精神疾病具有治疗作用,并对神经细胞有保护作用。例如褪黑素有镇静作用,还可以治疗忧郁症和精神病,可以保护神经,可以镇痛、调节下丘脑释放的激素等等。
4.褪黑素(melatonin)是近几年关于抗衰老研究的热点之一。现已发现人体褪黑素除主要由松果体分泌外,视网膜是体内重要的合成场所,对全身各系统均有作用。本文参考有关文献,总结了褪黑素在视网膜上合成及其过程中色氨酸,色氨酸羟化酶,5
‑ꢀ
羟色胺-n-乙酰转移酶(nat)和羟基吲哚-o-甲基转移酶(hiomt),多巴胺等几种物质的影响。褪黑素在视网膜上的生理药理作用,主要涉及对扩散性抑制,光敏阈和膜传导及环鸟苷酸的影响,以及抗氧化和缺血等方面的作用。
5.我们合成了若干褪黑素衍生物,以期望获得较好的溶解度、稳定性,并且眼部组织具有较好的吸收渗透性,能够在视网膜和角膜组织有较高的药物浓度的分布,发现下述化合物能够满足上述要求,具有相对较好的溶解度和稳定性,在用药后6小时检测角膜的药物浓度,药物浓度显著高于褪黑素,适宜用于制备眼组织药物制剂,治疗角膜相关的疾病。褪黑素在角膜的0.5小时浓度较高,但在8小时浓度均明显低于化合物1、2、3。化合物2、化合物1和化合物3在视网膜的药物浓度显著高于褪黑素组,且在视网膜的药物半衰期也显著长于褪黑素组,更适宜于治疗视网膜相关的眼部疾病。
技术实现要素:
6.本发明的目的是提供一种吲哚化合物及其药学上可接受的盐。
7.本发明所提供的吲哚化合物的结构通式如式i所示:
[0008][0009]
所述式(ⅰ)中,r1选自下述任一基团:甲基、乙基、三氟甲基、ch2=ch-(乙烯基)。
[0010]
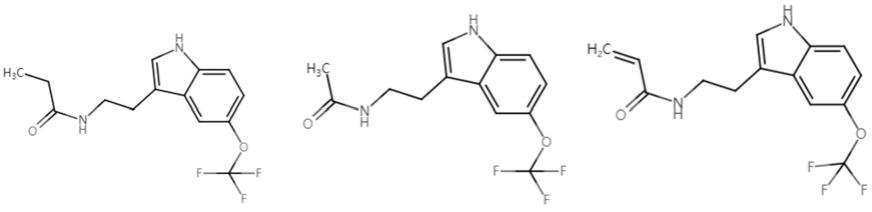
在本发明的一些实施方案中,本发明所述的式i所示化合物可以列举为如下所示结构,但不局限于以下结构:
[0011][0012]
式i所示化合物药学上可接受的盐是指在可靠的医学判断范围内,适合用于与人类和低等动物的组织接触而不出现过度的毒性、刺激、过敏反应等,且与合理的效果/ 风险比相称的盐。式i所示化合物药学上可接受的盐包括但不限于柠檬酸盐、反丁烯二酸盐、水杨酸盐、l-酒石酸盐、富马酸盐、钠盐、钾盐、钙盐、盐酸盐、醋酸盐、硝酸盐、硫酸盐、硫酸氢盐、磷酸盐、磷酸氢盐、乙酸盐、草酸盐、乳酸盐、赖氨酸盐、天冬氨酸盐等。
[0013]
本发明另一个目的是提供上述式i所示化合物的应用。
[0014]
本发明所提供的应用是式i所示化合物或其药学上可接受的盐在制备预防和/或治疗眼部疾病的产品中的应用。
[0015]
所述产品可为药物或药物制剂。
[0016]
本发明中,所述眼部疾病进一步可为视网膜相关疾病或角膜相关疾病。
[0017]
以式i所示的化合物为活性成分制备的预防和/或治疗眼部疾病的药物也属于本发明的保护范围。
[0018]
所述药物可通过注射、喷射、滴鼻、滴眼、渗透、吸收、物理或化学介导的方法导入机体如肌肉、皮内、皮下、静脉、粘膜组织;或是被其他物质混合或包裹后导入机体。
[0019]
需要的时候,在上述药物中还可以加入一种或多种药学上可接受的载体。所述载体包括药学领域常规的溶剂、抗氧剂、助溶剂等。
[0020]
上述药物可以制成片剂、滴眼液、注射液(局部)等多种形式;上述各种剂型的药物均可以按照药学领域的常规方法制备。
[0021]
本发明提供的褪黑素的衍生物(式i所示的化合物),具有较好的溶解度、稳定性,在角膜和视网膜能够有较好的组织分布和较高的药物浓度,在给药时未发现眼部刺激性反应,适宜于制备治疗角膜和视网膜的眼部疾病。
具体实施方式
[0022]
下面结合具体实施例对本发明作进一步阐述,但本发明并不限于以下实施例。所
述方法如无特别说明均为常规方法。所述原材料如无特别说明均能从公开商业途径获得。
[0023]
实施例1、化合物cdp-y123-p1的合成(化合物1)
[0024]
1.1、cdp-y123-2的合成:
[0025][0026]
1l反应瓶中加入起始物料cdp-y123-sm2(36.8g),加入甲苯(368ml),依次加入三乙胺(48ml)和苯酐(50.7l),搅拌均匀,加热回流反应8h。tlc监测至原料消失,将反应液温度降至室温,加入乙酸乙酯(300ml),用饱和氯化铵水溶液洗2次,干燥浓缩。粗品经柱层析纯化得51g化合物cdp-y123-2。
[0027]
1.2、cdp-y123-3的合成:
[0028][0029]
称取cdp-y123-1(5g),溶于乙醇(120ml)和水(20ml)中,依次加入 cdp-y123-2(9.5g)和盐酸(15ml),搅拌均匀,加热回流反应8h。tlc监测至原料消失,将反应液温度降至室温,加入乙酸乙酯(100ml)萃取,有机相在冰水浴降温下用碳酸钠溶液调ph=7,再用饱和食盐水洗涤3次,无水硫酸钠干燥,过滤,滤液旋干得粗品。粗品经柱层析纯化得4.2g化合物cdp-y123-3。
[0030]
1.3、cdp-y123-4的合成:
[0031][0032]
称取cdp-y123-3(4.2g),溶于乙醇(63ml)中,向反应液中加入一水水合肼(1.3g),搅拌均匀,加热回流反应过夜。tlc监测至原料消失,将反应液温度降至室温,抽滤,滤液浓缩得到粗品。粗品经柱层析纯化得2.1g化合物cdp-y123-4。
[0033]
1.4、cdp-y123-p1的合成:
[0034]
[0035]
在三口瓶中加入cdp-y123-4(6.4g),溶于dcm(128ml)中,加入三乙胺(5.3g),搅拌均匀,0℃下滴加乙酰氯(3.2g),加完后室温反应1h。tlc监测至原料消失,向反应液中加入氯化铵饱和溶液搅拌,dcm萃取3次,干燥浓缩得粗品。粗品经柱层析纯化得5g化合物cdp-y123-p1。
[0036]1hnmr cdcl3δ:8.71(s,1h),7.43(s,1h),7.37-7.34(d,j=8.8hz,1h),7.11-7.07 (m,2h),5.88(s,1h),3.61-3.56(q,j=6.4hz,2h),2.97-2.94(t,j=6.4hz,2h),1.95(s, 3h).
[0037]
lc-ms:m/z=287(m+1).
[0038]
实施例2、cdp-y123-p2的合成(化合物2)
[0039][0040]
在三口瓶中加入cdp-y123-4(8.5g),溶于dcm(128ml)中,加入三乙胺(7.0g),搅拌均匀,0℃下滴加丙酰氯(4.0g),加完后室温反应1h。tlc监测至原料消失,向反应液中加入氯化铵饱和溶液搅拌,dcm萃取3次,干燥浓缩得粗品。粗品经柱层析纯化得5g化合物cdp-y123-p2。
[0041]1hnmr cdcl3δ:8.62(s,1h),7.44(s,1h),7.37-7.35(d,j=8.8hz,1h),7.11-7.08
[0042]
(m,2h),5.75(s,1h),3.63-3.58(q,j=6.4hz,2h),2.98-2.95(t,j=6.8hz,2h),2.21-2.16
[0043]
(q,j=7.6hz,2h),1.15-1.11(t,j=7.6hz,3h).
[0044]
lc-ms:m/z=301(m+1).
[0045]
实施例3、cdp-y123-p3的合成(化合物3)
[0046][0047]
在三口瓶中加入cdp-y123-4(2.4g),溶于dcm(48ml)中,加入三乙胺(2.0g),搅拌均匀,0℃下滴加丙烯酰氯(1.1g),加完后室温反应1h。tlc监测至原料消失,向反应液中加入氯化铵饱和溶液搅拌,dcm萃取3次,干燥浓缩得粗品。粗品经柱层析纯化得1.7g化合物cdp-y123-p3。
[0048]1hnmr cdcl3δ:8.52(s,1h),7.44(s,1h),7.37-7.35(d,j=8.8hz,1h),7.12-7.08 (m,2h),6.31-6.26(m,1h),6.09-6.02(m,1h),5.84(s,1h),5.65-5.63(m,1h), 3.71-3.66(q,j=6.8hz,2h),3.02-2.99(t,j=6.8hz,2h).
[0049]
lc-ms:m/z=299(m+1).
[0050]
实施例4、系列化合物眼部药代动力学实验:
[0051]
实验系统
[0052]
动物种系:新西兰兔。
[0053]
动物级别:普通级。
[0054]
动物数量:购买84只。
[0055]
购买时动物年龄:3~5月龄。
[0056]
购买时动物体重:1.5~2.0kg。
[0057]
适应性饲养:新领到的动物适应性饲养5天。其间观察动物饮水、摄食和健康状况,以及是否存在疾病和死亡征兆。
[0058]
标识:耳部标号笔编号。
[0059]
试验设计依据
[0060]
采用标准:国家食品药品监督管理局颁布的药物非临床药代动力学研究技术指导原则。
[0061]
剂量与分组
[0062]
分组:84只雄性新西兰兔,随机分为4组,每组21只。
[0063]
供试品:褪黑素(mtn)、化合物1(m1)、化合物2(m2)、化合物3(m3)。
[0064]
检测化合物:各组分别检测褪黑素、化合物1、化合物2和化合物3
[0065]
给药浓度均为:1mm(即mtn:232.3μg/ml,m1:286.25μg/ml,m2:300.28μg/ml, m3:298.26μg/ml)
[0066]
溶剂:生理盐水+0.05%聚山梨酯80+0.2%聚氧乙烯氢化蓖麻油
[0067]
空白对照(0h点给药动物)给予单纯溶剂点眼100ul/只新西兰兔(50ul/只眼)
[0068]
给药方法采用与临床用药一致的给药方式,即眼部给药,兔左右眼同时给药。
[0069]
供试品的给予:兔左右眼同时给药,给药体积为每只眼睛50μl。采用移液枪精确给药:轻轻将兔眼睑拉低呈杯状,移液枪精确吸取滴眼液50μl滴入眼睑,兔眼被动闭合10秒。
[0070]
观测的指标、时间和内容:样品的采集:选择给药后不同时间点(0h、0.5h、1h、 2h、4h、6h、8h)进行房水、角膜、结膜的采集。
[0071]
房水的采集:处死的动物,用1ml注射器从瞳孔与虹膜交界处进针抽取房水约 200μl(注意抽取房水时注射器针的切面朝下,防止房水喷出)。
[0072]
角膜的采集:用镊子固定眼球,用弯剪剪破角膜与虹膜,沿两者交界处剪下角膜。取下的角膜用生理盐水清洗后,再用滤纸吸干表面液体,精密称量,冷冻保存。
[0073]
视网膜的采集:用剪刀将巩膜剪成6花瓣状,以展开整个巩膜,然后用镊子刮出内层视网膜。取下的视网膜用生理盐水清洗后,再用滤纸吸干表面液体,精密称量,冷冻保存。
[0074]
组织样品的处理:角膜/视网膜匀浆液制备:首先使用小剪子把左右眼角膜/视网膜剪碎成小块,然后加入50%甲醇水溶液(质量体积比1:10),使用研磨器研磨(程序为循环研磨4次,每个循环6500rpm研磨30s等待20s),使用低速离心机4000rpm 离心10min,吸取上清液,冷冻保存待测。
[0075]
检测定量下限:1ng/ml
[0076]
液相色谱:
[0077]
分析柱:gemini nx-c18,3μm,2x 50mm(phenomenex)
[0078]
流动相:甲醇-0.1%甲酸水。
[0079]
进样量:2μl。
[0080]
柱温:40℃。
[0081]
lc方法如下:
[0082][0083]
采用esi离子源。在正离子检测方式下,选择mrm工作方式进行二级质谱分析。质谱检测工作参数如下:
[0084][0085]
给药浓度下,没有对新西兰兔眼睛产生刺激。褪黑素在角膜的0.5小时浓度较高,但在8小时浓度均明显低于化合物1、2、3。化合物1、2、3在视网膜的浓度明显高于褪黑素组。
[0086]
角膜药物浓度检测结果:
[0087]
角膜加入50%甲醇水匀浆稀释5倍后前处理,匀浆液浓度低于定量下限(1ng/ml) 的样品浓度值记为“0.000”[0088]
表1角膜药物浓度检测结果
[0089]
[0090][0091]
视网膜药物浓度检测结果:
[0092]
视网膜2h-3加入50%甲醇水匀浆稀释15倍后前处理,其它加入50%甲醇水匀浆稀释10倍后前处理,匀浆液浓度低于定量下限(1ng/ml)的样品浓度值记为“0.000”[0093]
表2视网膜药物浓度检测结果
[0094][0095]
房水药物浓度检测结果:
[0096]
表3房水药物浓度检测结果
[0097]
[0098][0099]
表4、新西兰兔眼部分别给予m1、m2、m3和mtn后,角膜中药代动力学参数
[0100][0101][0102]
表5、新西兰兔眼部分别给予m1、m2、m3和mtn后,视网膜中药代动力学参数
[0103][0104]
表6、新西兰兔眼部分别给予m1、m2、m3和mtn后,房水中药代动力学参数
[0105]
[0106][0107]
由上述结果可知,化合物1、2、3在视网膜的药物浓度显著高于褪黑素组,且半衰期也显著长于褪黑素组,说明化合物1、2、3更有利于用于治疗眼组织疾病。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1