一种基于合成生物学自组装的新冠病毒疫苗产生系统和方法
1.本发明涉及生物医药技术领域,具体涉及一种基于合成生物学自组装的新冠病毒疫苗产生系统和方法,用于新型的新冠疫苗的开发。
背景技术:
2.covid-19是一种由冠状病毒2(sars-cov-2)引起的严重急性呼吸综合征。sars-cov-2是一种新型冠状病毒,目前,针对新冠病毒的特效药仍然处于空缺状态,安全而有效的新冠疫苗的开发和生产成为控制新冠疫情的首要任务。
3.目前,在研及已经进入临床的新冠疫苗主要包括灭活疫苗、减毒活疫苗、亚单位疫苗、核酸类疫苗以及病毒载体类疫苗等。其中,mrna类疫苗属于核酸类疫苗,是目前最有前景的新冠疫苗,其序列灵活、可编辑,可以迅速响应新冠病毒可能产生的各种突变,但是由于mrna本身化学性质不稳定,容易在体内被降解,mrna疫苗的递送需要载体的保护,同时也对运输及储存的条件提出了更高的要求,此外,mrna疫苗需要体外合成,成本也相对较高。减毒活疫苗所选用的毒株是活的,安全性方面,不容易被大众接受。其他疫苗类型也普遍存在着研发周期长、成本高等问题
4.因此,如果能够开发一种新型的疫苗类型,则可能对于本领域而言是一个重大变革,其将带来很多新的优势和新的希望。
5.外泌体是一类直径50-200nm的双层膜结构囊泡,几乎所有的细胞都可以分泌外泌体,多项研究表明外泌体在细胞间通讯中发挥了重要作用。本技术人和发明人团队在对于外泌体的研究中一直处于领先地位,也有不少研究成果。在近期相关的研究中发现,体内递送可编辑的基因组件,利用生物体组织或脏器自组装的方式可以将特定的多肽/蛋白展示于外泌体的表面并可以通过循环系统运输至全身的主要组织、脏器。基于上述信息,本发明人团队开发了一种全新的疫苗类型,其通过基因组件等相关的碱基序列的体内外泌体自组装的方法,利用外泌体呈递抗原并引发免疫反应从而实现体内免疫,该新型的疫苗类型和制备疫苗的方法有望成为一种具有极佳应用前景的全新疫苗。
技术实现要素:
6.本发明针对现有技术的缺陷提供了一种基于合成生物学自组装的新冠病毒疫苗产生系统和方法,旨在克服现有技术中的不足。
7.本发明的目的是通过以下技术方案来实现:
8.本发明的一个发明点为提供一种基于合成生物学自组装的新冠病毒疫苗产生系统,所述系统包括能够表达新冠病毒抗原的碱基序列组件,该系统为能够在宿主体内组织器官中富集且将抗原表达于囊泡表面并自组装成囊泡复合体的序列,所述囊泡复合体为能够引发免疫应答反应的疫苗。
9.进一步地,所述碱基序列组件为可编辑或可合成的基因组件。
10.进一步地,新冠病毒包括病毒本身以及其突变体,所述新冠病毒抗原包括新冠病
毒已有抗原以及已有抗原序列中的任意一个或几个氨基酸突变以后的序列。
11.进一步地,所述碱基序列组件选自以下序列中的至少一种:
12.q1:pcdna6.2-rbd-his或与该pcdna6.2-rbd-his序列70%以上同源的序列;
13.q2:pcdna6.2-his或与该pcdna6.2-his序列70%以上同源的序列;
14.q3:pcdna6.2-rbd(wt)或与该pcdna6.2-rbd(wt)序列70%以上同源的序列;该同源的序列包括但不限于pcdna6.2-rbd(e484k)、pcdna6.2-rbd(n501y)、 pcdna6.2-s1(d614g)等,这几种是已经发现的,很多没有发现的可囊括在内。
15.上述同源的序列包括在原有序列基础上增加一个或几个碱基、减少一个或几个碱基、替换其中任意一个或几个碱基后得到的序列;几个包括2及2以上的数量。
16.进一步地,所述系统还包括能够使新冠病毒抗原表达于囊泡表面的信号肽碱基序列片段。优选地,所述碱基序列组件位于所述信号肽碱基序列片段的下游,即位于信号肽的3'端。
17.进一步地,所述信号肽碱基序列片段优选包括第一序列,所述第一序列为含有seq1的序列或与该seq1序列70%以上同源的序列;该同源的序列包括在 seq1基础上增加一个或几个碱基、减少一个或几个碱基、替换其中任意一个或几个碱基后得到的序列;几个包括2及2以上的数量。
18.seq1为序列表中的第一个序列。
19.进一步地,所述系统还包括能够使新冠病毒抗原锚定在囊泡表面并自组装形成囊泡复合体的跨膜蛋白碱基序列片段。优选地,所述碱基序列组件位于所述跨膜蛋白碱基序列片段的上游,即位于跨膜蛋白的5’端。
20.进一步地,所述跨膜蛋白碱基序列片段包括第二序列,所述第二序列为含有seq2的序列或与该seq2序列70%以上同源的序列;该同源的序列包括在seq2 基础上增加一个或几个碱基、减少一个或几个碱基、替换其中任意一个或几个碱基后得到的序列;几个包括2及2以上的数量。
21.seq2参见序列表中的第二个序列。
22.进一步地,所述系统还包括启动子,所述启动子优选为cmv启动子;所述启动子设置于所述碱基序列组件的上游,若含有信号肽碱基序列片段,则该启动子位于信号肽碱基序列片段的上游。
23.所述系统还包括终止信号,所述终止信号位于所述跨膜蛋白碱基序列片段的下游,所述终止信号优选为hsv终止信号。
24.进一步地,所述系统中的任意一个或几个碱基均独立地为修饰过的碱基或未经过修饰的碱基;其中,所述修饰包括硫代修饰、氟代修饰、氨代修饰、甲氧基修饰。
25.进一步地,所述组织器官包括宿主的所有细胞、组织和器官,所述囊泡为外泌体,所述囊泡复合体为外泌体复合体。
26.进一步地,所述系统为通过质粒或病毒系统传送。
27.本发明另一个发明点为提供一种基于合成生物学自组装的病毒疫苗产生方法,所述方法包括构建以上任意一段所述的系统,该系统为能够在宿主细胞、组织和/或器官中富集且将抗原表达于囊泡表面并自组装成囊泡复合体的序列,所述囊泡复合体为能够引发免疫应答反应的疫苗。具体地,合成碱基序列组件以及其他序列,按照本技术记载的任意一种
排列方式合成。
28.本发明还有一个发明点为提供一种疫苗,其包括以上任意一段所述的系统。
29.进一步地,所述疫苗的给药方式包括但不限于口服、吸入、皮下注射、肌肉注射、静脉注射。
30.本发明最后一个发明点为提供了一种载体体系,所述体系包含以上任意一段所述的系统以及装载或携带该系统的载体。所述载体包括但不限于质粒和病毒。
31.本发明的主要具有的有益效果为:
32.本发明的疫苗产生系统中,能够根据病毒本身或其不同的突变体的需求,选择相应的碱基序列组件(如基因组件),仅需要合成相应的序列便可,该碱基序列组件的生产成本低廉,周期短,且理化性质稳定,保藏条件温和,保藏方便,保藏成本低,且便于储存、运输等。
33.该疫苗产生系统能够在生物体内的细胞、组织或器官中进行富集,并通过碱基序列组件使得与该序列组件对应疾病的抗原展示于囊泡(如外泌体)的表面,并自组装形成囊泡复合体(如外泌体复合体),且利用囊泡(如外泌体)对抗原进行全身递送,并引起特异性免疫反应。
34.由于本发明的系统可自组装成囊泡复合体,非人为合成,且囊泡复合体能够通过循环系统运输至全身的主要组织、脏器等中,再在碱基序列组件的原始作用下,实现对新冠病毒的免疫,故其抗原组装、分泌过程高效,引发的免疫反应强,且安全性、保护性高等。且避免了现有技术中的一些毒副作用。
35.该系统中的碱基序列组件具有高度可编辑性,其可以针对新冠病毒或其任意突变进行迅速的响应编辑,反应快。因此,其可避免目前由于突变等使得疫苗失效,而新的疫苗又需要重新、长周期的研究的不足。
36.本发明中的系统和方法的整体效果佳,其为一种全新的新冠疫苗类型以及疫苗合成方法,其在生物和医药领域中均是巨大的突破,具有里程碑式的重要意义。
附图说明
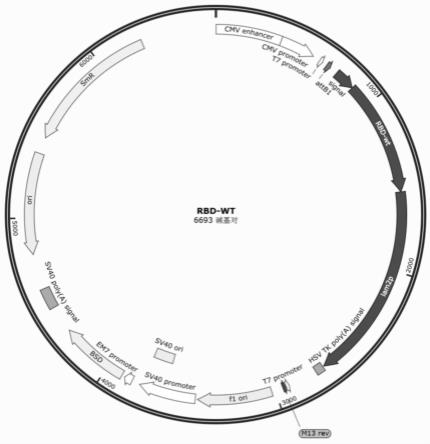
37.图1为本发明实施例所构建的质粒的示意图。
38.图2为本发明实施例中,不同的跨膜蛋白碱基序列所产生的rbd不同表达水平效果图。
39.图3为本发明实施例中,基因组件可以正确表达rbd抗原的elisa检测结果。
40.图4为本发明实施例中,lamp2b骨架可以将rbd抗原呈递到外泌体上的 elisa检测结果。
41.图5为本发明实施例中,体内实验证明该基因组件可以促使rbd呈递外泌体的检测结果。
42.图6为本发明实施例中,体内实验验证基因组件可以引起免疫反应产生抗体。
43.图7为本发明实施例中,第二轮免疫后10天处死小鼠,再以肽库刺激后 rbd特异性t细胞的反应结果汇总。
具体实施方式
44.为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明具体实施例对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
45.本发明中所述上游指5’端,下游指3’端。
46.实施例1
47.一种基于合成生物学自组装的新冠病毒疫苗产生系统,所述系统包括能够表达新冠病毒抗原的基因组件,该基因组件由于是碱基序列,其可编辑或可合成。含有这些基因组件的所述系统能够在宿主体内组织器官中富集且将抗原表达于囊泡表面并自组装成囊泡复合体的序列,所述囊泡复合体能够引发免疫应答反应,则所述系统或所述囊泡复合体可称为疫苗。
48.上述的新冠病毒包括病毒本身以及其突变体。对应地,所述新冠病毒抗原包括新冠病毒目前已有抗原以及已有抗原序列中的任意一个或几个氨基酸突变以后的序列,此处的几个指2个或2个以上。
49.本实施例中能够表达的新冠病毒抗原序列及突变序列列举如下:
50.1、新冠病毒n501y:
51.seq no.5:(编码新冠病毒n501y抗原的核酸序列)
52.agagtccagcccacagaaagcatcgtgcgcttccccaacatcaccaacctatgcccgtttggagaggtctttaatg ccaccaggtttgccagcgtctacgcttggaatcggaagaggatctctaactgtgtggcagactattctgtgctttacaactc tgcctcgttctccactttcaaatgctacggggtgagccctaccaagctgaatgacctgtgcttcaccaatgtgtatgccgac agctttgtgatcaggggagatgaagtgaggcaaatagccccagggcagacagggaagattgctgactacaattacaaa ctgcctgatgacttcactggctgcgtaattgcctggaacagcaacaacttggattctaaggtgggtggcaactataacta cctgtaccggctcttcagaaagagcaatctgaagccctttgaacgggacatctctacagagatctatcaggctggcagca cgccctgcaatggcgtggagggcttcaactgctatttccctctgcagagctacggattccagccaacatacggagtgggc taccagccttacagagtggtggtcctctcctttgagctgctgcacgctccagccaccgtgtgtggccctaagaagtcaact aacctggtgaaaaacaagtgtgtcaacttc;
53.seq no.6:(新冠病毒n501y抗原氨基酸序列)
54.rvqptesivrfpnitnlcpfgevfnatrfasvyawnrkrisncvadysvlynsasfstfkcy gvsptklndlcftnvyadsfvirgdevrqiapgqtgkiadynyklpddftgcviawnsnnldsk vggnynylyrlfrksnlkpferdisteiyqagstpcngvegfncyfplqsygfqptygvgyqpyr vvvlsfellhapatvcgpkkstnlvknkcvnf。
55.2、新冠病毒deta:
56.seq no.7:(编码新冠病毒deta抗原的核酸序列)
57.agagtccagcccacagaaagcatcgtgcgcttccccaacatcaccaacctatgcccgtttggagaggtctttaatg ccaccaggtttgccagcgtctacgcttggaatcggaagaggatctctaactgtgtggcagactattctgtgctttacaactc tgcctcgttctccactttcaaatgctacggggtgagccctaccaagctgaatgacctgtgcttcaccaatgtgtatgccgac agctttgtgatcaggggagatgaagtgaggcaaatagccccagggcagacagg
gaagattgctgactacaattacaaa ctgcctgatgacttcactggctgcgtaattgcctggaacagcaacaacttggattctaaggtgggtggcaactataacta ccgctaccggctcttcagaaagagcaatctgaagccctttgaacgggacatctctacagagatctatcaggctggcagca aaccctgcaatggcgtggagggcttcaactgctatttccctctgcagagctacggattccagccaacaaatggagtgggc taccagccttacagagtggtggtcctctcctttgagctgctgcacgctccagccaccgtgtgtggccctaagaagtcaact aacctggtgaaaaacaagtgtgtcaacttc;
58.seq no.8:(新冠病毒deta抗原氨基酸序列)
59.rvqptesivrfpnitnlcpfgevfnatrfasvyawnrkrisncvadysvlynsasfstfkcy gvsptklndlcftnvyadsfvirgdevrqiapgqtgkiadynyklpddftgcviawnsnnldsk vggnynyryrlfrksnlkpferdisteiyqagskpcngvegfncyfplqsygfqptngvgyqpy rvvvlsfellhapatvcgpkkstnlvknkcvnf。
60.3、新冠病毒omicron:
61.seq no.9:(编码新冠病毒omicron抗原的核酸序列)
62.agagtccaaccaacagaatctattgttagatttcctaatattacaaacttgtgcccttttgatgaagtttttaacgcc accaaatttgcatctgtttatgcttggaacaggaagagaatcagcaactgtgttgctgattattctgtcctatataattttgc accatttttcacttttaagtgttatggagtgtctcctactaaattaaatgatctctgctttactaatgtctatgcagattcattt gtaattagaggtgatgaagtcagacaaatcgctccagggcaaactggaaatattgctgattataattataaattaccaga tgattttacaggctgcgttatagcttggaattctaacaagcttgattctaaggttagtggtaattataattacctgtatagatt gtttaggaagtctaatctcaaaccttttgagagagatatttcaactgaaatctatcaggccggtaacaaaccttgtaatgg tgttgcaggttttaattgttactttcctttacgatcatatggtttccgacccacttatggtgttggtcaccaaccatacagagt agtagtactttcttttgaacttctacatgcaccagcaactgtttgtggacctaaaaagtctactaatttggttaaaaacaaa tgtgtcaatttc;
63.seq no.10:(新冠病毒omicron抗原氨基酸序列)
64.rvqptesivrfpnitnlcpfdevfnatkfasvyawnrkrisncvadysvlynfapfftfkcy gvsptklndlcftnvyadsfvirgdevrqiapgqtgniadynyklpddftgcviawnsnkldsk vsgnynylyrlfrksnlkpferdisteiyqagnkpcngvagfncyfplrsygfrptygvghqpyr vvvlsfellhapatvcgpkkstnlvknkcvnf。
65.作为进一步优选的实施方式,所述基因组件选自以下序列中的至少一种: q1:pcdna6.2-rbd-his或与该pcdna6.2-rbd-his序列70%以上同源的序列;
66.q2:pcdna6.2-his或与该pcdna6.2-his序列70%以上同源的序列;
67.q3:pcdna6.2-rbd(wt)或与该pcdna6.2-rbd(wt)序列70%以上同源的序列;该同源的序列包括但不限于pcdna6.2-rbd(e484k)、pcdna6.2-rbd(n501y)、 pcdna6.2-s1(d614g)等,这几种是已经发现的,其他没有发现的或未来可能出现的等等均在该范围内。
68.例如,所述基因组件可选自q1、q2或q3中的一种或几种,若不止一种时,可同时选自q1和q2中、q2和q3中、q1和q3中或者q1、q2和q3中等等。
69.上述同源的序列包括在原有序列基础上增加一个或几个碱基、减少一个或几个碱基、替换其中任意一个或几个碱基后得到的序列;几个包括2及2以上的数量。因此,目前新冠病毒以及其突变体疫苗的制备均在本技术的保护范围内。
70.作为进一步优选的实施方式,所述疫苗产生系统还包括能够使新冠病毒抗原表达于囊泡表面的信号肽碱基序列片段。优选地,所述上述基因组件位于所述信号肽碱基序列片段的下游,即位于信号肽的3'端。
71.本实施例中的信号肽碱基序列列举如下:
72.seq no.11:(tpa表达序列)
73.atggatgcaatgaagagagggctctgctgtgtgctgctgctgtgtggagcagtcttcgtttcgcccagccaggaaa tccatgcccgattcagaagaggagccaga;
74.seq no.12:(sp信号肽)
75.gatgcaatgaagagagggctctgctgtgtgctgctgctgtgtggagcagtcttcgtttcgcccagccaggaaatcc atgcccgattcagaaga。
76.作为进一步优选的实施方式,所述信号肽碱基序列片段优选包括第一序列,所述第一序列为含有seq1的序列或与该seq1序列70%以上同源的序列,如70%、75%、80%、85%、90%、95%等等;该同源的序列包括在seq1基础上增加一个或几个碱基、减少一个或几个碱基、替换其中任意一个或几个碱基后得到的序列;几个包括2及2以上的数量。虽然可选用其他类型的信号肽,但通过试验发现,采用seq1或其同源序列与本技术其他的基因片段配合,其效率更高、抗原浓度和抗体滴度均较好,抗体能够与现有技术中成熟的疫苗相当,因此,优选该序列。
77.seq1为atgtgcctctctccggttaaaggcgcaaagctcatcctgatc tttctgttcctaggagccgttcagtccaatgcattgatagttaatttgacagattcaaaggg tacttgcctttatgctcga。
78.作为进一步优选的实施方式,所述疫苗产生系统还包括能够使新冠病毒抗原锚定在囊泡表面并自组装形成囊泡复合体的跨膜蛋白碱基序列片段。优选地,所述基因组件位于所述跨膜蛋白碱基序列片段的上游,即位于跨膜蛋白的5’端。
79.作为进一步优选的实施方式,所述跨膜蛋白碱基序列片段包括第二序列,所述第二序列为含有seq2的序列或与该seq2序列70%以上同源的序列,如70%、75%、80%、85%、90%、95%、98%、99%等等;该同源的序列包括在seq2基础上增加一个或几个碱基、减少一个或几个碱基、替换其中任意一个或几个碱基后得到的序列;几个包括2及2以上的数量。虽然可选用其他类型的跨膜蛋白,但通过试验发现,采用seq2或其同源序列与本技术其他的基因片段配合,其效率更高、抗原浓度和抗体滴度均较好,抗体能够与现有技术中成熟的疫苗相当,因此,优选该序列。
80.跨膜蛋白即lamp2b跨膜蛋白,基因组件可以正确表达rbd抗原且lamp2b 骨架可以将rbd抗原呈递到外泌体上的检测结果如图3-4所示。
81.seq2参见序列表中第二个序列,即 tccggaggtgcagaatgggagatgaatttcacaataacatatgaaactacaaaccaaaccaataaaactataa ccattgcagtacctgacaaggcgacacacgatggaagcagttgtggggatgaccggaatagtgccaaaata atgatacaatttggattcgctgtctcttgggctgtgaattttaccaaggaagcatctcattattcaattcatgac atcgtgctttcctacaacactagtgatagcacagtatttcctggtgctgtagctaaaggagttcatactgttaa aaatcctgagaatttcaaagttccattggatgtcatctttaagtgcaatagtgttttaacttacaacctgactcc tgtcgttcagaaatattggggtattcacctgcaagcttttgtccaaaatggtacagtgagtaaaaatgaacaa gtgtgtgaagaagaccaaactcccaccactgtggcacccatcattcacaccactgccccgtcgactacaacta cactcactccaacttcaacacccactccaactccaactccaactccaac
cgttggaaactacagcattagaaa tggcaatactacctgtctgctggctaccatggggctgcagctgaacatcactgaggagaaggtgcctttcatt tttaacatcaaccctgccacaaccaacttcaccggcagctgtcaacctcaaagtgctcaacttaggctgaaca acagccaaattaagtatcttgactttatctttgctgtgaaaaatgaaaaacggttctatctgaaggaagtgaat gtctacatgtatttggctaatggctcagctttcaacatttccaacaagaaccttagcttctgggatgcccctct gggaagttcttatatgtgcaacaaagagcaggtgctttctgtgtctagagcgtttcagatcaacacctttaac ctaaaggtgcaaccttttaatgtgacaaaaggacagtattctacagcccaggagtgttcgctggatgatgac accattctaataccaattatagttggtgctggtctttcaggcttgattatcgttatagtgattgcttacctaattg gcagaagaaagacctatgctggatatcagactctgtaa。
82.本实施例中的能够使抗原锚定在囊泡表面并自组装形成囊泡复合体的跨膜蛋白碱基序列还可以是cd9,cd81两种骨架,此两种骨架不需要信号肽,直接可以将抗原呈递到外泌体上,具体序列如下所示:
83.seq no.13:(cd81骨架序列)
84.atgggggtggagggctgcaccaaatgcatcaaatacctgctcttcgtcttcaatttcgtcttctggctggctggaggcgtg atcctaggtgtagctctgtggttgcgtcatgatccacagaccaccagcctgctgtacctggaactg— agatctctagccacc(中间为抗原序列位置)accggtggagctcgaatcagatct— ggaaacaaaccggcacccaacaccttctacgtgggcatctacattctcattgctgtgggagctgtgatgatgtttgtaggc ttcctggggtgctatggggccatccaggagtcccagtgtctgctggggacgttcttcacctgccttgtgatcctgtttgcctg tgaggtggctgcaggcatctggggcttcgtaaacaaagaccagatcgccaaggatgtgaagcagttctatgaccaggcc cttcagcaagctgtgatggatgatgatgccaacaatgccaaggctgtggtgaagactttccatgagacgctcaactgttgt ggctccaacgcactgaccacactgactaccaccatactgaggaacagcctgtgtccctcaggcggcaacatactcaccc ccttactgcagcaagattgtcatcagaaaatcgatgagctcttctctgggaagctgtacctcattggaattgcagccattgt ggtagctgtcattatgatctttgagatgattctgagcatggtgctgtgctgtggcatccggaacagctccgtgtactga;
85.seq no.14:(cd9骨架序列)
86.atgccggtcaaaggaggtagcaagtgcatcaaatacctgctcttcggatttaacttcatcttctggctcgctggcat tgcagtgcttgctattggactatggctccgattcgactctcagaccaagagcatcttcgagcaagagaataac— agatctctagccacc(中间为抗原序列位置)accggtggagctcgaatcagatct— cattccagtttctacacaggagtgtacattctgattggagccggggccctcatgatgctggttggtttcctgggctgctgtg gagctgtacaagagtcccagtgcatgctgggattgttcttcgggttcctcttggtgatattcgccattgagatagccgccgc cgtctggggctatacccacaaggatgaggtgattaaagaactccaggagttttacaaggacacctaccaaaagttacgg agcaaggatgaaccccagcgggaaacactcaaagccatccatatggcgttggactgctgtggcatagctggtcctttgg agcagtttatctcggacacctgccccaagaaacagcttttggaaagtttccaggttaagccctgccctgaagccatcagtg aggtcttcaacaacaagttccacatcattggagcagtgggtatcggcatcgccgtggtgatgatcttcggcatgatcttca gcatgatcctgtgctgcgccatccgcaggagccgagaaatggtctag;
87.上述不同的跨膜蛋白骨架在外泌体中的表达结果如图2所示。
88.作为进一步优选的实施方式,所述系统还包括启动子,该启动子优选为cmv 启动子;所述启动子设置于所述碱基序列组件的上游,若含有信号肽碱基序列片段,则该启动子位于信号肽碱基序列片段的上游。
89.启动子的序列包括第三序列,该第三序列为含有seq3的序列或与该seq3 序列70%以上同源的序列,如70%、75%、80%、85%、90%、95%等等;该同源的序列包括在seq3基础上增加一个或几个碱基、减少一个或几个碱基、替换其中任意一个或几个碱基后得到的序列;几个包括2及2以上的数量。虽然可选用其他类型的启动子,但通过试验发现,采用seq3或其同源序列与本技术其他的基因片段配合,其效率更高、抗原浓度和抗体滴度均较好,抗体能够与现有技术中成熟的疫苗相当,因此,优选该序列。
90.seq3: gacattgattattgactagttattaatagtaatcaattacggggtcattagttcatagccca tatatggagttccgcgttacataacttacggtaaatggcccgcctggctgaccgcccaacg acccccgcccattgacgtcaataatgacgtatgttcccatagtaacgccaatagggactttc cattgacgtcaatgggtggagtatttacggtaaactgcccacttggcagtacatcaagtgt atcatatgccaagtacgccccctattgacgtcaatgacggtaaatggcccgcctggcatta tgcccagtacatgaccttatgggactttcctacttggcagtacatctacgtattagtcatcg ctattaccatggtgatgcggttttggcagtacatcaatgggcgtggatagcggtttgactc acggggatttccaagtctccaccccattgacgtcaatgggagtttgttttggcaccaaaat caacgggactttccaaaatgtcgtaacaactccgccccattgacgcaaatgggcggtagg cgtgtacggtgggaggtctatataagcagagct。参见序列表中第三个序列。
91.作为进一步优选的实施方式,所述系统还包括终止信号,所述终止信号位于所述跨膜蛋白碱基序列片段的下游,所述终止信号优选为hsv终止信号。
92.所述终止信号的序列包括第四序列,该第四序列为含有seq4的序列或与该 seq4序列70%以上同源的序列;如70%、75%、80%、85%、90%、95%等等,该同源的序列包括在seq4基础上增加一个或几个碱基、减少一个或几个碱基、替换其中任意一个或几个碱基后得到的序列;几个包括2及2以上的数量。虽然可选用其他类型的终止信号,但通过试验发现,采用seq4或其同源序列与本技术其他的基因片段配合,其效率更高、抗原浓度和抗体滴度均较好,抗体能够与现有技术中成熟的疫苗相当,因此,优选该序列。
93.seq4:cggcaataaaaagacagaataaaacgcacgggtgttgggtcgtttgttc。参见序列表中第四个序列。
94.作为进一步优选的实施方式,所述系统中的任意一个或几个碱基均独立地为修饰过的碱基或未经过修饰的碱基;其中,所述修饰包括硫代修饰、氟代修饰、氨代修饰、甲氧基修饰。通过合适的修饰可增加碱基序列的稳定性。
95.在本实施例中,所述组织器官包括宿主的所有细胞、组织和器官,包括不限于血液、肌肉、肝脏、脾、肺、胃、肠、胆、胰腺、脑、心、肾等等,所述囊泡为外泌体,所述囊泡复合体为外泌体复合体。
96.上述系统或上述疫苗的给药方式包括但不限于口服、吸入、皮下注射、肌肉注射、静脉注射等。
97.实施例2
98.在实施例1的基础上,一种基于合成生物学自组装的病毒疫苗产生方法,所述方法包括构建以上任意一段所述的系统,该系统为能够在宿主细胞、组织和/或器官中富集且将抗原表达于囊泡表面并自组装成囊泡复合体的序列,所述囊泡复合体为能够引发免疫应答反应的疫苗。具体地,合成碱基序列组件以及其他序列,按照本技术记载的任意一种排列方式合成。
99.本实施例中的方法简单、快速,能够短期内合成大量不同的序列,因此,本发明的疫苗产生系统能够快速、高效的生产。
100.实施例3
101.在实施例1或2的基础上,一种载体体系,该体系包含实施例1或实施例 2中所述的疫苗产生系统以及装载或携带该系统的载体。该载体可以为质粒或病毒,当然,也可以是其他类型的载体。
102.实施例4:体外实验
103.本发明通过体外分别合成pcdna6.2-rbd-his;pcdna6.2-his基因组件,该基因组件的上游为信号肽,下游为lamp2b,并在信号肽上游连接启动子,lamp2b 下游连接终止信号,构成本技术中的系统,并分别构建含有前述两个系统的质粒;转染细胞,注射小鼠,验证基因组件可以正确的组装含有抗原的外泌体。
104.①
实验过程/方法:转染293t、huh-7细胞株,试剂盒提取培液外泌体进行 western blot,分别使用sars-cov/sars-cov-2spike antibody,rabbit pab, antigen affinity purified(40150-t62-cov2),his-tag monoclonal antibody作为一抗。
105.结果发现含有外泌体his的表达以及rbd的表达,说明本发明中的系统能够表达对应上述基因片段的抗原,且表达于外泌体上。
106.②
实验过程/方法:mock,his(阴性对照),his-rbd(阳性对照)、rbd (阴性对照)转染293t、huh-7细胞株,分别收集培液、培液提取的外泌体,进行elisa实验检测rbd的表达。
107.结果发现转染质粒可以让细胞分泌表面含有rbd的外泌体。
108.③
实验过程/方法:通过免疫沉淀实验,使用his-tag单克隆抗体及 40150-t62-cov2进行pull down实验。
109.结果发现蛋白正确表达在外泌体表面。
110.实施例5:体内实验
111.分别将含有pcdna6.2-rbd(wt)、pcdna6.2-rbd(e484k)、 pcdna6.2-rbd(n501y)、pcdna6.2-s1(d614g)基因组件的系统进行体内肌肉注射及尾静脉注射后检测抗原及抗体的表达从而验证其可以发挥疫苗的作用。
112.实验过程:体外分别合成pcdna6.2-rbd(wt)、pcdna6.2-rbd(e484k)、 pcdna6.2-rbd(n501y)、pcdna6.2-s1(d614g)基因组件,对于每种基因组件,其上游为信号肽,下游为lamp2b,并在信号肽上游连接启动子,lamp2b下游连接终止信号,构成本技术中的系统。并分别构建含有前述四个系统的质粒。
113.利用天根去内毒素质粒大提试剂盒大量提取上述基因组件: pcdna6.2-rbd(wt)、pcdna6.2-rbd(e484k)、pcdna6.2-rbd(n501y)、pcdna6.2-s1 (d614g),以5mg/kg注射,分别采用尾静脉和肌肉注射,以及肌肉+lipo注射的方式,体积50-100μl,在注射后6、9、12、24小时对小鼠进行眼眶采血,并使用elisa方法检测抗原的表达,7天,14天,28天眼眶采血,利用elisa检测抗原和抗体表达。
114.具体的抗原检测如下所示:
115.1.ace2(ace-hm401)以5μg/ml浓度包板,100μl/孔,4摄氏度过夜孵育;
116.2.pbst(0.05%tween20的pbs)洗3次,每孔300μl,加5%bsa/pbs,4 摄氏度封闭12h;
117.3.弃液,pbst洗2次;
118.4.每孔加入100μl梯度稀释的血清以及rbd标准品(sars-cov-2rbd-hisrecombinantprotein40592-v08b)室温孵育1h,
119.4.pbs洗三次,sars-cov-2(2019-ncov)spikes1antibody(sinobiological)用pbst以1:5000室温1h;
120.5.pbst洗三次,goatanti-rabbitigg-fcsecondaryantibody(hrp)以0.2μg/ml的比例稀释后,每孔100μl,室温1h后加入100μltmb显色液,37度避光孵育10-30min;
121.6.加入等体积1m硫酸,检测od450/650.(od=od450-650)
122.结果发现:如图5所示,注射后可以在血清外泌体中检测到上述基因对应的抗原的表达。
123.具体的抗体检测如下所示:
124.血清样本使用前在56度下灭活30min。
125.1.rbd(目前得到的1.5mg/mlinpbs)用包被液(0.75g碳酸钠,1.46g碳酸氢钠,500mlddw,ph9.6)稀释至5μg/ml,每孔100μl(相当于500ngrbd/孔),4度静置过夜;
126.2.pbst(0.05%tweeninpbs)每孔300μl,静置30s,弃液加新pbst,重复洗3次;在吸水纸上拍干;
127.3.5%(2%)bsa(pbs),4度静置封闭12h(室温2h);
128.4.弃液,pbst洗2次;
129.5.用pbs稀释血清100倍之后按照2倍梯度稀释,共7个梯度(覆盖10000滴度),每孔加100μl,稀释步骤(不算复孔,用单独的板先稀释好再加入elisa板中)。起始孔原始血清2μl+pbs198μl(3μl+247μl),吹打混匀,下一孔吸90μl+pbs90μl(120+120),吹打混匀,后每个梯度都用同样的方式稀释,稀释完成后吸50μl(100μl)至elisa板中。37度30min培养箱静置孵育(37度,60min)
130.6.pbst洗3次,goatanti-mouseigg以1:5000在pbs中稀释,每孔加100μl,37度静置孵育30min;
131.7.pbst洗5次,加入100μltmb反应液37度静置孵育10-30min,加入100μl(50μl),2m硫酸终止反应后测450nm波长,以od》阴性血清2(1.4)倍作为终止点计算滴度。
132.结果发现:如图6所示,注射后可以在血清中检测到由上述抗原引发产生的抗体。
133.同时,发明人还验证了多肽文库刺激对rbd特异性t细胞反应的影响,具体是采用上述相同的实验小鼠,二轮免疫后10天处死,眼眶采血,以多肽文库刺激后,呈现出了rbd特异性t细胞(cd4
+
、cd8
+
)的反应结果,如图7所示。
134.通过以上结果可知,基因组件注射导致小鼠获得高滴度的特异性抗体和中和抗体,抗体滴度与商品化疫苗相当。
135.实施例4和5所用的插入了本发明系统的质粒结构如图1所示。当然,本技术的系统插入至其他类型的质粒或病毒等中均可以,均能达到较佳效果。
136.在本发明中,本发明人还选取了信号肽某些位点突变后的序列、跨膜蛋白(如lamp2b)的某些位点突变后的序列分别进行了试验,结果发现,突变后的序列也能够与抗原基因作用实现体内抗体的产生。
137.对于本技术中的pcdna6.2-rbd-his、pcdna6.2-his、pcdna6.2-rbd(wt)等均为现
有技术,由于序列太长,本技术不再列举。对于pcdna6.2-rbd(e484k)、 pcdna6.2-rbd(n501y)、pcdna6.2-s1(d614g)均是在pcdna6.2-rbd(wt)基础上在括号中所示的具体位点突变后的序列。
138.本发明对于相关联的结构均给出明确的序列。但是本领域人员应当理解,在上述序列基础上进行微小的变动是不影响本发明所述序列的保护,均在本发明的保护范围内。即本技术中所有的序列均包括在其基础上增加、缺少或替换一个或多个碱基或氨基酸,此处的多个指2个或多于2个。
139.最后应说明的是:以上所述的各实施例仅用于说明本发明的技术方案,而非对其限制;尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述实施例所记载的技术方案进行修改,或者对其中部分或全部技术特征进行等同替换;而这些修改或替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1