检测猫口炎病原体并分型的组合物、试剂盒、方法及其用途与流程
1.本发明属于分子生物学检测领域;具体地,涉及猫口炎病原体的检测;更具体地,涉及猫杯状病毒、猫疱疹病毒、猫白血病毒、猫艾滋病毒共4种猫口炎病原体的检测。
背景技术:
2.随着社会经济发展及人们生活品质的提升,我国宠物行业得到了飞速发展,宠物健康也日益受到宠物主人和宠物医师的重视。猫口炎(feline stomatitis)疾病是临床中非常常见的疾病之一,临床中流浪猫和家猫均有发病,其中又以流浪猫居多。猫口腔发炎溃疡性疾病(猫口炎)是发生在猫口腔黏膜表层或深层组织的炎症,可以由口腔的原发性疾病或全身性疾病继发形成,炎症的表现可能是局部性的也可能是弥漫性的。该病诱因较为复杂,例如由各种尖锐的异物,如骨片、刺、铁丝、钢针、木刺等的刺激,不整齐的牙齿受损伤,以及吞食具有腐蚀性的化学毒素或缺乏维生素a、b2等,都可能会导致口炎的发生。另外,像某些传染病,比如猫气管炎病毒、猫萼状病毒,是造成猫溃疡性舌炎的病原。j.o.knowles等在1989年提出,猫患口炎表现的临床症状比其他任何动物都严重,治疗也尚缺乏有效手段。
3.猫杯状病毒(fcv),为杯状病毒科,水疮性病毒属,是一种单链rna病毒。fcv是猫病毒性呼吸道传染病主要表现为口腔溃疡、眼鼻分泌物增多、流涎、结膜炎、羞明、口腔炎、气管炎、支气管炎,伴有双相热。是猫的多发病,发病率高,强毒株感染可发生肺炎、呼吸困难、甚至死亡。主要传染源为病猫和带毒猫,病猫在急性期可随分泌物和排泄物排出大量病毒,直接传染易感猫。带毒猫经治疗,可成为无症状的病原携带者,但临床康复后仍长期排毒,是危险的传染源。近年来在中国、美国、英国和意大利等国家相继暴发了由fcv感染引起猫的恶性系统性疾病(fcv-associateedvirulentsystemicdisease),该毒株被称为fcv-vsd株,可感染成年猫并导致高热、水肿、头部和四肢溃疡及黄疸等症状,并且呈现较高的死亡率。fcv不仅可以感染猫,也可感染虎、狮等野生猫科动物,是流行于猫科动物中的一种重要的病原。
4.猫疱疹病毒i型(feline herpesvirus type1,fhv-i)又叫猫鼻气管炎病毒,属疱疹病毒科,甲型疱疹病毒亚科,是一种有囊膜的双链dna病毒。fhv-i可引起猫的急性和高度接触性的上呼吸道感染,发病率可高达100%。虽然成年猫感染后大多能够痊愈,主要侵害幼猫的上呼吸道和眼部,感染症状严重时,出现体温升高,精神沉郁、咳嗽、打喷嚏等明显的上呼吸道感染症状以及眼脓性分泌物、角膜结膜炎等眼部症状,严重感染可造成小叶性肺炎,眼周皮肤溃疡。幼猫病死率可达50%,而且终生带毒排毒,并可垂直传播,危害很大。病毒在病猫的鼻、咽喉、气管和支气管以及舌、结膜等部位增殖。此外,患病猫康复后fhv-i仍可潜伏于三叉神经、视神经、扁桃体等部位造成终身带毒,在猫免疫力低下或发生应激反应时引起二次感染,引起慢性鼻窦炎、鼻甲骨变性、树枝状角膜炎等临床症状。该病最早从美国发现,随后在加拿大、英国、荷兰、瑞士、匈牙利、越南等地发现和流行,我国已多次发现可疑病例,并分离到病毒。但目前在实验动物国家标准及地方标准中,均没有对实验用猫的检测要求及相关规定。
5.猫白血病病毒(feline leukemia virus,felv)属肿瘤病毒亚科,c型肿瘤病毒属,哺乳动物c型肿瘤病毒亚属的一种反转录病毒,是一种有囊膜的单链rna病毒。felv有felv-a、felv-b、felv-c和felv-t四个亚型。a型几乎存在于所有felv感染猫中,可以导致严重的免疫抑制。b型存在于大约50%felv感染猫中,可以引起肿瘤。c型仅存在于约1%felv感染猫中,可导致严重的贫血。猫白血病的常发病症有恶性淋巴肿瘤、骨髓性白血病以及变性性胸腺萎缩和非再生性贫血等,其中对猫最严重的是恶性淋巴肿瘤。猫白血病病毒(felv)的特征在于会引发猫的终生感染,早期并不会出现明显的症状,随之会出现持续性的病毒血症,后期治疗十分困难,最终会产生致命的结果。在发病早期准确确诊猫白血病并及时给予治疗,是治愈猫白血病的最佳选择。持续性感染的病猫成为了猫白血病病毒的直接传染源,其唾液、粪便、尿、乳汁、鼻腔分泌物均含有病毒,通过呼吸道、消化道传染到健康猫。将确诊的病猫隔离是控制猫白血病病毒的有效途径。若感染机体后不发生免疫反应,病毒可能会导致持续的病毒血症(40%)成为病毒的携带者。病毒血症通常在felv感染2~4周后出现,大约50%患持续病毒血症的猫感染felv后在1年内死亡。
6.猫免疫缺陷病毒(feline immunodeficiency virus,fiv)是逆转录病毒科,慢病毒属,猫慢病毒群中的一名成员,成熟的fiv粒子呈圆形或椭圆形,大小为105nm~125nm,其主要构成成分是囊膜、衣壳及核芯,并含有逆转录酶,在体外具有嗜t淋巴细胞活性及镁离子依赖的反转录酶活性。由于在病原学、临床症状、致病机理等方面与人艾滋病极其相似,故又称为猫艾滋病。fiv主要存在于血液、唾液和脑脊髓液等组织液中,常常经由撕咬或异性间的舔舐传染,fiv自然情况下感染20多种猫科动物,在世界范围内广泛存在。在家猫中主要发生于流浪猫,因而流浪猫被定义为高度危险群体,感染率随年龄增长而增高,且与流浪猫的密度成正比,一般家猫发病率在3%(北美)~40%(日本),某些地区非家猫的感染率达100%。同时fiv潜伏期长,从感染到出现临床症状约需3~10年。既然目前尚无有效保护野生猫科动物的fiv疫苗,那么实践中只能以早期诊断、切断传播途径为主要预防措施。
7.猫的这几种主要疾病临床症状相似,都会表现口炎症状,并常有混合感染,给诊断造成困难。因此,本领域需求一种能够同时检测这几种病原体的组合物,以便能够给予针对性的治疗,同时成本低,灵敏度高。
技术实现要素:
8.有鉴于此,第一方面,本发明提供一种用于检测猫口炎病原体并分型的组合物,所述组合物包括:
9.如seq id no:1所示的fhv-i上游引物、如seq id no:2所示的fhv-i下游引物,和如seq id no:3所示的fhv-i探针;
10.如seq id no:4所示的fcv上游引物、如seq id no:5所示的fcv下游引物,和如seq id no:6所示的fcv探针;
11.如seq id no:7所示的felv上游引物、如seq id no:8所示的felv下游引物,和如seq id no:9所示的felv探针;
12.如seq id no:10所示的fiv上游引物、如seq id no:11所示的fiv下游引物,和如seq id no:12所示的fiv探针。
13.进一步地,组合物内的探针的荧光基团彼此互不相同且互不干扰。
14.在本文中,“互不相同且互不干扰”是指组合物中每个探针所用的荧光基团是不一样的,并且不会影响彼此的检测,即可以利用不同的通道进行检测。例如可以使用fam、hex、rox和cy5,这些基团吸光值不接近,能选择不同的通道,因而不会互相干扰。
15.在一些具体的实施方案中,本发明组合物用于荧光pcr。
16.在本发明中,荧光报告基团可以选自fam、hex、rox、vic、cy5、5-tamra、tet、cy3和joe,但不限于此。
17.进一步地,探针的3’末端还具有淬灭基团,例如bhq1、bhq2,或mgb。
18.在一个具体的实施方案中,探针的3’末端为bhq1。
19.在一个具体的实施方案中,探针的3’末端为mgb。
20.进一步地,所述组合物中引物的用量为0.02μm~0.25μm;所述组合物中探针的用量为0.02μm~0.25μm。
21.进一步地,所述组合物还包括如seq id no:13所示的内标上游引物和如seq id no:14所示的内标下游引物。
22.本发明提供的检测猫口炎病原体并分型的组合物,主要利用多重荧光pcr和熔解曲线分析方法,对猫杯状病毒、猫疱疹病毒、猫白血病毒、猫艾滋病毒等多种病原体以及内标,在一管内进行检测,使得不同病原体能够得到区别对待,从而使得治疗和预防更有效。本发明的组合物,结合荧光探针熔解曲线法,其成本低,通量高。并且操作简便,结果读取过程通过ct值和熔解峰tm值即可以判定。
23.进一步地,在一些实施方案中,本发明的组合物可以包括上述引物和探针中的一对或多对。在本发明中,“对”是指检测一个靶点的互相匹配的上游、下游引物和探针,或者互相匹配的上游、下游引物。
24.在一个具体的实施方案中,本发明的组合物的各成分分别存在于单独包装中。
25.进一步地,本发明的组合物的各成分以混合的形式存在。
26.第二方面,本发明提供了上述本发明的组合物在制备检测猫口炎病原体并分型的试剂盒中的用途。
27.第三方面,本发明提供了一种检测猫口炎病原体并分型的试剂盒,所述试剂盒包括如上所述本发明的组合物。
28.进一步地,所述试剂盒还包括阴性质控品和阳性质控品。
29.进一步地,所述试剂盒还包括dntp、pcr缓冲液以及mg
2+
中的至少一种。
30.更进一步地,所述试剂盒还包括:核酸释放剂、核酸提取试剂、尿嘧啶糖基化酶以及dna聚合酶中的至少一种。
31.更进一步地,所述试剂盒还包括核酸释放试剂、核酸提取试剂、dntp、尿嘧啶糖基化酶、dna聚合酶、pcr缓冲液以及mg
2+
中的至少一种。
32.进一步地,所述dna聚合酶的浓度为3u/反应~15u/反应,例如dna聚合酶可以是taq酶。
33.在一个具体的实施方案中,本发明试剂盒包括:taq酶、尿嘧啶糖基化酶、mg
2+
、mn
2+
、rnasin、dntp、引物、探针和pcr缓冲液。
34.常见的pcr缓冲液由tris-hcl、mgcl2、kcl、triton x-100等缓冲体系构成。一般单个pcr反应管中总体积为20μl~100μl。
35.在一个具体的实施方案中,本发明试剂盒可以兼容数字pcr扩增体系,即可以直接用于数字pcr仪上进行扩增。
36.第四方面,提供了一种用于检测猫口炎病原体并分型的方法,所述方法包括以下步骤:
37.1)提取或释放待测样本的核酸;
38.2)使用如上所述本发明的组合物或上述本发明的试剂盒对步骤1)获得的核酸进行荧光定量pcr分析;
39.3)获得并分析结果。
40.在本发明中,用于检测的样本可以是咽、鼻、眼拭子/edta抗凝全血(血清)等,但不限于此。
41.进一步地,所述荧光定量pcr的反应条件为:
42.逆转录,温度为50℃~60℃,时间5~15分钟,1次循环;taq酶活化,温度为95℃,时间1~10分钟,1次循环;变性,温度为95℃,时间为5~20秒,退火,温度为55℃~60℃,更优选60℃,时间为20~60秒,更优选25s,40~50次循环,熔解曲线分析,62℃~75℃,一次循环。
43.在一个具体的实施方案中,提供了一种用于以非诊断目的检测猫口炎病原体并分型的方法,所述方法包括以下步骤:
44.1)提取或释放待测样本的核酸;
45.2)使用如上述本发明的组合物或上述本发明的试剂盒对步骤1)获得的核酸进行荧光定量pcr分析;
46.3)获得并分析结果。
47.进一步地,所述荧光定量pcr的反应条件为:
48.逆转录,温度为50℃~60℃,时间5~15分钟,1次循环;taq酶活化,温度为95℃,时间1~10分钟,1次循环;变性,温度为95℃,时间为5~20秒,退火,温度为55℃~60℃,更优选60℃,时间为20~60秒,更优选25s,40~50次循环,熔解曲线分析,62℃~75℃,一次循环。
附图说明
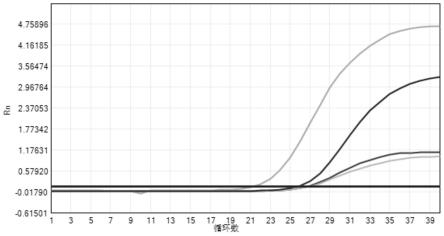
49.图1为本发明组合物检测结果(荧光通道);
50.图2为本发明组合物检测结果(熔解曲线);
51.图3~6为本发明组合物灵敏度检测结果(分别为fam、hex、rox、cy5通道);
52.图7~9为本发明组合物特异性检测结果;
53.图10~18为本发明对比例组合物检测结果;
54.图19~20为本发明组合物不同条件检测结果(fam通道)。
具体实施方式
55.下文将结合具体实施方案和实施例,具体阐述本发明,本发明的优点和各种效果将由此更加清楚地呈现。本领域技术人员应理解,这些具体实施方案和实施例是用于说明本发明,而非限制本发明。
56.实施例1、本发明所使用的引物及探针
57.表1
58.名称序列编号fhv-i-fccgacgtgaccctaatcatagaseq.id no 01fhv-i-rcaggaggttctcgtggaagtgttseq.id no 02fhv-i-ptctctggtctgtttcccactcgcaagataseq.id no 03fcv-fttgtcaatgacagtgttaggttggseq.id no 04fcv-rcgacgaagagcccaggccseq.id no 05fcv-paatcagcatgtggtaaccgttaattcggseq.id no 06felv-fatgtatgattccatttagtccccaseq.id no 07felv-rggtaattttccatgccttgtgaaseq.id no 08felv-pcctaccccaaaaacctagccagctattseq.id no 09fiv-fattactattatggtggggatttgaseq.id no 10fiv-rttgtttttgctgtattgaccatgseq.id no 11fiv-paccccggaagacaaattacaagaagaacseq.id no 12ic-ftaattgaaattgcacccatatcggseq.id no 13ic-rccacttaaatcctaaagttccagaseq.id no 14
59.其中,fhv-i探针的荧光基团是fam;fcv探针的荧光基团是hex;felv探针的荧光基团是rox;fiv探针的荧光基团是cy5。内标下游引物的荧光基团是fam。
60.实施例2、检测猫口炎病原体的方法
61.本发明检测样本为咽、鼻、眼拭子/edta抗凝全血(血清),用本公司磁珠法提取dna,在样本处理室进行如下操作:
62.磁珠法提取:
63.1、根据待测样本数量取预分溶液1若干,每管加入200μl样品;
64.2、加入40μl预分溶液2,盖上管盖,震荡混匀30s,60℃加热4min;
65.3、低速瞬时离心,将离心管置于4孔磁性分离器上,2min~3min后缓慢吸弃废液(*注意不要碰到吸附于管壁内侧的磁珠);离心管在磁性分离器上静置1min~2min后,再次完全吸弃管底废液;
66.4、加入100μl预分溶液3,反复吹打混匀5~10次,将离心管壁上磁珠洗脱到管底,室温静置2min;将离心管置于磁性分离器上磁吸2min,然后将洗脱下来的核酸取适量加入配套扩增试剂中(推荐使用10μl核酸/扩增反应)。
67.所述预分溶液1的配方包括如下原料:
68.0.5%~1.0%(w/v)sds、10%~15%(v/v)甲酰胺、nacl 300mmol/l~650mmol/l、tris-cl 20mmol/l~100mmol/l、edta 1mmol/l~2mmol/l、pmsf 0.8mmol/l~1.2mmol/l、所述tris-cl的ph值为7.0~8.0。
69.所述预分溶液2的配方包括如下原料:
70.proteinase k、0.3%~1.0%(w/v)sds、nacl 100mmol/l~150mmol/l、tris-hcl 10mmol/l~20mmol/l、edta 1mmol/l~2mmol/l、10%~20%(v/v)硅油。
71.所述预分溶液3的配方包括如下原料:
72.0.05%~0.2%(w/v)sds、nahco
3 20mmol/l~60mmol/l,tris-hcl 10mmol/l~20mmol/l。
73.本发明所提供的检测试剂盒还包括如下实时荧光pcr反应体系:
[0074][0075][0076]
pcr扩增程序
[0077][0078]
结果分析:
[0079]
1)目标靶点检测信号为fam和hex(或vic),rox,以及cy5通道,内标检测信号为反应液中fam通道的熔解曲线。
[0080]
2)baseline的设置:baseline一般设置为3-15个循环,具体可根据实际情况进行调整;其调整原则为:选择指数扩增前荧光信号较稳定的区域。
[0081]
起点(start)避开荧光采集起始阶段的信号波动,终点(end)比最早出现指数扩增的样本ct减少1-2个循环。threshold的设置:设定原则以阈值线刚好超过正常阴性对照品的最高点。
[0082]
3)结果阴阳性判定:先分析内标在反应液中fam通道是否检测到熔解曲线,且tm值在判定范围内,若有,表示本次检测有效,可继续进行后续分析。
[0083]
4)若内标在反应液中hex通道没有检测到熔解曲线或tm不在判定范围内,表示本次检测样本浓度太低或者有干扰物质抑制反应,需重新准备实验。
[0084]
5)判读规则:
[0085][0086]
实施例3、本发明组合物测试样本的检测结果
[0087]
将实施例1所示的引物和探针,按照实施例2的方法对各种阳性病原体进行检测,实验结果如图1~2所示。结果表明,各通道均能正常进行检测,该多重pcr体系能够检测对应靶标的情况,并所有病原体进行分型。
[0088]
实施例4、本发明组合物的灵敏度
[0089]
将阳性样本分别用阴性样本稀释浓度至500、5000、50000拷贝/ml,以验证本试剂及检测方法的灵敏度。部分检测结果如图3~6所示,结果表明本发明的方法灵敏度高,检测浓度可达500拷贝/ml。
[0090]
实施例5、本发明组合物的特异性
[0091]
将实施例1所示的引物和探针,按照实施例2所述的方法,对核酸序列具有同源性、易引起相同或相似的临床症状的病原体(如猫上呼吸道病原体猫支原体、猫衣原体、支气管败血波氏杆菌等)在荧光定量pcr仪上进行多重pcr检测,结果如图7~9所示。从图中可以看出,各靶点检测均为阴性,证明本发明组合物有很好的特异性。
[0092]
对比例1、本发明设计的其余的效果不好的引物和探针
[0093]
由于碱基互补配对原则,引物和(或)探针之间会形成二聚体,但这种概率很少,在设计之初就可以排除掉。但多种病原体联合检测时,引物和探针众多,引物和引物、探针和探针或者引物和探针之间容易发生二聚体,要保证设计的保守性(保守性对检测的准确性至关重要),又要考虑不同引物探针之间的相互干扰,需要精心对引物探针进行设计。
[0094]
因此,发明人还设计了其余一些引物和探针(序列未示出)组成了不同的检测体系,同样用于检测各种病原体。具体检测结果如图10-18所示,从图中可以看出检测扩增曲线荧光增幅低,灵敏度检测效果差,而部分靶标甚至无扩增曲线,因此,整体检测效果差。
[0095]
同时,发明人还针对退火温度进行了一系列的对比实验,部分实验结果如图19~20所示,从图中可以看出,退火温度为60℃,25s时效果最好。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1