一种伏硫西汀的合成方法及应用与流程
:
1.本发明属于化学药物合成技术领域,更具体地涉及一种伏硫西汀的合成方 法。
背景技术:
2.伏硫西汀是由丹麦著名的制药公司lunabeck研发的一种用于缓解重度抑郁 症的新型药物。
[0003][0004]
伏硫西汀的作用机理被认为是通过抑制血清素(5-ht)浓度发挥抗抑郁作 用,与其他抑制剂相比,伏硫西汀对去甲肾上腺素和多巴胺能神经元几乎没有 影响。多项临床试验表明伏硫西汀对于治疗重度抑郁有较好的效果,同时研究 表明其安全性和耐受性也取得较好表现。
[0005]
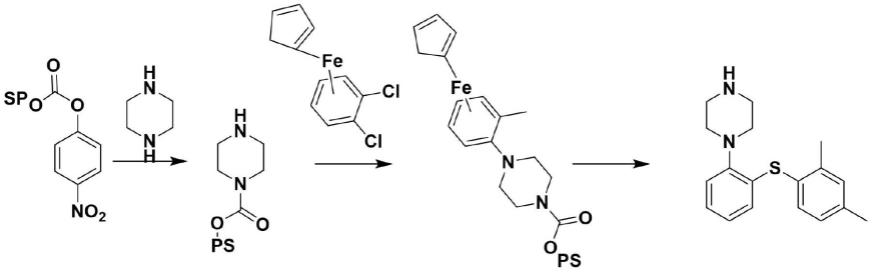
据其原研专利us7144884描述,以4-[(4-硝基苯氧基)羰基氧甲基]苯氧基 甲基聚苯乙烯为起始原料,通过与哌嗪环偶联,然后和邻二氯苯的二茂铁复合 物偶联,最后脱出茂铁和树脂,得到伏硫西汀产物。其主要合成路线如下:
[0006]
不可避免地,4-[(4-硝基苯氧基)羰基氧甲基]苯氧基甲基聚苯乙烯和哌嗪 偶联反应时收率比较低,有大量的化合物1生成。
[0007][0008]
专利wo2013102573中公布了一种伏硫西汀的“一锅法”合成路线,2,4-二 甲基苯硫酚和邻溴碘苯和哌嗪环“一锅法”合成伏硫西汀,但是该反应存在溴 和碘的双卤素竞争反应问题,且用到了昂贵的钯催化剂和磷配体,直接导致了 反应路线的成本提升和反应收
率低等问题。
[0009][0010]
为了避免哌嗪环的副反应,专利cn102617513a中采用了对哌嗪环进行boc (叔丁氧羰基)保护,使得化合物3与哌嗪环反应时效率更高,带来的后果就 是后续又增加了一步脱boc保护的反应步骤,工序较为麻烦且对最终的产品收 率影响较大。
[0011][0012]
专利cn103936694a中报道了一种伏硫西汀得合成方法,用邻硝基氟苯和 2,4-二甲基苯硫酚为原料,中间以双(2-氯乙基)胺盐酸盐作为环化反应得到产 品,但是其用到铁酸还原,还原效果较差,且后处理比较麻烦。
[0013][0014]
近期,基于专利cn103936694a中报道了一种伏硫西汀得合成方法,进行一 些改进:将邻硝基氟苯替换成邻氨基氟苯,和2,4-二甲基苯硫酚为原料,中间 以双(2-氯乙基)胺盐酸盐作为环化反应得到产品,能够避免铁酸还原,但是邻 氨基氟苯与2,4-二甲基苯硫酚的反应效果较差,反应位点较多容易出现大量副 产物,这可能是由于在邻氨基氟苯与2,4-二甲基苯酚的反应条件下,邻氨基氟 苯可能会发生自身的缩合反应,卤素基团在反应条件下可能会进攻邻位的氨基, 从而影响整个反应的进程。
[0015]
在现有技术中,伏硫西汀的合成方法多种多样,但基本都存在合成困难、 副反应多、纯度较差、收率较低或者纯化过程繁琐,纯化困难等各种问题。
技术实现要素:
[0016]
为解决上述问题,克服现有技术的不足,本发明提供了一种氢溴酸伏硫西 汀的合成方法,能够有效的解决上述的问题。
[0017]
本发明解决上述技术问题的具体技术方案为:伏硫西汀的合成方法,其特 征在于
包括如下步骤:
[0018]
步骤1:在氮气保护条件下,将邻氨基苯硫酚与双(2-氯乙基)胺盐酸盐加入 反应溶剂ⅰ中,并经过加热回流反应,生成含有邻哌嗪基苯硫酚的反应液ⅰ;
[0019]
步骤2:含有邻哌嗪基苯硫酚的反应液ⅰ经过提取、纯化和干燥获得邻哌嗪 基苯硫酚;
[0020]
步骤3:在氮气保护条件下,将2,4-二甲基卤代苯和步骤2中获得的邻哌 嗪基苯硫酚加入反应溶剂ⅱ中,加入碱性试剂,在高温条件下搅拌反应生成含 有伏硫西汀的反应液ⅱ,
[0021]
步骤4:含有伏硫西汀的反应液ⅱ经过提取、纯化和干燥获得伏硫西汀;
[0022]
进一步地,所述的反应溶剂ⅰ为乙醇或乙腈或二氧六环或四氢呋喃;
[0023]
进一步地,所述的邻氨基苯硫酚、双(2-氯乙基)胺盐酸盐和反应溶剂ⅰ的摩 尔比为1:1.0~1.5:20;
[0024]
进一步地,所述步骤2的提取、纯化和干燥步骤包括:在含有邻哌嗪基苯 硫酚的反应液ⅰ中,加入纯化水进行淬灭反应,再加入萃取剂萃取分层,取有 机层用饱和食盐水溶液洗涤,无水硫酸镁干燥,减压蒸除溶剂,在55-65℃真空 干燥,得邻哌嗪基苯硫酚;
[0025]
进一步地,所述步骤3中的反应溶剂ⅱ为dmf或dmso或甲苯,反应温 度为110℃~130℃,碱性试剂为叔丁醇钠或氢化钠或乙醇钠,
[0026]
进一步地,所述步骤3中邻氨基苯硫酚、二(2-氯乙基)胺盐、反应溶剂ⅱ和 碱性试剂的摩尔比为1:(0.8~1.2):20:(0.5~7.0);
[0027]
进一步地,所述步骤4的提取、纯化和干燥包括:将含有伏硫西汀的反应 液ⅱ加入纯化水猝灭反应,利用萃取剂萃取,将有机层用饱和食盐水溶液洗涤, 活性炭脱色,过滤,合并有机层,减压蒸除溶剂,真空干燥得伏硫西汀;
[0028]
进一步地,所述步骤2的反应溶剂ⅰ与纯化水、萃取剂的体积比为1:1: (0.3~0.5);步骤4的反应溶剂ⅱ与纯化水、萃取剂的摩尔比为1:1:(0.3~0.5), 所述步骤2和步骤4的萃取剂均为乙酸乙酯;
[0029]
进一步地,所述伏硫西汀用于制备氢溴酸伏硫西汀,制备方法包括:将伏 硫西汀溶于异丙醇溶液中,升温至45℃,搅拌全溶,缓慢滴入45%氢溴酸溶液, 有固体析出时,搅拌30min,然后将剩余45%氢溴酸溶液加入体系中,50℃反 应1h,趁热过滤,滤饼用异丙醇、45%氢溴酸混合溶液冲洗,收集滤饼,加入 甲基叔丁基醚,控温25~30℃,搅拌打浆3h,抽滤至无滤液滴落时,继续抽滤, 用少量甲基叔丁基醚冲洗滤饼,收集滤饼,55℃真空干燥12h,得氢溴酸伏硫西 汀;
[0030]
进一步地,w
伏硫西汀
:v
异丙醇
:v
45%氢溴酸溶液
:v
冲洗水
:v
甲基叔丁基醚
=(2~2.5g):10ml: 1ml:10ml:10ml。
[0031]
本发明的有益效果是:
[0032]
不涉及到基团的保护与脱保护,可以缩短工艺流程,同时避免了副反应的 发生,减少了产物后期纯化的操作步骤,利于工业化生产。
[0033]
具体实施方式:
[0034]
在本发明的描述中具体细节仅仅是为了能够充分理解本发明的实施例,但 是作为本领域的技术人员应该知道本发明的实施并不限于这些细节。另外,公 知的结构和功能没有被详细的描述或者展示,以避免模糊了本发明实施例的要 点。对于本领域的普通技术人员而言,可以具体情况理解上述术语在本发明中 的具体含义。
[0035]
本发明的具体实施方式:
[0036]
为了更好的理解本发明特以具体的实施例进行说明,值得强调的是该实施 例的效果与本发明保护范围内的各种实施例无实质性差异,均能够实现本发明 所描述的效果及解决上述问题;
[0037]
实施例1:
[0038]
(1)邻哌嗪基苯硫酚的合成
[0039]
氮气保护条件下,将2.48g邻氨基苯硫酚(20mmol)溶于乙醇25ml中,加 入双(2-氯乙基)胺盐酸盐3.0g,80℃加热回流,tlc监测反应过程。反应结束后 加入20ml纯化水淬灭反应,加入乙酸乙酯(20ml
×
3)萃取分层,有机层用饱和 食盐水溶液洗涤,无水硫酸镁干燥,减压蒸除溶剂,60℃真空干燥,得类白色 固体2.98g,收率76.8%;
[0040]
(2)伏硫西汀的合成
[0041]
氮气保护条件下,将5.8g叔丁醇钠(60mmol)投入dmf(15ml)中,然后 加入1.9g邻哌嗪基苯硫酚(10mmol),搅拌30min后加入2,4-二甲基碘苯 (12mmol),升温至120℃,搅拌反应过夜。向料液中加入15ml纯化水猝灭反 应,乙酸乙酯(30ml)萃取三次,有机层用饱和食盐水溶液洗涤,活性炭脱色, 过滤,合并有机层,减压蒸除溶剂,真空干燥得白色粉末2.42g,收率81.5%;
[0042]
(3)氢溴酸伏硫西汀的合成
[0043]
将1.2g伏硫西汀溶于50ml异丙醇溶液中,升温至45℃,搅拌全溶,缓慢滴 入45%氢溴酸溶液,有固体析出时停止加入,继续搅拌30min,然后将剩余45% 氢溴酸溶液加入体系中(共计5ml),升温至50℃反应1h,趁热过滤,滤饼用 10ml异丙醇、45%氢溴酸混合溶液(v异丙醇:45%氢溴酸=10:1)冲洗。收 集滤饼,加入甲基叔丁基醚,控温25~30℃,搅拌打浆3h,抽滤至无滤液滴落 时,继续抽滤15min,用少量甲基叔丁基醚冲洗滤饼,收集滤饼,55℃真空干燥 12h,得白色结晶粉末1.32g,收率86.8%,hplc纯度为99.93%。
[0044]
实施例2:
[0045]
(1)邻哌嗪基苯硫酚的合成
[0046]
氮气保护条件下,将1.24g邻氨基苯硫酚(10mmol)溶于10ml乙腈中,加 入双(2-氯乙基)胺盐酸盐1.5g,80℃加热回流,tlc监测反应过程。反应结束后 加入5ml纯化水淬灭反应,加入乙酸乙酯(5ml
×
3)萃取分层,有机层用饱和食 盐水溶液洗涤,无水硫酸镁干燥,减压蒸除溶剂,60℃真空干燥,得类白色固 体1.45g,收率75.1%,
[0047]
(2)伏硫西汀的合成
[0048]
氮气保护条件下,将0.24g氢化钠(10mmol)投入dmso(15ml)中,然 后加入1.9g邻哌嗪基苯硫酚(10mmol),搅拌30min后加入2,4-二甲基碘苯 (11mmol),升温至120℃,搅拌反应过夜。向料液中加入5ml纯化水猝灭反应, 乙酸乙酯(5ml)萃取三次,有机层用饱和食盐水溶液洗涤,活性炭脱色,过滤, 合并有机层,减压蒸除溶剂,真空干燥得白色粉粉末2.47g,收率82.8%。
[0049]
(3)氢溴酸伏硫西汀的合成
[0050]
将2.0g伏硫西汀溶于100ml异丙醇溶液中,升温至45℃,搅拌全溶,缓慢 滴入45%氢溴酸溶液,有固体析出时,搅拌30min,然后将剩余45%氢溴酸溶 液加入体系中(共计10ml),50℃反应1h,趁热过滤,滤饼用20ml异丙醇、45% 氢溴酸混合溶液(v异丙醇:45%氢溴酸=10:1)冲洗。收集滤饼,加入甲基叔 丁基醚,控温25~30℃,搅拌打浆3h,抽滤至无滤液滴落时,继续抽滤15min, 用少量甲基叔丁基醚冲洗滤饼,收集滤饼,55℃真空干燥12h,得白色结晶粉末 2.18g,收率85.8%,hplc纯度为99.93%。
[0051]
实施例3:
[0052]
(1)邻哌嗪基苯硫酚的合成
[0053]
氮气保护条件下,将2.51g邻氨基苯硫酚(20mmol)溶于二氧六环35ml中, 加入双(2-氯乙基)胺盐酸盐2.6g,100℃加热回流,tlc监测反应过程。反应结 束后加入15ml纯化水淬灭反应,加入乙酸乙酯(15ml
×
3)萃取分层,有机层用 饱和食盐水溶液洗涤,无水硫酸镁干燥,减压蒸除溶剂,60℃真空干燥,得类 白色固体2.79g,收率71.9%,
[0054]
(2)伏硫西汀的合成
[0055]
氮气保护条件下,将0.68g乙醇钠(10mmol)投入甲苯(25ml)中,然后加 入1.9g邻哌嗪基苯硫酚(10mmol),搅拌30min后加入2,4-二甲基碘苯 (10mmol),升温至120℃,搅拌反应过夜。向料液中加入5ml纯化水猝灭反应, 乙酸乙酯(10ml)萃取三次,有机层用饱和食盐水溶液洗涤,活性炭脱色,过 滤,合并有机层,减压蒸除溶剂,真空干燥得白色粉末2.48g,收率83.2%。
[0056]
(3)氢溴酸伏硫西汀的合成
[0057]
将1.0g伏硫西汀溶于50ml异丙醇溶液中,升温至45℃,搅拌全溶,缓慢滴 入45%氢溴酸溶液,有固体析出时,搅拌30min,然后将剩余45%氢溴酸溶液 加入体系中(共计5ml),50℃反应1h,趁热过滤,滤饼用10ml异丙醇、45% 氢溴酸混合溶液(v异丙醇:45%氢溴酸=10:1)冲洗。收集滤饼,加入甲基叔 丁基醚,控温25~30℃,搅拌打浆3h,抽滤至无滤液滴落时,继续抽滤15min, 用少量甲基叔丁基醚冲洗滤饼,收集滤饼,55℃真空干燥12h,得白色结晶粉末 1.12g,收率88.2%,hplc纯度为99.93%。
[0058]
实施例4:
[0059]
(1)邻哌嗪基苯硫酚的合成
[0060]
氮气保护条件下,将1.86g邻氨基苯硫酚(15mmol)溶于四氢呋喃25ml中, 加入双(2-氯乙基)胺盐酸盐2.1g,60℃加热回流,tlc监测反应过程。反应结束 后加入10ml纯化水淬灭反应,加入乙酸乙酯(10ml
×
3)萃取分层,有机层用饱 和食盐水溶液洗涤,无水硫酸镁干燥,减压蒸除溶剂,60℃真空干燥,得类白 色固体2.15g,收率73.8%,
[0061]
(2)伏硫西汀的合成
[0062]
氮气保护条件下,将1.2g乙醇钠(60mmol)投入dmf(15ml)中,然后加 入1.9g邻哌嗪基苯硫酚(10mmol),搅拌30min后加入2,4-二甲基碘苯 (10mmol),升温至120℃,搅拌反应过夜。向料液中加入5ml纯化水猝灭反应, 乙酸乙酯(5ml)萃取三次,有机层用饱和食盐水溶液洗涤,活性炭脱色,过滤, 合并有机层,减压蒸除溶剂,真空干燥得白色粉末2.51g,收率84.3%。
[0063]
(3)氢溴酸伏硫西汀的合成
[0064]
将1.2g伏硫西汀溶于50ml异丙醇溶液中,升温至45℃,搅拌全溶,缓慢滴 入45%氢溴酸溶液,有固体析出时,搅拌30min,然后将剩余45%氢溴酸溶液 加入体系中(共计5ml),50℃反应1h,趁热过滤,滤饼用10ml异丙醇、45% 氢溴酸混合溶液(v异丙醇:45%氢溴酸=10:1)冲洗。收集滤饼,加入甲基叔 丁基醚,控温25~30℃,搅拌打浆3h,抽滤至无滤液滴落时,继续抽滤15min, 用少量甲基叔丁基醚冲洗滤饼,收集滤饼,55℃真空干燥12h,得白色结晶粉末 1.33g,收率87.5%,hplc纯度为99.93%。
[0065]
为了更加直观的展现本发明的产品优势,特以本发明一种伏硫西汀的合成方 法与对比例1中报道了一种伏硫西汀得合成方法进行对比(按照国家发明专利 cn103936694a,所述的方法进行生产伏硫西汀得合成方法,以援引方式引入),
[0066]
对比例2:
[0067]
制备方法同对比例1,所不同的是:本对比例的制备过程中,将邻硝基氟苯 替换成邻氨基氟苯;更换起始原料可以避免铁酸还原的步骤,但是邻氨基氟苯 中,氨基为强给电子集团,卤素为强吸电子基团,两者产生推拉电子效应发生 分子内反应从而影响邻氨基氟苯与2,4-二甲基苯硫酚的反应效率,
[0068]
而本发明提供的邻氨基苯硫酚,与氨基相比,巯基仅表现出极弱的给电子 效应,第一步反应中利用氨基的强推电子效应与双(2-氯乙基)胺盐酸盐优先反应 生成邻哌嗪基苯硫酚,然后再与2,4-二甲基碘苯反应生成伏硫西汀,副产物极少, 大大提升了反应效率。
[0069]
综上所述:本发明的伏硫西汀的合成方法不涉及到基团的保护与脱保护, 可以缩短工艺流程,同时避免了副反应的发生,减少了产物后期纯化的操作步 骤,利于工业化生产。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1