靶向CCR8的嵌合抗原受体及其用途的制作方法
本发明属于肿瘤免疫治疗。更具体地,本发明涉及一种靶向ccr8的嵌合抗原受体及其用途。
背景技术:
1、近几年,肿瘤免疫治疗进入了快速发展阶段,嵌合抗原受体t细胞(car-t)疗法作为其中一种重要的方法在血液瘤领域取得了非常令人振奋的治疗效果。目前,国内越来越多的企业、医院及学术机构加入到这一研究领域中,共同推进car-t细胞疗法的发展,探索其更为广泛的潜在应用价值。
2、目前,在car-t细胞治疗领域,主要是采用自体car-t细胞进行治疗,基本过程是采集患者自己的外周血,分离t细胞,并完成car-t细胞的制备和回输。由于免疫系统自身的某些限制性因素,如car-t异体回输时由于免疫原性等原因导致的宿主抗移植物反应(hvgd)、移植物抗宿主反应(gvhd)等,自体car-t细胞疗法的广泛性和便捷性应用受到限制,这同时也在一定程度上提高了生产成本,因此,具有低成本、现货供应等优势的通用型car-t技术将是今后的一个重要发展方向。然,而,与自体car t技术相比,通用型car t技术仍面临着一些挑战。
3、在通用型car t技术所面临的挑战中,体内持久性较差是一个最重要的问题。目前的解决方案一般有两种,一种是敲除car-t细胞中引起宿主免疫排异的基因例如tcr、hla-i类基因等,这种方案会使car-t细胞的持久性得到一定程度的改善;另一种方案则是针对性地清除或抑制宿主体内的nk细胞和激活型t细胞,从而降低这些免疫细胞对外源性car-t细胞的排斥和杀伤,提高car-t细胞的持久性。
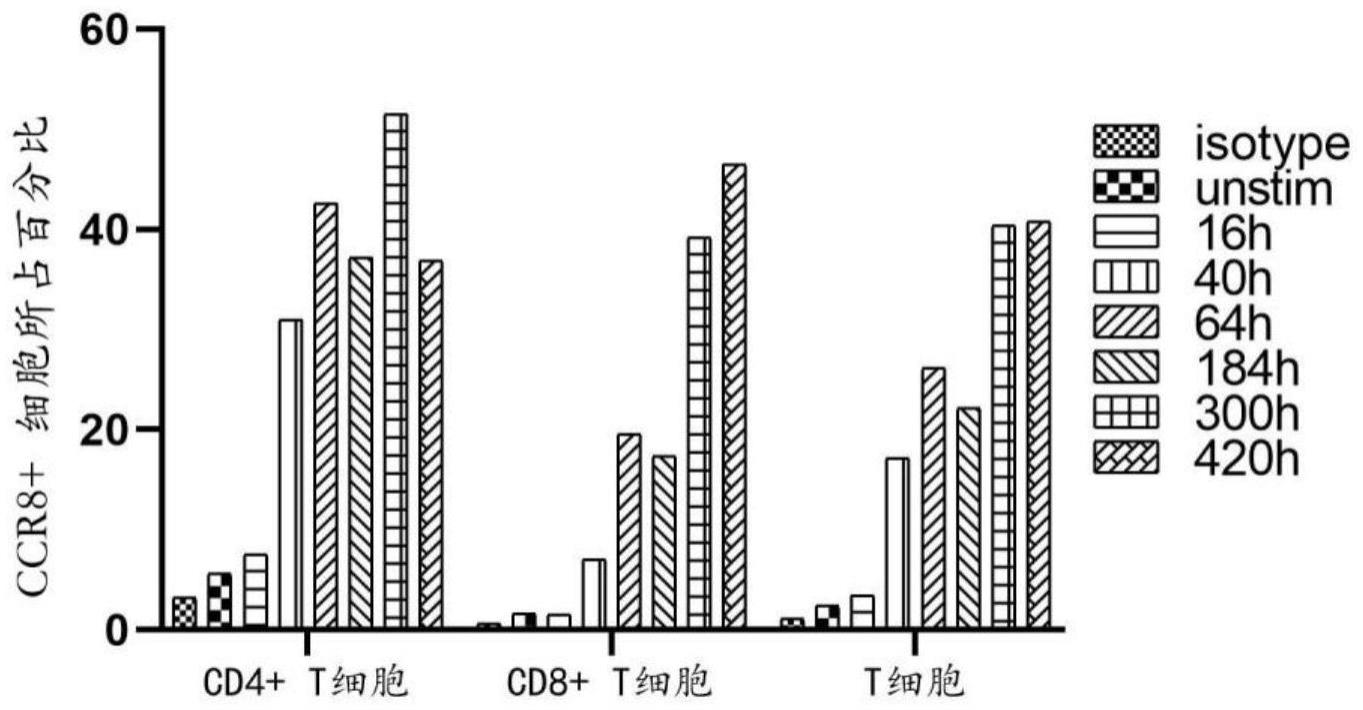
4、ccr8是趋化因子受体亚家族的成员,属于gpcr类蛋白。已有研究表明,ccr8主要表达在单核细胞、th2细胞和treg细胞上。近年来的研究表明,ccr8特异性表达于免疫抑制性的treg细胞,尤其是肿瘤部位的treg高表达ccr8。大量研究表明高表达的ccr8与多种癌症相关,包括结肠和直肠癌、乳腺癌、胃癌、转移性脑癌、转移性肝癌等。已有研究表明,nk细胞表达ccr8分子;我们的研究证实,激活的t细胞也表达ccr8。
5、因此,本发明提供表达靶向ccr8的嵌合抗原受体的工程化免疫细胞,其同时具有清除肿瘤细胞、患者自身nk细胞和激活型t细胞的能力,能显著提高对靶细胞的杀伤功能。另外,在自身免疫性疾病和器官移植伴随的移植物抗宿主病(gvhd)、宿主抗移植物病(hvgd)中,同样存在着t细胞过度激活、不正常激活等现象,靶向ccr8的工程化免疫细胞同样可用于这些情形的治疗、控制。
技术实现思路
1、本发明的目的在提供一种靶向ccr8的嵌合抗原受体及表达其的工程化免疫细胞,其可用于细胞免疫治疗中对患者自身nk细胞和激活型t细胞的杀伤,进而降低患者的免疫排斥反应,增强细胞治疗的效果。同时,其也可用于治疗和控制自身免疫性疾病和器官移植伴随的gvhd和hvgd。
2、因此,在第一个方面,本发明提供一种嵌合抗原受体,其包含靶向ccr8的抗体、跨膜结构域和胞内信号传导结构域,其中所述靶向ccr8的抗体包含如seq id no:1或11所示的cdr-h1、如seq id no:2或12所示的cdr-h2、如seq id no:3或13所示的cdr-h3、如seq idno:4或14所示的cdr-l1、如seq id no:5或15所示的cdr-l2、如seq id no:6或16所示的cdr-l3。优选地,所述靶向ccr8的抗体包含与seq id no:7或17所示的氨基酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的重链可变区序列和与seq id no:8或18所示的氨基酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的轻链可变区序列。更为优选地,所述靶向ccr8的抗体包含与seq id no:9或19所示的氨基酸序列,或seq id no:10或20所示的核苷酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的序列。
3、在一个实施方案中,所述嵌合抗原受体还包含靶向第二靶点的抗体,所述第二靶点与ccr8相同或不同。优选地,所述第二靶点选自:tshr、cd7、cd19、cd123、cd22、baff-r、cd30、cd171、cs-1、cll-1、cd33、egfrviii、gd2、gd3、bcma、gprc5d、tn ag、psma、ror1、flt3、fap、tag72、cd38、cd44v6、cea、epcam、b7h3、kit、il-13ra2、间皮素、il-l lra、psca、prss21、vegfr2、lewisy、cd24、pdgfr-β、ssea-4、cd20、folate受体α、erbb2(her2/neu)、muc1、egfr、ncam、claudin18.2、prostase、pap、elf2m、ephrin b2、igf-i受体、caix、lmp2、gploo、bcr-abl、酪氨酸酶、epha2、fucosyl gml、sle、gm3、tgs5、hmwmaa、o-乙酰基-gd2、folate受体β、tem1/cd248、tem7r、cldn6、gprc5d、cxorf61、cd97、cd179a、alk、多聚唾液酸、plac1、globoh、ny-br-1、upk2、havcr1、adrb3、panx3、gpr20、ly6k、or51e2、tarp、wt1、ny-eso-1、lage-la、mage-a1、豆荚蛋白、hpv e6、e7、mage al、etv6-aml、精子蛋白17、xage1、tie 2、mad-ct-1、mad-ct-2、fos相关抗原1、p53、p53突变体、前列腺特异性蛋白、存活蛋白和端粒酶、pcta-l/galectin 8、melana/martl、ras突变体、htert、肉瘤易位断点、ml-iap、erg(tmprss2 ets融合基因)、na17、pax3、雄激素受体、cyclin bl、mycn、rhoc、trp-2、cyp1b1、boris、sart3、pax5、oy-tes 1、lck、akap-4、ssx2、rage-1、人端粒酶逆转录酶、ru1、ru2、肠道羧酸酯酶、mut hsp70-2、cd79a、cd79b、cd72、lair1、fcar、lilra2、cd300lf、clec12a、bst2、emr2、ly75、gpc3、fcrl5、igll1、pd1、pdl1、pdl2、tgfβ、april、nkg2d或其任意组合。更为优选地,所述第二靶点选自:cd7、cd19、cd20、cd22、cd30、cd33、cd38、cd123、cd138、cd171、muc1、afp、folate受体α、cea、psca、psma、her2、egfr、il13ra2、gd2、nkg2d、egfrviii、cs1、bcma、间皮素、cluadin18.2、ror1、ny-eso-1、mage-a4或其任意组合。
4、在一个实施方案中,所述嵌合抗原受体还包含靶向cd19的抗体,其包含如seq idno:21所示的cdr-h1、如seq id no:22所示的cdr-h2、如seq id no:23所示的cdr-h3、如seqid no:24所示的cdr-l1、如seq id no:25所示的cdr-l2、如seq id no:26所示的cdr-l3。优选地,所述靶向cd19的抗体包含与seq id no:27、31、33任一所示的氨基酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的重链可变区序列和与seq id no:28、32、34任一所示的氨基酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的轻链可变区序列。更为优选地,所述靶向cd19的抗体包含与seq id no:29、35-38任一所示的氨基酸序列,或seq id no:30、39-42任一所示的核苷酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的序列。
5、在一个实施方案中,所述嵌合抗原受体中靶向ccr8的抗体和靶向第二靶点的抗体是串联的形式,所述嵌合抗原受体包含:(1)抗原结合区,包含靶向ccr8的抗体和靶向第二靶点的抗体;(2)跨膜结构域;和(3)胞内信号传导结构域。
6、在另一个实施方案中,所述嵌合抗原受体中靶向ccr8的抗体和靶向第二靶点的抗体是并联的形式,所述嵌合抗原受体包含:(1)靶向ccr8的第一单元结构,包含靶向ccr8的抗体、跨膜结构域和胞内信号传导结构域;和(2)靶向第二靶点的第二单元结构,包含靶向第二靶点的抗体、跨膜结构域和胞内信号传导结构域。
7、在一个实施方案中,本发明中所述的抗体选自免疫球蛋白分子、fab、fab'、f(ab')2、fv片段、scfv、二硫键-连接的fv(sdfv)、抗体的重链可变区(vh)或轻链可变区(vl)、由vh和ch1结构域组成的fd片段、线性抗体、单结构域抗体、纳米抗体和所述抗原的天然配体或其功能性片段。
8、在一个实施方案中,所述跨膜结构域选自以下蛋白质的跨膜结构域:tcrα链、tcrβ链、tcrγ链、tcrδ链、cd3ζ亚基、cd3ε亚基、cd3γ亚基、cd3δ亚基、cd45、cd4、cd5、cd8α、cd9、cd16、cd22、cd33、cd28、cd37、cd64、cd80、cd86、cd134、cd137、cd154或其任意组合。优选地,所述跨膜结构域选自cd8α、cd4、cd28或cd278的跨膜结构域。
9、在一个实施方案中,所述胞内信号传导结构域包含共刺激结构域和/或初级信号传导结构域。
10、在一个实施方案中,所述共刺激结构域选自以下蛋白质的共刺激信号传导结构域:ltb、cd94、tlr1、tlr2、tlr3、tlr4、tlr5、tlr6、tlr7、tlr8、tlr9、tlr10、card11、cd2、cd7、cd8、cd18、cd27、cd28、cd30、cd40、cd54、cd83、cd134(ox40)、cd137(4-1bb)、cd270(hvem)、cd272(btla)、cd276(b7-h3)、cd278(icos)、cd357(gitr)、dap10、dap12、lat、nkg2c、slp76、pd-1、light、trim、zap70或其任意组合。优选地,所述共刺激结构域选自4-1bb、cd28、cd27、ox40、cd278或其任意组合。
11、在一个实施方案中,所述初级信号传导结构域选自以下蛋白的信号传导结构域:fcrγ、fcrβ、cd3γ、cd3δ、cd3ε、cd3ζ、cd22、cd79a、cd79b、cd66d或其任意组合。优选地,所述初级信号传导结构域包含cd3ζ的信号传导结构域。
12、在第二个方面,本发明提供编码上述嵌合抗原受体的核酸分子以及包含该核酸分子的载体。
13、在第三个方面,本发明提供含上述核酸分子或载体,或表达上述嵌合抗原受体的工程化免疫细胞。
14、在一个实施方案中,所述免疫细胞是t细胞、b细胞、巨噬细胞、树突状细胞、单核细胞、nk细胞和/或nkt细胞等。优选地,所述免疫细胞是t细胞、nk细胞或nkt细胞。更为优选地,所述t细胞是cd4+cd8+t细胞、cd4+t细胞、cd8+t细胞、cd4-cd8-t细胞、肿瘤浸润细胞、记忆t细胞、幼稚t细胞、γδ-t细胞和/或αβ-t细胞。
15、在一个实施方案中,所述工程化免疫细胞中,至少一种mhc相关基因的表达被抑制或沉默。所述mhc相关基因选自hla-a、hla-b、hla-c、b2m、hla-dpa、hla-dq、hla-dra、tap1、tap2、lmp2、lmp7、rfx5、rfxap、rfxank、ciita或其任意组合,优选hla-a、hla-b、hla-c、b2m、rfx5、rfxap、rfxank、ciita或其任意组合。
16、在一个实施方案中,所述工程化免疫细胞中,至少一种tcr/cd3相关基因的表达被抑制或沉默。所述tcr/cd3基因选自trac、trbc、cd3γ、cd3δ、cd3ε、cd3ζ或其任意组合。
17、在一个优选的实施方案中,所述工程化免疫细胞的至少一种tcr/cd3基因和至少一种mhc相关基因的表达被抑制或沉默,其中所述至少一种tcr/cd3基因选自trac、trbc或其任意组合,所述至少一种mhc相关基因是b2m、rfx5、rfxap、rfxank、ciita或其任意组合。在一个实施方案中,所述工程化免疫细胞的trac或trbc,和b2m的表达被抑制或沉默。在一个实施方案中,所述工程化免疫细胞的trac或trbc,和ciita的表达被抑制或沉默。在一个优选的实施方案中,所述工程化免疫细胞的trac或trbc、b2m和ciita的表达被抑制或沉默。在一个优选的实施方案中,所述工程化免疫细胞的trac或trbc、b2m和rfx5的表达被抑制或沉默。
18、在第四个方面,本发明提供一种药物组合物,包含上述的本发明的工程化免疫细胞和一种或多种药学上可接受的载体和/或赋型剂。
19、在第五个方面,本发明提供上述嵌合抗原受体或工程化免疫细胞或药物组合物在制备治疗/预防/诊断癌症、感染或自身免疫性疾病药物中的用途及在制备治疗/缓解/消除gvhd或hvgd药物中的用途。
20、在一个实施方案中,所述癌症选自:脑神经胶质瘤、胚细胞瘤、肉瘤、白血病、基底细胞癌、胆道癌、膀胱癌、骨癌、脑和cns癌症、乳腺癌、腹膜癌、宫颈癌、绒毛膜癌、结肠和直肠癌、结缔组织癌症、消化系统的癌症、子宫内膜癌、食管癌、眼癌、头颈癌、胃癌、胶质母细胞瘤(gbm)、肝癌、肝细胞瘤、上皮内肿瘤、肾癌、喉癌、肝肿瘤、肺癌、淋巴瘤、黑色素瘤、骨髓瘤、神经母细胞瘤、口腔癌、卵巢癌、胰腺癌、前列腺癌、视网膜母细胞瘤、横纹肌肉瘤、直肠癌、呼吸系统的癌症、唾液腺癌、皮肤癌、鳞状细胞癌、胃癌、睾丸癌、甲状腺癌、子宫或子宫内膜癌、泌尿系统的恶性肿瘤、外阴癌以及其它癌和肉瘤、以及b细胞淋巴瘤、套细胞淋巴瘤、aids相关淋巴瘤、以及waldenstrom巨球蛋白血症、慢性淋巴细胞白血病(cll)、急性淋巴细胞白血病(all)、b细胞急性淋巴细胞白血病(b-all)、t细胞急性淋巴细胞白血病(t-all)、b细胞幼淋巴细胞白血病、母细胞性浆细胞样树突状细胞瘤、伯基特氏淋巴瘤、弥散性大b细胞淋巴瘤、滤泡性淋巴瘤、慢性骨髓性白血病(cml)、恶性淋巴组织增生疾病、malt淋巴瘤、毛细胞白血病、边缘区淋巴瘤、多发性骨髓瘤、骨髓发育不良、浆母细胞性淋巴瘤、白血病前期、浆细胞样树突状细胞瘤、以及移植后淋巴细胞增生性紊乱(ptld)。
21、发明详述
22、除非另有说明,否则本文中所使用的所有科学技术术语的含义与本发明所属领域的普通技术人员通常所了解的相同。
23、嵌合抗原受体
24、如本文所用,术语“嵌合抗原受体”是指人工构建的杂合多肽,该杂合多肽的基础结构包括抗原结合结构域(例如抗体的抗原结合部分)、跨膜结构域和胞内信号传导结构域。嵌合抗原受体能够利用抗原结合结构域的抗原结合特性以非mhc限制性的方式将t细胞和其它免疫细胞的特异性和反应性重定向至所选择的靶标。非mhc限制性的抗原识别给予表达嵌合抗原受体的t细胞与抗原处理无关的识别抗原的能力,因此绕过了肿瘤逃逸的主要机制。
25、本发明提供一种嵌合抗原受体,其包含靶向ccr8的抗体、跨膜结构域和胞内信号传导结构域。
26、在一个实施方案中,所述靶向ccr8的抗体包含如seq id no:1或11所示的cdr-h1或在seq id no:1或11的基础上取代、缺失或添加至多3个氨基酸的变体、如seq id no:2或12所示的cdr-h2或在seq id no:2或12的基础上取代、缺失或添加至多3个氨基酸的变体、如seq id no:3或13所示的cdr-h3或在seq id no:3或13的基础上取代、缺失或添加至多3个氨基酸的变体、如seq id no:4或所示的cdr-l1或在seq id no:4或14的基础上取代、缺失或添加至多3个氨基酸的变体、如seq id no:5或15所示的cdr-l2或在seq id no:5或15的基础上取代、缺失或添加至多3个氨基酸的变体、如seq id no:6所示的cdr-l3或在seqid no:6或16的基础上取代、缺失或添加至多3个氨基酸的变体。优选地,所述靶向ccr8的抗体包含与seq id no:7或17所示的氨基酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的重链可变区序列和与seq id no:8或18所示的氨基酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的轻链可变区序列。更为优选地,所述靶向ccr8的抗体包含与seq id no:9或19所示的氨基酸序列,或seq id no:10或20所示的核苷酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的序列。
27、在另一个实施方案中,所述嵌合抗原受体还包含靶向第二靶点的抗体,所述第二靶点与ccr8相同或不同。在一个实施方案中,靶向ccr8的抗体和靶向第二靶点的抗体是串联或并联的形式。在本文中,“串联”是指靶向ccr8的抗体和靶向第二靶点的抗体通过接头连接成为嵌合抗原受体的抗原结合区,并共享同一个跨膜结构域和胞内信号传导结构域。换言之,在“串联”的情况下,本发明的嵌合抗原受体包含:(1)抗原结合区,包含靶向ccr8的抗体和靶向第二靶点的抗体;(2)跨膜结构域;和(3)胞内信号传导结构域。本领域技术人员知晓,在串联形式下,靶向ccr8的抗体和靶向第二靶点的抗体可以通过接头以任何顺序连接。并且,当两个抗体均为scfv时,还可以以例如以下顺序连接(从n端至c端):vl1-vl2-接头-vh2-vh1、vl2-vl1-接头-vh1-vh2、vh1-vh2-接头-vl2-vl1、vh12-vh1-接头-vl1-vl2。在本文中,“并联”是指靶向ccr8的抗体和靶向第二靶点的抗体位于两个不同的单元结构中,各自分别连接跨膜结构域和胞内信号传导结构域,所述两个不同的单元结构可以位于同一载体(例如,通过2a肽将两个单元结构连接,使其分别表达),或位于不同载体(例如,每个载体包含一个靶向ccr8或第二靶点的单元结构,然后将两个载体一起导入免疫细胞)。换言之,在“并联”的情况下,本发明的嵌合抗原受体包含:(1)靶向ccr8的第一单元结构,包含靶向ccr8的抗体、跨膜结构域和胞内信号传导结构域;和(2)靶向第二靶点的第二单元结构,包含靶向第二靶点的抗体、跨膜结构域和胞内信号传导结构域。任选地,所述第一单元结构和第二单元结构位于同一载体或不同载体。
28、在一个实施方案中,本发明的第二靶点选自:cd2、cd3、cd4、cd7、cd8、cd14、cd15、cd19、cd20、cd21、cd22、cd23、cd24、cd25、cd30、cd33、cd37、cd38、cd40、cd40l、cd44、cd46、cd47、cd52、cd54、cd56、cd70、cd73、cd80、cd97、cd123、cd126、cd138、cd171、cd 179a、dr4、dr5、tac、tem1/cd248、vegf、gucy2c、egp40、egp-2、egp-4、cd133、ifnar1、dll3、kappa轻链、tim3、tshr、cd19、baff-r、cll-1、egfrviii、tegfr、gd2、gd3、bcma、tn抗原、psma、ror1、flt3、fap、tag72、cd44v6、cea、epcam、b7h3、kit、il-13ra2、il-llra、il-22ra、il-2、间皮素、psca、prss21、vegfr2、lewisy、pdgfr-β、ssea-4、afp、folate受体α、erbb2(her2/neu)、erbb3、erbb4、muc1、muc16、egfr、cs1、ncam、claudin18.2、c-met、prostase、pap、elf2m、ephrin b2、igf-i受体、caix、lmp2、gpl00、bcr-abl、酪氨酸酶、epha2、fucosyl gml、sle、gm3、tgs5、hmwmaa、o-乙酰基-gd2、folate受体β、tem7r、cldn6、gprc5d、cxorf61、alk、多聚唾液酸、plac1、globoh、ny-br-1、upk2、havcr1、adrb3、panx3、gpr20、ly6k、or51e2、tarp、wt1、ny-eso-1、lage-la、mage-a1、mage-a3、mage-a6、豆荚蛋白、hpv e6、e7、etv6-aml、精子蛋白17、xage1、tie 2、mad-ct-1、mad-ct-2、fos相关抗原1、p53、p53突变体、psa、存活蛋白和端粒酶、pcta-l/galectin 8、melana/martl、ras突变体、htert、肉瘤易位断点、ml-iap、tmprss2 ets融合基因、na17、pax3、雄激素受体、孕酮受体、cyclin bl、mycn、rhoc、trp-2、cyp1b 1、boris、sart3、pax5、oy-tes 1、lck、akap-4、ssx2、rage-1、人端粒酶逆转录酶、ru1、ru2、肠道羧酸酯酶、mut hsp70-2、cd79a、cd79b、cd72、lair1、fcar、lilra2、cd300lf、clec12a、bst2、emr2、ly75、gpc3、fcrl5、igll1、pd1、pdl1、pdl2、tgfβ、april、nkg2d、nkg2d配体,和/或病原体特异性抗原、生物素化分子、由hiv、hcv、hbv和/或其他病原体表达的分子;和/或新表位或新抗原。优选地,所述第二靶点选自cd7、cd19、cd20、cd22、cd30、cd33、cd38、cd123、cd138、cd171、muc1、afp、folate受体α、cea、psca、psma、her2、egfr、il13ra2、gd2、nkg2d、claudin18.2、ror1、egfrviii、cs1、bcma、gprc5d和间皮素,更优选选自cd19、claudin18.2和bcma。
29、在一个实施方案中,第二靶点是cd19。优选地,靶向cd19的抗体包含如seq id no:21所示的cdr-h1、如seq id no:22所示的cdr-h2、如seq id no:23所示的cdr-h3、如seq idno:24所示的cdr-l1、如seq id no:25所示的cdr-l2、如seq id no:26所示的cdr-l3。优选地,所述靶向cd19的抗体包含与seq id no:27、31、33任一所示的氨基酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的重链可变区序列和与seq id no:28、32、34任一所示的氨基酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的轻链可变区序列。更为优选地,所述靶向cd19的抗体包含与seq id no:29、35-38任一所示的氨基酸序列,或seq id no:30、39-42任一所示的核苷酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%序列同一性的序列。
30、如本文所用,术语“抗体”具有本领域技术人员所理解的最广泛的含义,并且包括单克隆抗体(包含完整抗体)、多克隆抗体、多价抗体、和能够表现期望的生物活性的携带一个或多个cdr序列的抗体片段或合成多肽。本发明所述抗体可为任何种类(例如igg、ige、igm、igd、iga等)或亚类(例如igg1、igg2、igg2a、igg3、igg4、iga1、iga2等)。本发明的抗体也包含重组抗体、人抗体、人源化抗体、驼源抗体、鼠源抗体、嵌合抗体及其抗原结合部分。在一个实施方案中,本发明中所述的抗体选自免疫球蛋白分子、fab、fab'、f(ab')2、fv片段、scfv、二硫键-连接的fv(sdfv)、抗体的重链可变区(vh)或轻链可变区(vl)、由vh和ch1结构域组成的fd片段、线性抗体、单结构域抗体、纳米抗体和所述抗原的天然配体或其功能性片段。
31、术语“功能性变体”或“功能性片段”是指基本上包含亲本的氨基酸序列但与该亲本氨基酸序列相比含有至少一个氨基酸修饰(即取代、缺失或插入)的变体,条件是所述变体保留亲本氨基酸序列的生物活性。在一个实施方案中,所述氨基酸修饰优选是保守型修饰。
32、如本文所用,术语“保守性修饰”是指不会明显影响或改变含有该氨基酸序列的抗体或抗体片段的结合特征的氨基酸修饰。这些保守修饰包括氨基酸取代、添加及缺失。修饰可以通过本领域中已知的标准技术,如定点诱变和pcr介导的诱变而引入本发明的嵌合抗原受体或fc融合多肽中。保守氨基酸取代是氨基酸残基被具有类似侧链的氨基酸残基置换的取代。具有类似侧链的氨基酸残基家族已在本领域中有定义,包括碱性侧链(例如赖氨酸、精氨酸、组氨酸)、酸性侧链(例如天冬氨酸、谷氨酸)、不带电荷极性侧链(例如甘氨酸、天冬酰胺、谷氨酰胺、丝氨酸、苏氨酸、酪氨酸、半胱氨酸)、非极性侧链(例如丙氨酸、缬氨酸、亮氨酸、异亮氨酸、脯氨酸、苯丙氨酸、甲硫氨酸、色氨酸)、β-分支侧链(例如苏氨酸、缬氨酸、异亮氨酸)及芳香族侧链(例如酪氨酸、苯丙氨酸、色氨酸、组氨酸)。保守性修饰可以例如基于极性、电荷、溶解度、疏水性、亲水性和/或所涉及残基的两亲性质的相似性来进行选择。
33、因此,“功能性变体”或“功能性片段”与亲本氨基酸序列具有至少75%,优选至少76%、77%、78%、79%、80%、81%、82%、83%、84%、85%、86%、87%、88%、89%、90%、91%、92%、93%、94%、95%、96%、97%、98%或99%序列同一性,并且保留亲本氨基酸的生物活性,例如结合活性。
34、如本文所用,术语“序列同一性”表示两个(核苷酸或氨基酸)序列在比对中在相同位置处具有相同残基的程度,并且通常表示为百分数。优选地,同一性在被比较的序列的整体长度上确定。因此,具有完全相同序列的两个拷贝具有100%同一性。
35、如本文所用,术语“跨膜结构域”是指能够使嵌合抗原受体在免疫细胞(例如淋巴细胞、nk细胞或nkt细胞)表面上表达,并且引导免疫细胞针对靶细胞的细胞应答的多肽结构。跨膜结构域可以是天然或合成的,也可以源自任何膜结合蛋白或跨膜蛋白。当嵌合受体多肽与靶抗原结合时,跨膜结构域能够进行信号传导。特别适用于本发明中的跨膜结构域可以源自例如tcrα链、tcrβ链、tcrγ链、tcrδ链、cd3ζ亚基、cd3ε亚基、cd3γ亚基、cd3δ亚基、cd45、cd4、cd5、cd8α、cd9、cd16、cd22、cd33、cd28、cd37、cd64、cd80、cd86、cd134、cd137、cd154或它们的任意组合。优选地,所述跨膜结构域选自cd8α、cd4、cd28或cd278的跨膜结构域。更为优选地,所述跨膜结构域为cd8α跨膜结构域,与seq id no:49所示的氨基酸序列,或与seq id no:50或51具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%的序列同一性。
36、在一个实施方案中,本发明的嵌合抗原受体还可以包含位于抗体和跨膜结构域之间的铰链区。如本文所用,术语“铰链区”一般是指作用为连接跨膜结构域至抗原结合区的任何寡肽或多肽。具体地,铰链区用来为抗体提供更大的灵活性和可及性。铰链区可以包含最多达300个氨基酸,优选10至100个氨基酸并且最优选25至50个氨基酸。铰链区可以源自全部或部分的天然分子,如源自全部或部分的cd8、cd4或cd28的胞外区,或源自全部或部分的抗体恒定区。或者,铰链区可以是对应于天然存在的铰链序列的合成序列,或可以是完全合成的铰链序列。优选地,所述铰链区包含cd8α链的铰链区部分,与seq id no:55所示的氨基酸序列,或与seq id no:56或57具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%的序列同一性。
37、如本文所用,术语“胞内信号传导结构域”是指转导效应子功能信号并指导细胞进行指定功能的蛋白质部分,其包含共刺激结构域和/或初级信号传导结构域。胞内信号传导结构域负责在抗原结合区结合抗原以后的细胞内信号传递,从而导致免疫细胞和免疫反应的活化。换言之,胞内信号传导结构域负责活化其中表达嵌合抗原受体的免疫细胞的正常的效应子功能的至少一种。例如,t细胞的效应子功能可以是细胞溶解活性或辅助活性,包括细胞因子的分泌。
38、在一个实施方案中,本发明的嵌合抗原受体包含的初级信号传导结构域可以是t细胞受体和共受体的细胞质序列,其在抗原受体结合以后一同起作用以引发信号传导,以及这些序列的任何衍生物或变体和具有相同或相似功能的任何合成序列。初级信号传导结构域包含两种不同类型的细胞质信号序列:引发抗原依赖性初级活化的那些,以及以不依赖抗原的方式起作用以提供次级或共刺激信号的那些。初级细胞质信号序列可以包含许多免疫受体酪氨酸激活基序(itam)。本发明的初级信号传导结构域包括单不限于源自fcrγ、fcrβ、cd3γ、cd3δ、cd3ε、cd3ζ、cd22、cd79a、cd79b、cd66d或其任意组合。优选地,所述初级信号传导结构域包含cd3ζ的信号传导结构域。更为优选地,所述初级信号传导结构域与seqid no:46所示的氨基酸,或与seq id no:47或48序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%的序列同一性。
39、在一个实施方案中,本发明的嵌合抗原受体还包含一个或多个共刺激结构域。共刺激结构域可以是来自共刺激分子的细胞内功能性信号传导结构域,其可以包含所述共刺激分子的整个细胞内部分,或其功能片段。“共刺激分子”是指在t细胞上与共刺激配体特异性结合,由此介导t细胞的共刺激反应(例如增殖)的同源结合配偶体。共刺激分子包括但不限于1类mhc分子、btla和toll配体受体。本发明的共刺激结构域的非限制性施例包括但不限于源自以下蛋白质的共刺激信号传导结构域:tlr9、tlr10、card11、cd2、cd7、cd8、cd18、cd27、cd28、cd30、cd40、cd54、cd83、cd134(ox40)、cd137(4-1bb)、cd270(hvem)、cd272(btla)、cd276(b7-h3)、cd278(icos)、cd357(gitr)、dap10、dap12、lat、nkg2c、slp76、pd-1、light、trim、zap70或其任意组合。优选地,所述共刺激结构域选自4-1bb、cd28、cd27、ox40、cd278或其任意组合。更为优选地,所述共刺激结构域为4-1bb,与seq id no:43所示的氨基酸序列,或与seq id no:44或45所示具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%的序列同一性。
40、在一些实施方案中,本发明的car还包含信号肽,所述信号肽选自以下蛋白的信号肽:cd8α、igg1、gm-csfrα、igg4或其任意组合。优选地,所述信号肽包含cd8α的信号肽。更为优选地,所述信号肽与seq id no:52所示的氨基酸序列,或与seq id no:53或54所示的核苷酸序列具有至少70%,优选至少80%,更优选至少90%、95%、97%或99%或100%的序列同一性。
41、在一些实施方案中,本发明的car还包含接头,其用于隔开任何本文中所述的结构域/区。例如,接头可位于信号肽与抗体之间、抗体的vh与vl之间、抗体与铰链区之间、铰链区与跨膜结构域之间、侧接共刺激结构域或在共刺激结构域的n-或c-区上、和/或在跨膜结构域与初级信号传导结构域之间。接头可以是长度为约6至约40个氨基酸、或长度为约6至约25个氨基酸的肽。本领域常用的接头序列包括例如seq id no:58或seq id no:59。
42、工程化免疫细胞及其制备方法
43、本发明提供工程化免疫细胞,其包含上述嵌合抗原受体或其编码核酸分子。
44、本发明还提供一种组合物,其包含:(1)表达第一结构单元的第一工程化免疫细胞群,所述第一结构单元包含靶向ccr8的抗体、跨膜结构域和胞内信号传导结构域;和(2)表达第二单元结构的第二工程化免疫细胞群,所述第二单元结构包含靶向第二靶点的抗体、跨膜结构域和胞内信号传导结构域。在该实施方案中,第一工程化免疫细胞群和第二工程化免疫细胞群可以同时或顺次向受试者施用。
45、如本文所用,术语“免疫细胞”是指免疫系统的具有一种或多种效应子功能(例如,细胞毒性细胞杀伤活性、分泌细胞因子、诱导adcc和/或cdc)的任何细胞。例如,免疫细胞可以是t细胞、巨噬细胞、树突状细胞、单核细胞、nk细胞和/或nkt细胞,或者是衍生自干细胞,例如成体干细胞、胚胎干细胞、脐带血干细胞、祖细胞、骨髓干细胞、诱导多能干细胞、全能干细胞或造血干细胞等的免疫细胞。优选地,免疫细胞是t细胞。t细胞可以是任何t细胞,如体外培养的t细胞,例如原代t细胞,或者来自体外培养的t细胞系例如jurkat、supt1等的t细胞,或获得自受试者的t细胞。受试者的实例包括人、狗、猫、小鼠、大鼠及其转基因物种。t细胞可以从多种来源获得,包括外周血单核细胞、骨髓、淋巴结组织、脐血、胸腺组织、来自感染部位的组织、腹水、胸膜积液、脾组织及肿瘤。t细胞也可以被浓缩或纯化。t细胞可以是任何类型的t细胞并且可以处于任何发育阶段,包括但不限于,cd4+cd8+t细胞、cd4+t细胞(例如th1和th2细胞)、cd8+t细胞(例如,细胞毒性t细胞)、cd4-cd8-t细胞、肿瘤浸润细胞、记忆t细胞、幼稚t细胞、γδ-t细胞、αβ-t细胞等。在一个优选的实施方案中,免疫细胞是人t细胞。可以使用本领域技术人员已知的多种技术,如ficoll分离从受试者的血液获得t细胞。在本发明中,免疫细胞被工程化以表达嵌合抗原受体和fc融合多肽。
46、采用本领域已知的常规方法(如通过转导、转染、转化等)可以将编码嵌合抗原受体的核酸分子序列引入免疫细胞,使其表达本发明的嵌合抗原受体。
47、在一个实施方案中,靶向ccr8的第一单元结构与靶向第二靶点的第二单元结构位于同一载体,例如通过2a肽连接使得两个单元结构可以独立表达而互不影响。如本文所用,术语“2a肽”是一种cis-水解酶作用元件(chysels),最初在口蹄疫病毒(fmdv)中发现。2a肽的平均长度为18~22氨基酸。在蛋白翻译时,2a肽可以通过核糖体跳跃从自身最后2个氨基酸c末端断裂。具体地,甘氨酸和脯氨酸之间的肽链结合群在2a位点是受损的,能引发核糖体跳跃而从第2个密码子开始翻译,从而使1个转录单元里的2个蛋白独立表达。这种2a肽介导的剪切广泛存在于真核动物细胞中。利用2a肽较高的剪切效率及其促使上下游基因平衡表达的能力,可以改进异源多聚蛋白(如细胞表面受体、细胞因子、免疫球蛋白等)的表达效率。常见的2a肽包括但不限于p2a、t2a、e2a、f2a等。
48、如本文所用,术语“载体”是用作将(外源)遗传材料转移到免疫细胞中的媒介核酸分子,在免疫细胞中所述核酸分子可以例如复制和/或表达。
49、在一个实施方案中,本发明的载体包括但不限于线性核酸分子(例如dna或rna)、质粒、病毒(例如逆转录病毒、慢病毒、腺病毒、牛痘病毒、劳氏肉瘤病毒(rsv、多瘤病毒和腺相关病毒(aav)等)、噬菌体、噬菌粒、粘粒和人工染色体(包括bac和yac)。载体本身通常是核苷酸序列,通常是包含插入物(转基因)的dna序列和作为载体“骨架”的较大序列。工程化载体通常还包含在免疫细胞中自主复制的起点(如果需要多核苷酸的稳定表达)、选择标记和限制酶切割位点(如多克隆位点,mcs)。
50、在一个实施方案中,本发明的工程化免疫细胞还包含至少一种mhc相关基因表达被抑制或沉默,例如使至少一种mhc基因的表达被抑制或沉默,或使与至少一种mhc基因相互作用或调控其表达的基因的表达被抑制或沉默。
51、在一个实施方案中,mhc相关基因表达被抑制或沉默是指使选自以下的一个或多个基因的表达被抑制或沉默:hla-a、hla-b、hla-c、b2m、hla-dpa、hla-dq、hla-dra、tap1、tap2、lmp2、lmp7、rfx5、rfxap、rfxank、ciita或其任意组合,优选选自hla-a、hla-b、hla-c、b2m、rfx5、rfxap、rfxank、ciita或其任意组合。
52、在一个实施方案中,本发明的工程化免疫细胞还包含至少一种tcr/cd3基因的表达被抑制或沉默。
53、在一个实施方案中,使至少一种tcr/cd3基因表达被抑制或沉默是指使选自以下的一个或多个基因的表达被抑制或沉默:trac、trbc、cd3γ、cd3δ、cd3ε、cd3ζ。
54、在一个实施方案中,除了mhc相关基因和任选的tcr/cd3基因,本发明的工程化免疫细胞还可以包含至少一种选自以下的基因的表达被抑制或沉默:cd52、gr、dck和免疫检查点基因,如pd1、lag3、tim3、ctla4、ppp2ca、ppp2cb、ptpn6、ptpn22、pdcd1、havcr2、btla、cd160、tigit、cd96、crtam、tnfrsf10b、tnfrsf10a、casp8、casp10、casp3、casp6、casp7、fadd、fas、tgfbrii、tgfrbri、smad2、smad3、smad4、smad10、ski、skil、tgif1、il10ra、il10rb、hmox2、il6r、il6st、eif2ak4、csk、pag1、sit、foxp3、prdm1、batf、gucy1a2、gucy1a3、gucy1b2和gucy1b3。
55、在一个实施方案中,所述工程化免疫细胞还表达细胞自杀元件。优选地,所述的细胞自杀元件位于car的n端或c端,所述的自剪切元件包括2a肽或ires肽,优选p2a和t2a。更优选地,所述的细胞自杀元件选自下组:hsv-tk、icasp9、δcd20、mtmpk、δcd19、rqr8、egfrt或其任意组合。
56、抑制基因表达或使基因沉默的方法是本领域技术人员熟知的,包括但不限于例如通过大范围核酸分子酶、锌指核酸分子酶、tale核酸分子酶或crispr系统中的cas酶介导dna断裂、或通过反义寡核苷酸、rnai、shrna等技术使基因失活。
57、药物组合物和试剂盒
58、本发明还提供一种药物组合物,其包含本发明所述的工程化免疫细胞作为活性剂,和一种或多种药学上可接受的赋型剂。因此,本发明还涵盖所述工程化免疫细胞在制备药物组合物或药物中的用途。
59、如本文所用,术语“药学上可接受的赋型剂”是指在药理学和/或生理学上与受试者和活性成分相容(即,能够引发所需的治疗效果而不会引起任何不希望的局部或全身作用)的载体和/或赋形剂。药学上可接受的赋型剂的实例包括但不限于填充剂、粘合剂、崩解剂、包衣剂、吸附剂、抗粘附剂、助流剂、抗氧化剂、调味剂、着色剂、甜味剂、溶剂、共溶剂、缓冲剂、螯合剂、表面活性剂、稀释剂、润湿剂、防腐剂、乳化剂、包覆剂、等渗剂、吸收延迟剂、稳定剂和张力调节剂。本领域技术人员已知选择合适的赋型剂以制备本发明期望的药物组合物。用于本发明的药物组合物中的示例性赋型剂包括盐水、缓冲盐水、葡萄糖和水。通常,合适的赋形剂的选择尤其取决于所使用的活性剂、待治疗的疾病和药物组合物的期望剂型。
60、根据本发明的药物组合物可适用于多种途径施用。通常,通过胃肠外完成施用。胃肠外递送方法包括局部、动脉内、肌内、皮下、髓内、鞘内、心室内、静脉内、腹膜内、子宫内、阴道内、舌下或鼻内施用。
61、根据本发明的药物组合物也可以制备成各种形式,如固态、液态、气态或冻干形式,特别可以是软膏、乳膏、透皮贴剂、凝胶、粉末、片剂、溶液、气雾剂、颗粒、丸剂、混悬剂、乳剂、胶囊、糖浆、酏剂、浸膏剂、酊剂或流浸膏提取物的形式,或者是特别适用于所需施用方法的形式。本发明已知的用于生产药物的过程可包括例如常规混合、溶解、制粒、制糖衣、研磨、乳化、包封、包埋或冻干过程。包含例如本文所述的免疫细胞的药物组合物通常以溶液形式提供,并且优选包含药学上可接受的缓冲剂。
62、根据本发明的药物组合物还可以与一种或多种适用于治疗和/或预防待治疗疾病的其它药剂组合施用。适用于组合的药剂的优选实例包括已知的抗癌药物,比如顺铂、美登素衍生物、雷查霉素(rachelmycin)、卡里奇霉素(calicheamicin)、多西紫杉醇、依托泊苷、吉西他滨、异环磷酰胺、伊立替康、美法仑、米托蒽醌、sorfimer卟啉钠ii(sorfimersodiumphotofrin ii)、替莫唑胺、拓扑替康、葡萄糖醛酸曲美沙特(trimetreateglucuronate)、奥利斯他汀e(auristatin e)、长春新碱和阿霉素;肽细胞毒素,比如蓖麻毒素、白喉毒素、假单胞菌细菌外毒素a、dna酶和rna酶;放射性核素,比如碘131、铼186、铟111、铱90、铋210和213、锕225和砹213;前药,比如抗体定向的酶前药;免疫刺激剂,比如il-2,趋化因子比如il-8、血小板因子4、黑色素瘤生长刺激蛋白等;抗体或其片段,比如抗cd3抗体或其片段,补体活化剂,异种蛋白结构域,同种蛋白结构域,病毒/细菌蛋白结构域和病毒/细菌肽。
63、用途
64、本发明还提供上述嵌合抗原受体或工程化免疫细胞或药物组合物在制备治疗/预防/诊断癌症、感染或自身免疫性疾病药物中的用途。本发明还提供上述嵌合抗原受体或工程化免疫细胞或药物组合物在治疗/缓解gvhd或hvgd中的用途。
65、在一个实施方案中,所述疾病是与ccr8或第二靶点表达有关的癌症。例如,所述癌症包括但不限于:脑神经胶质瘤、胚细胞瘤、肉瘤、白血病、基底细胞癌、胆道癌、膀胱癌、骨癌、脑和cns癌症、乳腺癌、腹膜癌、宫颈癌、绒毛膜癌、结肠和直肠癌、结缔组织癌症、消化系统的癌症、子宫内膜癌、食管癌、眼癌、头颈癌、胃癌(包括胃肠癌)、胶质母细胞瘤(gbm)、肝癌、肝细胞瘤、上皮内肿瘤、肾癌、喉癌、肝肿瘤、肺癌(例如小细胞肺癌、非小细胞肺癌、腺状肺癌和鳞状肺癌)、淋巴瘤(包括霍奇金淋巴瘤和非霍奇金淋巴瘤)、黑色素瘤、骨髓瘤、神经母细胞瘤、口腔癌(例如唇、舌、口和咽)、卵巢癌、胰腺癌、前列腺癌、视网膜母细胞瘤、横纹肌肉瘤、直肠癌、呼吸系统的癌症、唾液腺癌、皮肤癌、鳞状细胞癌、胃癌、睾丸癌、甲状腺癌、子宫或子宫内膜癌、泌尿系统的恶性肿瘤、外阴癌以及其它癌和肉瘤、以及b细胞淋巴瘤(包括低级/滤泡性非霍奇金淋巴瘤(nhl)、小淋巴细胞性(sl)nhl、中间级/滤泡性nhl、中间级扩散性nhl、高级成免疫细胞性nhl、高级成淋巴细胞性nhl、高级小型非裂化细胞性nhl、大肿块病nhl)、套细胞淋巴瘤、aids相关淋巴瘤、以及waldenstrom巨球蛋白血症、慢性淋巴细胞白血病(cll)、急性淋巴细胞白血病(all)、b细胞急性淋巴细胞白血病(b-all)、t细胞急性淋巴细胞白血病(t-all)、b细胞幼淋巴细胞白血病、母细胞性浆细胞样树突状细胞瘤、伯基特氏淋巴瘤、弥散性大b细胞淋巴瘤、滤泡性淋巴瘤、慢性骨髓性白血病(cml)、恶性淋巴组织增生疾病、malt淋巴瘤、毛细胞白血病、边缘区淋巴瘤、多发性骨髓瘤、骨髓发育不良、浆母细胞性淋巴瘤、白血病前期、浆细胞样树突状细胞瘤、以及移植后淋巴细胞增生性紊乱(ptld);以及其他与靶标表达有关的疾病。优选地,可以用本发明的工程化免疫细胞或药物组合物治疗的疾病选自:白血病、淋巴瘤、多发性骨髓瘤、脑神经胶质瘤、胰腺癌、胃癌等。
66、下面将参考附图并结合实施例来详细说明本发明。需要说明的是,本领域的技术人员应该理解本发明的附图及其实施例仅仅是为了举例,并不能对本发明构成任何限制。在不矛盾的情况下,本技术中的实施例及实施例中的特征可以相互组合。
- 还没有人留言评论。精彩留言会获得点赞!