含喹啉或异喹啉的异羟肟酸类化合物及其制备与应用
:
1.本发明属于医药技术领域,具体涉及含喹啉或异喹啉的异羟肟酸类化合物及其制备与应用,具体包括作为组蛋白去乙酰化酶抑制剂用于预防和/或治疗与组蛋白去乙酰化酶相关的疾病的应用。
背景技术:
2.癌症,由于其高发病率和高死亡率已成为全球主要的死亡原因,是人类最可怕的杀手之一。
3.在癌症研究的新兴领域中,表观遗传改变在肿瘤的发生、发展和侵袭转移中具有不可或缺的功能。组蛋白翻译后修饰是表观遗传调控的关键过程,大量研究表明,组蛋白乙酰化水平的异常降低与癌症及多种免疫类疾病密切相关。组蛋白去乙酰化酶hdacs是调节体内组蛋白以及非组蛋白乙酰化和去乙酰化平衡的关键酶之一,在多种癌症中均发现hdacs的异常表达。由此可见,hdacs已成为癌症研究的一个重要靶点。
4.hdacs介导的组蛋白去乙酰化在调节细胞分化、增殖和存活过程中发挥重要作用。由 hdacs突变或异常表达引起的组蛋白过度去乙酰化与肿瘤的增殖、侵袭和迁移密切相关。大量研究表明,不同类型的癌症中均观察到hdacs的过度表达,而且大多数情况下与不良预后密切相关。相关研究表明,hdacs抑制剂可通过诱导肿瘤细胞凋亡、抑制肿瘤组织微血管形成等发挥其抗肿瘤作用,因而被开发作为一种新型的抗肿瘤药物。
技术实现要素:
5.本发明的目的是克服上述现有技术存在的不足,提供一类含喹啉或异喹啉的异羟肟酸类化合物及其制备与应用,以及该类化合物作为组蛋白去乙酰化酶抑制剂在预防和/或治疗肿瘤中的应用。
6.为实现上述目的,本发明采用以下技术方案:
7.本发明提供了如通式i所示的含喹啉或异喹啉的异羟肟酸类化合物及其药学上可接受的盐或水合物。
[0008][0009]
其中:
[0010]
x为n或ch,y为ch或n;其中,当x为n时,y为ch;当x为ch,y为n;
[0011]
w为羰基或(c
3-c5)α,β-不饱和羰基;
[0012]
a环为芳基或杂芳基,其中芳基或杂芳基各自独立地任选被一个或多个r取代,r为氢、 (c
1-c6)烷基、氰基、卤素、卤代(c
1-c6)烷基、羟基、巯基或烷氧基;
[0013]
其中,所述芳基是6-10元芳基;所述杂芳基为五元或六元杂芳基,其中含有1-3个
n、 o或s的杂原子,其余环原子为c;所述芳基为苯基;所述五元杂芳基为吡咯基、呋喃基、噻吩基、咪唑基、吡唑基、噁唑基、异噁唑基、噻唑基或异噻唑基;所述六元杂芳基为吡啶基、嘧啶基、吡嗪基或哒嗪基;
[0014]
本发明优选如下结构的化合物及其盐和水合物:
[0015]
x是n,则y是ch;或x是ch,则y是n;
[0016]
w是羰基或(c
3-c5)α,β-不饱和羰基;
[0017]
a环是芳基或杂芳基;
[0018]
其中,所述芳基是苯基;所述五元杂芳基是吡咯基、呋喃基、噻吩基、咪唑基、吡唑基、噁唑基、异噁唑基、噻唑基、异噻唑基;所述六元杂芳基是吡啶基、嘧啶基、吡嗪基、哒嗪基。
[0019]
本发明优选如下结构的化合物及其盐和水合物:
[0020]
x是n,则y是ch;或x是ch,则y是n;
[0021]
w是羰基或(c
3-c5)α,β-不饱和羰基;
[0022]
a环是芳基或杂芳基;
[0023]
其中,所述芳基是苯基;所述杂芳基是吡啶基、吡嗪基;
[0024]
进一步地,a环为苯基时,苯基为
[0025]
进一步地,a环为吡啶基时,吡啶基为
[0026]
进一步地,a环为吡嗪基时,吡嗪基为
[0027]
本发明优选如下结构的化合物及其盐和水合物:
[0028]
x是n,则y是ch;或x是ch,则y是n;
[0029]
w是羰基或(c
3-c5)α,β-不饱和羰基;
[0030]
a环是芳基;
[0031]
其中,所述芳基是苯基;
[0032]
进一步地,a环为苯基时,苯基为
[0033]
本发明优选如下结构的化合物及其盐和水合物:
[0034]
x是n,则y是ch;或x是ch,则y是n;
[0035]
w是-ch=ch-co-;
[0036]
a环是芳基;
[0037]
其中,所述芳基是苯基;
[0038]
进一步地,a环为苯基时,苯基为
[0039]
具体的,本发明优选如下化合物:
[0040]
(e)-n-羟基-3-(4-(n-(喹啉-2-基)磺胺基)苯基)丙烯酰胺(i-1);
[0041]
(e)-n-羟基-3-(4-(n-(喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-2);
[0042]
(e)-n-羟基-3-(4-(n-(喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-3);
[0043]
(e)-n-羟基-3-(4-(n-(喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-4);
[0044]
(e)-n-羟基-3-(4-(n-(喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-5);
[0045]
(e)-n-羟基-3-(4-(n-(喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-6);
[0046]
(e)-n-羟基-3-(4-(n-(喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-7);
[0047]
(e)-n-羟基-3-(4-(n-(异喹啉-1-基)磺胺基)苯基)丙烯酰胺(i-8);
[0048]
(e)-n-羟基-3-(4-(n-(异喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-9);
[0049]
(e)-n-羟基-3-(4-(n-(异喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-10);
[0050]
(e)-n-羟基-3-(4-(n-(异喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-11);
[0051]
(e)-n-羟基-3-(4-(n-(异喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-12);
[0052]
(e)-n-羟基-3-(4-(n-(异喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-13);
[0053]
(e)-n-羟基-3-(4-(n-(异喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-14);
[0054]
(e)-n-羟基-3-(3-(n-(喹啉-2-基)磺胺基)苯基)丙烯酰胺(i-15);
[0055]
(e)-n-羟基-3-(3-(n-(喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-16);
[0056]
(e)-n-羟基-3-(3-(n-(喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-17);
[0057]
(e)-n-羟基-3-(3-(n-(喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-18);
[0058]
(e)-n-羟基-3-(3-(n-(喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-19);
[0059]
(e)-n-羟基-3-(3-(n-(喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-20);
[0060]
(e)-n-羟基-3-(3-(n-(喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-21);
[0061]
(e)-n-羟基-3-(3-(n-(异喹啉-1-基)磺胺基)苯基)丙烯酰胺(i-22);
[0062]
(e)-n-羟基-3-(3-(n-(异喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-23);
[0063]
(e)-n-羟基-3-(3-(n-(异喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-24);
[0064]
(e)-n-羟基-3-(3-(n-(异喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-25);
[0065]
(e)-n-羟基-3-(3-(n-(异喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-26);
[0066]
(e)-n-羟基-3-(3-(n-(异喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-27);
[0067]
(e)-n-羟基-3-(3-(n-(异喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-28);
[0068]
或其盐及水合物;
[0069]
除非另外指出,本发明所用的术语“卤素”是指氟、氯、溴或碘,优选氟、氯或溴;“烷基”是指直链或支链的烷基。
[0070]
根据本发明,所述药学上可接受的盐可以为无机酸盐或有机酸盐;优选地,所述无机酸盐选自下述任意一种无机酸形成的盐:盐酸、氢溴酸、硫酸或磷酸;优选地,所述有机酸盐选自下述任意一种有机酸形成的盐:乙酸、丙酸、三氟乙酸、乙二酸、丙二酸、丁二酸、戊二酸、柠檬酸、水杨酸、酒石酸或对甲苯磺酸。
[0071]
本发明还包括本发明的化合物的前药。药学上可接受的前药是指前药自身可能具有较弱的活性或甚至没有活性,但是在给药后,在生理条件下(例如通过代谢、溶剂分解或另外的形式)可以转化为-cooh、-nh2、-oh等的官能团,从而形成本发明化合物的化合物。
[0072]
本发明包括药物组合物,该组合物含有作为活性成分的上述喹啉或异喹啉结构的异羟肟酸类化合物和可药用辅料。所述可药用辅料包括药学领域常规的稀释剂、赋形剂、填充剂、粘合剂、湿润剂、崩解剂、吸收促进剂、表面活性剂、吸附载体、润滑剂等。
[0073]
本发明的药物组合物可配制成若干种剂型,如注射剂、片剂、粉剂、颗粒剂、胶囊、口服液、膏剂、霜剂等。上述各种剂型的药物均可以按照药学领域的常规方法制备。
[0074]
本发明的化合物和包含本发明的化合物的药物组合物可以配制为适于静脉内、口服、直肠、胃肠外、鼻内或经皮施用的形式,或适于通过吸入施用或通过栓剂施用的形式。口服和静脉内给药是优选。
[0075]
本发明的含喹啉或异喹啉的异羟肟酸类化合物及其药物组合物作为组蛋白去乙酰化酶抑制剂用于与组蛋白去乙酰化酶异常表达相关的疾病在预防和/或治疗中的应用,所述的疾病如各种癌症,包括肝癌、结肠癌、胰腺癌、肺癌、胃癌、乳腺癌和卵巢癌等。
[0076]
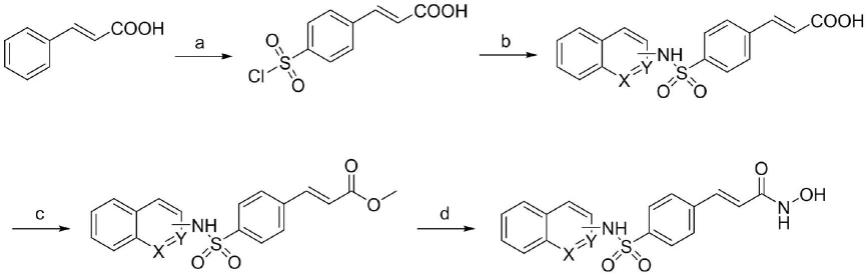
所述的含喹啉或异喹啉的异羟肟酸类化合物的制备,采用以下两种路线中的一种:
[0077]
路线一:
[0078][0079]
各取代基如
技术实现要素:
部分所定义,试剂和条件:a.hso3cl,12h;b.rnh2,ch2cl2,pyridine, 1h;c.ch3oh,h2so4,4h;d.nh2oh,1n naoh,ch3oh,1h.
[0080]
路线二:
[0081][0082]
各取代基如发明内容部分所定义,试剂和条件:a.rnh2,ch2cl2,pyridine,2h;b.methyl acrylate,pd(oac)2,pot,et3n,ch3cn,60℃,12h;c.nh2oh,1n naoh,ch3oh,1h.
[0083]
本发明的有益效果:
[0084]
本发明的含喹啉或异喹啉的异羟肟酸类化合物均具有良好的抗肿瘤细胞增殖活性,且制备方法操作简单、条件温和。
具体实施方式:
[0085]
下面结合实施例对本发明作进一步的详细说明。
[0086]
实施例1:(e)-n-羟基-3-(4-(n-(喹啉-2-基)磺胺基)苯基)丙烯酰胺(i-1)的制备
[0087]
化合物(i-1)结构式
[0088][0089]
步骤a:(e)-3-(4-(氯磺酰基)苯基)丙烯酸的制备
[0090][0091]
在0℃,搅拌条件下,将肉桂酸(1g,6.76mmol)缓慢分批加入到氯磺酸(7.84g,67.6mmol) 中,继续搅拌30min后缓慢恢复至室温,再继续搅拌12h。反应结束后,将反应液缓慢滴加至冰水中,抽滤后经真空干燥得到黄色固体,将固体加入到1,4-二氧六环中经重结晶得 (e)-3-(4-(氯磺酰基)苯基)丙烯酸白色结晶(0.55g,产率33%)。
[0092]
步骤b:(e)-3-(4-(n-(喹啉-2-基)磺胺酰基)苯基)丙烯酸的制备
[0093][0094]
在0℃,搅拌条件下,向2-氨基喹啉(0.49g,3.4mmol)二氯甲烷(50ml)溶液中依次添加吡啶(1ml)和(e)-3-(4-(氯磺酰基)苯基)丙烯酸(1g,4.06mmol)。加毕后,反应液在0℃条件下继续搅拌1h。反应结束后,减压蒸除溶剂,残留物用硅胶层析柱色谱分离纯化,得(e)-3-(4-(n-(喹啉-2-基)磺胺酰基)苯基)丙烯酸淡黄色固体(0.6g,产率50%)。
[0095]
步骤c:甲基(e)-3-(4-(n-(喹啉-2-基)磺胺酰基)苯基)丙烯酸酯的制备
[0096][0097]
向(e)-3-(4-(n-(喹啉-2-基)磺胺酰基)苯基)丙烯酸(0.6g,1.7mmol)的甲醇(40ml)溶液中加入 1滴浓h2so4。加毕后,将反应液加热回流4h。反应结束后,乙酸乙酯(50ml
×
3)萃取,合并有机相,有机相以饱和食盐水(20ml)洗涤3次,无水硫酸钠干燥,过滤,浓缩。粗产品用硅胶层析柱色谱分离纯化,得甲基(e)-3-(4-(n-(喹啉-2-基)磺胺酰基)苯基)丙烯酸酯白色固体 (0.5g,产率80%)。
[0098]
步骤d:(e)-n-羟基-3-(4-(n-(喹啉-2-基)磺胺基)苯基)丙烯酰胺的制备
[0099][0100]
在0℃,搅拌条件下,向甲基(e)-3-(4-(n-(喹啉-2-基)磺胺酰基)苯基)丙烯酸酯
(0.5g, 1.36mmol)的甲醇(20ml)溶液中缓慢滴加1mol/l的naoh溶液(3ml),搅拌10分钟后,继续向其中缓慢滴加nh2oh溶液(3ml),滴加完毕后,缓慢恢复至室温并继续搅拌1h。反应结束后,减压蒸除溶剂,向其中加入水(20ml),用2mol/l盐酸调节ph至中性,有固体析出,抽滤,经真空干燥后得(e)-n-羟基-3-(4-(n-(喹啉-2-基)磺胺基)苯基)丙烯酰胺(i-1)白色固体(0.36g,产率73%)。mp:171.6-173.3℃,1h-nmr(600mhz,dmso-d6)δ8.09(d,j=9.0hz,1h),7.91(d,j =8.3hz,2h),7.74(d,j=7.8hz,1h),7.65(d,j=8.3hz,2h),7.59(t,j=7.4hz,1h),7.52(d,j =8.3hz,1h),7.45(d,j=15.8hz,1h),7.29(t,j=7.4hz,2h),6.53(d,j=15.8hz,1h). esi-ms m/z:392.08[m+na]
+
.
[0101]
按照实施例1的制备方法,选择适当的原料,制得实施例2-实施例14的化合物。
[0102]
实施例2:(e)-n-羟基-3-(4-(n-(喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-2)的制备
[0103]
化合物(i-2)结构式
[0104][0105]
(e)-n-羟基-3-(4-(n-(喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-2)淡黄色固体,产率85%。mp: 185.7-187.9℃,1h-nmr(600mhz,dmso-d6)δ10.82(s,1h),9.10(s,1h),8.55(d,j=2.5hz, 1h),7.83(dd,j=27.4,8.2hz,6h),7.66(d,j=8.4hz,2h),7.55(t,j=7.2hz,1h),7.49(t,j= 7.4hz,1h),7.42(d,j=15.8hz,1h),6.50(d,j=15.8hz,1h).esi-ms m/z:370.11[m+h]
+
.
[0106]
实施例3:(e)-n-羟基-3-(4-(n-(喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-3)的制备
[0107]
化合物(i-3)结构式
[0108][0109]
(e)-n-羟基-3-(4-(n-(喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-3)白色固体,产率79%。mp: 228.9-230.1℃,1h-nmr(600mhz,dmso-d6)δ8.39(d,j=8.1hz,1h),8.18(d,j=6.3hz,1h), 7.83(d,j=8.3hz,2h),7.65(dd,j=8.9,1.4hz,2h),7.61(d,j=8.2hz,2h),7.41(ddd,j=11.8, 8.6,8.1hz,2h),6.98(d,j=6.3hz,1h),6.49(d,j=15.8hz,1h).esi-ms m/z:370.11[m+h]
+
.
[0110]
实施例4:(e)-n-羟基-3-(4-(n-(喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-4)的制备
[0111]
化合物(i-4)结构式
[0112]
[0113]
(e)-n-羟基-3-(4-(n-(喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-4)淡黄色固体,产率77%。mp: 199.0-201.7℃,1h-nmr(600mhz,dmso-d6)δ10.84(s,1h),10.45(s,1h),9.12(s,1h),8.85 (dd,j=4.1,1.5hz,1h),8.40(d,j=8.5hz,1h),7.85(d,j=8.5hz,1h),7.70
–
7.61(m,5h), 7.47
–
7.41(m,2h),7.20(d,j=7.4hz,1h),6.52(d,j=15.8hz,1h).esi-ms m/z:370.11[m+ h]
+
.
[0114]
实施例5:(e)-n-羟基-3-(4-(n-(喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-5)的制备
[0115]
化合物(i-5)结构式
[0116][0117]
(e)-n-羟基-3-(4-(n-(喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-5)白色固体,产率70%。mp: 177.9-179.6℃,1h-nmr(600mhz,dmso-d6)δ10.58(s,1h),8.60(d,j=3.0hz,1h),8.05(d,j =8.2hz,1h),7.79(d,j=8.3hz,2h),7.74(d,j=8.8hz,1h),7.60(d,j=8.2hz,2h),7.43
–ꢀ
7.36(m,3h),7.32(dd,j=8.3,4.1hz,1h),6.48(d,j=15.8hz,1h).esi-ms m/z:370.11[m+ h]
+
.
[0118]
实施例6:(e)-n-羟基-3-(4-(n-(喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-6)的制备
[0119]
化合物(i-6)结构式
[0120][0121]
(e)-n-羟基-3-(4-(n-(喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-6)白色固体,产率73%。mp: 182.2-185.3℃,1h-nmr(600mhz,dmso-d6)δ8.76(dd,j=4.1,1.4hz,1h),8.20(d,j=7.9hz, 1h),7.83(t,j=9.8hz,3h),7.69(d,j=8.3hz,2h),7.62(d,j=0.8hz,1h),7.41(d,j=15.8hz, 1h),7.38(dd,j=8.8,1.9hz,1h),7.35(dd,j=8.2,4.2hz,1h),6.52(d,j=15.8hz,1h). esi-ms m/z:370.10[m+h]
+
.
[0122]
实施例7:(e)-n-羟基-3-(4-(n-(喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-7)的制备
[0123]
化合物(i-7)结构式
[0124][0125]
(e)-n-羟基-3-(4-(n-(喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-7)淡黄色固体,产率85%。mp: 158.2-160.6℃,1h-nmr(600mhz,dmso-d6)δ10.20(s,1h),9.36(s,1h),8.81(d,j=2.3hz, 1h),8.27(d,j=8.1hz,1h),7.89(d,j=5.1hz,2h),7.73
–
7.34(m,8h),6.49(d,j=15.8hz, 1h).esi-ms m/z:370.10[m+h]
+
.
[0126]
实施例8:(e)-n-羟基-3-(4-(n-(异喹啉-1-基)磺胺基)苯基)丙烯酰胺(i-8)的制备
[0127]
化合物(i-8)结构式
[0128][0129]
(e)-n-羟基-3-(4-(n-(异喹啉-1-基)磺胺基)苯基)丙烯酰胺(i-8)淡黄色固体,产率70%。mp: 215.5-217.7℃,1h-nmr(600mhz,dmso-d6)δ8.38(d,j=8.2hz,1h),7.95(d,j=8.3hz,2h), 7.72(t,j=8.5hz,2h),7.65(d,j=8.1hz,2h),7.59(d,j=6.7hz,1h),7.56
–
7.50(m,1h),7.45 (d,j=15.8hz,1h),6.97(d,j=6.0hz,1h),6.52(d,j=15.8hz,1h).esi-ms m/z:370.11[m+ h]
+
.
[0130]
实施例9:(e)-n-羟基-3-(4-(n-(异喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-9)的制备
[0131]
化合物(i-9)结构式
[0132][0133]
(e)-n-羟基-3-(4-(n-(异喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-9)淡黄色固体,产率71%。mp: 225.4-228.1℃,1h-nmr(600mhz,dmso-d6)δ8.91(s,1h),7.88(t,j=7.9hz,3h),7.69(d,j= 7.9hz,1h),7.63(d,j=8.2hz,2h),7.55(t,j=7.5hz,1h),7.41(d,j=15.8hz,1h),7.36
–ꢀ
7.32(m,1h),7.29(s,1h),6.52(d,j=15.8hz,1h). esi-ms m/z:370.14[m+h]
+
.
[0134]
实施例10:(e)-n-羟基-3-(4-(n-(异喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-10)的制备
[0135]
化合物(i-10)结构式
[0136][0137]
(e)-n-羟基-3-(4-(n-(异喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-10)淡黄色固体,产率83%。 mp:110.1-112.2℃,1h-nmr(600mhz,dmso-d6)δ10.87(s,1h),8.98(s,1h),8.08(d,j=10.0 hz,1h),8.03(d,j=7.9hz,1h),7.72
–
7.60(m,7h),7.43(d,j=15.7hz,1h),6.53(d,j=15.8 hz,1h).esi-ms m/z:370.11[m+h]
+
.
[0138]
实施例11:(e)-n-羟基-3-(4-(n-(异喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-11)的制备
[0139]
化合物(i-11)结构式
[0140][0141]
(e)-n-羟基-3-(4-(n-(异喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-11)白色固体,产率80%。mp: 170.7-172.8℃,1h-nmr(600mhz,dmso-d6)δ10.81(s,1h),9.12(s,1h),8.33(d,j=5.8hz, 1h),8.00(d,j=5.8hz,1h),7.70(d,j=8.2hz,3h),7.58(d,j=8.2hz,3h),7.40(dd,j=15.0, 7.0hz,2h),7.30(d,j=7.5hz,1h),6.48(d,j=15.8hz,1h).esi-ms m/z:370.10[m+h]
+
.
[0142]
实施例12:(e)-n-羟基-3-(4-(n-(异喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-12)的制备
[0143]
化合物(i-12)结构式
[0144][0145]
(e)-n-羟基-3-(4-(n-(异喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-12)淡黄色固体,产率77%。 mp:166.0-168.2℃,1h-nmr(600mhz,dmso-d6)δ10.84(s,1h),9.03(s,1h),8.30(d,j=5.8 hz,1h),7.89(d,j=8.8hz,1h),7.85(d,j=8.4hz,2h),7.66(d,j=8.3hz,2h),7.58(d,j=5.8 hz,1h),7.46(s,1h),7.41(d,j=15.8hz,1h),7.35(dd,j=8.8,1.8hz,1h),6.52(d,j=15.8hz, 1h).esi-ms m/z:370.11[m+h]
+
.
[0146]
实施例13:(e)-n-羟基-3-(4-(n-(异喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-13)的制备
[0147]
化合物(i-13)结构式
[0148][0149]
(e)-n-羟基-3-(4-(n-(异喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-13)淡黄色固体,产率79%。 mp:171.2-173.2℃,1h-nmr(600mhz,dmso-d6)δ10.84(s,1h),9.15(s,1h),8.34(d,j=5.6 hz,1h),7.82(t,j=7.6hz,3h),7.71(s,1h),7.68
–
7.65(m,3h),7.49(dd,j=8.8,1.9hz,1h), 7.41(d,j=15.8hz,1h),6.51(d,j=15.8hz,1h).esi-ms m/z:370.12[m+h]
+
.
[0150]
实施例14:(e)-n-羟基-3-(4-(n-(异喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-14)的制备
[0151]
化合物(i-14)结构式
[0152][0153]
(e)-n-羟基-3-(4-(n-(异喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-14)淡黄色固体,产率75%。 mp:175.2-177.9℃,1h-nmr(600mhz,dmso-d6)δ10.85(s,1h),9.37(s,1h),8.43(d,j=5.6 hz,1h),7.77
–
7.60(m,7h),7.44(d,j=15.8hz,1h),7.27(d,j=7.5hz,1h),6.52(d,j=15.9 hz,1h).esi-ms m/z:370.11[m+h]
+
.
[0154]
实施例15:(e)-n-羟基-3-(3-(n-(喹啉-2-基)磺胺基)苯基)丙烯酰胺(i-15)的制备
[0155]
化合物(i-15)结构式
[0156][0157]
步骤a:3-溴-n-(喹啉-2-基)苯磺酰胺的制备
[0158][0159]
在0℃,搅拌条件下,向2-氨基喹啉(0.47g,3.26mmol)的二氯甲烷(50ml)溶液中添加吡啶 (1ml)和3-溴苯磺酰氯(1g,3.92mmol)。加毕后,反应液在0℃下继续搅拌2h。反应结束后,减压蒸除溶剂,残留物用硅胶层析柱色谱分离纯化,得3-溴-n-(喹啉-2-基)苯磺酰胺淡黄色固体(0.91g,产率77%)。
[0160]
步骤b:甲基(e)-3-(3-(n-(喹啉-2-基)磺胺酰基)苯基)丙烯酸酯的制备
[0161][0162]
室温下,向乙腈(50ml)中依次加入3-溴-n-(喹啉-2-基)苯磺酰胺(1g,2.76mmol),丙烯酸甲酯(0.28g,3.31mmol),醋酸钯(6.20mg,0.0276mmol),三(邻甲基苯基)磷(25.20mg,0.0828mmol) 和三乙胺(6.18mg,5.52mmol)。在n2保护下,将该反应液加热至60℃反应12h。反应结束后,乙酸乙酯(40ml
×
3)萃取,合并有机相,有机相以饱和食盐水(20ml)洗涤3次,无水硫酸钠干燥,过滤,浓缩。粗产品用硅胶层析柱色谱分离纯化,得甲基(e)-3-(3-(n-(喹啉-2-基)磺胺酰基)苯基)丙烯酸酯白色固体(0.89g,产率88%)。
[0163]
步骤c:(e)-n-羟基-3-(3-(n-(喹啉-2-基)磺胺基)苯基)丙烯酰胺的制备
[0164][0165]
在0℃,搅拌条件下,向甲基(e)-3-(3-(n-(喹啉-2-基)磺胺酰基)苯基)丙烯酸酯
(0.5g, 1.36mmol)的甲醇(20ml)溶液中缓慢滴加1mol/l的naoh溶液(3ml)。搅拌10分钟后,继续向其中缓慢滴加nh2oh溶液(3ml),滴加完毕后,缓慢恢复至室温并继续搅拌1h。反应结束后,减压蒸除溶剂,向其中加入水(20ml),用2mol/l盐酸调节ph至中性,有固体析出,抽滤,经真空干燥后得(e)-n-羟基-3-(3-(n-(喹啉-2-基)磺胺基)苯基)丙烯酰胺(i-15)白色固体(0.42g,产率85%)。mp:197.2-199.4℃,1h-nmr(600mhz,dmso-d6)δ8.11(s,1h),8.08(d,j=6.5hz, 1h),7.87(d,j=7.8hz,1h),7.72(d,j=7.7hz,1h),7.66(d,j=7.3hz,1h),7.58(t,j=7.5hz, 1h),7.50(dd,j=16.6,9.0hz,3h),7.33
–
7.23(m,2h),6.59(d,j=15.8hz,1h).esi-ms m/z: 370.11[m+h]
+
.
[0166]
按照实施例15的制备方法,选择适当的原料,制得实施例16-实施例20、实施例22-实施例28的化合物。
[0167]
实施例16:(e)-n-羟基-3-(3-(n-(喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-16)的制备
[0168]
化合物(i-16)结构式
[0169][0170]
(e)-n-羟基-3-(3-(n-(喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-16)白色固体,产率83%。mp: 182.7-184.4℃,1h-nmr(600mhz,dmso-d6)δ10.81(s,1h),9.13(s,1h),8.54(d,j=2.4hz, 1h),8.01(s,1h),7.87
–
7.73(m,4h),7.69(d,j=7.7hz,1h),7.55
–
7.42(m,4h),6.52(d,j= 15.8hz,1h).esi-ms m/z:370.10[m+h]
+
.
[0171]
实施例17:(e)-n-羟基-3-(3-(n-(喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-17)的制备
[0172]
化合物(i-17)结构式
[0173][0174]
(e)-n-羟基-3-(3-(n-(喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-17)淡黄色固体,产率79%。mp: 203.1-205.6℃,1h-nmr(600mhz,dmso-d6)δ8.39(d,j=8.1hz,1h),8.18(d,j=6.2hz,1h), 8.00(s,1h),7.79(d,j=6.3hz,1h),7.66(d,j=8.1hz,1h),7.64
–
7.59(m,2h),7.49
–
7.43(m, 2h),7.38(t,j=7.3hz,1h),6.96(d,j=6.1hz,1h),6.54(d,j=15.8hz,1h).esi-ms m/z: 370.10[m+h]
+
.
[0175]
实施例18:(e)-n-羟基-3-(3-(n-(喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-18)的制备
[0176]
化合物(i-18)结构式
[0177]
[0178]
(e)-n-羟基-3-(3-(n-(喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-18)淡黄色固体,产率66%。mp: 222.8-224.6℃,1h-nmr(600mhz,dmso-d6)δ10.79(s,1h),10.27(s,1h),9.11(s,1h),8.85 (dd,j=4.0,1.2hz,1h),8.42(d,j=8.5hz,1h),7.84(d,j=12.6hz,2h),7.76(d,j=7.7hz, 1h),7.62(dd,j=15.2,7.3hz,2h),7.52(t,j=7.8hz,1h),7.48
–
7.40(m,2h),7.18(d,j=7.5 hz,1h),6.45(d,j=15.8hz,1h).esi-ms m/z:370.10[m+h]
+
.
[0179]
实施例19:(e)-n-羟基-3-(3-(n-(喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-19)的制备
[0180]
化合物(i-19)结构式
[0181][0182]
(e)-n-羟基-3-(3-(n-(喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-19)淡黄色固体,产率61%。mp: 186.3-189.4℃,1h-nmr(600mhz,dmso-d6)δ10.80(s,1h),9.13(s,1h),8.76
–
8.72(m,1h), 8.23(d,j=8.2hz,1h),8.01(s,1h),7.88(d,j=9.0hz,1h),7.80
–
7.72(m,2h),7.59(d,j=1.7 hz,1h),7.54(t,j=7.8hz,1h),7.50(dd,j=9.1,2.3hz,1h),7.48
–
7.40(m,2h),6.51(d,j=15.8hz,1h).esi-ms m/z:370.11[m+h]
+
.
[0183]
实施例20:(e)-n-羟基-3-(3-(n-(喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-20)的制备
[0184]
化合物(i-20)结构式
[0185][0186]
(e)-n-羟基-3-(3-(n-(喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-20)淡黄色固体,产率90%。mp: 170.5-173.5℃,1h-nmr(600mhz,dmso-d6)δ8.74(dd,j=4.1,1.5hz,1h),8.17(d,j=7.8hz, 1h),8.02(s,1h),7.79(t,j=7.4hz,2h),7.73(d,j=7.7hz,1h),7.58(s,1h),7.54(t,j=7.8hz, 1h),7.45(d,j=15.8hz,1h),7.36(dd,j=8.8,1.9hz,1h),7.32(dd,j=8.1,4.2hz,1h),6.53(d, j=15.9hz,1h).esi-ms m/z:370.09[m+h]
+
.
[0187]
实施例22:(e)-n-羟基-3-(3-(n-(异喹啉-1-基)磺胺基)苯基)丙烯酰胺(i-22)的制备
[0188]
化合物(i-22)结构式
[0189][0190]
(e)-n-羟基-3-(3-(n-(异喹啉-1-基)磺胺基)苯基)丙烯酰胺(i-22)白色固体,产率64%。mp: 175.9-177.8℃,1h-nmr(600mhz,dmso-d6)δ10.86(s,1h),9.10(s,1h),8.38(d,j=8.3hz, 1h),8.16(s,1h),7.91(d,j=7.7hz,1h),7.75
–
7.59(m,5h),7.48(d,j=15.6hz,3h),6.94(s, 1h),6.56(d,j=15.8hz,1h).esi-ms m/z:370.10[m+h]
+
.
[0191]
实施例23:(e)-n-羟基-3-(3-(n-(异喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-23)的
制备
[0192]
化合物(i-23)结构式
[0193][0194]
(e)-n-羟基-3-(3-(n-(异喹啉-3-基)磺胺基)苯基)丙烯酰胺(i-23)淡黄色固体,产率89%。 mp:92.3-95.1℃,1h-nmr(600mhz,dmso-d6)δ10.85(s,1h),8.96(s,1h),8.11(s,1h),7.91 (d,j=8.1hz,1h),7.86(d,j=7.8hz,1h),7.76(d,j=8.1hz,1h),7.70(d,j=7.7hz,1h),7.60 (t,j=7.4hz,1h),7.52(t,j=7.8hz,1h),7.46(d,j=15.8hz,1h),7.39(dd,j=15.9,8.6hz, 2h),6.56(d,j=15.8hz,1h).esi-ms m/z:370.12[m+h]
+
.
[0195]
实施例24:(e)-n-羟基-3-(3-(n-(异喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-24)的制备
[0196]
化合物(i-24)结构式
[0197][0198]
(e)-n-羟基-3-(3-(n-(异喹啉-4-基)磺胺基)苯基)丙烯酰胺(i-24)淡黄色固体,产率82%。 mp:175.4-177.7℃,1h-nmr(600mhz,dmso-d6)δ10.81(s,1h),9.11(s,1h),9.07(s,1h), 8.09(s,1h),8.07(d,j=8.1hz,1h),8.02(d,j=8.4hz,1h),7.84(s,1h),7.74(d,j=7.6hz, 1h),7.68(t,j=7.5hz,1h),7.66
–
7.61(m,2h),7.51(t,j=7.7hz,1h),7.42(d,j=15.7hz,1h), 6.46(d,j=15.8hz,1h).esi-ms m/z:370.09[m+h]
+
.
[0199]
实施例25:(e)-n-羟基-3-(3-(n-(异喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-25)的制备
[0200]
化合物(i-25)结构式
[0201][0202]
(e)-n-羟基-3-(3-(n-(异喹啉-5-基)磺胺基)苯基)丙烯酰胺(i-25)淡黄色固体,产率69%。 mp:173.0-176.3℃,1h-nmr(600mhz,dmso-d6)δ10.77(s,1h),10.26(s,1h),9.20(s,1h), 8.37(d,j=5.9hz,1h),7.90(d,j=5.8hz,1h),7.84(s,1h),7.79(s,1h),7.70(d,j=7.5hz, 1h),7.64(d,j=7.8hz,1h),7.49(dt,j=15.5,7.8hz,2h),7.42(d,j=15.8hz,1h),7.36(d,j= 7.5hz,1h),6.45(d,j=15.8hz,1h).esi-ms m/z:370.09[m+h]
+
.
[0203]
实施例26:(e)-n-羟基-3-(3-(n-(异喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-26)的制备
[0204]
化合物(i-26)结构式
[0205][0206]
(e)-n-羟基-3-(3-(n-(异喹啉-6-基)磺胺基)苯基)丙烯酰胺(i-26)白色固体,产率78%。mp: 205.3-207.7℃,1h-nmr(600mhz,dmso-d6)δ10.85(s,1h),9.12(s,1h),8.37(d,j=5.7hz, 1h),8.06(s,1h),8.00(d,j=8.8hz,1h),7.82(d,j=7.8hz,1h),7.77(d,j=7.7hz,1h),7.70 (d,j=5.7hz,1h),7.60
–
7.55(m,2h),7.47(d,j=16.3hz,1h),7.44(d,j=8.9hz,1h),6.54(d, j=15.9hz,1h).esi-ms m/z:370.11[m+h]
+
.
[0207]
实施例27:(e)-n-羟基-3-(3-(n-(异喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-27)的制备
[0208]
化合物(i-27)结构式
[0209][0210]
(e)-n-羟基-3-(3-(n-(异喹啉-7-基)磺胺基)苯基)丙烯酰胺(i-27)白色固体,产率65%。mp: 197.2-199.5℃,1h-nmr(600mhz,dmso-d6)δ10.83(s,1h),9.19(s,1h),8.37(d,j=5.6hz, 1h),8.02(s,1h),7.85(d,j=8.9hz,1h),7.77(dd,j=11.6,7.6hz,3h),7.69(d,j=5.6hz,1h), 7.56
–
7.51(m,2h),7.46(d,j=15.8hz,1h),6.52(d,j=15.9hz,1h).esi-ms m/z:370.12[m+ h]
+
.
[0211]
实施例28:(e)-n-羟基-3-(3-(n-(异喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-28)的制备
[0212]
化合物(i-28)结构式
[0213][0214]
(e)-n-羟基-3-(3-(n-(异喹啉-8-基)磺胺基)苯基)丙烯酰胺(i-28)淡黄色固体,产率88%。 mp:142.4-145.1℃,1h-nmr(600mhz,dmso-d6)δ10.77(s,1h),9.46(s,1h),8.37(d,j=5.6 hz,1h),7.89(s,1h),7.67(d,j=7.9hz,2h),7.65(d,j=5.6hz,1h),7.51(t,j=7.8hz,1h), 7.47(t,j=7.7hz,2h),7.42(d,j=15.8hz,1h),7.18(d,j=7.5hz,1h),6.47(d,j=15.8hz, 1h).esi-ms m/z:370.13[m+h]
+
.
[0215]
实施例29.目标化合物的体外抗肿瘤细胞增殖活性测试
[0216]
采用mtt法测试目标化合物对a549和mcf-7两类细胞株的体外抗增殖活性。将细胞置于含有10%胎牛血清(fbs)的rpmi-1640培养基中,并在含有5%co2的37℃培养箱中培养。取对数生长期的细胞以每孔3
×
103个细胞的密度将其接种于96孔板中,放于含有5%co2的 37℃恒温培养箱中继续培养18-24h左右。根据实验设计每孔加入100μl不同浓度梯度的化合物,空白对照组不加入化合物,阳性对照组加入相同浓度梯度的belinostat,继续于培养箱中培养48h。待药物作用时间达到时,每孔避光加入20μl浓度为5mg/ml的mtt溶液,于培养箱中孵育4-6h,随后弃去培养液,每孔加入100μl dmso溶液,避光震荡5min。将96孔板放
于酶标仪中,于570nm波长处检测od值,分别计算待测化合物的抑制率,抑制率 (%)=(100%吸光度平均值-化合物吸光度平均值)/(100%吸光度平均值-空白组吸光度平均值)
×
100,并用spss软件计算出ic
50
值。
[0217]
表1.目标化合物对两类癌细胞株的抗增殖活性结果
[0218][0219]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1