一种低共熔溶剂可持续提取β-胡萝卜素的方法及应用
一种低共熔溶剂可持续提取
β-胡萝卜素的方法及应用
技术领域
1.本发明涉及一种低共熔溶剂可持续提取β-胡萝卜素的方法及应用,属于活性物质萃取技术领域。
背景技术:
2.β-胡萝卜素是类胡萝卜素之一,是一种脂溶性化合物,它也是维生素a的主要前体。β-胡萝卜素具有抗氧化、抗癌、抗炎和增强免疫功能等有益健康的作用。由于人体不能合成类胡萝卜素,它们必须通过饮食摄入。人们逐渐关注从植物中提取获得β-胡萝卜素。小米是一种被中国等亚洲国家广泛种植的重要谷类作物,与小麦、水稻等谷物相比,小米中含有较丰富的β-胡萝卜素。小米具有抗氧化、预防癌症、增强人体免疫力的功能,可能是β-胡萝卜素的原因。从小米中分离β-胡萝卜素在食品、药品等领域的应用具有重要意义。
3.选择合适的提取溶剂对活性物质的简单、快速、高效的提取和回收起着重要的作用。β-胡萝卜素的提取一般采用乙醇,甲醇,乙腈,正己烷,石油醚等有机溶剂作为提取剂。然而,由于其毒性大,挥发性强,提取效率低,限制了它们在β-胡萝卜素提取方面的应用。近年来,由于低共熔溶剂成本低、毒性低、不易挥发、可生物降解、得率高,被认为是替代挥发性有机溶剂对天然产物进行提取分离的一类新型可持续溶剂。目前大量低共熔溶剂以氯化胆碱和有机酸合成为主,在目标物的分离时需要采用大孔树脂吸附法,存在成本高,操作复杂,耗时长的缺点。因此开发一种新型的功能性的低共熔溶剂,实现小米β-胡萝卜素的高效提取及从提取剂中简单快速的分离,具有重要的实际意义。
技术实现要素:
4.(一)要解决的技术问题
5.为了解决有机溶剂提取得率低,毒性较高,生物降解性差,环境污染严重,及现有的低共熔溶剂提取液中的提取物不易从提取剂中回收的问题,本发明提供一种低共熔溶剂可持续提取小米中的β-胡萝卜素的方法及应用。
6.(二)技术方案
7.为了达到上述目的,本发明采用的主要技术方案包括:
8.一种低共熔溶剂可持续提取β-胡萝卜素的方法,其包括如下步骤:
9.将物料粉碎后,加入含有抗氧化剂的低共熔溶剂,进行研磨提取,得到含β-胡萝卜素的提取液,向含β-胡萝卜素的提取液加入酸溶液,疏水性低共熔溶剂转换为亲水性,进行固液分离,得到小米β-胡萝卜素固体;
10.分离后的液体加入碱后,进行两相分离,收集上层的疏水性低共熔溶剂用于提取新的含β-胡萝卜素的物料。
11.如上所述的方法,可用于谷物、蔬菜、植物等富含胡萝卜素的物料都可以提取β-胡萝卜素,进一步地,优选小米物料。
12.如上所述的方法,优选地,所述粉碎为超微粉碎,使得其粒径达到10~25μm。
13.如上所述的方法,优选地,所述抗氧化剂为酚类抗氧化剂,优选为bht、bha或tbhq中的任一种或任两种的组合或三种;最优选为bht;
14.所述低共熔溶剂为摩尔比为5~1:1~3的n,n-二甲基环己胺,n,n-二甲基正辛胺或n,n-二甲基苄胺中的一种或任两种或三种与正丁醇的混合物;最优选为n,n-二甲基环己胺与正丁醇的混合物;最优选的摩尔比为3:1;
15.所述抗氧化剂在低共熔溶剂中的浓度为2~4mg ml-1
,最优选为3mg ml-1
。
16.如上所述的方法,优选地,粉碎后的物料与含有抗氧化剂的低共熔溶剂的料液比按单位g:ml为1:3~10进行;最优选为1:4。
17.如上所述的方法,优选地,所述酸溶液为盐酸或硫酸,酸溶液的加入量为使得低共熔溶剂的ph为1.5~2.5,此时低共熔溶剂为亲水性。
18.如上所述的方法,优选地,研磨提取的时间为5~40s,固液分离可采用离心或过滤。
19.如上所述的方法,优选地,碱为naoh、koh、na2co3粉末或溶液,使其ph为8.5~9.5时停止加碱。
20.低共熔溶剂在提取β-胡萝卜素中的应用,所述低共熔溶剂为n,n-二甲基环己胺,n,n-二甲基正辛胺或n,n-二甲基苄胺中的一种或任两种或三种与正丁醇的混合物。
21.如上所述的应用,优选地,胺与正丁醇按摩尔比为5~1:1~3进行,所述低共熔溶剂中含有浓度为2~4mg ml-1
的酚类抗氧化剂,酚类抗氧化剂为bht、bha或tbhq中的任一种或任两种的组合或三种。
22.如上所述的应用,优选地,所述低共熔溶剂为n,n-二甲基环己胺与正丁醇的混合物,其摩尔比为3:1,所述低共熔溶剂中含有浓度为3mg ml-1
的bht。
23.(三)有益效果
24.本发明的有益效果是:
25.1.本发明提供了一种低共熔溶剂可持续提取β-胡萝卜素的方法,采用超微粉碎预处理小米样品,增大了小米粉的比表面积。采用新的功能性低共熔溶剂作为提取剂(n,n-二甲基环己胺-正丁醇)研磨提取小米β-胡萝卜素。在提取过程中,加入酚类抗氧化剂,增加了β-胡萝卜素的稳定性。最终,实现了小米β-胡萝卜素的高效提取。
26.2.本发明提供的一种低共熔溶剂可持续提取β-胡萝卜素的方法,使用新的低共熔溶剂作为提取剂,只需转换溶液的ph就可以实现提取剂亲水疏水性的转换,使提取剂在疏水状态提取小米β-胡萝卜素,当提取剂转换为亲水状态,疏水的β-胡萝卜素固体从提取剂中析出,实现了目标物从提取剂中简单快速的分离。
27.3.本发明提供的一种低共熔溶剂可持续提取β-胡萝卜素的方法,利用提取剂可以实现亲水疏水性转换的性质,使提取剂得到回收,并用于提取新的小米样品,选定的低共熔溶剂经过五次回收再利用,β-胡萝卜素得率没有显著下降,β-胡萝卜素的回收率均保持在91%以上,实现了提取剂的回收再利用。
28.4.本发明的方法简单、快速、高效、可持续、无毒、绿色环保,在提取和回收疏水性生物活性物质方面有较好的应用前景。
附图说明
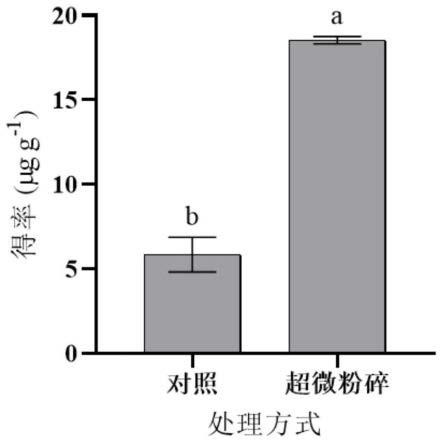
29.图1为预处理方式对β-胡萝卜素得率的影响;
30.图2为提取剂种类对β-胡萝卜素得率的影响;
31.图3为低共熔溶剂摩尔比对小米β-胡萝卜素得率的影响;
32.图4为酚类抗氧化剂种类对小米β-胡萝卜素得率的影响;
33.图5为bht浓度对小米β-胡萝卜素得率的影响;
34.图6为固液比对小米β-胡萝卜素得率的影响;
35.图7为提取方式对小米β-胡萝卜素得率的影响;
36.图8为提取时间对小米β-胡萝卜素得率的影响;
37.图9为低共熔溶剂重复使用次数对小米β-胡萝卜素得率的影响;
38.图10为低共熔溶剂重复使用次数对小米β-胡萝卜素固体回收率的影响。
39.图11为现有传统方法不同提取剂的提取小米β-胡萝卜素的得率。
具体实施方式
40.本发明的发明原理是:采用低共熔溶剂结合酚类抗氧化剂提取小米β-胡萝卜素,并对低共熔溶剂的回收再利用能力进行评价。本发明创新性的建立是通过设计合成新的功能性低共熔溶剂作为提取剂,其在改变ph的条件下可以实现亲水疏水性的转换。新配置的疏水低共熔溶剂的ph为6-7,其是疏水的,是与水互不相溶的两相,加入盐酸水溶液如果没有转换完成的话是可以看到是有分相的,完全转换成亲水相以后与水是相容的,可以看到没有分相,是均匀的一相,此时,其溶液ph为1.5~2.5时,即为亲水低共熔溶剂,之后加氢氧化钠,可以看到有一部分疏水低共熔溶剂被转换为疏水性了,有一部分与水互不相容,氢氧化钠加到一定量转换完成以后,可以看到溶液被分为两层,上层是回收到的疏水低共熔溶剂,体积与开始未转化为亲水前的低共熔溶剂几乎一致,即ph为8.5-9.5,也就是说明低共熔溶剂此时为疏水低共熔溶剂;而下层为水相。胡萝卜素是溶于疏水溶剂的,转换为亲水性以后,胡萝卜素不溶了,就可析出来了,所以提取剂在疏水状态提取小米β-胡萝卜素,亲水状态回收β-胡萝卜素固体和提取剂,并且回收的提取剂可以用于新的提取。该方法解决了目前很多现有技术面临的提取成本高、不绿色、得率低以及所提取的化合物需要通过蒸馏、沉淀、过柱、冻干等操作从提取剂中分离出来的问题。
41.为了更好的解释本发明,以便于理解,下面结合附图,通过具体实施方式,对本发明作详细描述。
42.实施例1超微粉碎预处理小米粉
43.(1)实验方法将300g小米样品置于普通粉碎机中磨成粉末,然后将小米粉放入超微粉碎机中进行10min超微粉碎预处理,使其粒径达到10~25μm,然后收集。准确称取0.25g小米粉,并加入1ml含有3mg ml-1
bht(2,6-二叔丁基对甲酚)的低共熔溶剂(摩尔比为3:1的n,n-二甲基环己胺与正丁醇的混合液),于2ml离心管中,使用研磨仪在30hz的频率下研磨提取40s,然后在3600g下离心5min,收集上清液,得到小米β-胡萝卜素提取液。
44.其中,上述含bht的低共熔溶剂的制备方法为:以n,n-二甲基环己胺作为氢键受体,正丁醇作为氢键供体,按摩尔比3:1混合,然后将混合物搅拌,直到形成均匀透明的液体,然后向合成的低共熔溶剂中按3mg/ml加入bht,并使其溶解。
45.同时以不进行超微粉碎预处理作为对照,按上述操作进行β-胡萝卜素的提取。
46.(2)以β-胡萝卜素作为标准品,溶于含bht的低共熔溶剂(n,n-二甲基环己胺-正丁醇)中,配制成不同浓度的β-胡萝卜素标准溶液(0.2,0.4,0.6,0.8,1.0μg ml-1
),以含bht的低共熔溶剂(n,n-二甲基环己胺-正丁醇)作为空白对照,于450nm波长处检测其吸光值,以标准溶液的浓度为横坐标,吸光值为纵坐标,绘制标准曲线。然后在450nm波长处测定样品的吸光值,代入标准曲线得到提取液中β-胡萝卜素的浓度,然后根据公式(1)计算小米β-胡萝卜素得率。
47.β-胡萝卜素得率(μg g-1
)=cv/m
ꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀꢀ
(1)
48.式中:c为β-胡萝卜素的质量浓度,μg ml-1
;v为提取液的体积,ml;m为小米粉的质量,g。
49.实验结果:如图1所示。
50.结果表明经过超微粉碎预处理后的小米β-胡萝卜素的得率显著高于(约4倍)没有经过超微粉碎预处理的。这可能是因为超微粉碎预处理使小米粉的破碎粒度更小,比表面积增大,促进了小米β-胡萝卜素的提取。因此,选择对小米粉进行超微粉碎预处理。
51.实施例2提取剂的优化
52.a.提取剂种类
53.(1)实验方法:与实施例1中的方法相同,不同之处在于分别采用不同种类的提取剂,三种低共熔溶剂(n,n-二甲基环己胺-正丁醇,n,n-二甲基正辛胺-正丁醇,n,n-二甲基苄胺-正丁醇)和乙醇。
54.三种低共熔溶剂的制备方法分别为:
55.分别以n,n-二甲基环己胺,n,n-二甲基正辛胺,n,n-二甲基苄胺作为氢键受体,正丁醇作为氢键供体,按摩尔比3:1混合,然后将混合物在搅拌,直到形成均匀透明的液体,分别合成三种不同的低共熔溶剂(n,n-二甲基环己胺-正丁醇,n,n-二甲基正辛胺-正丁醇,n,n-二甲基苄胺-正丁醇),然后向合成的低共熔溶剂中按3mg/ml加入bht,并使其溶解。(2)同实施例1中的检测方法测定β-胡萝卜素,不同提取剂的得率结果如图2所示。
56.结果表明采用低共熔溶剂要显著高于乙醇提取小米β-胡萝卜素的得率,并且n,n-二甲基环己胺-正丁醇提取小米β-胡萝卜素的能力最强。原因可能与低共熔溶剂与小米β-胡萝卜素的氢键相互作用和疏水相互作用有关。因此选择n,n-二甲基环己胺-正丁醇作为提取剂。
57.b.低共熔溶剂的摩尔比
58.(1)实验方法:与实施例1中的方法相同,不同之处在于分别采用不同的合成低共熔溶剂的摩尔比(6:1,5:1,4:1,3:1,2:1,1:1,1:2,1:3)。
59.低共熔溶剂的制备方法:n,n-二甲基环己胺与正丁醇分别按照摩尔比为6:1,5:1,4:1,3:1,2:1,1:1,1:2,1:3搅拌均匀形成透明澄清的液体,然后向合成的低共熔溶剂中按3mg/ml加入bht,并使其溶解。(2)同实施例1中的检测方法测定β-胡萝卜素,获得制备的低共熔溶剂的不同摩尔比的结果如图3所示。
60.结果表明随着n,n-二甲基环己胺:正丁醇的比值的不断减小,β-胡萝卜素的得率逐渐升高,当摩尔比为3:1时得率最高,然后得率下降。这可能是因为不同的摩尔比会影响低共熔溶剂的表面张力和向样品的渗透,以及β-胡萝卜素的溶解度。因此优选n,n-二甲基
环己胺与正丁醇为3:1的摩尔比制备的低共熔溶剂。
61.实施例3酚类抗氧化剂优化
62.a.酚类抗氧化剂种类
63.(1)实验方法:与实施例1中的方法相同,不同之处在于分别采用不同种类的酚类抗氧化剂(bht(2,6-二叔丁基对甲酚),bha(丁基羟基茴香醚),tbhq(叔丁基对苯二酚))。
64.低共熔溶剂的制备方法,同实施例1,不同在于添加的酚类抗氧化剂种类不同,以低共熔溶剂(n,n-二甲基环己胺-正丁醇)作为提取剂。
65.对照是不添加酚类抗氧化剂。
66.(2)同实施例1中的检测方法测定β-胡萝卜素,不同酚类抗氧化剂的提取结果如图4所示。
67.结果表明添加酚类抗氧化剂显著地提高了小米β-胡萝卜素的得率。同时,bht的辅助提取效果显著高于其它两种。这可能与酚类抗氧化剂的o-h键的解离能大小有关,酚类抗氧化剂提高了β-胡萝卜素的稳定性。因此,选择bht辅助提取β-胡萝卜素。
68.b.酚类抗氧化剂的添加浓度
69.(1)实验方法:与实施例1中的方法相同,不同之处在于分别采用不同浓度的bht(0.1,1,2,3,4,10,15mg ml-1
)。
70.(2)同实施例1中的检测方法测定β-胡萝卜素,不同浓度的bht的提取结果如图5所示。
71.结果表明当bht的浓度为0.1-3mg ml-1
时,β-胡萝卜素的得率不断增加,当bht的浓度超过3mg ml-1
时,得率下降。原因可能是当bht的浓度较低时,不能够充分发挥其抗氧化作用。然而当浓度过高时,反而会促进β-胡萝卜素发生氧化。因此,选择bht浓度为优选为3mg ml-1
。
72.实施例4提取条件优化
73.a.料液比
74.(1)实验方法:与实施例1中的方法相同,不同之处在于分别采用不同的料液比,即小米粉的质量(g):提取剂的体积(ml)分别按1:2,1:3,1:4,1:5,1:6,1:10进行。
75.(2)同实施例1中的检测方法测定β-胡萝卜素,不同料液比的结果如图6所示。
76.结果表明当料液比为1:2-1:4g ml-1
,小米β-胡萝卜素的得率不断增加,当料液比超过1:4g ml-1
时,得率没有显著提高。原因可能是,当提取剂的量不充足时,目标物不能实现充分提取。因此,选择料液比为1:4g ml-1
。
77.b.提取方式
78.(1)实验方法:与实施例1中的方法相同,不同之处在于分别采用不同的提取方式(研磨提取、水浴提取、超声提取)
79.研磨提取:采用研磨频率30hz,40s;
80.水浴提取:50℃,120min,
81.超声频率40khz,功率540w,50℃,15min。
82.(2)同实施例1中的检测方法测定β-胡萝卜素,如图7所示。
83.结果说明研磨提取法在更短提取时间内小米β-胡萝卜素得率显著高于水浴提取法和超声提取法。原因可能是研磨提取法使样品和提取剂的接触更充分,使β-胡萝卜素被
高效提取。因此,优选研磨处理来提取β-胡萝卜素。
84.c.提取时间
85.(1)实验方法:与实施例1中的方法相同,不同之处在于分别采用不同的提取时间(5,10,20,30,40,50,60s)。
86.具体是指研磨提取的时间分别为5s,10s,20s,30s,40s,50s,60s进行提取。
87.(2)同实施例1中的检测方法测定β-胡萝卜素,不同研磨时间的提取结果如图8所示。
88.结果表明当提取时间为5-40s时,小米β-胡萝卜素的得率不断增加,当提取时间超过40s,得率基本达到稳定。原因可能是在一定的时间内,随着提取时间的延长,β-胡萝卜素的溶出率增加,但当β-胡萝卜素充分提取后,继续延长提取时间对得率没有显著影响。因此,优选提取时间为40s。
89.实施例5小米β-胡萝卜素固体的回收
90.向实施例1中的得到小米β-胡萝卜素提取液900μl中加入5400μl1mol l-1
的hcl溶液,变为透明澄清均匀的一相,此时测得其ph是2,而本身低共熔溶剂的提取液的ph是6,因为低共熔溶剂是疏水性的,然后向其中加入hcl水溶液,如果没有转化完成的话,可以看到还是有分相的,转化完成以后没有分相,并且变为透明澄清均匀的一相,此时疏水性低共熔溶剂转换为亲水性低共熔溶剂,提取液中的β-胡萝卜素与提取剂分离,可以看到管壁析出黄色的胡萝卜素固体,并且提取剂的颜色也从黄色变为接近无色,此时将胡萝卜素与溶液(亲水性低共熔溶剂)进行分离,同时将分离开的溶液中继续加naoh,待溶液分层,回收上层体积与开始未转化为亲水前的低共熔溶剂几乎一致,即得到疏水低共熔溶剂,测得其ph为9;测定上层疏水相中含有的β-胡萝卜素的量,发现其中几乎不含有β-胡萝卜素,表明提取液中大部分β-胡萝卜素固体被回收,下层为水相。
91.实施例6低共熔溶剂的回收及新的提取
92.a.低共熔溶剂多次使用提取小米β-胡萝卜素的得率
93.(1)实验方法:将实施例5转换得到的亲水性低共熔溶剂(6.3ml)转移到离心管中,并向其中加入5.4ml的naoh溶液(1mol l-1
),离心(2862
×
g,5min),出现两相分离,上层是被回收的疏水低共熔溶剂相;下层是水相(两者互不相溶,且上层相的体积与初始所用的疏水低共熔溶剂的体积几乎一致。因此根据此判定上层是被回收的疏水低共熔溶剂相;下层是水相。)收集上层的疏水性低共熔溶剂用于提取新的小米样品(0.25g)。
94.(2)同实施例1中的检测方法测定β-胡萝卜素,同一低共熔溶剂重复使用不同次数的结果如图9所示。
95.结果表明低共熔溶剂经过五次重复使用,β-胡萝卜素的得率没有显著下降。同时可以看到β-胡萝卜素得率稍有上升,这可能是由于疏水低共熔溶剂中含有部分未被回收的β-胡萝卜素导致。
96.b.小米β-胡萝卜素的回收率
97.(1)实验方法:与实施例5的方法相同,并进行多次β-胡萝卜素的回收,计算每次的回收率(析出固体中β-胡萝卜素的含量/疏水低共熔溶剂中β-胡萝卜素的含量)。
98.疏水低共熔溶剂中β-胡萝卜素的含量是指初始提取液(疏水低共熔溶剂)中含有的β-胡萝卜素的量。
99.其中,1表示低共熔溶剂第一次使用,没有被重复使用回收过,2表示低共熔溶剂第二次使用提取β-胡萝卜素,第一次被回收重复使用,依次类推,6表示低共熔溶剂第六次使用提取β-胡萝卜素,第五次被回收重复使用。
100.(2)同实施例1中的检测方法测定β-胡萝卜素,结果如下表1,绘制成图如图10所示。
101.表1
[0102][0103]
(3)结果表明低共熔溶剂重复使用五次,小米β-胡萝卜素的回收率均可以保持在91.0%以上。表明实验选定的低共熔溶剂在小米β-胡萝卜素提取中具有良好的可循环利用性。
[0104]
实施例7
[0105]
取超微粉碎的小米粉,按小米粉的质量(g):提取剂的体积(ml)的比值为1:4加入含有3mg ml-1
bht的疏水低共熔溶剂(摩尔比为3:1的n,n-二甲基环己胺:正丁醇),使用研磨仪在30hz的频率下研磨提取40s,然后在3600
×
g下离心5min,收集上清液,得到小米β-胡萝卜素提取液。根据实施例1中所述的方法测定小米β-胡萝卜素的得率,得率可达到18.39μg g-1
。向提取液中加入1mol l-1
的hcl溶液,疏水性低共熔溶剂转换为亲水性低共熔溶剂,提取液中的β-胡萝卜素与提取剂分离,管壁出现胡萝卜素固体,收集胡萝卜素固体。
[0106]
对比例1
[0107]
对现有技术中采用的传统提取剂对小米β-胡萝卜素的得率的影响进行研究,具体操作为:
[0108]
取超微粉碎的小米粉,按小米粉的质量(g):提取剂的体积(ml)的比值为1:4分别加入含有3mg ml-1
bht的提取剂(乙醇、甲醇、乙腈、正己烷、石油醚),使用研磨仪在30hz的频率下研磨提取40s,然后在3600
×
g下离心5min,收集上清液,得到小米β-胡萝卜素提取液。同实施例1中的检测方法测定β-胡萝卜素得率,不同之处在于根据提取剂的不同分别选择不同的溶剂(乙醇、甲醇、乙腈、正己烷、石油醚)溶解β-胡萝卜素,配制成不同浓度的β-胡萝卜素标准溶液,分别制作不同提取剂的β-胡萝卜素标准曲线。
[0109]
结果如下表2,绘制成图如图11所示。
[0110]
对传统提取剂提取小米β-胡萝卜素的效果进行研究,五种传统提取剂中乙醇的提取效果最好,得率为5.55μg g-1
,可见,本发明合成的低共熔溶剂最佳得率为18.39μg g-1
,远高于传统乙醇提取法。
[0111]
表2
[0112]
[0113]
对比例2
[0114]
以三乙胺作为氢键受体和正丁醇合成的低共熔溶剂,以及以n,n-二甲基环己胺、n,n-二甲基正辛胺、n,n-二甲基苄胺作为氢键受体,和芳樟醇、薄荷醇、香叶醇、松油醇、香茅醇、乙二醇、乳酸作为氢键供体合成的低共熔溶剂,亲水和疏水性相互转换的效果不佳,不利于β-胡萝卜素的回收和提取剂的回收再利用。
[0115]
以上所述,仅是本发明的较佳实施例而已,并非是对本发明做其它形式的限制,任何本领域技术人员可以利用上述公开的技术内容加以变更或改型为等同变化的等效实施例。但是凡是未脱离本发明技术方案内容,依据本发明的技术实质对以上实施例所作的任何简单修改、等同变化与改型,仍属于本发明技术方案的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1