试剂控释模块、生物反应器以及生物检测装置的制作方法
1.本发明涉及微流控芯片技术领域,特别涉及一种试剂控释模块、生物反应器以及生物检测装置。
背景技术:
2.微流控芯片技术是将各种生物、化学或医学分析过程的样品制备、分离、反应及检测等基本操作集成在几平方厘米到几十平方厘米的芯片之上的一种技术,由于其具有集成化、自动化、样品和试剂消耗量小等特点,已广泛应用于生化检测、核酸检测、免疫分析、细胞分选、食品安全和环境监测等领域。
3.以核酸检测为例,核酸检测通常包括样本裂解、核酸提取纯化以及扩增检测三个步骤,每个步骤又有多步操作流程。特别的在核酸提取纯化过程中,试剂按照特定的顺序释放,但是,目前用于试剂释放的结构复杂,装配难度大,且需要外接额外的驱动控制装置。
4.因此,如何简化核酸检测的结构,成为本领域技术人员亟待解决的技术问题。
技术实现要素:
5.本发明提出了一种试剂控释模块、生物反应器以及生物检测装置,以简化结构。
6.为了实现上述目的,本发明提供如下技术方案:第一方面,本发明提供了一种试剂控释模块,包括:用于接收加注溶剂的溶剂存储单元和多个用于存储干燥试剂并顺序释放的试剂存储释放单元;溶剂存储单元与试剂存储释放单元由近心端至远心端依次排布,且试剂存储释放单元通过流体管道与溶剂存储单元的下游连通;溶剂存储单元加注溶剂后,溶剂存储单元内的溶剂通过对应的流体管道按照第一顺序进入至对应的试剂存储释放单元中以复溶干燥试剂;试剂存储释放单元与对应的毛细阀连通;当试剂控释模块受驱于预设转速的离心力作用时,多个试剂存储释放单元通过对应的毛细阀按照第二顺序释放各自复溶后的试剂。
7.本发明一些可能的实施方式中,溶剂存储单元包括用于加注溶剂的溶剂口和与溶剂口连通并用于存储溶剂的溶剂池,溶剂池与多个试剂存储释放单元均连通。
8.本发明一些可能的实施方式中,试剂存储释放单元的数量为j个,按照第1试剂存储释放单元至第j试剂存储释放单元的顺序依次释放复溶后的试剂,其中,第i试剂存储释放单元包括i个试剂池,i为1
…
j;j为大于1的自然数。
9.本发明一些可能的实施方式中,溶剂存储单元的容积不小于第1试剂存储释放单元至第j试剂存储释放单元的总容积。
10.本发明一些可能的实施方式中,试剂存储释放单元的数量为三个,分别为第一试剂存储释放单元、第二试剂存储释放单元和第三试剂存储释放单元,第一试剂存储释放单
元通过第一流体管道与溶剂存储单元的下游连通,第二试剂存储释放单元通过第二流体管道与溶剂存储单元的下游连通,第三试剂存储释放单元通过第三流体管道与溶剂存储单元的下游连通。
11.本发明一些可能的实施方式中,第一流体管道的管径小于第二流体管道的管径以及第三流体管道的管径。
12.本发明一些可能的实施方式中,第二流体管道的管径与第三流体管道的管径相同。
13.本发明一些可能的实施方式中,第一试剂存储释放单元包括存储第一干燥试剂的第一试剂池,第一试剂池的上游通过第一流体管道与溶剂存储单元的下游连通,第一试剂池的下游通过第一毛细阀与样本处理池的上游连通。
14.本发明一些可能的实施方式中,第二试剂存储释放单元包括第二试剂池和一级试剂池,第二试剂池的上游通过第二流体管道与溶剂存储单元的下游连通,第二试剂池的下游通过第二毛细阀与一级试剂池的上游连通,一级试剂池的下游通过第三毛细阀与样本处理池的上游连通,第二试剂池或一级试剂池存储第二干燥试剂。
15.本发明一些可能的实施方式中,第三试剂存储释放单元包括第三试剂池、二级试剂池和三级试剂池,第三试剂池的上游通过第三流体管道与溶剂存储单元的下游连通,第三试剂池的下游通过第四毛细阀与二级试剂池的上游连通,二级试剂池的下游通过第五毛细阀与三级试剂池的上游连通,三级试剂池的下游通过第六毛细阀与样本处理池的上游连通,第三试剂池、二级试剂池或三级试剂池存储第三干燥试剂。
16.本发明一些可能的实施方式中,第一试剂存储释放单元、第二试剂存储释放单元和第三试剂存储释放单元呈两列布置,其中,第一试剂存储释放单元和第二试剂存储释放单元位于同一列,第三试剂存储释放单元位于另一列。
17.本发明一些可能的实施方式中,由近心端至远心端,第二试剂池的上游、一级试剂池的上游和第一试剂池的上游与溶剂存储单元的下游之间的距离逐渐变大;由近心端至远心端,第三试剂池的上游、二级试剂池的上游和三级试剂池的上游与溶剂存储单元的下游之间的距离逐渐变大。
18.本发明一些可能的实施方式中,由近心端至远心端,第二毛细阀的拱起部相较于第二试剂池的上游靠近近心端。
19.本发明一些可能的实施方式中,由近心端至远心端,第三毛细阀的拱起部相较于一级试剂池的上游靠近近心端。
20.本发明一些可能的实施方式中,由近心端至远心端,第一毛细阀的拱起部相较于第一试剂池的上游靠近近心端。
21.本发明一些可能的实施方式中,由近心端至远心端,第四毛细阀的拱起部相较于第三试剂池的上游靠近近心端。
22.本发明一些可能的实施方式中,由近心端至远心端,第五毛细阀的拱起部相较于二级试剂池的上游靠近近心端。
23.本发明一些可能的实施方式中,由近心端至远心端,第六毛细阀的拱起部相较于三级试剂池的上游靠近近心端。
24.本发明一些可能的实施方式中,存储干燥试剂的试剂池内预置有可在内部活动的
活动体。
25.本发明一些可能的实施方式中,活动体为金属材料、磁性材料、聚合物材料中的一种或多种。
26.本发明一些可能的实施方式中,活动体为钢珠、磁珠和磁棒中的至少一种。
27.第二方面,本发明公开了一种生物反应器,包括反应主体和设置于反应主体上的如上述任一项的试剂控释模块。
28.本发明一些可能的实施方式中,还包括设置于反应主体上的气路模块,气路模块用于气相交换。
29.本发明一些可能的实施方式中,气路模块包括设置于反应主体上的导气孔、平衡气室和连通孔,其中,导气孔与对应的腔体连通;平衡气室设置于反应主体的一个端面,仅通过连通孔与导气孔连通。
30.本发明一些可能的实施方式中,导气孔位于反应主体的第一端面,平衡气室位于反应主体的第二端面。
31.本发明一些可能的实施方式中,腔体的周边设置有密封凸台,密封凸台隔绝对应的腔体与平衡气室。
32.本发明一些可能的实施方式中,还包括设置于反应主体上用于收纳废液的液体收纳模块,液体收纳模块包括废液排放口和废液收纳池,废液排放口连通对应的腔体与废液收纳池。
33.本发明一些可能的实施方式中,废液收纳池设置于反应主体的第一端面时,废液排放口设置于废液收纳池的上游。
34.本发明一些可能的实施方式中,废液收纳池设置于反应主体的第二端面时,废液排放口贯穿反应主体。
35.本发明一些可能的实施方式中,废液排放口与废液收纳池衔接的部位设置有防止废液回流的回液遮挡部。
36.本发明一些可能的实施方式中,生物反应器为核酸提取扩增反应器、核酸杂交反应器、固相萃取反应器或者蛋白/抗原免疫检测反应器。
37.本发明一些可能的实施方式中,生物反应器为核酸提取扩增反应器时,生物反应器包括反应主体和设置于反应主体上的第一样本池、试剂控释模块、第一缓冲池、第一萃取池、第一流体控制阀、混合池、流体阀、第一分配池、第一反应池和液体收纳模块,其中,试剂控释模块、第一缓冲池、第一萃取池、第一流体控制阀、混合池、流体阀、第一分配池和第一反应池由近心端至远心端依次连通;第一样本池与试剂控释模块相比靠近反应主体近心端,并与第一缓冲池连通;液体收纳模块与第一流体控制阀连通。
38.本发明一些可能的实施方式中,生物反应器为核酸杂交反应器时,生物反应器包括反应主体和设置于反应主体上的第二样本池、试剂控释模块、第二缓冲池、杂交池、第二流体控制阀和液体收纳模块,其中,试剂控释模块、第二缓冲池、杂交池、第二流体控制阀和液体收纳模块由近心端至远心端依次连通;第二样本池与试剂控释模块相比靠近反应主体近心端,并与第二缓冲池连通。
39.本发明一些可能的实施方式中,生物反应器为固相萃取反应器时,生物反应器包括反应主体和设置于反应主体上的第三样本池、试剂控释模块、第三缓冲池、第二萃取池、
第三流体控制阀、取样口、收集池和液体收纳模块,其中,试剂控释模块、第三缓冲池、第二萃取池、第三流体控制阀和液体收纳模块由近心端至远心端依次连通;第三样本池与试剂控释模块相比靠近反应主体近心端,并与第三缓冲池连通;取样口通过一段管道和收集池远心端连通,且收集池与第三流体控制阀连通。
40.本发明一些可能的实施方式中,生物反应器为蛋白/抗原免疫检测反应器时,生物反应器包括反应主体和设置于反应主体上的第四样本池、试剂控释模块、第四缓冲池、第二分配池、第二反应池、第四流体控制阀和液体收纳模块,其中,试剂控释模块、第四缓冲池、第二分配池、第二反应池、第四流体控制阀和液体收纳模块由近心端至远心端依次连通;第四样本池与试剂控释模块相比靠近反应主体近心端,并与第四缓冲池连通。
41.第三方面,本发明提供了一种生物检测装置,包括检测托盘和如上述任一项的生物反应器,检测托盘设置有安装生物反应器的安装槽。
42.本发明一些可能的实施方式中,安装槽的数量为一个或者多个,多个安装槽对称布置于检测托盘。
43.本发明一些可能的实施方式中,生物检测装置上设置有用于控制生物反应器对应部位温度的加热部件和/或制冷部件。
44.本发明一些可能的实施方式中,加热部件和/或制冷部件为加热膜或帕尔贴。
45.本发明一些可能的实施方式中,生物检测装置上设置有吸引生物反应器中预置的活动体的永磁铁或电磁体。
46.由上述描述可知,本发明实施例试剂控释模块的试剂存储释放单元通过流体管道与溶剂存储单元的下游连通,试剂存储释放单元与对应的毛细阀连通以释放各自复溶后的试剂。本发明实施例中的试剂控释模块使用时,将溶剂注入至溶剂存储单元中,溶剂存储单元内的溶剂通过对应流体管道按照第一顺序进入至对应的试剂存储释放单元中复溶干燥试剂。试剂控释模块受驱于预设转速的离心力作用时,多个试剂存储释放单元通过对应的毛细阀按照第二顺序释放各自复溶后的试剂。因此,本发明实施例试剂控释模块仅通过简单的结构配合预设转速就可以实现试剂的稳定存储和顺序释放,且释放过程无需额外驱动机构。另外,本发明实施例中,用于释放的试剂以干燥状态预存,方便存储运输。
附图说明
47.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍。显而易见地,下面描述中的附图仅仅是本发明的一些示例或实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图,而且还可以根据提供的附图将本发明应用于其它类似情景。除非从语言环境中显而易见或另做说明,图中相同标号代表相同结构或操作。
48.图1为本发明实施例所提供的一种试剂控释模块的结构示意图;图2为本发明实施例所提供的另一种试剂控释模块的结构示意图;图3为本发明实施例所提供的第一种生物反应器的主视结构示意图;图4为本发明实施例所提供的第一种生物反应器的仰视结构示意图;图5为本发明实施例所提供的第二种生物反应器的结构示意图;图6为本发明实施例所提供的第三种生物反应器的结构示意图;
图7为本发明实施例所提供的第四种生物反应器的结构示意图;图8至图18为本发明实施例所提供的第四种生物反应器反应过程示意图;图19为本发明实施例所提供的一种生物检测装置的结构示意图;图20为本发明实施例所提供的另一种生物检测装置的结构示意图;图21为本发明实施例所提供的又一种生物检测装置的结构示意图。
49.其中,100为试剂控释模块、200为反应主体、300为气路模块、400为液体收纳模块、900为检测托盘;101为溶剂存储单元、102为试剂存储释放单元、1021为第一试剂存储释放单元、1022为第二试剂存储释放单元、1023为第三试剂存储释放单元、1031为第一流体管道、1032为第二流体管道、1033为第三流体管道、1041为第一毛细阀、1042为第二毛细阀、1043为第三毛细阀、1044为第四毛细阀、1045为第五毛细阀、1046为第六毛细阀;1021a为第一试剂池、1022a为第二试剂池、1022b为一级试剂池、1023a为第三试剂池、1023b为二级试剂池、1023c为三级试剂池;301为平衡气室、302a为第一导气孔、303a为第一连通孔、302b为第二导气孔、303b为第二连通孔、302c为第三导气孔、303c为第三连通孔、302d为第四导气孔、303d为第四连通孔、302e为第五导气孔、303e为第五连通孔;401为废液排放口、402为废液收纳池、403为回液遮挡部;501为第一样本池、502为第一缓冲池、503为第一萃取池、504为第一流体控制阀、505为混合池、506为流体阀、507为第一分配池、508为第一反应池;601为第二样本池、602为第二缓冲池、603为杂交池、604为第二流体控制阀;701为第三样本池、702为第三缓冲池、703为第二萃取池、704为第三流体控制阀、705为取样口、706为收集池;801为第四样本池、802为第四缓冲池、803为第二分配池、804为第二反应池、805为第四流体控制阀。
具体实施方式
50.下面结合附图和实施例对本发明作进一步的详细说明。可以理解的是,此处所描述的具体实施例仅仅用于解释相关发明,而非对该发明的限定。所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
51.微流控芯片是将各种化学、生物和医学分析等领域所涉及的样品制备、反应、分离和检测等基本操作单元集成到几个平方厘米大小的具有微米级通道结构的芯片上, 采用可控流体, 完成常规化学和生物医学实验室的各种功能的一种微技术平台技术,由于其具有小型化、集成化、高通量、低能耗、分析快速等特性,目前已广泛应用于生物、医学、环保、食品安全和新药研究等领域。
52.以核酸检测为例,核酸检测通常包括样本裂解、核酸提取纯化以及扩增检测三个步骤,每个步骤又有多步操作流程,现有技术中多采用手动操作的方式,不仅操作繁琐、费时费力,操作过程中相互交叉的风险高,人工操作导致结果不稳定。此外,针对烈性传染病检测来说,操作人员存在暴露风险。同样的,由于操作步骤多、液体转移精度高,通过全自动
化仪器来实现全流程操作过程也非常难以实现。
53.基于以上原因,本发明提供了一种试剂控释模块、生物反应器以及生物检测装置,以简化结构。以下结合几个实施例具体介绍。
54.实施例一参阅图1至图2,本发明实施例所提供的试剂控释模块100包括:用于接收加注溶剂的溶剂存储单元101和多个用于存储干燥试剂并顺序释放的试剂存储释放单元102;溶剂存储单元101与试剂存储释放单元102由近心端a至远心端b依次排布,且试剂存储释放单元102通过流体管道与溶剂存储单元101的下游连通;溶剂存储单元101加注溶剂后,溶剂存储单元101内的溶剂通过对应流体管道按照第一顺序进入至对应的试剂存储释放单元102中以复溶干燥试剂;试剂存储释放单元102与对应的毛细阀连通;当试剂控释模块100受驱于预设转速的离心力作用时,多个试剂存储释放单元102通过对应的毛细阀按照第二顺序释放各自复溶后的试剂。
55.本发明实施例中的试剂控释模块100使用时,将溶剂注入至溶剂存储单元101中,溶剂存储单元101内的溶剂通过对应的流体管道按照第一顺序进入至对应的试剂存储释放单元102中复溶干燥试剂。试剂控释模块100受驱于预设转速的离心力作用时,多个试剂存储释放单元102通过对应的毛细阀按照第二顺序释放各自复溶后的试剂。本发明实施例的试剂控释模块100释放仅通过调整预设转速实现,且该试剂控释模块100的试剂存储释放单元102通过流体管道与溶剂存储单元101的下游连通,试剂存储释放单元102与对应的毛细阀连通以释放各自复溶后的试剂,因此,本发明实施例的试剂控释模块100仅通过简单的结构就可以实现试剂的稳定存储和顺序释放,且顺序释放过程无需额外设置驱动机构。另外,本发明实施例中,用于释放的试剂以干燥状态预存,方便存储运输。
56.需要说明的是,试剂控释模块100安装于生物检测装置时,靠近旋转中心的一端为近心端a,远离旋转中心的一端为远心端b。针对试剂控释模块100中各个单元,上游为引入试剂的结构,其在布置时,上游还可以理解为靠近近心端a的面;下游为引出试剂的结构,其在布置时,还可以理解为靠近远心端b的面。不同结构的单元中,上游和下游有所差别,当为流体管道时,上游可以理解为入口,下游可以理解为出口;当为试剂池等盛放或者暂存试剂的结构时,上游为靠近近心端a的面,下游为靠近远心端b的面,上述面可以为曲面或者平面,进一步为以旋转中心为中心的圆弧面。
57.试剂存储释放单元102的数量为j个,按照第1试剂存储释放单元至第j试剂存储释放单元的顺序依次释放复溶后的试剂,其中,第i试剂存储释放单元包括i个试剂池,i为1
…
j;j为大于1的自然数。例如,当试剂存储释放单元102为2个时,2个试剂存储释放单元102分别为第1试剂存储释放单元、第2试剂存储释放单元;当试剂存储释放单元102为3个时,3个试剂存储释放单元102分别为第1试剂存储释放单元、第2试剂存储释放单元、第3试剂存储释放单元;当试剂存储释放单元102为4个时,4个试剂存储释放单元102分别为第1试剂存储释放单元、第2试剂存储释放单元、第3试剂存储释放单元、第4试剂存储释放单元,以此类推。
58.当j个试剂存储释放单元按照第1试剂存储释放单元至第j试剂存储释放单元的顺序依次释放复溶后的试剂时,第i试剂存储释放单元包括i个试剂池,i为1
…
j,j为大于1的自然数。可以理解为,当试剂存储释放单元102为2个时,第1试剂存储释放单元包括1个试剂
池,第2试剂存储释放单元包括2个试剂池;当试剂存储释放单元102为3个时,第1试剂存储释放单元包括1个试剂池,第2试剂存储释放单元包括2个试剂池,第3试剂存储释放单元包括3个试剂池;当试剂存储释放单元102为4个时,第1试剂存储释放单元包括1个试剂池,第2试剂存储释放单元包括2个试剂池,第3试剂存储释放单元包括3个试剂池、第4试剂存储释放单元包括4个试剂池,以此类推。且每个试剂池根据其功能可作为复溶干燥试剂的器皿,也可作为暂存试剂的器皿,此处不具体描述,将在后续内容展开描述。
59.溶剂存储单元101的容积不小于第1试剂存储释放单元至第j试剂存储释放单元的总容积。需要说明的是,此处的容积为能够定量的容积,对于暂存位置的容积不作考虑。例如,当试剂存储释放单元102为2个时,第1试剂存储释放单元的容积为1个试剂池的容积,第2试剂存储释放单元的容积为位于第2试剂存储释放单元上游的试剂池的容积,位于其下游的试剂池仅用于暂存。当试剂存储释放单元102为3个时,第1试剂存储释放单元的容积为1个试剂池的容积,第2试剂存储释放单元的容积为位于第2试剂存储释放单元上游的试剂池的容积,第3试剂存储释放单元的容积为位于第3试剂存储释放单元上游的试剂池的容积。
60.溶剂存储单元101用于接收加注溶剂,该溶剂为但不限于纯净水。本发明一个示例中,该溶剂存储单元101包括用于加注溶剂的溶剂口和与溶剂口连通并用于存储溶剂的溶剂池,溶剂池与多个试剂存储释放单元102均连通。
61.试剂存储释放单元102为多个,并根据具体生化反应确定试剂存储释放单元102。参见图1,图1所示的试剂存储释放单元102的数量为两个,分别为第一试剂存储释放单元1021和第二试剂存储释放单元1022,第一试剂存储释放单元1021通过第一流体管道1031与溶剂存储单元101的下游连通,第二试剂存储释放单元1022通过第二流体管道1032与溶剂存储单元101的下游连通。
62.第一步:启动离心,液体溶剂在离心力作用下填充至第一试剂存储释放单元1021和第二试剂存储释放单元1022。
63.第二步:降低离心转速,毛细阀在毛细力作用下完成毛细管的填充。
64.第三步:再次启动离心,各试剂池中液体按照顺序进行释放。
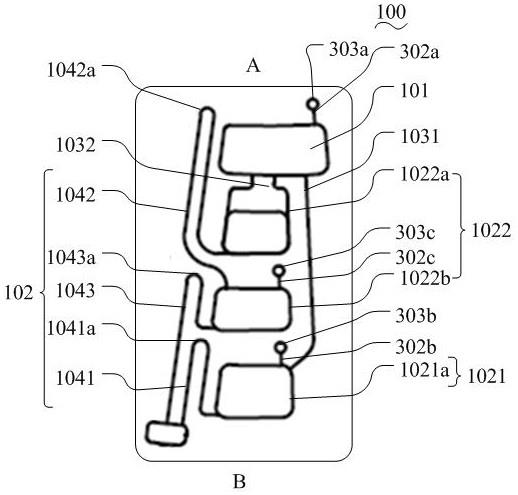
65.参见图2,图2所示的试剂存储释放单元102的数量为三个,分别为第一试剂存储释放单元1021、第二试剂存储释放单元1022和第三试剂存储释放单元1023,第一试剂存储释放单元1021通过第一流体管道1031与溶剂存储单元101的下游连通,第二试剂存储释放单元1022通过第二流体管道1032与溶剂存储单元101的下游连通,第三试剂存储释放单元1023通过第三流体管道1033与溶剂存储单元101的下游连通。
66.第一步:启动离心,液体溶剂在离心力作用下填充至第一试剂存储释放单元1021、第二试剂存储释放单元1022和第三试剂存储释放单元1023。
67.第二步:降低离心转速,毛细阀在毛细力作用下完成毛细管的填充。
68.第三步:再次启动离心,各试剂池中液体按照顺序进行释放。
69.以下本发明实施例中,以试剂存储释放单元102的数量为三个的情况详细展开说明,而试剂存储释放单元102为其他数量的可相互参考。
70.需要说明的是,溶剂存储单元101的溶剂按照第一顺序进入至对应的试剂存储释放单元102中,例如,溶剂同时进入至第二试剂存储释放单元1022和第三试剂存储释放单元1023中,再进入至第一试剂存储释放单元1021中;或者,依次进入第一试剂存储释放单元
1021、第二试剂存储释放单元1022和第三试剂存储释放单元1023等。
71.本发明实施例中,溶剂率先进入至第二试剂存储释放单元1022和第三试剂存储释放单元1023,为此,第一流体管道1031的管径小于第二流体管道1032的管径以及第三流体管道1033的管径。管径越小阻力越大,为此,溶剂会最先通过管径较大的第二流体管道1032和第三流体管道1033中。由于第一流体管道1031的管径小,阻力相对更大一些,为此溶剂先通过第二流体管道1032和第三流体管道1033进入至第二试剂池1022a和第三试剂池1023a中。
72.本发明一些示例中,第二流体管道1032的管径与第三流体管道1033的管径相同。本发明另一示例中,第二流体管道1032的管径与第三流体管道1033的管径相异。
73.以上是对于第一流体管道1031、第二流体管道1032和第三流体管道1033的一些介绍,本发明还对各个试剂存储释放单元102做出了一定改进:第一试剂存储释放单元1021的作用是用于存储和释放第一干燥试剂,本发明一些示例中,第一试剂存储释放单元1021包括存储第一干燥试剂的第一试剂池1021a,第一试剂池1021a的上游通过第一流体管道1031与溶剂存储单元101的下游连通,第一试剂池1021a的下游通过第一毛细阀1041释放复溶后的第一干燥试剂。溶剂在通过第一流体管道1031进入至第一试剂池1021a后,与第一试剂池1021a中预存的第一干燥试剂充分混合后复溶,并达到第一预设转速时,复溶后的第一干燥试剂通过第一毛细阀1041进行释放,其中,复溶后的第一干燥试剂称之为第一试剂。
74.第二试剂存储释放单元1022的作用是用于存储和释放第二干燥试剂,本发明一些示例中,第二试剂存储释放单元1022包括存储第二干燥试剂的第二试剂池1022a和一级试剂池1022b,第二试剂池1022a的上游通过第二流体管道1032与溶剂存储单元101的下游连通,第二试剂池1022a的下游通过第二毛细阀1042与一级试剂池1022b的上游连通,一级试剂池1022b的下游通过第三毛细阀1043与样本处理池的上游连通。溶剂在通过第二流体管道1032进入至第二试剂池1022a后,与第二试剂池1022a中预存的第二干燥试剂充分混合后复溶,并达到第二预设转速时,复溶后的第二干燥试剂通过第二毛细阀1042进入至一级试剂池1022b中,并在达到第三预设转速时通过第三毛细阀1043进行释放,其中,复溶后的第二干燥试剂称之为第二试剂。
75.上述第二试剂存储释放单元1022中第二干燥试剂存储于第二试剂池1022a,第二干燥试剂还可存储于一级试剂池1022b。第二干燥试剂在一级试剂池1022b中复溶。
76.第三试剂存储释放单元1023的作用是用于存储和释放第三干燥试剂,本发明一些示例中,第三试剂存储释放单元1023包括存储第三干燥试剂的第三试剂池1023a、二级试剂池1023b和三级试剂池1023c,第三试剂池1023a的上游通过第三流体管道1033与溶剂存储单元101的下游连通,第三试剂池1023a的下游通过第四毛细阀1044与二级试剂池1023b的上游连通,二级试剂池1023b的下游通过第五毛细阀1045与三级试剂池1023c的上游连通,三级试剂池1023c的下游通过第六毛细阀1046与样本处理池的上游连通。溶剂在通过第三流体管道1033进入至第三试剂池1023a后,与第三试剂池1023a中预存的第三干燥试剂充分混合后复溶,并达到第四预设转速时,复溶后的第三干燥试剂通过第四毛细阀1044进入至二级试剂池1023b中,并在达到第五预设转速时通过第五毛细阀1045进入至三级试剂池1023c中,并在达到第六预设转速时通过第六毛细阀1046进行释放,其中,复溶后的第三干
燥试剂称之为第三试剂。
77.上述第三试剂存储释放单元1023中第三干燥试剂存储于第三试剂池1023a,第三干燥试剂还可存储于二级试剂池1023b或三级试剂池1023c。第三干燥试剂存储于二级试剂池1023b中时,第三干燥试剂在二级试剂池1023b中复溶;第三干燥试剂还可存储于三级试剂池1023c中时,第三干燥试剂在三级试剂池1023c中复溶。
78.上述第一预设转速、第二预设转速、第三预设转速、第四预设转速、第五预设转速和第六预设转速,可结合第一试剂存储释放单元1021、第二试剂存储释放单元1022和第三试剂存储释放单元1023的具体排布、结构以及释放要求设置为相同或者相异。
79.本发明一些实例中,为了提高试剂控释模块100的集成度,减小占用体积,第一试剂存储释放单元1021、第二试剂存储释放单元1022和第三试剂存储释放单元1023呈两列布置,其中,第一试剂存储释放单元1021和第二试剂存储释放单元1022位于同一列,第三试剂存储释放单元1023位于另一列。
80.具体的,由近心端a至远心端b,第二试剂池1022a的上游、一级试剂池1022b的上游和第一试剂池1021a的上游与溶剂存储单元101的下游之间的距离逐渐变大;由近心端a至远心端b,第三试剂池1023a的上游、二级试剂池1023b的上游和三级试剂池1023c的上游与溶剂存储单元101的下游之间的距离逐渐变大。
81.同时,本发明实施例中为了各试剂存储释放单元102实现流体控制,由近心端a至远心端b,第二毛细阀1042的拱起部1042a与第二试剂池1022a的上游相比靠近近心端a。
82.由近心端a至远心端b,第三毛细阀1043的拱起部1043a与一级试剂池1022b的上游相比靠近近心端a。
83.由近心端a至远心端b,第一毛细阀1041的拱起部1041a与第一试剂池1021a的上游相比靠近近心端a。
84.由近心端a至远心端b,第四毛细阀1044的拱起部1044a与第三试剂池1023a的近心端a。
85.由近心端a至远心端b,第五毛细阀1045的拱起部1045a与二级试剂池1023b的上游相比靠近近心端a。
86.由近心端a至远心端b,第六毛细阀1046的拱起部1046a与三级试剂池1023c的上游相比靠近近心端a。
87.另外,由于第一试剂池1021a、第二试剂池1022a和第三试剂池1023a预存有干燥试剂,为了加速复溶,第一试剂池1021a、第二试剂池1022a和第三试剂池1023a内预置有可在其内部活动的活动体,该活动体为金属材料、磁性材料、聚合物材料中的一种或多种。进一步的,活动体为钢珠、磁珠和磁棒中的至少一种。配合生物检测装置的特定结构,驱动钢珠、磁珠和磁棒中在第一试剂池1021a、第二试剂池1022a和第三试剂池1023a往复运动以混合溶剂和干燥试剂。
88.第一步:启动离心,液体溶剂在离心力作用下填充至第二试剂池1022a与第三试剂池1023a中,并在第二试剂池1022a、第三试剂池1023a填满后再填充至第一试剂池1021a填充,从而实现各个试剂池液体的准确定量,以满足溶解干燥试剂后试剂有效浓度得到保证;并完成三个试剂池中干燥试剂的复溶。
89.第二步:降低离心转速,第一毛细阀1041、第二毛细阀1042以及第四毛细阀1044在
毛细力作用下完成毛细管道的填充。
90.第三步:再次启动离心,第一试剂池1021a中液体通过第一毛细阀1041进行释放,第二试剂池1022a中液体通过第二毛细阀1042填充至一级试剂池1022b中,第三试剂池1023a中液体通过第四毛细阀1044填充至二级试剂池1023b中;同理,再次降低离心转速:第三毛细阀1043、第五毛细阀1045在毛细力作用下完成毛细管道的填充,再次启动离心,一级试剂池1022b中液体通过第三毛细阀1043进行释放,二级试剂池1023b中液体通过第五毛细阀1045填充至三级试剂池1023c中;同理,再次降低离心转速,第六毛细阀1046在毛细力作用下完成毛细管道的填充,再次启动离心,三级试剂池1023c中液体通过第六毛细阀1046进行释放。可见本发明示例中的试剂控释模块100通过多次离心速度切换,实现了干燥试剂的复溶,以及复溶后的液体试剂的依次释放。
91.实施例二请参阅图3至图18,本发明公开的生物反应器,包括反应主体200和设置于反应主体200上的如上述任一项的试剂控释模块100。由于试剂控释模块100具有以上效果,包括该试剂控释模块100的生物反应器具有相应的效果,此处不再赘述。
92.需要说明的是反应主体200具有第一端面和第二端面,其中第一端面和第二端面相对布置,通常情况下,生物反应器各腔体设置在第一端面上,例如,实施例一所述的试剂控释模块100中的各试剂池均可以理解为腔体。当然,各腔体并不是绝对的设置在反应主体200的第一端面,还可根据需求设置在反应主体200的第二端面,此处不再赘述,后续将详细展开描述。
93.本发明一些可能的实施方式中,还包括设置于反应主体200上的气路模块300,气路模块300用于气相交换。气路模块300为能够导通反应主体200,通过气相交换辅助液相交换的顺利进行。上述气路模块300可以为连通各个腔室的气路、导气孔等结构。
94.本发明一些示例中,气路模块300包括设置于反应主体200上的一个端面上的平衡气室301,平衡气室301与对应的腔体连通,以实现气相交换。平衡气室301设置于反应主体200的一个端面可以理解为,平衡气室301设置于反应主体200的第一端面或者第二端面,由于反应主体200承载试剂控释模块100等,为此,将平衡气室301设置在反应主体200的一个端面上,那么对应的腔体可直接通过连通孔与平衡气室301连通,如此不需要在反应主体200上布置较长的气路,从而节省了反应主体200的体积。
95.需要说明的是,上述腔体对应反应主体200上各种腔体,例如试剂控释模块100中各个试剂池均为腔体。
96.当平衡气室301位于反应主体200的第一端面时,该气路模块300还包括导气孔,平衡气室301通过导气孔与对应的腔体连通;当平衡气室301位于反应主体200的第二端面时,该气路模块300还包括导气孔和连通孔,导气孔位于反应主体200的第一端面,并与对应的腔体连通;连通孔贯穿反应主体200,且平衡气室301通过连通孔与导气孔连通。
97.本发明一些可能的实施方式中,腔体的周边设置有密封凸台,密封凸台隔绝对应的腔体与平衡气室301。
98.以平衡气室301位于反应主体200的第二端面为例,上述连通孔和导气孔为多组,一组对应有一个腔体。
99.下面结合各模块对应介绍气路模块300的具体结构:
连通孔与导气孔为多组,且试剂存储释放单元102的数量为三个。
100.第一连通孔303a贯穿反应主体200,第一导气孔302a开设于反应主体200的第一端面,并与试剂控释模块100中溶剂存储单元101的溶剂池连通;第二连通孔303b贯穿反应主体200,第二导气孔302b开设于反应主体200的第一端面,并与试剂控释模块100中第一试剂存储释放单元1021的第一试剂池1021a连通;第三连通孔303c贯穿反应主体200,第三导气孔302c开设于反应主体200的第一端面,并与试剂控释模块100中第二试剂存储释放单元1022的一级试剂池1022b连通;第四连通孔303d贯穿反应主体200,第四导气孔302d开设于反应主体200的第一端面,并与试剂控释模块100中第三试剂存储释放单元1023的二级试剂池1023b连通;第五连通孔303e贯穿反应主体200,第五导气孔302e开设于反应主体200的第一端面,并与试剂控释模块100中第三试剂存储释放单元1023的三级试剂池1023c。
101.以上仅以试剂存储释放单元102的数量为三个为例进行介绍,当然其他数量的试剂存储释放单元102可参考试剂存储释放单元102的数量为三个的情况,此处不再赘述。另外,针对不同的生物反应器,其他模块的腔体的气路设置可参考试剂存储释放单元102的设置,此处也不做赘述。
102.生物反应器在反应过程中会产生废液,为此本发明的生物反应器还包括设置于反应主体200上用于收纳废液的液体收纳模块400,液体收纳模块400包括废液排放口401和废液收纳池402,废液排放口401连通对应的腔体与废液收纳池402。
103.本发明一些示例中,废液收纳池402可设置于反应主体200的第一端面时,废液排放口401设置于废液收纳池402的上游。本发明有一些示例中,废液收纳池402设置于反应主体200的第二端面时,废液排放口401贯穿反应主体200。使得该生物反应器所占据的空间更加紧凑,提高了集成度。
104.当废液收纳池402设置于反应主体200的第二端面时,废液排放口401与废液收纳池402衔接的部位设置有防止废液回流的回液遮挡部403。废液通过废液排放口401进入至废液收纳池402时,一旦生物反应器停止转动或者转速方向改变时,废液在回液遮挡部403的遮挡下不易回流至对应腔体中。
105.进一步的,废液收纳池402内设置有预存有能够锁水的锁水层。上述锁水层包括但不限于高分子吸水树脂、海绵和棉球。
106.需要说明的是,本发明的生物反应器可为核酸杂交反应器、固相萃取反应器、核酸提取扩增反应器或者蛋白/抗原免疫检测反应器。请参阅图3和图4,图3和图4展示的生物反应器为核酸提取扩增反应器。图示的核酸提取扩增反应器包括反应主体200和设置于反应主体200上的第一样本池501、试剂控释模块100、第一缓冲池502、第一萃取池503、第一流体控制阀504、混合池505、流体阀506、第一分配池507、第一反应池508和液体收纳模块400,其中,试剂控释模块100、第一缓冲池502、第一萃取池503、第一流体控制阀504、混合池505、流体阀506、第一分配池507和第一反应池508由近心端a至远心端b依次连通;第一样本池501与试剂控释模块100相比靠近反应主体200近心端a,并与第一缓冲池502连通;液体收纳模块400与第一流体控制阀504连通。
107.需要说明的是,图示的第一流体控制阀504是一种具有选择性通断的阀门,可以是但不限于科氏阀、旋转导通阀等;第一萃取池503的萃取材料可以是硅胶膜、玻璃纤维、磁珠等材料;流体阀506可以是机械阀、虹吸阀、爆破阀或者相变阀等;液体收纳模块400设置于
反应主体200的第二端面,以节省芯片面积。
108.请参阅图5,图5展示的生物反应器为核酸杂交反应器。图示的核酸杂交反应器包括反应主体200和设置于反应主体200上的第二样本池601、试剂控释模块100、第二缓冲池602、杂交池603、第二流体控制阀604和液体收纳模块400,其中,试剂控释模块100、第二缓冲池602、杂交池603、第二流体控制阀604和液体收纳模块400由近心端a至远心端b依次连通;第二样本池601与试剂控释模块100相比靠近反应主体200近心端a,并与第二缓冲池602连通。
109.需要说明的是,杂交池603中提前点制有核酸或者蛋白探针阵列,当目标待测物经过时,会与杂交池603中探针特异性结合,然后通过多步骤的清洗,去除未结合的物质以及杂质,从而实现特异检测。
110.请参阅图6,图6展示的生物反应器为固相萃取反应器。图示的固相萃取反应器包括反应主体200和设置于反应主体200上的第三样本池701、试剂控释模块100、第三缓冲池702、第二萃取池703、第三流体控制阀704、取样口705、收集池706和液体收纳模块400,其中,试剂控释模块100、第三缓冲池702、第二萃取池703、第三流体控制阀704和液体收纳模块400由近心端a至远心端b依次连通;第三样本池701与试剂控释模块100相比靠近反应主体200近心端a,并与第三缓冲池702连通;取样口705通过一段管道和收集池706远心端b连通,且收集池706与第三流体控制阀704连通。
111.需要说明的是,图示的第三流体控制阀704是一种具有选择性通断的阀门,可以是但不限于科氏阀、旋转导通阀等;第二萃取池703的萃取材料可以是玻璃、陶瓷、高分子化合物等材料。萃取过程完成后通过取样口705吸出目标液体。
112.请参阅图7至图18,图7展示的生物反应器为蛋白/抗原免疫检测反应器;图8至图18展示了生物反应器反应过程示意图。图示的蛋白/抗原免疫检测反应器包括反应主体200和设置于反应主体200上的第四样本池801、试剂控释模块100、第四缓冲池802、第二分配池803、第二反应池804、第四流体控制阀805和液体收纳模块400,其中,试剂控释模块100、第四缓冲池802、第二分配池803、第二反应池804、第四流体控制阀805和液体收纳模块400由近心端a至远心端b依次连通;第四样本池801与试剂控释模块100相比靠近反应主体200近心端a,并与第四缓冲池802连通。
113.通过在各个反应池中提前包被有特异性的抗体,当目标抗原出现后可以特异的结合,然后多步流体过程,实现清洗,荧光标记,再清洗等步骤,从而实现特异检测。
114.实施例三如图19至图21所示,本发明公开了一种生物检测装置,包括检测托盘900和如实施例二任一项的生物反应器,检测托盘900设置有安装生物反应器的安装槽901。由于上述生物反应器具有以上效果,包括该生物反应器的生物检测装置具有相应效果,此处不再赘述。
115.上述用于安装生物反应器的安装槽901的数量为一个或者多个,多个安装槽901对称布置于检测托盘900。
116.为了适应生物反应器的温度需求,生物检测装置还包括控制生物反应器对应部位温度的加热部件和/或制冷部件。当生物反应器对应部位需要加热时,加热部件启动,当生物反应器达到设定温度时,加热部件停止加热。加热部件为但不限于加热膜或帕尔贴;当生物反应器对应部位需要降温时,制冷部件启动,当生物反应器达到设定温度时,制冷部件停
止制冷。制冷部件为但不限于帕尔贴。
117.由于生物反应器内部存储有钢珠、磁珠或磁棒以混匀试剂和溶液,生物检测装置上设置有吸引生物反应器中预置的钢珠、磁珠或磁棒的永磁铁或电磁体。当生物检测装置运行到相应步骤时,钢珠、磁珠或磁棒在永磁铁的吸引下往复移动,从而达到混匀试剂和溶液的目的。
118.需要说明的是,为了便于描述,附图中仅示出了与有关发明相关的部分。在不冲突的情况下,本发明中的实施例及实施例中的特征可以相互组合。
119.应当理解,本发明中使用的“系统”、“装置”、“单元”和/或“模块”是用于区分不同级别的不同组件、元件、部件、部分或装配的一种方法。然而,如果其他词语可实现相同的目的,则可通过其他表达来替换该词语。
120.如本发明和权利要求书中所示,除非上下文明确提示例外情形,“一”、“一个”、“一种”和/或“该”等词并非特指单数,也可包括复数。一般说来,术语“包括”与“包含”仅提示包括已明确标识的步骤和元素,而这些步骤和元素不构成一个排它性的罗列,方法或者设备也可能包含其它的步骤或元素。由语句“包括一个
……”
限定的要素,并不排除在包括要素的过程、方法、商品或者设备中还存在另外的相同要素。
121.其中,在本发明实施例的描述中,除非另有说明,“/”表示或的意思,例如,a/b可以表示a或b;本文中的“和/或”仅仅是一种描述关联对象的关联关系,表示可以存在三种关系,例如,a和/或b,可以表示:单独存在a,同时存在a和b,单独存在b这三种情况。另外,在本发明实施例的描述中,“多个”是指两个或多于两个。
122.以下,术语“第一”、“第二”仅用于描述目的,而不能理解为指示或暗示相对重要性或者隐含指明所指示的技术特征的数量。由此,限定有“第一”、“第二”的特征可以明示或者隐含地包括一个或者更多个该特征。
123.本发明中使用了流程图用来说明根据本发明的实施例的系统所执行的操作。应当理解的是,前面或后面操作不一定按照顺序来精确地执行。相反,可以按照倒序或同时处理各个步骤。同时,也可以将其他操作添加到这些过程中,或从这些过程移除某一步或数步操作。
124.以上描述仅为本发明的较佳实施例以及对所运用技术原理的说明而已,并不用于限制本发明。对于本领域技术人员来说,本发明可以有各种更改和变化。本发明中所涉及的发明范围,并不限于上述技术特征的特定组合而成的技术方案,同时也应涵盖在不脱离上述发明构思的情况下,由上述技术特征或其等同特征进行任意组合而形成的其它技术方案。例如上述特征与本发明中公开的(但不限于)具有类似功能的技术特征进行互相替换而形成的技术方案。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1