一种5-甲基间苯二甲酸混合配体的金属有机配位化合物及其制备方法与应用与流程
1.本发明属于金属有机配位化合物技术领域,具体涉及一种5-甲基间苯二甲酸混合配体的金属有机配位化合物及其制备方法与应用。
背景技术:
2.水是人类需要的最重要的能源之一。随着全球人口和经济的快速增长,水污染已被确定为威胁水生和人类健康的主要世界性问题。特别是在许多工业过程中产生的废水中含有有毒的有机污染物,不适合直接进行生物处理,从而导致严重的环境问题。作为众多有机污染物之一,有机染料往往具有很强的化学稳定性和不可生物降解性,因此,为解决环境污染问题,探索一种经济有效的降解这些有机染料的技术一直是研究的热点。
3.近几十年来,金属-有机骨架(mofs)作为一种经典的无机-有机杂化多孔材料,由于其结构的多样性和可修饰性以及潜在的应用价值,如催化、分离、储气、传感、荧光、磁性、质子传导等。许多基于mof的活性催化剂的光催化过程可以被认为是降解有机染料的有效方法,因为这些基于mof的催化剂可以将合成的有机染料矿化成最小的组分,如co2、h2o等。然而,这些金属有机框架的一个重要先决条件是光催化剂是半导体在暴露于光照射时存在的特性。
技术实现要素:
4.有鉴于此,本发明的目的是针对现有技术中存在的问题,提供一种利用5-甲基间苯二甲酸和过渡金属作为混合配体的金属有机配位化合物。
5.为了实现上述目的,本发明采用如下技术方案:
6.一种5-甲基间苯二甲酸混合配体的金属有机配位化合物,通式为[m(l)(mipa)]n,其中,m表示金属离子,所述金属为zn或cd;l表示n-给体有机配体;mipa表示5-甲基间苯二甲酸;n表示配位数,n为整数,1≤n≤2。
[0007]
进一步的,所述n-给体有机配体为2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮。
[0008]
更进一步的,所述金属有机配位化合物包括c
39h30
znn2o5或c
39h30
cdn2o5。
[0009]
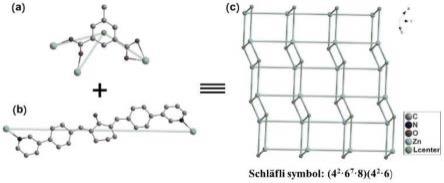
本发明通过混合使用主配体2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮及辅助配体5-甲基间苯二甲酸构建出两个新型mofs材料。是同构的化合物1[zn(l)(mipa)]n和化合物2[cd(l)(mipa)]n。通过引入双吡啶衍生物和羧酸混合配体,所述化合物1和化合物2呈现了新颖的3,5-连接的二维层状结构,其拓扑符号为(42·67
·
8)(42·
6),并且这两个化合物具有相对窄的光学带隙,从而导致了化合物在紫外光照射下具有一定的光催化降解染料的能力。
[0010]
本发明的第二个目的在于,提供所述的5-甲基间苯二甲酸混合配体的金属有机配位化合物的制备方法。
[0011]
为了实现上述目的,本发明提供如下技术方案:
[0012]
所述的5-甲基间苯二甲酸混合配体的金属有机配位化合物的制备方法,步骤包括:
[0013]
i、2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体的合成:在4-(吡啶-3-基)亚苄基加入koh溶液并溶解于乙醇中得到混合溶液,然后将环己酮乙醇溶液缓慢滴加于混合溶液中,搅拌,最后用10ml水和10ml乙醇的混合溶剂洗涤,得到2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体;
[0014]
ii、5-甲基间苯二甲酸混合配体的金属有机配位化合物的合成:将2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体、5-甲基间苯二甲酸、金属盐、n,n-二甲基甲酰胺、乙醇和水于80℃下在不锈钢反应器中加热48h,产物过滤,收集晶体,并用去离子水洗涤后干燥,得到的晶体即为所述金属有机配位化合物。
[0015]
进一步的,所述步骤ii中的金属盐为zn(no3)2·
6h2o或cd(no3)2·
4h2o。
[0016]
其中,化合物1zn-mof为黄色透明块状晶体,化合物2cd-mof为浅黄色透明块状晶体。
[0017]
进一步的,所述混合溶液中4-(吡啶-3-基)亚苄基:koh:乙醇=5mmol:4ml:30ml。
[0018]
进一步的,所述步骤i中环己酮乙醇溶液中环己酮:乙醇为2.5mmol:20ml。
[0019]
进一步的,所述步骤ii中2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体、5-甲基间苯二甲酸、金属盐的摩尔比为1:1:1,n,n-二甲基甲酰胺、乙醇和水的体积比为4:1:1,且溶剂中2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体的浓度为0.05mmol/6ml。
[0020]
本发明的第三个目的在于提供所述的5-甲基间苯二甲酸混合配体的金属有机配位化合物在染料降解方面的应用。
[0021]
进一步的,所述金属有机配位化合物作为绿色光催化剂,用于降解废水中的亚甲蓝、盐酸副玫瑰苯胺、罗丹明b、甲基橙、罗丹明6g、靛红和碱性红2。
[0022]
与现有技术相比,本发明采用混配策略,使用主配体2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮及辅助配体5-甲基间苯二甲酸构建出两个新型mofs,分别是c
39h30
znn2o5或c
39h30
cdn2o5。作为一种构筑mofs的有效策略,本发明通过引入双吡啶衍生物和羧酸混合配体,所述化合物1和化合物2呈现了新颖的3,5-连接的二维层状结构,其拓扑符号为(42·67
·
8)(42·
6),并且这两个化合物具有相对窄的光学带隙,从而导致了化合物在紫外光照射下具有一定的光催化降解染料的能力。
附图说明
[0023]
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据提供的附图获得其他的附图
[0024]
图1为本发明实验例1化合物1的拓扑简化图。
[0025]
图2为本发明实验例1化合物1的结构:(a)1的不对称单元。(b)zn2+离子的配位环境对称代码:ii,1-x,-y,2-z;vi,x-1,y-1,1+z;ⅶ,x,1+y,z。(c)梯形链。(d)二维层结构。
[0026]
图3为本发明实验例2中l的ir光谱。
[0027]
图4为本发明实验例2中mof1的ir光谱。
[0028]
图5为本发明实验例2中mof2的ir光谱。
[0029]
图6为本发明实施例3中的化合物1和化合物2的固态紫外可见漫反射(drs)谱图。
[0030]
图7为本发明实施例3中的光催化降解性能结果。
[0031]
图8为本发明实验例4中化合物1的pxrd图。
[0032]
图9为本发明实验例4中化合物2的pxrd图。
[0033]
图10为本发明实验例5中mof1的热重分析结果。
[0034]
图11为本发明实验例5中mof2的热重分析结果。
[0035]
图12为本发明实施例1公开的化合物1的核磁谱图。
[0036]
图13为本发明实施例2公开的化合物2的核磁谱图。
具体实施方式
[0037]
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0038]
在这里专用的词“实施例”,作为“示例性”所说明的任何实施例不必解释为优于或好于其它实施例。本发明实施例中性能指标测试,除非特别说明,采用本领域常规试验方法。应理解,本发明中所述的术语仅仅是为描述特别的实施方式,并非用于限制本发明公开的内容。
[0039]
除非另有说明,否则本文使用的技术和科学术语具有本发明所属技术领域的普通技术人员通常理解的相同含义;作为本发明中其它未特别注明的试验方法和技术手段均指本领域内普通技术人员通常采用的实验方法和技术手段。
[0040]
本文所用的术语“基本”和“大约”用于描述小的波动。例如,它们可以是指小于或等于
±
5%,如小于或等于
±
2%,如小于或等于
±
1%,如小于或等于
±
0.5%,如小于或等于
±
0.2%,如小于或等于
±
0.1%,如小于或等于
±
0.05%。在本文中以范围格式表示或呈现的数值数据,仅为方便和简要起见使用,因此应灵活解释为不仅包括作为该范围的界限明确列举的数值,还包括该范围内包含的所有独立的数值或子范围。例如,“1~5%”的数值范围应被解释为不仅包括1%至5%的明确列举的值,还包括在所示范围内的独立值和子范围。因此,在这一数值范围中包括独立值,如2%、3.5%和4%,和子范围,如1%~3%、2%~4%和3%~5%等。这一原理同样适用于仅列举一个数值的范围。此外,无论该范围的宽度或所述特征如何,这样的解释都适用。
[0041]
为了更好的说明本发明内容,在下文的具体实施例中给出了众多的具体细节。本领域技术人员应当理解,没有某些具体细节,本发明同样可以实施。在实施例中,对于本领域技术人员熟知的一些方法、手段、仪器、设备等未作详细描述,以便凸显本发明的主旨。
[0042]
在不冲突的前提下,本发明实施例公开的技术特征可以任意组合,得到的技术方案属于本发明实施例公开的内容。
[0043]
实施例1
[0044]
一种5-甲基间苯二甲酸混合配体的金属有机配位化合物及其制备方法:
[0045]
i、2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体的合成:准确称量并在4-(吡
啶-3-基)亚苄基(0.9g,5mmol)中加入4ml koh溶液,溶解于30ml乙醇中形成混合溶液,然后将环己酮(0.25g,2.5mmol)溶解于20ml乙醇溶液中,并缓慢滴加于混合溶液中,搅拌,最后用10ml水和10ml乙醇溶剂洗涤,得到2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体(l);
[0046]
ii、5-甲基间苯二甲酸混合配体的金属有机配位化合物的合成:将2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体(0.02g,0.05mmol)、5-甲基间苯二甲酸(0.009g,0.05mmol)、zn(no3)2·
6h2o(0.015g,0.05mmol)、dmf(4ml)、乙醇(1ml)和水(1ml)在不锈钢反应器中加热,于80℃下加热48h,产物过滤,收集晶体,并用去离子水洗涤后干燥,得到的黄色透明块状晶体即为化合物1c
39h30
znn2o5。结构表征的核磁图谱如图12所示。
[0047]
实施例2
[0048]
一种5-甲基间苯二甲酸混合配体的金属有机配位化合物及其制备方法:
[0049]
i、2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体的合成:准确称量并在4-(吡啶-3-基)亚苄基(0.9g,5mmol)中加入4ml koh溶液,溶解于30ml乙醇中形成混合溶液,然后将环己酮(0.25g,2.5mmol)溶解于20ml乙醇溶液中,并缓慢滴加于混合溶液中,搅拌,最后用10ml水和10ml乙醇溶剂洗涤,得到2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体(l);
[0050]
ii、5-甲基间苯二甲酸混合配体的金属有机配位化合物的合成:将2,6-双((e)-4-(吡啶-3-基)亚苄基)环己酮配体(0.02g,0.05mmol)、5-甲基间苯二甲酸(0.009g,0.05mmol)、cd(no3)2·
4h2o(0.0154mg,0.05mmol)、dmf(4ml)、乙醇(1ml)和水(1ml)在不锈钢反应器中加热,于80℃下加热48h,产物过滤,收集晶体,并用去离子水洗涤后干燥,得到的浅黄色透明块状晶体即为化合物2c
39h30
cdn2o5。结构表征的核磁图谱如图13所示。
[0051]
为了进一步证明本发明的有益效果以更好地理解本发明,下面通过以下测定试验进一步阐明本发明所述的系列混合配体金属有机配位化合物具有的性质及应用性能,但不可理解为对本发明的限定,对于本领域的技术人员根据上述发明内容所作的其他测定实验得到的产品性质及根据上述性质进行的应用,也视为落在本发明的保护范围内。
[0052]
实验例1
[0053]
晶体结构测定
[0054]
金属有机配位化合物mofs 1-2的x-射线粉末衍射(pxrd)数据通在oxford diffraction gemini r ultra衍射仪上收集,用经石墨单色器单色化的cu-kα射线在296k温度下以方式收集衍射数据。部分结构的衍射数据使用sadabs程序进行吸收校正。晶体结构由直接法结合差值fourier合解。所有非氢原子坐标及各向异性参数进行全矩阵最小二乘法修正,c
–
h原子的位置按理论模式计算从而确定,o-h原子首先根据差值fourier找到,然后,其氢原子坐标及各向同性参数进行全矩阵最小二乘法修正,并参与最终结构精修。
[0055]
单晶x射线衍射分析表明,化合物1和2在三斜空间群p中结晶。由于化合物1和化合物2是同构的,因此只详细讨论了化合物1的结构。化合物1的不对称单元包含一个zn
2+
离子、一个l配体和一个mipa
2-配体。zn
2+
离子与zno4n2配位环境为六配位,呈现八面体构型,由三个mipa配体的四个o原子(o2、o3ii、o4vii和o5vii)和两个l配体的两个n原子(n1vi和n2)组成。zn-o的键长范围分别为2.012至和zn-n的键长范围分别为2.162至完全去质子化的mip
2-配体的羧酸盐基团显示出螯合双齿和桥连双齿配位模式。不对称单元中
的两个六配位zn
2+
离子由两个mipa
2-配体的两个羧酸盐桥接,形成一个双核核心,其zn
…
zn距离为一个双核单元通过两个mipa
2-与两个相邻的双核单元连接,生成梯形链,配位的l配体固定在两条链之间,形成二维层状网络。相邻层通过几个经典交互进一步连接以形成3d框架(图1~2,表1~3)。通过拓扑分析得到了一个简化的网络,其中所有的mipa
2-配体可以看作是一3-连接节点,每个桥接l配体可以看作是一个连接子。因此,该框架是一个不寻常的3,5-连接网络,由topos4.0程序包26点符号为(42·67
·
8)(42·
6)。
[0056]
表1 目标化合物的晶体学参数
[0057]
[0058][0059]
表2 compound 1的选择键长和键角(
°
)
[0060][0061]
表3 compound 2的选择键长和键角(
°
)
[0062]
[0063][0064]
symmetry codes:(i)x,y-1,z;(ii)x-1,1+y,1+z;(iii)1-x,2-y,2-z;
[0065]
表明l配体在单斜空间群p21/c中结晶。不对称单元仅由一个l配体组成,相邻分子通过氢键相互作用(c16-h16a
…
n1ii和c29-h29
…
n2i)连接,并通过π
…
πiii相互作用相互堆叠质心-质心距离为形成3d超分子框架。
[0066]
实验例2
[0067]
红外性能分析
[0068]
l的ir光谱如图3所示,以3427cm-1
为中心的中宽带归因于自由水分子的o-h伸缩振动。3027cm-1
处的谱带归因于苯环的c-h伸缩振动。环己酮上ch2基团的不对称或对称伸缩带分别位于2958、2919或2834cm-1
附近。1658cm-1
处的峰归属于羰基的c=o伸缩振动。1598、1567和1551cm-1
处的峰归因于苯环和吡啶环的c=c或c=n骨架振动。1473cm-1
处的谱带归因于ch2基团的c-h面内变形振动。1157cm-1
处的峰归属于环己酮的c-c伸缩振动。而806cm-1
处的峰来自苯环的对位取代特征峰,而712cm-1
则归因于=c-h面外弯曲振动。化合物1和化合物2的ir光谱如图4~5所示,将它们与l进行比较,特征不对称和羧酸酯基团的对称伸缩振动分别在1557和1383cm-1
(对于化合物1)和1543和1377cm-1
(对于化合物2)处观察到。
[0069]
实验例3
[0070]
紫外性能分析
[0071]
将30mg化合物1或化合物2加入到含有50ml有机染料(6mg/l)的水溶液中。在打开紫外灯(100w,365nm)之前,将所得悬浮液在没有光源的情况下连续搅拌30min以建立催化剂的吸附/解吸平衡。然后,在光催化反应过程中,每1h从反应器中取出4ml溶液进行uv测量。
[0072]
为了研究光催化能力,对化合物1和化合物2进行固态紫外可见漫反射(drs)实验,通过kubelka-munk函数研究它们的带隙(eg):f=(1-r)2/2r,其中r是来自drs集合的给定波长的反射率。如图6所示,化合物1和化合物2的光吸收在310nm处表现出显着的吸收。并且化合物1和化合物2的能带能量分别为2.50ev和2.52ev,表明它们具有适合紫外光下光催化的eg。金属有机框架可用作绿色光催化剂,用于降解废水中的有机污染物。本研究选取亚甲
蓝(mb)、盐酸副玫瑰苯胺(ph)、罗丹明b(rhb)、甲基橙(mo)、罗丹明6g(rh6g)、靛红(isatin)和碱性红2(br2)作为模型污染物,研究它们在化合物1和2存在下的降解过程。
[0073]
此外,在没有催化剂的情况下监测降解过程作为对照。清楚地显示了催化剂1在mb、ph、rhb、mo、rh6g、isatin和br2染料分子溶液中的光催化效果,图7左说明了浓度比(c/c0)与照射时间(h)。mb(60.3%)、ph(71.1%)、rhb(50.9%)、mo(28.2%)、rh6g(24.9%)、isatin(19.3%)和br2(12.4%)的降解率计算为催化剂1在7小时后,催化剂1对七种染料的光催化活性顺序为:ph》mb》rhb》mo》rh6g》isatin》br2。催化剂2对七种染料的效率为如图所示,浓度比(c/c0)与照射时间(h)的线性关系如图7右所示。mb(63.5%)、ph(54.7%)、rhb(49.6%)、mo(31.9%)、rh6g(29.7%)、isatin(17.0%)、br2(10.5%)的降解率计算为7h后化合物2,化合物2对上述染料的光催化活性顺序为mb》ph》rhb》mo》rh6g》isatin。
[0074]
实验例4
[0075]
粉末x射线衍射(pxrd)
[0076]
化合物1和化合物2粉末x射线衍射(pxrd)谱图的实验结果与模拟结果基本一致,表明化合物1和化合物2的块状产品具有高相纯度。为了证明两种mof具有良好的化学稳定性,将它们浸泡在不同的溶剂(如meoh、mecn、dmf、etoh和水)中7天后记录pxrd图。如图所示,化合物1(图8)和化合物2(图9)都显示出在常见溶剂中的高稳定性。同时,化合物1和化合物2的骨架也可以在ph=2-13的水溶液中保留3天,这充分证明了这两种mof都具有很好的耐酸碱性。
[0077]
实验例5
[0078]
热重分析(tga)
[0079]
mofs 1和2的tga实验于氮气气氛下在sdt 2960差热分析仪上进行,升温速率为10℃
·
min-1
。溶液的uv-vis测量在thermo ev 201cp上进行。如图10(mofs 1)和图11(mofs 2)所示,它们显示出高热稳定性和相同的一步热分解行为。随着温度分别升至350℃(1)和360℃(2),由于有机配体的分解,mofs 1和mofs 2的骨架开始坍塌。这进一步证明了化合物1和化合物2的同构性质的证据。
[0080]
对所公开的实施例的上述说明,使本领域专业技术人员能够实现或使用本发明。对这些实施例的多种修改对本领域的专业技术人员来说将是显而易见的,本文中所定义的一般原理可以在不脱离本发明的精神或范围的情况下,在其它实施例中实现。因此,本发明将不会被限制于本文所示的这些实施例,而是要符合与本文所公开的原理和新颖特点相一致的最宽的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1