一种牛蒡子苷元衍生物、制备方法及应用
1.本发明化合物技术领域,具体涉一种牛蒡子苷元衍生物、制备方法及应用。
背景技术:
2.炎症作为严重威胁到人类健康的一种常见病和多发病,多种外界刺激以及细菌感染均可导致机体发生炎症反应。它通过促进细胞因子,趋化因子和急性期蛋白的产生并协调转运等一系列步骤,使免疫系统细胞迁移至刺激靶点。一方面炎症快速应答可保护机体,清除伤害性刺激使创伤部位逐渐恢复原状。另一方面,过度的炎症反应和慢性炎症会导致组织损伤和纤维化,因此,它与多种疾病密切相关。
3.同时,在治疗炎症反应中,最初使用的最多的是可以良好的控制炎症并且能高效地消除炎症反应引起的机体功能性障碍的糖皮质激素类固醇类。抗炎药物中有一些皮质类固醇等甾体抗炎药物,价格昂贵之外可能还会引起机体的几种不利影响,如可引起机体肾上腺皮质功能障碍以及器官性骨质疏松等并发症。非甾体类抗炎药是最早从含水杨酸的植物中提取出来的一类具有镇痛、解热、抗炎作用的药物,非留体类抗炎药的抗炎作用机制是通过抑制机体环氧化酶活性,进一步来抑制机体局部前列腺素的产生,从而发挥抗炎药理作用。自古以来,很多人患有炎症的病人会用植物中的化学物质来处理,这一事实从阿司匹林的发现中可以看出,这时在抗炎研究中具有生物活性的天然产物以及他的修饰是值得关注的。
技术实现要素:
4.针对现有技术的不足,本发明旨在提供一种牛蒡子苷元衍生物、制备方法及应用。
5.为了实现上述目的,本发明采用如下技术方案:
6.一种牛蒡子苷元衍生物,其特征在于,所述牛蒡子苷元衍生物的结构式如下:
[0007][0008]
其中,所述牛蒡子苷元衍生物的分子式为:c
31h32
fn3o7;分子量为:577.61。
[0009]
需要说明的是,本发明的牛蒡子苷元衍生物名称为:
[0010]
2-(2-(4-(((3r,4r)-4-(3,4-dimethoxybenzyl)-2-oxotetrahydrofuran-3-yl)methyl)-2-methoxyphenoxy)ethyl)-4-(4-fluorophenyl)-2,4-dihydro-3h-1,2,4-triazol-3-one。简称:c2。
[0011]
本发明还提供一种牛蒡子苷元衍生物的制备方法,所述方法包括以下步骤:
[0012]
s1将4-氟苯胺(1.11g,0.01mol),肼基甲酸甲酯(1.45g,0.015mol),原甲酸三乙酯(2.22g,0.015mol),乙醇(25ml)置于圆底烧瓶中,78℃搅拌48小时;接着加入甲醇钠(0.81g,0.015mol)在78℃回流24h;将反应物倒入冰水中搅拌,析出大量白色固体,抽滤烘干得到中间体a;
[0013]
s2中间体a(100mg,0.56mmol)和1,2-二溴乙烷(209mg,1.11mmol),k2co3(231mg,1.68mmol)在dmf(5ml)中60℃搅拌4h;用tlc测试反应完全后,用etoac萃取3次,有机相用饱和氯化钠溶液洗涤,洗涤2次,用适量的无水na2so4干燥,减压过滤旋干,得到粗产物b;
[0014]
s3再称取牛蒡子苷元(50mg,0.11mmol),中间体b(135mg,0.13mmol)加入k2co3(41.4mg,0.30mmol)和dmf(5ml),全部置于25ml的圆底烧瓶中,在60℃的剧烈搅拌下过夜反应。用tlc测试反应完全后,用etoac萃取3次,有机相用饱和碳酸氢钠溶液和盐水洗涤,洗涤2次,用适量的无水na2so4干燥,减压过滤旋干,得到粗产物。用硅胶色谱法进行纯化,得到化合物c
31h32
fn3o7。
[0015]
需要说明的是,上述制备过程的反应式如下:
[0016][0017]
本发明还提供一种牛蒡子苷元衍生物的应用,所述牛蒡子苷元衍生物可用于抗炎药物的成分之一。
[0018]
本发明有益效果在于:
[0019]
提供了一种新的化合物—牛蒡子苷元衍生物,体外毒性实验表明,化合物在100μm没有毒性。体外抗炎症活性实验表明,该化合物在30μm显著的减少了lps诱导的raw264.7细胞释放no,抑制率达38.01%,且抑制能力显著优于先导化合物牛蒡子苷元(抑制率为21.41%),可以有效抑制lps诱导的巨噬细胞炎症反应,用于抗炎药物制备领域。本发明化合物的制备方法具有反应过程操作简单,反应条件温和,所用试剂便宜易得的优点。
附图说明
[0020]
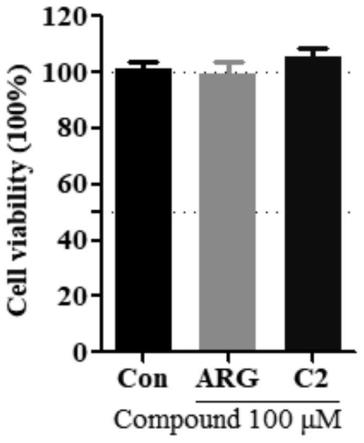
图1为牛蒡子苷元(arg)和化合物c2在100μm浓度下对小白鼠巨噬细胞(raw264.7)的细胞存活率影响;
[0021]
图2为牛蒡子苷元(arg)和化合物c2对lps诱导的raw264.7细胞no释放的抑制作用。
具体实施方式
[0022]
以下将对本发明作进一步的描述,需要说明的是,以下实施例以本技术方案为前提,给出了详细的实施方式和具体的操作过程,但本发明的保护范围并不限于本实施例。
[0023]
实施例
[0024]
本发明的牛蒡子苷元衍生物的制备方法如下:
[0025]
s1将4-氟苯胺(1.11g,0.01mol),肼基甲酸甲酯(1.45g,0.015mol),原甲酸三乙酯(2.22g,0.015mol),乙醇(25ml)置于圆底烧瓶中,78℃搅拌48小时;接着加入甲醇钠(0.81g,0.015mol)在78℃回流24h;将反应物倒入冰水中搅拌,析出大量白色固体,抽滤烘干得到中间体a;
[0026]
s2中间体a(100mg,0.56mmol)和1,2-二溴乙烷(209mg,1.11mmol),k2co3(231mg,1.68mmol)在dmf(5ml)中60℃搅拌4h;用tlc测试反应完全后,用etoac萃取3次,有机相用饱和氯化钠溶液洗涤,洗涤2次,用适量的无水na2so4干燥,减压过滤旋干,得到粗产物b;
[0027]
s3再称取牛蒡子苷元(50mg,0.11mmol),中间体b(135mg,0.13mmol)加入k2co3(41.4mg,0.30mmol)和dmf(5ml),全部置于25ml的圆底烧瓶中,在60℃的剧烈搅拌下过夜反应。用tlc测试反应完全后,用etoac萃取3次,有机相用饱和碳酸氢钠溶液和盐水洗涤,洗涤2次,用适量的无水na2so4干燥,减压过滤旋干,得到粗产物。用硅胶色谱法进行纯化,得到化合物c
31h32
fn3o7。
[0028]
所述牛蒡子苷元衍生物的结构式如下:
[0029][0030]
c2核磁共振数据如下:yield 83%.1h-nmr(300mhz,cdcl3)δ:7.67(s,1h,triazolone-h),7.53(s,2h,ar-h),7.19(t,j=9hz,2h,ar-h),6.89(t,j=9hz,1h,ar-h),6.78-6.64(m,3h,ar-h),6.58-6.48(m,2h,ar-h),4.38-4.10(m,5h),3.84(t,j=9hz,10h),2.95(s,2h),2.71-2.51(m,4h).
13
c-nmr(75mhz,cdcl3)δ:178.63,151.70,150.04,149.03,147.87,146.69,133.39,132.92,132.78(2c),131.68,130.39,123.26(2c),121.46,121.12,120.55,114.88,113.31,111.85,111.37,71.21,66.47,56.08,56.00,55.92,46.54,45.07,41.11,38.16,34.51.
[0031]
通过以下实施例进一步验证本发明的具备抗炎能力。
[0032]
实施例2
[0033]
药物组合物
[0034]
每片含100mg活性成分的1000片片剂配方:
[0035]
化合物c2 100g
[0036]
羟丙基纤维素 2g
[0037]
小麦淀粉 10g
[0038]
乳糖 100g
[0039]
硬质酸镁 3g
[0040]
滑石 3g
[0041]
所用剂量应适应与疾病的性质和严重程度,给药途径以及患者的年龄和体重。日剂量在0.1mg-1.0g之间变化,而且可以一次或数次给药。
[0042]
实施例3
[0043]
采用mtt法通过观察的细胞活力分析评估牛蒡子苷元(arg)及牛蒡子苷元衍生物c2在100μm浓度下对raw264.7细胞的毒性。
[0044]
实验材料:培养箱(美国thermo公司)、小白鼠巨噬细胞(raw264.7)细胞株(美国atcc公司)、dmem培养基、胎牛血清(fbs)、青霉素、链霉素、mtt(美国sigma公司)。
[0045]
实验方法:将raw264.7巨噬细胞以1
×
104细胞/孔的密度接种在96孔板中的完全培养基中,待细胞贴壁后,分别用牛蒡子苷元和衍生物c2(100μm)预处理细胞24小时后,弃去培养液,加入mtt溶液,终浓度为2mg/ml,避光,继续孵育4h,取出mtt溶液,再加入150μl dmso溶解,摇床震荡10min,在波长为492nm的酶标仪(elx 800,biotek,highland park,winooski,vt,usa)上读取光密度(od),然后分析数据。
[0046]
实验结果:在100μm浓度下,牛蒡子苷元及其衍生物c2无明显细胞毒性。
[0047]
实施例4
[0048]
通过构建lps诱导的raw264.7细胞模型,采用griess法检测合物对no释放量的影响来评价化合物的抗炎活性。
[0049]
实验材料:培养箱(美国thermo公司)、小白鼠巨噬细胞(raw264.7)细胞株(美国atcc公司)、dmem培养基、胎牛血清(fbs)、青霉素、链霉素(美国sigma公司),griess试剂盒(碧云天生物技术有限公司)。
[0050]
实验方法:将raw264.7小鼠巨噬细胞接种在24孔板上,密度为3
×
105至5
×
105细胞/孔,将接种过细胞的24孔板置于细胞培养箱中孵育12小时。吸除原培养基,实验组加入溶解牛蒡子苷元或衍生物c2(30μm)的dmem培养基,剩余组加入等体积的空白dmem培养基,预处理1小时后,模型组和实验组加入含有lps(0.5μg/ml)的dmem培养基,空白组给予相同体积的空白dmem培养基,孵育24小时,收集培养上清液,使用griess法,参照试剂盒附带说明书逐步操作,最终测定并计算no含量。
[0051]
实验结果:化合物c2可显著减少lps诱导的raw264.7细胞释放no。与同浓度(30μm)的先导化合物牛蒡子苷元(arg)相比,化合物c2的抑制能力明显增强。说明化合物c2可以有效抑制lps诱导的巨噬细胞炎症反应。
[0052]
对于本领域的技术人员来说,可以根据以上的技术方案和构思,给出各种相应的改变和变形,而所有的这些改变和变形,都应该包括在本发明权利要求的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1