一种化合物及其制备方法以及氧化损伤修护上的应用与流程
1.本发明涉及有机合成技术领域,尤其是涉及一种化合物及其制备方法以及氧化损伤修护上的应用。
背景技术:
2.4-羟基肉桂酸做为一种天然化合物是木质素的主要成分,具备一定的抗氧化活性,由于具备亲水性的酚羟基及羧基,其脂溶性较差。
3.自由基和活性氧是重要的生物活性物质,在生物体系中,氧化损伤不仅存在,而且自由基和活性氧导致的氧化损伤在许多疾病发生和发展中发挥十分重要的作用。
4.从某种角度来看,人体几乎所有的器官确实会受到氧化应激带来的伤害,如疲倦、全身无力、机头和关节痛等。由氧化应激水平升高又发的常见疾病有心脏病,癌症等。
5.但是过去采用抗氧化手段没有获得特别有效的效果,因此,提供一种新的分子结构,以期望在提升脂溶性同时提升化合物的抗氧化能力是非常必要的。
技术实现要素:
6.有鉴于此,本发明要解决的技术问题在于提供一种化合物,本发明提供的化合物在提升脂溶性同时提升化合物的抗氧化能力。
7.本发明提供了一种式(i)结构的化合物,
[0008][0009]
其中,r为c2~c9的烷烃。
[0010]
本发明提供了一种式(i)结构的化合物的制备方法,包括如下步骤:
[0011]
a)fmoc-l-蛋氨酸、c2~c9烷烃醇在催化剂、溶剂和缚酸剂的作用下反应,得到反应产物;
[0012]
b)将所述反应产物和二乙胺混合反应,纯化,蒸馏,得到第一中间体;
[0013]
c)将所述第一中间体、对羟基肉桂酸在催化剂、溶剂和缚酸剂的作用下反应,将反应产物萃取、洗涤、干燥、纯化即得。
[0014]
优选的,所述催化剂为hobt和edci;所述hobt和edci的摩尔比为(1.0~1.5):(1.2~1.8);
[0015]
所述缚酸剂为三乙胺;所述溶剂为二氯甲烷。
[0016]
优选的,所述fmoc-l-蛋氨酸、c2~c9烷烃醇、催化剂和缚酸剂的摩尔比为:1:(1.0~1.5):(2.0~3.3):2。
[0017]
优选的,步骤a)所述反应温度为20~30℃,反应时间为8~12h;
[0018]
所述反应后还包括加入饱和碳酸氢钠水溶液萃取,收集有机相,有机相再用饱和nacl水溶液洗涤,无水硫酸钠干燥。
[0019]
优选的,步骤b)所述反应产物和二乙胺的体积比为1:0.1~0.2;所述反应温度为20~30℃,反应时间为6~8h;所述纯化为硅胶柱纯化。
[0020]
优选的,步骤c)所述第一中间体:对羟基肉桂酸:催化剂:三乙胺的摩尔比为1:(1.0~1.5):(2.2~3.3):2。
[0021]
优选的,步骤c)所述反应温度为10~15℃,反应时间为6~8h;
[0022]
所述反应后还包括加入饱和碳酸氢钠水溶液萃取,再用饱和nacl水溶液洗涤,无水硫酸钠干燥、硅胶柱纯化、减压浓缩。
[0023]
本发明提供了所述的式(i)结构的化合物或上述技术方案所述的制备方法制备得到的式(i)结构的化合物在制备抗氧化损伤产品中的应用。
[0024]
本发明提供了一种抗氧化损伤产品,包括本发明上述技术方案所述的式(i)结构的化合物或上述技术方案所述的制备方法制备得到的式(i)结构的化合物。
[0025]
与现有技术相比,本发明提供了一种式(i)结构的化合物,其中,r为c2~c9的烷烃。本发明上述结构的化合物在脂溶性好同时抗氧化能力强。特别对于双氧水损伤的细胞有较好的修护效果,相较于对羟基肉桂酸亦有着显著性差异。
附图说明
[0026]
图1实施例3nmr氢谱;
[0027]
图2实施例3nmr碳谱;
[0028]
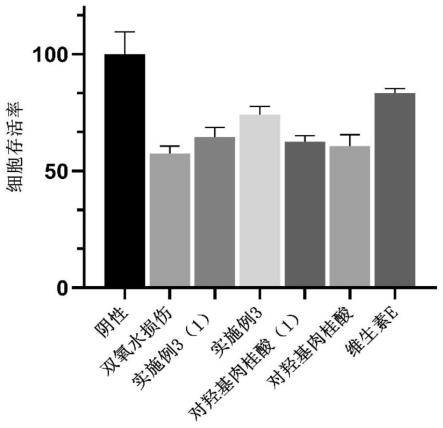
图3为实施例3的细胞活力百分比图。
具体实施方式
[0029]
本发明提供了一种化合物及其制备方法以及氧化损伤修护上的应用,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都属于本发明保护的范围。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
[0030]
本发明提供了一种式(i)结构的化合物,
[0031][0032]
其中,r为c2~c9的烷烃。具体可以为乙烷、丙烷、丁烷、戊烷、己烷、庚烷、辛烷、壬烷。
[0033]
按照本发明,所述式(i)结构的化合物具体为为式(i-1)~式(i-4)
[0034][0035][0036]
本发明提供了一种式(i)结构的化合物的制备方法,包括如下步骤:
[0037]
a)fmoc-l-蛋氨酸、c2~c9烷烃醇在催化剂、溶剂和缚酸剂的作用下反应,得到反应产物;
[0038]
b)将所述反应产物和二乙胺混合反应,纯化,蒸馏,得到第一中间体;
[0039]
c)将所述第一中间体、对羟基肉桂酸在催化剂、溶剂和缚酸剂的作用下反应,将反应产物萃取、洗涤、干燥、纯化即得。
[0040]
本发明提供的式(i)结构的化合物的制备方法首先将fmoc-l-蛋氨酸、c2~c9烷烃醇在催化剂、溶剂和缚酸剂的作用下反应,得到反应产物;
[0041]
本发明所述催化剂为hobt和edci;所述hobt和edci的摩尔比优选为(1.0~1.5):(1.2~1.8);更优选为(1.1~1.4):(1.3~1.7);所述缚酸剂为三乙胺;所述溶剂为二氯甲烷。
[0042]
按照本发明,所述fmoc-l-蛋氨酸、c2~c9烷烃醇、催化剂和缚酸剂的摩尔比优选
为:1:(1.0~1.5):(2.0~3.3):2;更优选为1:(1.1~1.4):(2.4~3.1):2。
[0043]
本发明所述反应温度为20~30℃,反应时间为8~12h;更优选为22~28℃,反应时间为9~11h。
[0044]
tlc跟检,所述反应后还包括加入饱和碳酸氢钠水溶液萃取,收集有机相,有机相再用饱和nacl水溶液洗涤,无水硫酸钠干燥。
[0045]
将所述反应产物和二乙胺混合反应,纯化,蒸馏,得到第一中间体。
[0046]
将上述得到的有机溶液置于反应瓶中,加入二乙胺溶液,控制温度在反应,硅胶柱纯化,减压蒸馏得到第一中间体。
[0047]
本发明所述反应产物和二乙胺的体积比为1:0.1~0.2;所述反应温度为20~30℃,反应时间为6~8h;tlc检测反应,所述纯化为硅胶柱纯化。
[0048]
本发明对于所述硅胶柱纯化和减压蒸馏不进行限定,本领域技术人员熟知的即可。
[0049]
将所述第一中间体、对羟基肉桂酸在催化剂、溶剂和缚酸剂的作用下反应。
[0050]
本发明所述催化剂为hobt和edci;所述hobt和edci的摩尔比优选为(1.0~1.5):(1.2~1.8);更优选为(1.1~1.4):(1.3~1.7);所述缚酸剂为三乙胺;所述溶剂为二氯甲烷。
[0051]
按照本发明,所述第一中间体:对羟基肉桂酸:催化剂:三乙胺的摩尔比优选为1:(1.0~1.5):(2.2~3.3):2;更优选为1:(1.1~1.4):(2.4~3.1):2。
[0052]
本发明所述反应温度优选为10~15℃,反应时间为6~8h;更优选的反应温度为11~14℃,反应时间为6~8h。
[0053]
tlc监测反应,反应完全后,还包括加入饱和碳酸氢钠水溶液萃取,再用饱和nacl水溶液洗涤,无水硫酸钠干燥、硅胶柱纯化、减压浓缩。本发明对于所述硅胶柱纯化和减压蒸馏不进行限定,本领域技术人员熟知的即可。
[0054]
本发明提供了所述的式(i)结构的化合物或上述技术方案所述的制备方法制备得到的式(i)结构的化合物在制备抗氧化损伤产品中的应用。
[0055]
本发明所述氧化损伤可以为双氧水损伤。
[0056]
本发明提供了一种抗氧化损伤产品,包括本发明上述技术方案所述的式(i)结构的化合物或上述技术方案所述的制备方法制备得到的式(i)结构的化合物。
[0057]
本发明对于上述具体化合物和具体制备方法已经有了清楚的描述,在此不再赘述。
[0058]
本发明提供了一种式(i)结构的化合物,其中,r为c2~c9的烷烃。本发明上述结构的化合物在脂溶性好同时抗氧化能力强。特别对于双氧水损伤的细胞有较好的修护效果,相较于对羟基肉桂酸亦有着显著性差异。
[0059]
本发明人发现,本发明的式(i)结构的化合物在dpph自由基清除测试效果上均有良好的提升;
[0060]
本发明人发现,本发明的式(i)结构的化合物对双氧水损伤的hacat细胞有较好的修护效果,相较于对羟基肉桂酸亦有着显著性差异。
[0061]
为了进一步说明本发明,以下结合实施例对本发明提供的一种化合物及其制备方法以及氧化损伤修护上的应用进行详细描述。
[0062]
实施例1
[0063][0064]
反应步骤1:称取1gfmoc-l-蛋氨酸(1.0equiv)、0.24g正丁醇(1.2equiv)和0.43g hobt(1.2equiv)分散在30ml二氯甲烷溶液中,搅拌条件下加入0.78g edci(1.5equiv)与20ml二氯甲烷的混合溶液,最后加入0.55g(2.0equiv)三乙胺,室温下反应,tlc跟检,反应完成后,加入100ml饱和碳酸氢钠水溶液萃取,收集有机相,有机相再用饱和nacl水溶液洗涤,收集有机相,无水硫酸钠干燥后,直接进入下一步反应
[0065]
反应步骤2:将反应1得到的有机溶液置于250ml反应瓶中,加入5ml二乙胺溶液,tlc检测反应,反应完全后,硅胶柱纯化,减压蒸馏有机溶剂得到中间体1,
[0066]
反应步骤3:分别取0.5g中间体1(1.0equiv)、0.48g对羟基肉桂酸(1.2equiv)和0.39g hobt(1.2equiv)分散在30ml二氯甲烷溶液中,控制温度在10-15℃搅拌,达到温度后,加入0.7gedci(1.5equiv)与20ml二氯甲烷得混合溶液以及0.49g三乙胺(2.0equiv),tlc监测反应,反应完全后,加入100ml饱和碳酸氢钠溶液搅拌,萃取分离后再用50ml饱和碳酸氢钠溶液萃取,收集有机相,最后再用饱和氯化钠溶液洗涤萃取,有机相经无水硫酸钠干燥后减压蒸馏得到目标化合物,合并收率:65%。1h nmr(400mhz,dmso-d6)δ9.97(s,1h),8.41(s,1h),7.42(d,j=8.4hz,2h),7.35(d,j=15.7hz,1h),6.80(d,j=8.3hz,2h),6.48(d,j=15.8hz,1h),4.48(dd,j=14.8,6.7hz,1h),4.14-3.99(m,2h),2.57-2.48(m,2h),2.05(s,5h),1.61-1.47(m,2h),1.32(q,j=7.3hz,2h),0.87(t,j=7.4hz,3h).
13
c nmr(101mhz,dmso)δ172.51,166.19,159.47,140.13,129.83,126.17,118.15,116.25,64.69,51.69,31.05,30.58,30.02,19.00,14.96,13.98.ec-ms[m+h]:352.1504
[0067]
实施例2
[0068][0069]
反应步骤1:称取1gfmoc-l-蛋氨酸(1.0equiv)、0.33g正己醇(1.2equiv)和0.43g hobt(1.2equiv)分散在30ml二氯甲烷溶液中,搅拌条件下加入0.78g edci(1.5equiv)与20ml二氯甲烷的混合溶液,最后加入0.55g(2.0equiv)三乙胺,室温下反应,tlc跟检,反应
完成后,加入100ml饱和碳酸氢钠水溶液萃取,收集有机相,有机相再用饱和nacl水溶液洗涤,收集有机相,无水硫酸钠干燥后,直接进入下一步反应
[0070]
反应步骤2:将反应1得到的有机溶液置于250ml反应瓶中,加入5ml二乙胺溶液,tlc检测反应,反应完全后,硅胶柱纯化,减压蒸馏有机溶剂得到中间体1,
[0071]
反应步骤3:分别取0.5g中间体1(1.0equiv)、0.43g对羟基肉桂酸(1.2equiv)和0.35g hobt(equiv)分散在30ml二氯甲烷溶液中,控制温度在10-15℃搅拌,达到温度后,加入0.62gedci(1.5equiv)与20ml二氯甲烷得混合溶液以及0.44g三乙胺(2.0equiv),tlc监测反应,反应完全后,加入100ml饱和碳酸氢钠溶液搅拌,萃取分离后再用50ml饱和碳酸氢钠溶液萃取,收集有机相,最后再用饱和氯化钠溶液洗涤萃取,有机相经无水硫酸钠干燥后减压蒸馏得到目标化合物,合并收率:67%。1h nmr(400mhz,dmso-d6)δ9.91(s,1h),8.39(d,j=7.5hz,1h),7.41(d,j=8.6hz,2h),7.35(d,j=15.8hz,1h),6.80(d,j=8.6hz,2h),6.46(s,1h),4.60-4.36(m,1h),4.15
–
3.93(m,2h),2.51(tq,j=4.6,2.6hz,2h),2.05(s,5h),1.66-1.46(m,2h),1.28(dd,j=21.8,4.8hz,6h),0.92-0.75(m,3h).
13
c nmr(101mhz,dmso)δ172.46,166.19,159.11,140.13,129.79,125.82,118.15,116.23,64.95,51.79,31.27,31.08,30.04,27.96,25.44,22.47,14.95,14.26.ec-ms[m+h]:380.1817。
[0072]
实施例3
[0073][0074]
反应步骤1:称取1gfmoc-l-蛋氨酸(1.0equiv)、0.42g正辛醇(1.2equiv)和0.43g hobt(1.2equiv)分散在30ml二氯甲烷溶液中,搅拌条件下加入0.78g edci(1.5equiv)与20ml二氯甲烷的混合溶液,最后加入0.55g(2.0equiv)三乙胺,室温下反应,tlc跟检,反应完成后,加入100ml饱和碳酸氢钠水溶液萃取,收集有机相,有机相再用饱和nacl水溶液洗涤,收集有机相,无水硫酸钠干燥后,直接进入下一步反应
[0075]
反应步骤2:将反应1得到的有机溶液置于250ml反应瓶中,加入5ml二乙胺溶液,tlc检测反应,反应完全后,硅胶柱纯化,减压蒸馏有机溶剂得到中间体1,
[0076]
反应步骤3:分别取0.5g中间体1(1.0equiv)、0.38g对羟基肉桂酸(1.2equiv)和0.31g hobt(equiv)分散在30ml二氯甲烷溶液中,控制温度在10-15℃搅拌,达到温度后,加入0.55gedci(1.5equiv)与20ml二氯甲烷得混合溶液以及0.39g三乙胺(2.0equiv),tlc监测反应,反应完全后,加入100ml饱和碳酸氢钠溶液搅拌,萃取分离后再用50ml饱和碳酸氢钠溶液萃取,收集有机相,最后再用饱和氯化钠溶液洗涤萃取,有机相经无水硫酸钠干燥后减压蒸馏得到目标化合物,合并收率:70%。1h nmr(400mhz,dmso-d6)δ9.89(s,1h),8.39(d,j=7.5hz,1h),7.41(d,j=8.7hz,2h),7.35(d,j=15.7hz,1h),6.80(d,j=8.6hz,2h),6.48(d,j=15.7hz,1h),4.47(dd,j=13.9,7.6hz,1h),4.18-3.93(m,2h),2.53-2.49(m,
2h),2.05(s,5h),1.55(q,j=6.7hz,2h),1.33
–
1.12(m,10h),0.84(d,j=6.7hz,3h).
13
c nmr(101mhz,dmso)δ172.45,166.17,159.49,140.11,129.77,126.17,118.13,116.22,64.93,51.73,31.65,31.07,30.04,29.11,29.05,28.54,25.80,22.54,14.96,14.36.ec-ms[m+h]:408.2130
[0077]
实施例4
[0078][0079]
反应步骤1:称取1gfmoc-l-蛋氨酸(1.0equiv)、0.42g异辛醇(1.2equiv)和0.43g hobt(1.2equiv)分散在30ml二氯甲烷溶液中,搅拌条件下加入0.78g edci(1.5equiv)与20ml二氯甲烷的混合溶液,最后加入0.55g(2.0equiv)三乙胺,室温下反应,tlc跟检,反应完成后,加入100ml饱和碳酸氢钠水溶液萃取,收集有机相,有机相再用饱和nacl水溶液洗涤,收集有机相,无水硫酸钠干燥后,直接进入下一步反应
[0080]
反应步骤2:将反应1得到的有机溶液置于250ml反应瓶中,加入5ml二乙胺溶液,tlc检测反应,反应完全后,硅胶柱纯化,减压蒸馏有机溶剂得到中间体1,
[0081]
反应步骤3:分别取0.5g中间体1(1.0equiv)、0.38g对羟基肉桂酸(1.2equiv)和0.31g hobt(equiv)分散在30ml二氯甲烷溶液中,控制温度在10-15℃搅拌,达到温度后,加入0.55gedci(1.5equiv)与20ml二氯甲烷得混合溶液以及0.39g三乙胺(2.0equiv),tlc监测反应,反应完全后,加入100ml饱和碳酸氢钠溶液搅拌,萃取分离后再用50ml饱和碳酸氢钠溶液萃取,收集有机相,最后再用饱和氯化钠溶液洗涤萃取,有机相经无水硫酸钠干燥后减压蒸馏得到目标化合物,合并收率:66%。1h nmr(400mhz,dmso-d6)δ9.91(s,1h),8.40(d,j=7.5hz,1h),7.41(d,j=8.6hz,2h),7.35(d,j=15.8hz,1h),6.80(d,j=8.5hz,2h),6.48(d,j=15.7hz,1h),4.49(td,j=8.3,5.1hz,1h),4.01(ddd,j=11.0,5.7,2.0hz,1h),2.61-2.46(m,3h),2.05(s,3h),2.02-1.86(m,2h),1.59-1.42(m,1h),1.42-1.06(m,9h),0.89-0.78(m,6h).
13
c nmr(101mhz,dmso)δ173.02,166.16,159.46,140.05,129.78,126.19,118.17,116.24,66.92,51.11,38.62,31.00,30.22,30.02,28.72,23.61,22.90,14.91,14.35,11.28.ec-ms[m+h]:408.2075
[0082]
实施例5实施例1-4与对羟基肉桂酸的dpph实验
[0083]
dpph实验按照标准规程进行,首先配置好的0.1mm的dpph溶液及待测母液,采用96孔板孵育,每个浓度设三组,每组设3个复孔。上板(避光操作,将配置的溶液按figure 1中的分布和比例加入96孔板中,室温下避光孵育30分钟,并测定吸光度)。测试结果如下:
[0084][0085]
从测试结果可以看出,实施例1至4相较于对照(对羟基肉桂酸)在dpph自由基清除测试效果上均有良好的提升,其中实施例3相较于对照提升了接近4倍。
[0086]
实施例6
[0087]
实施例3与对羟基肉桂酸的抗双氧水损伤实验
[0088]
1、培养基及溶液配制
[0089]
(1)dmem高糖培养基:将一袋dmem高糖培养基粉末加至800ml纯化水中搅拌溶解,后加入nahco33.7g继续搅拌至粉末完全溶解,调ph至7.1-7.2后定容至1l,用0.22μm过滤器过滤除菌后密封放于4℃保存
[0090]
(2)dmem高糖完全培养基:向dmem高糖培养基中加入fbs使其含量为10%
[0091]
(3)mtt溶液(5mg
·
ml-1
):避光条件下,将50mgmtt粉末溶于10ml1
×
pbs缓冲液中,置于60℃水浴中助溶,0.22μm过滤器过滤除菌后置于-20℃避光保存
[0092]
2、抗氧化损伤功效检测
[0093]
(1)人永生化角质形成细胞(hacat)接种:将细胞悬液密度调整至10000个/ml后接种于96孔板,100μl/孔,置于37℃,5%co2培养箱中培养24h
[0094]
(2)实验分组:设置阴性对照组(nc)、双氧水损伤组(pc)、维e组和样品组。样品组中每组样品设定两组浓度分别为12.5μg/ml,25μg/ml,各组均设6个复孔。
[0095]
(3)h2o2诱导损伤:弃去旧培养基,加入h2o2(50μg/ml)pbs溶液,100μl/孔,阴性对照组加入等量pbs,置于37℃,5%co2培养箱内培养4h后弃去
[0096]
(4)待测样品稀释与加样:以完全培养基为稀释液,按照样品试验浓度表配制不同浓度的样品工作液,100μl/孔,阴性对照组和阳性对照组加等量完全培养基,置于37℃,5%co2培养箱内培养24h后在显微镜下观察细胞形态
[0097]
(4)mtt检测:在避光条件下,每孔加入10μlmtt溶液(5mg
·
ml-1),将96孔板置于37℃,5%co2培养箱内充分反应4h后弃去孔板内上清液,加入dmso,150μl/孔,震荡溶解10min,使用酶标仪检测各孔570nm处吸光度值,以630nm为参考波长
[0098]
(5)计算:各组吸光度值减去本底吸收后,以细胞对照组吸光度值为100%,计算各浓度加样组细胞的细胞活力百分比,计算公式如下:
[0099]
细胞活力百分比(%)=样品孔平均od值/阴性对照组平均od值
×
100%。相关实验结果如图3所示:(实施例3(1):12.5μg/ml,实施例3:25μg/ml;对羟基肉桂酸(1):12.5μg/ml,对羟基肉桂酸:25μg/ml。)
[0100]
从实验结果可以看出,实施例3对双氧水损伤的hacat细胞有较好的修护效果,相较于对羟基肉桂酸亦有着显著性差异。
[0101]
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应
视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1