一种视网膜色素上皮细胞的扩增培养基及培养方法
1.本技术涉及视网膜色素上皮细胞培养技术,具体涉及一种视网膜色素上皮细胞的培养基及培养方法。具体地,本技术涉及含有myosin ii atpase抑制剂的培养基,含有所述myosin ii atpase抑制剂的试剂盒、试剂组合,以及使用所述培养基培养视网膜色素上皮细胞的方法。
背景技术:
2.干性年龄相关性黄斑变性(amd)是由视网膜色素上皮(rpe)细胞退化或者损伤引起的,是老年人致盲的主要原因之一,据不完全统计,该疾病严重影响着世界3-5千万人的生活质量,且不能通过传统的药物或者手术的方法得到有效治疗。
3.临床研究表明rpe细胞移植是治疗amd非常有效的手段。2012年,洛杉矶市加州大学朱尔斯
·
施泰因眼睛研究所视网膜部门主任steven schwartz首次将hesc诱导分化获得的rpe细胞运用于amd的临床治疗,并取得了一定的效果,为多能性干细胞分化获得的rpe细胞的临床应用开辟了道路。2013年6月日本厚生劳动省批准了高桥雅代(masayo takahashi)教授利用诱导的多能性干细胞(induced pluripotent stem cells,ipscs)开展视网膜再生临床研究的申请。高桥小组已经对首例病人进行了为期22个月的随访,部分患者的最佳矫正视力得到改善。该研究获得能使rpe细胞扩增的培养基和培养方法,也为rpe细胞的扩增和培养提供了更多的可能,也为rpe细胞的临床应用拓宽了种子资源细胞。
技术实现要素:
4.本发明人经过大量创造性劳动发现,通过调整培养基成分,添加myosin ii atpase抑制剂blebbistatin,可显著提高视网膜色素上皮细胞的扩增效率。这为后续稳定获得高品质视网膜色素上皮细胞,实现黄斑变性等多种视网膜色素上皮细胞缺损所致疾病的细胞疗法打下基础。
5.培养方法
6.因此,在一方面,本技术提供了一种视网膜色素上皮细胞的培养方法,其包括将所述视网膜色素上皮细胞置于含有myosin ii atpase抑制剂的培养基中进行培养的步骤;
7.其中,所述myosin ii atpase抑制剂的浓度低于5.0μm。
8.在某些实施方案中,所述myosin ii atpase抑制剂选自blebbistatin、blebbistatin衍生物(例如(s)-(-)-blebbistatin o-benzoate),及其任意组合。
9.在某些实施方案中,所述myosin ii atpase抑制剂为blebbistatin。
10.在某些实施方案中,所述myosin ii atpase抑制剂的浓度不低于0.1μm,例如,不低于0.5μm,不低于1.0μm。
11.在某些实施方案中,所述myosin ii atpase抑制剂的浓度为0.1-4.0μm(例如,0.1-1.0μm、0.2-4.0μm、0.2-1.0μm、0.5-4.0μm、0.5-1.0μm、0.5μm、1.0μm)。
12.在某些实施方案中,所述myosin ii atpase抑制剂为blebbistatin,并且,所述
kosr+1%的neaa+1%的cts-glutamax-i。
33.培养基
34.在另一方面,本技术还提供了一种培养基,其含有myosin ii atpase抑制剂,其中,所述myosin ii atpase抑制剂的浓度低于5.0μm。
35.在某些实施方案中,所述myosin ii atpase抑制剂的浓度不低于0.1μm,例如,不低于0.5μm,不低于1.0μm。
36.在某些实施方案中,所述myosin ii atpase抑制剂的浓度为0.1-4.0μm(例如,0.1-1.0μm、0.2-4.0μm、0.2-1.0μm、0.5-4.0μm、0.5-1.0μm、0.5μm、1.0μm)。
37.在某些实施方案中,所述myosin ii atpase抑制剂选自blebbistatin、blebbistatin衍生物(例如(s)-(-)-blebbistatin o-benzoate),及其任意组合。
38.优选地,所述myosin ii atpase抑制剂为blebbistatin。
39.在某些实施方案中,所述myosin ii atpase抑制剂为blebbistatin,并且,所述blebbistatin的浓度为0.1-4.0μm(例如,0.1-1.0μm、0.2-4.0μm、0.2-1.0μm、0.5-4.0μm、0.5-1.0μm、0.5μm、1.0μm)。
40.在某些实施方案中,所述培养基为适于视网膜色素上皮细胞的培养的培养基。
41.在某些实施方案中,所述培养基进一步包含添加了选自以下物质的基础培养基:一种或多种无血清替代物、谷氨酰胺或l-丙氨酰-l-谷氨酰胺的稳定化二肽、neaa添加剂、kosr,及其任意组合。
42.在某些实施方案中,所述基础培养基选自:ko-dmem、dmem、dmem/f12、neurobasal、neural induction media。
43.在某些实施方案中,所述培养基进一步包含添加了neaa添加剂、kosr和l-丙氨酰-l-谷氨酰胺的稳定化二肽的ko-dmem培养基。
44.在某些实施方案中,所述培养基进一步包含:70%-90%的ko-dmem培养基、10%-30%的kosr、0.5%-2%的neaa以及0.5%-2%的l-丙氨酰-l-谷氨酰胺的稳定化二肽。
45.在某些实施方案中,所述培养基进一步包含:70%-90%的cts knockout dmem、10%-30%的cts kosr、0.5%-2%的neaa以及0.5%-2%的cts-glutamax-i。
46.在某些实施方案中,所述培养基进一步包含:78%的cts knockout dmem+20%的cts kosr+1%的neaa+1%的cts-glutamax-i。
47.在某些实施方案中,所述培养基进一步包含egf、bfgf和/或rock抑制剂(例如y-27632)。
48.试剂组合
49.在另一方面,本技术还提供了试剂组合,其包含:(i)myosin ii atpase抑制剂,(ii)基础培养基,以及(iii)选自下列的添加剂:一种或多种无血清替代物、谷氨酰胺或l-丙氨酰-l-谷氨酰胺的稳定化二肽、neaa添加剂、kosr、及其任意组合。
50.在某些实施方案中,所述myosin ii atpase抑制剂选自blebbistatin、blebbistatin衍生物(例如(s)-(-)-blebbistatin o-benzoate),及其任意组合。在某些实施方案中,所述myosin ii atpase抑制剂为blebbistatin。
51.在某些实施方案中,所述基础培养基选自:ko-dmem、dmem、dmem/f12、neurobasal、neural induction media。
52.在某些实施方案中,所述试剂组合进一步包含(iv)egf、bfgf和/或rock抑制剂(例如y-27632)。
53.用途
54.在另一方面,本技术还提供了如上所述的试剂盒、培养基或试剂组合在培养视网膜色素上皮细胞中的用途。
55.在某些实施方案中,本技术还提供了以下示例性方案:
56.在第一个方面,本技术提供一种组合物,其含有一种或多种维持和/或提高视网膜色素上皮细胞活性和/或功能的添加剂,egf、bfgf、以及myosin ii atpase抑制剂。
57.在某些实施方案中,所述组合物含有myosin ii atpase抑制剂,任选地,其进一步含有rock抑制剂;
58.在某些实施方案中,所述组合物含有egf、myosin ii atpase抑制剂,任选地,其进一步含有rock抑制剂;
59.在某些实施方案中,所述组合物含有bfgf和myosin ii atpase抑制剂,任选地,其进一步含有rock抑制剂;
60.在某些实施方案中,所述组合物含有egf、bfgf、以及myosin ii atpase抑制剂,任选地,其进一步含有rock抑制剂;
61.在本技术的实施方案中,所述myosin ii atpase抑制剂是指肌球蛋白ii型atp酶抑制剂。在某些实施方案中,所述myosin ii atpase抑制剂选自blebbistatin及其衍生物。例如blebbistatin,即(s)-(-)-blebbistatin,结构式为例如(s)-(-)-blebbistatin o-benzoate,结构式为
62.在第二个方面,本技术提供一种培养基,其含有前述的组合物,以及基础培养基。
63.在某些实施方案中,所述基础培养基适于视网膜色素上皮细胞的培养。
64.在某些实施方案中,所述基础培养基选自kodmem培养基、dmem培养基、dmem/f12培养基。
65.在某些实施方案中,所述基础培养基为kodmem培养基。
66.在某些实施方案中,所述基础培养基是添加以下物质的基础培养基:一种或多种无血清替代物、谷氨酰胺或l-丙氨酰-l-谷氨酰胺的稳定化二肽。
67.在某些实施方案中,所述基础培养基是添加以下物质的基础培养基:n2添加剂和l-丙氨酰-l-谷氨酰胺的稳定化二肽。
68.在某些实施方案中,所述基础培养基组成如下:78%cts
tm
knockout
tm
dmem+20%cts
tm
kosr+1%cts
tm
neaa+1%cts-glutamax
tm-i。
69.在某些实施方案中,所述egf、bfgf和myosin ii atpase抑制剂的浓度可以为5-20μm,但不限于此。在一些具体实施方案中,所述myosin ii atpase抑制剂(例如
blebbistatin)的浓度为5μm、6μm、7μm、8μm、9μm、10μm、11μm、12μm、13μm、14μm、15μm、16μm、17μm、18μm、19μm或20μm。优选浓度为10μm。在一些具体实施方案中,所述egf的浓度为5μm、6μm、7μm、8μm、9μm、10μm、11μm、12μm、13μm、14μm、15μm、16μm、17μm、18μm、19μm或20μm。优选浓度为10μm。在一些具体实施方案中,所述bfgf的浓度为5μm、6μm、7μm、8μm、9μm、10μm、11μm、12μm、13μm、14μm、15μm、16μm、17μm、18μm、19μm或20μm。优选浓度为10μm。
70.在某些实施方案中,所述rock抑制剂的浓度可以为1-50μm,但不限于此。在某些实施方案中,所述rock抑制剂的浓度为1-30μm,例如5-30μm。在一些具体实施方案中,所述rock抑制剂(例如y-27632)的浓度为1μm、2μm、3μm、4μm、5μm、6μm、7μm、8μm、9μm、10μm、11μm、12μm、13μm、14μm、15μm、16μm、17μm、18μm、19μm、20μm、21μm、22μm、23μm、24μm、25μm、26μm、27μm、28μm、29μm或30μm。优选浓度为10μm。
71.在某些实施方案中,所述培养基适用于视网膜色素上皮细胞的培养,例如扩增培养。
72.在某些实施方案中,所述培养基适用于视网膜色素上皮细胞的培养,使视网膜色素上皮细胞扩增至少1.2倍、1.5倍、2倍、3倍、4倍、5倍、6倍、7倍、8倍、9倍、10倍、20倍、30倍、40倍、50倍、100倍。
73.在某些实施方案中,所述基础培养基为dmem/f12以及kodmem。
74.在某些实施方案中,所述培养基中含有78%ko-dmem/f12,20%kosr,1%neaa,1%glutmax添加剂,以及5-20μm blebbistatin。
75.在某些实施方案中,所述培养基中含有78%ko-dmem/f12,20%kosr,1%neaa,1%glutmax添加剂,5-20μm egf,以及5-20μm blebbistatin,。
76.在某些实施方案中,所述培养基中含有78%ko-dmem/f12,20%kosr,1%neaa,1%glutmax添加剂,5-20μm bfgf,以及5-20μm blebbistatin,。
77.在某些实施方案中,所述培养基中含有78%ko-dmem/f12,20%kosr,1%neaa,1%glutmax添加剂,5-20μm egf,5-20μm bfgf以及5-20μm blebbistatin,。
78.在另一个方面,本技术提供一种在体外维持或增加细胞数量的方法,其包括将所述细胞在前述的培养基中进行培养的步骤;或者本技术提供前述的培养基在体外维持或增加细胞数量中的用途。
79.在某些实施方案中,所述培养的方法为:将所述细胞制成单细胞悬液,以2
×
104/cm
2-6
×
104/cm2的密度接种至所述培养基,培养7-14天传代1次,其中各代培养条件相同。在某些实施方案中,以1
×
105/cm2的密度进行接种。
80.在某些实施方案中,所述贴壁培养条件为:将所述细胞制成单细胞悬液,以2
×
104/cm
2-6
×
104/cm2的密度接种至所述培养基,贴壁7-14天传代1次,其中各代培养条件相同。在某些实施方案中,以1
×
105/cm2的密度进行接种。
81.在某些实施方案中,所述细胞为视网膜色素上皮细胞。
82.在某些实施方案中,扩增得到的细胞与原代细胞基因组相同。
83.在另一个方面,本技术提供一种细胞或细胞群,其制备和扩增方法如以上所述的任意方法。在另一个方面,本技术提供一种细胞或细胞群,其中有》60%、》65%、》70%、》75%》、80%、》85%、》90%、》95%、》98%或》99%的细胞至少特异表达以下标志物中的一种或多种:rpe65,otx2,mitf,zo-1,best1,和cralbp。
84.在某些实施方案中,制备所述细胞或细胞群的方法包括上一方面所述的在体外维持或增加细胞数量的方法中所定义的步骤。
85.在另一个方面,本技术提供一种细胞或细胞群,其通过以下方法制备得到:
86.(1)将上述扩增得到的视网膜色素上皮细胞在第一培养基中培养7-14天;
87.(2)将步骤(1)中得到的细胞在第二培养基中培养,得到所述细胞或细胞群;其中,
88.所述第一培养基是添加以下物质的基础培养基:neaa、glutmax、血清替代物以及y-27632;优选地,所述第一培养基是添加以下物质的基础培养基:0.5%-2%neaa、0.5%-2%glutmax、10-20%kosr以及1-30mm y-27632;优选地,所述第一培养基是添加以下物质的基础培养基:1%neaa、1%glutmax、20%kosr以及10mm y-27632;
89.所述第二培养基是添加以下物质的基础培养基:neaa、glutmax、血清替代物、blebbistatin以及y-27632;优选地,所述第二培养基是添加以下物质的基础培养基:0.5%-2%neaa、0.5%-2%glutmax、10-20%kosr、5-20μm blebbistatin以及1-30mm y-27632;优选地,所述第二培养基是添加以下物质的基础培养基:1%neaa、1%glutmax、20%kosr、含有10μm blebbistatin的与egf或者bfgf组合,以及10mm y-27632;
90.在某些实施方案中,将上述扩增得到的视网膜色素上皮细胞制成单细胞悬液,以1
×
104/cm
2-1
×
106/cm2(例如,1
×
104/cm2、5
×
104/cm2、1
×
105/cm2、5
×
104/cm2或1
×
106/cm2)的密度接种至所述第一培养基。
91.在另一个方面,本技术还提供一种药物组合物,其含有上述任一项所述的细胞或细胞群。
92.在另一个方面,本技术还提供上述任一项方面所述的细胞或细胞群在制备治疗视网膜疾病(例如黄斑变性)的药物中的用途。
93.术语定义
94.在本发明中,除非另有说明,否则本文中使用的科学和技术名词具有本领域技术人员所通常理解的含义。同时,为了更好地理解本发明,下面提供相关术语的定义和解释。
95.当本文使用术语“例如”、“如”、“诸如”、“包括”、“包含”或其变体时,这些术语将不被认为是限制性术语,而将被解释为表示“但不限于”或“不限于”。
96.除非本文另外指明或根据上下文明显矛盾,否则术语“一个”和“一种”以及“该”和类似指称物在描述本发明的上下文中(尤其在以下权利要求的上下文中)应被解释成覆盖单数和复数。
97.如本文中所使用的,术语“视网膜色素上皮细胞”是指经人视网膜原代分离或分化、转分化等方式获得的,可形成紧密连接的含有色素颗粒的六边形单层上皮细胞。
98.如本文中所使用的,术语“抑制”、“阻断”或“阻碍”是指经化合物(即,抑制剂)处理的细胞其特定信号通路活性降低。
99.发明的有益效果
100.本技术通过调整培养基成分,添加myosin ii atpase抑制剂blebbistatin,可显著提高视网膜色素上皮细胞的扩增效率,为科学研究或商业化提供更好更多的细胞资源并为实现黄斑变性等多种视网膜色素上皮细胞缺损所致疾病的细胞疗法打下基础。
附图说明
101.此处所说明的附图用来提供对本发明的进一步理解,构成本技术的一部分,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
102.图1显示了由人胚干细胞分化获得视网膜色素上皮细胞并进行扩增培养的流程。
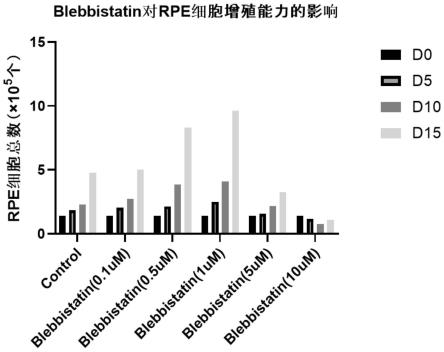
103.图2显示了不同浓度blebbistatin(0.1μm、0.5μm、1μm、5μm、10μm)对视网膜色素上皮细胞增殖的影响。
104.图3显示了不同浓度blebbistatin(0.1μm、0.5μm、1μm、5μm、10μm)培养视网膜色素上皮细胞的状态。
具体实施方式
105.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。以下对至少一个示例性实施例的描述实际上仅仅是说明性的,绝不作为对本发明及其应用或使用的任何限制。基于本发明中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
106.实施例:blebbistatin对视网膜色素上皮细胞的影响
107.1.实验所用试剂:
108.(1)blebbistatin溶液:工作浓度为1μm和10μm。4℃可保存两周。
109.(2)基础培养基配制:
110.78%cts
tm
knockout
tm
dmem+20%cts
tm
kosr+1%cts
tm
neaa+1%cts-glutamax
tm-i
111.2.视网膜色素上皮细胞扩增实验方法:
112.将人胚干细胞诱导分化并获得视网膜色素上皮细胞,以进行后续扩增、冻存实验。人胚干细胞来源于国家干细胞资源库,也可采用商业可得的人胚胎干细胞系。由人胚胎干细胞诱导为视网膜色素上皮细胞的方法可参考现有技术,例如maruotti j,wahlin k,gorrell d,bhutto i,lutty g,zack dj(2013)a simple and scalable process for the differentiation of retinal pigment epithelium from human pluripotent stem cells.stem cells transl med 2:341
–
354.
113.(1)视网膜色素上皮细胞具体获得方法:
114.1)vitronectin基质的配制:室温下,吸取6ml dpbs加入至15ml离心管中,然后吸取60μl vitronectin(购自gibco,货号:a14700)加入至上述dpbs中,移液枪吹打10次混匀,得到vitronectin基质,现用现配。六孔板每孔加入1ml配好的基质,室温孵育1h备用。
115.2)将人胚干细胞接种到包被基质的孔板中。放入37℃,5%co2培养箱培养。培养7-10天,克隆融合度达到95%时,更换成rpe分化培养基,若干天后可获得人胚干细胞分化的视网膜色素上皮细胞。
116.(2)视网膜色素上皮细胞扩增实验:
117.1)vitronectin基质的配制:室温下,吸取6ml dpbs加入至15ml离心管中,然后吸取60μl vitronectin加入至上述dpbs中,移液枪吹打10次混匀,得到vitronectin基质,现用现配。六孔板每孔加入1ml配好的基质,室温孵育1h备用。
118.2)将视网膜色素上皮细胞用tryple消化成单细胞悬液,取10μl上述悬液加入到10
μl ao-pi溶液中混匀,利用countstar细胞分析仪进行计数;然后吸弃vitronectin基质,按照接种密度1
×
105/cm2重新用2d的方法接种于含不同浓度blebbistatin(购自medchenexpress,mce,货号:#hy-13441/cs-4983)的扩增培养基的24孔板中,放入37℃,5%co2培养箱培养。
119.3)培养一定天数后,显微镜观察各组细胞形态;并且,用tryple将各组部分细胞消化成单细胞悬液,取10μl上述悬液加入到10μl ao-pi溶液中混匀,利用countstar细胞分析仪进行计数,绘制细胞增殖曲线。
120.3.视网膜色素上皮细胞扩增实验结果:
121.blebbistatin对视网膜色素上皮细胞增殖效率的影响如图2-3所示。其中,图2显示了不同浓度blebbistatin(0.1μm、0.5μm、1μm、5μm、10μm)对视网膜色素上皮细胞增殖的影响;图3显示了不同浓度blebbistatin(0.1μm、0.5μm、1μm、5μm、10μm)培养视网膜色素上皮细胞的状态。
122.根据图2-3的结果可知,相对于未加blebbistatin的扩增培养基,在含有相对较低浓度的blebbistatin(例如,0.1μm、0.5μm或1μm的blebbistatin)的扩增培养基中,rpe细胞增殖更快;在含有相对较高浓度的blebbistatin(例如,5μm或10μm的blebbistatin)的扩增培养基中,rpe细胞增殖减慢。
123.此外,在含有相对较低浓度的blebbistatin(例如,0.1μm、0.5μm或1μm的blebbistatin)的扩增培养基中,rpe细胞形态与control组一致;而在含有相对较高浓度的blebbistatin(例如,5μm或10μm的blebbistatin)的扩增培养基中,rpe细胞形态明显发生变化,细胞变小,且细胞边界逐渐模糊。
124.除本文中描述的那些外,根据前述描述,本发明的各种修改对本领域技术人员而言会是显而易见的。这样的修改也意图落入所附权利要求书的范围内。本技术中所引用的各参考文献(包括所有专利、专利申请、期刊文章、书籍及任何其它公开)均以其整体援引加入本文。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1