一种低体积收缩多环结构丙烯酸酯及其应用的制作方法
1.本发明属于光固化技术领域,具体涉及一种低体积收缩多环结构丙烯酸酯及其应用。
背景技术:
2.光固化技术由于其环保节能,性能优异,越来越受到用户的青睐,在诸如涂料、油墨、粘合剂等方面的应用越来越广泛。但从理论上讲,自由基光固化有他两个不可逾越的缺点,一是自由基聚合有氧气阻聚现象,使得光聚合材料的表面固化不完全,容易产生缺陷;另一个缺点就是自由基聚合时,由于自由体积的变化,会发生体积收缩,这就直接导致材料与基材的附着力发生变化,容易发生剥离或起皱。为解决体积收缩带来的问题,目前采用的方法主要是添加附着力促进剂,通过物理与化学的方法,使涂层与基材间的附着力增加,降低剥离的几率,但不能从根本上解决问题;另一个方法是合成具有较大分子量的丙烯酸酯树脂,通过自身体积增大来部分降低体积收缩的影响,虽然有效,但带来的问题是分子量增加,体系粘度增加,给施工及配方带来困难。
3.因而,寻求解决体积收缩带来的涂层性能瑕疵的技术,是一个长期课题,也是一个重要的研究方向。鉴于此,本发明特提出一种低体积收缩多环结构的丙烯酸酯及其在光固化反应中的应用。
技术实现要素:
4.针对现有技术中光固化技术自由基聚合反应时,由于体积收缩导致光固化材料与基材之间的附着力发生变化的缺陷,本发明在于提供了一种低体积收缩多环结构丙烯酸酯及其制备方法和应用,本发明提供了一种具有多个环状结构的丙烯酸酯单体,能够有效抵消由于自由基聚合反应时体积收缩带来的光固化材料易发生剥离和起皱的问题,从而提高涂层的性能。
5.本发明是通过如下技术方案实现的:
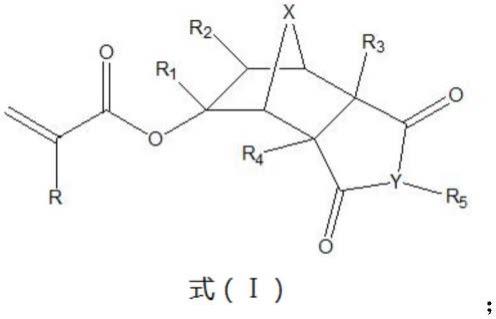
6.本发明提供一种低体积收缩多环结构丙烯酸酯,其具有如下式(ⅰ)所示结构:
[0007][0008]
其中,r1为h、或烷基、或含烷氧基团的结构;
[0009]
r2为h、或烷基、或脂环基团、含环氧基团的结构;
[0010]
r3为h、或烷基、或含羰基结构单元、或含烷氧基结构基团、或含环氧基结构单元;
[0011]
r4为h、或烷基、或酯基、或环烷基、或含环氧基团的结构、或含羧基基团的结构、或含烷氧基团的结构;
[0012]
r5为h、或烷基、或酯基、或环烷基、或含环氧基团的结构、或含羧基基团的结构、或含烷氧基团的结构、或不存在;
[0013]
r为h、或甲基;
[0014]
y为碳、或氧、或氮、或硫;
[0015]
x为碳、或氧、或硫。
[0016]
优选地,所述式(ⅰ)结构中,y为氧或硫时,r5不存在。
[0017]
所述低体积收缩多环结构丙烯酸酯可选地采用将双烯类化合物和亲双烯体在有机溶剂中进行d-a反应(diels-alder reaction),并向产物中加入环己烷进行结晶,得到中间产物含双键的环状化合物,然后根据需要在含双键的环状化合物上接枝r1、r2、r3、r4和r5基团,然后通过取代丙烯酸和催化剂进行加成反应,得到式(ⅰ)化合物。
[0018]
本发明还提供一种所述丙烯酸酯在光固化反应中的应用,所述丙烯酸酯作为反应单体参与到光固化聚合反应中。
[0019]
相对于现有技术,本发明的有益效果:
[0020]
(1)结构方面:本发明的丙烯酸酯具有多个环状结构,由于多环结构的引入,使得丙烯酸酯分子的自由体积增加,能够有效抵消由于自由基聚合反应时体积收缩带来的光固化材料易发生剥离和起皱的问题,提高涂层的性能。
[0021]
(2)制备方法方面:本发明首先选择具有环状结构的双烯类化合物和亲双烯体作为起始原料,进行双烯d-a反应,生成了六元环结构,使得中间产物式(ii)至少具有两个环状结构,大大增加了分子的体积,使得在发生自由基聚合反应时,其产生的体积收缩就会缩小;由于d-a反应产生的双键的自由基聚合活性很低,所以本发明采用取代丙烯酸与式(ii)化合物的双键进行反应,生成丙烯酸酯,引入丙烯酸酯双键,可以提高自由基聚合反应的聚合速度。
具体实施方式
[0022]
下面将对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。以下对至少一个示例性实施例的描述实际上仅仅是说明性的,决不作为对本发明及其应用或使用的任何限制。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
[0023]
下面提供本发明低体积收缩多环结构丙烯酸酯的实施例:
[0024]
所述丙烯酸酯,具有如下式(ⅰ)所示结构:
[0025][0026]
其中,r1为h、或烷基、或含烷氧基团的结构;
[0027]
r2为h、或烷基、或脂环基团、含环氧基团的结构;
[0028]
r3为h、或烷基、或含羰基结构单元、或含烷氧基结构基团、或含环氧基结构单元;
[0029]
r4为h、或烷基、或酯基、或环烷基、或含环氧基团的结构、或含羧基基团的结构、或含烷氧基团的结构;
[0030]
r5为h、或烷基、或酯基、或环烷基、或含环氧基团的结构、或含羧基基团的结构、或含烷氧基团的结构、或不存在;
[0031]
r为h、或甲基;
[0032]
y为碳、或氧、或氮、或硫;
[0033]
x为碳、或氧、或硫。
[0034]
实施例1
[0035]
本实施例提供一种低体积收缩多环结构丙烯酸酯,其结构式为:
[0036][0037]
本实施例还提供一种低体积收缩多环结构丙烯酸酯的制备方法,反应方程式如下:
[0038][0039]
制备步骤如下:
[0040]
(1)在安装有搅拌和温度计的三口烧瓶中,将马来酸酐(20g,203.9mmol)和呋喃(20.8g,305.5mmol)溶解在150ml甲苯中,30℃加热反应12小时,冷却后加入环己烷结晶出
化合物1
‑ⅲ
(33.4g,产率:98.5%);
[0041]
化合物1-iii的分析表征如下:
[0042]1h nmr(400mhz,cdcl3):δ6.57(s,2h),5.45(s,2h),3.18(s,2h);
[0043]
13
c nmr(400mhz,cdcl3):δ170.1,137.2,82.4,48.9。
[0044]
(2)将化合物1-iii(16.6g,100mmol)溶于二氧六环(150ml),加入甲基丙烯酸(8.7g,100mmol)和催化量的dabco(三乙烯二胺)(1.12g,10mmol),在110℃反应12小时,反应结束后将反应液淬灭至100ml饱和nahco3水溶液中,乙酸乙酯萃取(3*50ml),有机相合并后经饱和食盐水洗涤,无水硫酸钠干燥,过滤浓缩后得到化合物1(17.7g,产率70%)。
[0045]
化合物1的分析表征如下:
[0046]1h nmr(400mhz,cdcl3):δ6.15(s,1h),5.58(s,1h),4.23(m,1h),4.01(m,1h),3.42(m,1h),3.18(m,2h),1.93(d,3h),1.68(m,2h);
[0047]
13
c nmr(400mhz,cdcl3):δ172.2,167.2,136.1,125.2,90.2,80.9,77,52.8,46.8,38.1,18.0。
[0048]
本实施例步骤(2)中以“丙烯酸”代替“甲基丙烯酸”,采用相同的工艺条件可制备得到化合物1a,其结构式为:
[0049][0050]
实施例2
[0051]
本实施例提供一种低体积收缩多环结构丙烯酸酯,其结构式为:
[0052][0053]
本实施例还提供一种低体积收缩多环结构丙烯酸酯的制备方法,反应方程式如下:
[0054][0055]
制备步骤如下:
[0056]
(1)在安装有搅拌和温度计的三口烧瓶中,将n-苯基马来酰亚胺(17.62g,100mmol)和3-甲基呋喃(12.3g,150mmol)溶解在100ml二氧六环中,90℃加热回流12小时,
进行d-a反应,反应结束后冷却,加入环己烷结晶出化合物2-iii(22.3g,产率:88.4%)。
[0057]
化合物2-iii的分析表征如下:
[0058]1h nmr(400mhz,dmso-d6):δ7.58(d,1h),7.57(m,2h),7.43(m,2h),5.56(d,1h),4.63(m,2h),2.86(m,2h),1.79(s,3h);
[0059]
13
c nmr(400mhz,cdcl3):δ173,138.8,131.9,129.3,128.9,128.1,128.0,85.1,83.2,54.1,51.3,17.8。
[0060]
(2)将化合物2-iii(20.42g,80mmol)溶于二氧六环(50ml),加入甲基丙烯酸(8.95g,104mmol,1.3eq)和dbu(1,8-二氮杂二环[5.4.0]十一碳-7-烯)(1.2g,8mmol,0.1eq),加热至120℃搅拌反应10小时,反应结束后将反应液淬灭至100ml饱和nahco3溶液中,乙酸乙酯萃取(3*50ml),有机相合并后经饱和食盐水洗涤,无水硫酸钠干燥,过滤浓缩后,粗品经柱层析(石油醚/乙酸乙酯=1:1至0:1)分离得到无色油状产物,即为化合物2(24.6g,产率:90%)。
[0061]
化合物2的分析表征如下:
[0062]1h nmr(400mhz,dmso-d6):δ7.58(m,1h),7.57(m,2h),7.43(m,2h),6.48(s,1h),6.40(s,1h),4.71(t,1h),4.13(m,1h),3.44(m,1h),3.19(m,2h),2.33(m,1h),2.01(s,3h),0.88(d,3h);
[0063]
13
c nmr(400mhz,dmso):δ177.2,167.2,136.0,131.9,128.9,125.2,90.6,87.8,84.3,52.9,49.7,40.6,17.9,8.1。
[0064]
实施例3
[0065]
本实施例提供一种低体积收缩多环结构丙烯酸酯,其结构式为:
[0066][0067]
本实施例还提供一种低体积收缩多环结构丙烯酸酯的制备方法,反应方程式如下:
[0068][0069]
制备步骤如下:
[0070]
(1)将化合物1
‑ⅲ
(166g,1mol)添加到装有1l二氯甲烷的圆底烧瓶中,在冰水浴中搅拌20min,然后边搅拌边分批次加入m-cpba(400g,2mol,纯度为85%),加毕,室温下搅拌过夜。tlc监测反应完成后,将反应液淬灭至饱和硫代硫酸钠水溶液(1l)。室温下搅拌0.5小时后,乙酸乙酯(3*500ml)萃取,有机相合并后以饱和食盐水洗涤,无水硫酸钠干燥后,过滤浓缩,粗品经柱层析(石油醚/乙酸乙酯=1:1至0:1)分离得到白色固体化合物3-i(122g,收率67%)。
[0071]
化合物3-i的分析表征如下:
[0072]1h nmr(400mhz,dmso-d6):δ=4.85(s,2h,
–
choch
–
),3.71(s,2h,
–
choch
–
),3.54(s,2h,
–
ch
–
ch
–
)ppm;
[0073]
13
c nmr(400mhz,dmso-d6):δ=174.26,76.23,49.64,46.27,46.27ppm。
[0074]
(2)在安装有搅拌和温度计的三口烧瓶中,将甲基丙烯酸(94.7g,1.1mol)、环氧化合物3-i(182.1g,1mol)和三乙胺(111g,1.1mol)溶解在四氢呋喃(1l)中,室温下搅拌3h,反应结束后将反应液淬灭至饱和碳酸氢钠溶液(500ml)中,乙酸乙酯(3*500ml)萃取,有机相合并后以饱和食盐水洗涤,无水硫酸钠干燥后,过滤浓缩,粗品经柱层析(石油醚/乙酸乙酯=1:1至0:1)分离得到白色固体化合物3(236g,产率:88%)。
[0075]
化合物3的分析表征如下:
[0076]1h nmr(400mhz,dmso-d6):δ6.48(s,1h),6.4(s,1h),4.81(m,1h),4.51(s,1h),4.46(m,1h),4.33(m,2h),3.87(m,1h),3.10(m,2h),2.01(s,3h);
[0077]
13
c nmr(400mhz,dmso):δ172.2,167.2,136.0,125.2,89.4,86.5,86.0,83.3,77.9,47.2,46.7,17.9ppm。
[0078]
本实施例步骤(2)中以“丙烯酸”代替“甲基丙烯酸”,采用相同的工艺条件可制备得到化合物3a。
[0079]
实施例4
[0080]
本实施例提供一种低体积收缩多环结构丙烯酸酯,其结构式为:
[0081][0082]
本实施例还提供一种低体积收缩多环结构丙烯酸酯的制备方法,反应方程式如下:
[0083][0084]
制备步骤如下:
[0085]
在安装有搅拌和温度计的三口烧瓶中,在氮气保护下,在0℃将化合物3(26.8g,0.1mol)加入到dmf(300ml)中,混合均匀后氮气氛下缓慢加入氢化钠(6g,0.15mol,纯度60%),冰浴下搅拌10min后加入环氧氯丙烷(10.1g,0.11mol),混合物室温搅拌两小时,反应结束后将反应液淬灭至饱和氯化铵水溶液(500ml),乙酸乙酯(3*500ml)萃取,有机相合并后以饱和食盐水洗涤,无水硫酸钠干燥后,过滤浓缩,粗品经柱层析(石油醚/乙酸乙酯=1:0至1:1)分离得到白色固体化合物4(19.5g,产率60%)。
[0086]
化合物4的分析表征如下:
[0087]1h nmr(400mhz,dmso-d6):δ6.48(d,1h),6.40(d,1h),5.01(m,1h),4.46(m,1h),4.07(m,1h),4.03(m,1h),3.60(d,1h),3.35(d,1h),3.10(m,2h),2.74(m,1h),2.60(d,1h),2.35(d,1h),2.01(s,3h);
[0088]
13
c nmr(400mhz,dmso):δ172.2,167.2,136.0,125.2,88.5,87.2,86.3,84.3,69.8,52.6,47.2,47.0,44.2,17.9ppm。
[0089]
本实施例中以“化合物3a”代替“化合物3”,采用相同的工艺条件可制备得到化合物4a,其结构式为:
[0090][0091]
实施例5
[0092]
本实施例提供一种低体积收缩多环结构丙烯酸酯,其结构式为:
[0093][0094]
本实施例还提供一种低体积收缩多环结构丙烯酸酯的制备方法,反应方程式如下:
[0095][0096]
制备步骤如下:
[0097]
(1)将li2cucl4(0.1m/thf,250ml,25mmol)的溶液在-50℃下慢慢加入溶于250ml thf的环戊基溴化镁(270mmol)的悬浮液中。将悬浮液慢慢降至-10℃并搅拌0.5h。之后将混合物重新冷却至-78℃。通过蠕动泵将该混合物在-78℃下缓慢加入至化合物3-i(25.0g,250mmol)的thf(300ml)溶液中,并在-78℃下搅拌20分钟。反应结束后,将反应液淬灭至饱和nh4cl水溶液(500ml)。乙酸乙酯(3*500ml)萃取,有机相合并后以饱和食盐水洗涤,无水硫酸钠干燥后,过滤浓缩,粗品经柱层析(石油醚/乙酸乙酯=1:0至0:1)分离得到化合物5-i(41g,产率:65%)。
[0098]
化合物5-i的分析表征如下:
[0099]1h nmr(400mhz,dmso-d6):δ5.37(s,1h),3.87(m,1h),3.77(m,1h),3.64(m,1h),3.10(m,2h),1.90(m,2h),1.73(m,2h),1.65(m,2h),1.63(m,2h),1.44(m,1h),1.31(m,1h);
[0100]
13
c nmr(400mhz,dmso):δ172.2,93.5,82.3,79.1,51.3,50.8,47.0,31.8,31.5,25.4ppm。
[0101]
(2)将化合物5-i(37.8g,150mmol)与三乙胺(30g,0.3mol)溶于二氯甲烷(500ml)中,冰浴下缓慢加入甲基丙烯酰氯(16.7g,160mmol),0℃下继续搅拌2h。反应结束后将反应液淬灭至饱和nahco3(500ml),乙酸乙酯(3*500ml)萃取,有机相合并后以饱和食盐水(500ml)洗涤,无水硫酸钠干燥后,过滤浓缩,粗品经柱层析(石油醚/乙酸乙酯=1:0至0:1)洗涤干燥,减压抽滤得到化合物5(38.92g,产率:81%)。
[0102]
化合物5的分析表征如下:
[0103]1h nmr(400mhz,dmso-d6):δ6.48(s,1h),6.40(s,1h),4.71(m,1h),4.46(m,1h),3.77(m,1h),3.10(m,2h),2.03(m,1h),2.01(s,3h),1.90(m,2h),1.73(m,2h),1.65(m,2h),1.63(m,2h),1.31(m,1h);
[0104]
13
c nmr(400mhz,dmso):δ172.2,167.2,136.0,125.2,90.3,82.5,80.3,51.0,47.6,31.7,31.5,25.4,17.9ppm。
[0105]
本实施例步骤(2)中以“丙烯酰氯”代替“甲基丙烯酰氯”,采用相同的工艺条件可制备得到化合物5a。
[0106]
实施例6
[0107]
本实施例提供一种低体积收缩多环结构丙烯酸酯,其结构式为:
[0108][0109]
本实施例还提供一种低体积收缩多环结构丙烯酸酯的制备方法,反应方程式如下:
[0110][0111]
制备步骤如下:
[0112]
(1)化合物6-ii的合成方法与化合物1-iii的合成方法相同,不同之处仅在于,以“马来酰亚胺”代替“马来酸酐”。
[0113]
化合物6-ii的分析表征如下:
[0114]1h nmr(400mhz,dmso-d6):δ5.78(d,2h),4.64(t,2h),3.07(d,2h);
[0115]
13
c nmr(400mhz,dmso):δ177.9,136.4,81.4,56.3。
[0116]
(2)0℃下将m-cpba(间氯过氧苯甲酸)(1.73g,10mmol)加入到溶有化合物6-ii(2.89g,10mmol)的二氯甲烷(30ml)溶液中,室温下搅拌12小时,反应结束后以饱和nahco3水溶液淬灭,乙酸乙酯(3*30ml)萃取,有机相以饱和食盐水洗涤后,无水硫酸钠干燥后,过滤浓缩得到产物6-iii(2.3g,产率:75.3%)。
[0117]
化合物6-iii的分析表征如下:
[0118]1hnmr(400mhz,dmso-d6):δ3.51
–
3.33(m,2h),3.19
–
3.15(m,2h),3.01
–
2.89(m,2h);
[0119]
13
c nmr(400mhz,dmso):δ176.5,87.4,60.7,53.9。
[0120]
(3)化合物6-iii(18.1g,0.1mol)溶解于四氢呋喃(200ml)中,氩气保护下加入10%钯碳催化剂(1g),加毕,氢气置换3次后,将氢气压力保持在30psi并在室温下搅拌1h。反应结束后将反应液过滤,滤液经减压浓缩有得化合物6-iv(18.1g,粗品)直接用于下一步反应。
[0121]
化合物6-iv的分析表征如下:
[0122]1h nmr(400mhz,dmso-d6):δ3.51
–
3.48(m,1h),3.11
–
3.08(m,1h),3.01
–
2.89(m,3h),1.88
–
1.85(m,1h),1.71
–
1.65(m,1h);
[0123]
13
c nmr(400mhz,dmso):δ174.3,96,77,76,58,51.3,40.9。
[0124]
(4)化合物6-iv(18.1g,粗品,约0.1mol)和环氧氯丙烷(10.1g,0.11mol)溶解于丙酮(200ml)中,室温下分批加入固体氢氧化钠(4.4g,0.11mol),加毕,室温下继续搅拌6小时,反应结束后将反应液淬灭至饱和氯化铵水溶液(200ml)中,乙酸乙酯(3*300ml)萃取,有机相以饱和食盐水洗涤后,无水硫酸钠干燥后,过滤浓缩,粗品经柱层析分离(石油醚/乙酸乙酯=1:0至0:1),得到化合物6-v(16.7g,产率:70%)。
[0125]
化合物6-v的分析表征如下:
[0126]1h nmr(400mhz,dmso-d6):δ4.0
–
3.81(m,1h),3.48
–
3.41(m,2h),3.19
–
3.16(m,1h),3.09
–
2.89(m,4h),2.63
–
2.61(m,1h),2.41
–
2.38(m,1h),2.1(s,1h),1.88
–
1.85(m,1h),1.71
–
1.65(m,1h);
[0127]
13
c nmr(400mhz,dmso):δ176.1,174.3,97,78,76,58,51.3,48.5,45,43,40.9。
[0128]
(5)此步骤合成化合物6的合成方法与实施例5步骤(2)合成化合物5的方法相同。
[0129]
化合物6的分析表征如下:
[0130]1h nmr(400mhz,dmso):δ6.15(s,1h),5.58(s,1h),4.23(m,1h),3.78
–
3.73(m,1h),3.61
–
3.59(m,1h),3.51
–
3.49(m,1h),3.18
–
3.14(m,1h),3.01
–
2.89(m,3h),2.65
–
2.61(m,1h),2.39
–
2.37(m,1h),2.01(s,3h),1.89
–
1.85(m,1h),1.61
–
1.55(m,1h)。
[0131]
13
c nmr(400mhz,dmso):δ177,176,167.2,136.1,125.2,91.1,80.5,77.9,55.8,49.8,48.5,45,42.1,37.7,18。
[0132]
应用例
[0133]
以光聚合的方式对实施例1-6制备得到的化合物1-6的体积收缩进行测试,具体操作如下:将2重量份的光引发剂uvi-6976分别与100重量份本发明制备的化合物1-6混合均匀,均匀涂抹于玻璃片上,以高压汞灯(灯距5cm,光照强度i
365nm
=1mw/cm2)照射,得到光聚合的光固化膜,光固化后的薄膜均匀,目测无气泡。
[0134]
收缩率根据iso 4216:2021热固性树脂和紫外光固化树脂固化收缩率连续测量法,与甲基丙烯酸甲酯比较,测量结果如表1所示:
[0135]
表1
[0136][0137]
可见,本发明的多环结构丙烯酸酯由于具有多环结构,其分子自由体积增加,从而具有低的体积收缩,能够有效抵消由于自由基聚合反应时体积收缩带来的光固化材料易发生剥离和起皱的问题,提高涂层的性能。
[0138]
以上所述的具体实施例,对本发明的目的、技术方案和有益效果进行了进一步详细说明,所应理解的是,以上所述仅为本发明的具体实施例而已,并不用于限制本发明,凡在本发明的精神和原则之内,所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1