铱配合物及其制备方法与应用
1.本发明涉及生物检测技术领域,尤其涉及一种铱配合物及其制备方法与应用。
背景技术:
2.根据细菌在革兰氏染色后颜色的不同,将细菌分为革兰氏阳性菌(染色为紫色)和革兰氏阴性菌(染色为粉色),这两类细菌的主要区别在于细胞壁结构不同。革兰氏阳性菌的细胞壁较厚,主要有肽聚糖(petidoglycan,pg)和脂磷壁酸(lipoteichoic acid,lta)。相比之下,革兰氏阴性菌的细胞壁更薄,结构更复杂,除肽聚糖外,还含有独特的外膜和脂多糖。迄今为止,由革兰氏阳性菌(g
+
)引起的细菌感染目前是导致人类病发甚至死亡的最主要原因之一。g
+
引起多种感染,包括如皮肤和软组织感染、手术部位感染、血流感染和肺炎感染等,这些感染与心内膜炎、肺炎、关节炎、骨髓炎及败血症等疾病密切相关。此外,在肿瘤细胞中的一些g
+
可能会降低药物疗效,并引起化疗药物耐药性的产生。因此开发快速、灵敏检测g
+
的荧光探针应用于临床诊断、环境监测和食品药品分析等领域,对维护人类生命健康和公共卫生安全起着至关重要的意义。
3.目前,g
+
鉴定的主要方法有传统的革兰氏染色法、聚合酶链反应法(pcr)、核酸相关的检测法、免疫学相关技术和表面增强拉曼光谱法(sers)等,这些方法存在前期预处理时间长、准确度低、操作复杂、需要大型仪器等缺点。与上述方法相比,荧光检测技术具有灵敏度高、响应速度快、无创伤性、可实时检测等优点,成为一种可替代的方法应用于细菌检测和鉴定。
技术实现要素:
4.本发明所要解决的技术问题在于,提供一种铱配合物及其制备方法与应用,该铱配合物对革兰氏阳性菌具有特异选择识别效果。
5.具体的,本发明提供了式(ⅰ)所示的阳离子与阴离子形成的铱配合物;
[0006][0007]
具体的,本发明的铱配合物并不限定阴离子的种类,本领域常规阴离子均能实现
本发明目的,尤其是无机盐阴离子,如clo
4-、cl-、pf
6-等,但不限于此。优选的阴离子为cl-和/或clo
4-。
[0008]
本发明还提供了一种上述铱配合物的制备方法,其包括以下步骤:
[0009]
(1)将1,10-邻菲罗啉-5,6-二酮、乙酸铵、冰醋酸与3-氯苯胺,在氩气氛围下混合加热3~5h并冷凝回流,待混合物冷却至20~40℃后加入水,用碱中和,抽滤,收集沉淀,用水和乙醚洗涤后得到粗产物;
[0010]
(2)将粗产物用乙醇溶解,用60-100目的硅胶装柱,以乙醇作为淋洗剂淋洗,收集黄色组分,旋转蒸发得到中间产物(3-cpipba);
[0011]
(3)将所述中间产物与[ir(ppy)2cl2]
·
2h2o加入到体积比为3:1的二氯甲烷与甲醇的混合溶液中,在氩气保护下加热回流6~9h,冷却至20~40℃后滴加阴离子盐的饱和溶液产生沉淀,过滤,产物采用中性氧化铝柱提纯,以体积比为10:1的乙腈与乙醇混合溶液作为淋洗液进行洗脱,干燥得到铱配合物成品。
[0012]
具体的,在本发明的一个实施例之中,阴离子无机盐为naclo4或nh4cl,但不限于此。
[0013]
本发明还提供了上述的铱配合物在检测革兰氏阳性菌中的应用。具体的,本发明制备得到的铱配合物可与革兰氏阳性菌表面的lta键和,从而实现对革兰氏阳性菌的特异选择识别。
[0014]
其中,革兰氏阳性菌为金黄色葡萄球菌、耐甲氧西林金黄色葡萄球菌、枯草芽孢杆菌或粪肠球菌,但不限于此。
[0015]
本发明还提供了上述的铱配合物在区分革兰氏阳性菌与革兰氏阴性菌和/或真菌中的应用。
[0016]
其中,革兰氏阳性菌为金黄色葡萄球菌、耐甲氧西林金黄色葡萄球菌、枯草芽孢杆菌或粪肠球菌,但不限于此。革兰氏阴性菌为大肠杆菌、沙门氏菌或奇异变形杆菌,但不限于此。真菌为白色念珠菌,但不限于此。
[0017]
相应的,本发明还公开了一种用于检测革兰氏阳性菌的荧光探针,其包括上述的铱配合物。
[0018]
相应的,本发明还公开了一种用于检测革兰氏阳性菌的试剂盒,其包括上述的荧光探针。
[0019]
实施本发明,具有如下有益效果:
[0020]
本发明提供的铱配合物可与革兰氏阳性菌表面的lta键和,从而实现对革兰氏阳性菌的特异选择识别。
附图说明
[0021]
图1是本发明实施案例1中铱配合物的结构表征质谱图;
[0022]
图2是本发明实施例1中铱配合物的氢谱图;
[0023]
图3是本发明实施例2中铱配合物对革兰氏阳性菌、革兰氏阴性菌、真菌的荧光滴加实验结果图;
[0024]
图4是本发明实施例3中铱配合物对革兰氏阳性菌、革兰氏阴性菌、真菌的共聚焦成像实验结果图;
[0025]
图5是本发明实施例4中铱配合物对革兰氏阳性菌、革兰氏阴性菌、真菌的流式细胞术实验结果图;
[0026]
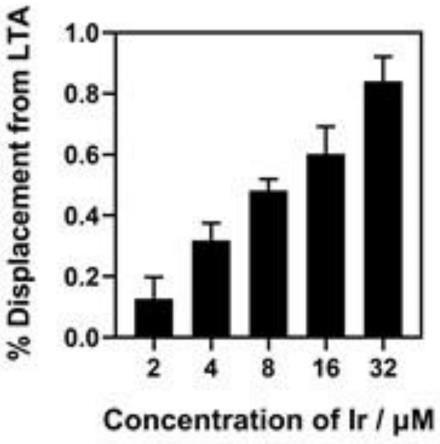
图6是本发明实施例5中铱配合物与bodipy-tr-cadaverine竞争lta实验结果图。
具体实施方式
[0027]
为使本发明的目的、技术方案和优点更加清楚,下面将结合附图及具体实施方式对本发明作进一步地详细描述。
[0028]
实施例1铱配合物的合成
[0029]
(1)3-cpipba的合成方法:
[0030]
以1,10-邻菲罗啉-5,6-二酮、乙酸铵、3-氯苯胺与冰醋酸在氩气氛围下混合加热冷凝回流4小时,混合物冷却至室温后加入去离子水,用25%氨水中和,抽滤,收集黄色沉淀并用水和乙醚洗涤,得到相应粗产物。粗产物用少量的乙醇溶解,用硅胶(60-100目)装柱,乙醇作为淋洗剂,收集黄色组分,旋转蒸发得到黄色粉末4-(1-(3-氯苯基)-1h咪唑并[4,5-f][1,10]菲咯啉-2-基)苯甲酸(4-(1-(3-chlorophenyl)-1h-imidazo[4,5-f][1,10]phenanthrolin-2-yl)benzoic acid,即配体3-cpipba)。
[0031]
该化合物的anal.calcd for c
26h15
n4o2cl:c,69.26;h,3.35;n,12.43.found:c,70.08;h,3.28;n,12.55%.
[0032]
该化合物的质谱(fab-ms)为:m/z=451(m+1)。
[0033]
(2)[ir(ppy)2(3-cpipba)]
+
的合成方法:
[0034]
[ir(ppy)2cl2]
·
2h2o和3-cpipba加入到二氯甲烷:甲醇(v:v=3:1)混合溶液中,氩气保护下加热回流8小时,冷却至室温后滴加阴离子无机盐(nh4cl)的饱和溶液产生沉淀,抽滤,产物采用中性氧化铝柱提纯,以乙腈与乙醇(v:v=10:1)的淋洗液进行洗脱,真空干燥得终产物[ir(ppy)2(3-cpipba)]cl。
[0035]
该化合物的anal.calcd for c
48h31
n6cl2o2ir:c,58.42;h,3.17;n,8.52%;found:c,58.36;h,3.38;n,8.47%.
[0036]
该化合物的质谱(es-ms)为:[ch3cn,m/z]:951([m
–
cl]
+
)(图1)。氢谱为:1h nmr(400mhz,dmso)δ9.34(d,j=8.2hz,1h),8.27(dd,j=19.0,7.6hz,3h),8.20
–
8.11(m,1h),8.10(d,j=4.8hz,1h),8.04
–
7.69(m,11h),7.61(d,j=8.4hz,1h),7.50(d,j=6.9hz,4h),7.14
–
6.88(m,6h),6.29(dd,j=13.2,7.5hz,2h)(图2)。
[0037]
实施例2铱配合物对革兰氏阳性菌、革兰氏阴性菌、真菌的荧光滴加实验将革兰氏阳性菌金黄色葡萄球菌(s.aureus,atcc25923)、耐甲氧西林金黄色葡萄球菌(mrsa,atcc43300)、枯草芽孢杆菌(b.subtilis,cmcc(b)63501)、粪肠球菌(e.faecalis,atcc29212),革兰氏阴性菌大肠杆菌(e.coli,atcc25922)、沙门氏菌(s.typhimurium,atcc14028)、奇异变形杆菌(p.mirabilis,pro10(ao250)),真菌白色念珠菌(c.albicans,atcc10231),孵育过夜后,调整细菌浓度为od
600
=1。向10μm配合物溶液中不断滴加菌液,每次滴加1μl,测其荧光发射强度,激发波长为398nm,发射波长为590nm。结果如图3和图4所示,革兰氏阳性菌的加入使配合物的荧光增强,革兰氏阴性菌和真菌的加入使配合物荧光减弱。
[0038]
实施例3铱配合物与革兰氏阳性菌、革兰氏阴性菌、真菌的共聚焦成像
[0039]
取上述几种革兰氏阳性菌、革兰氏阴性菌、真菌的对数生长期的菌液,稀释至菌液浓度为1
×
106至1
×
107cfu/ml,每管菌液加入配合物(10μm),孵育2h后,用pbs清洗三次,洗去多余的配合物。pbs重悬菌液后,取10μl制片,在激光共聚焦显微镜下观察。结果如图5所示,只有革兰氏阳性菌显示配合物的荧光,革兰氏阴性菌及真菌都不显示荧光。
[0040]
实施例4铱配合物与革兰氏阳性菌、革兰氏阴性菌、真菌的流式细胞术实验
[0041]
取上述几种革兰氏阳性菌、革兰氏阴性菌、真菌的对数生长期的菌液,稀释至菌液浓度为1
×
106至1
×
107cfu/ml,每管菌液加入配合物(10μm),孵育2h后,用pbs清洗三次,洗去多余的配合物。pbs重悬菌液后使用流式细胞仪定量检测其荧光强度,选用405为激发波长,525/40bp为发射波长的ko525通道进行检测。结果如图6所示,只有革兰氏阳性菌检测到荧光信号,革兰氏阴性菌及真菌没有检测到荧光信号。
[0042]
实施例5铱配合物与bodipy-tr-cadaverine竞争lta研究
[0043]
采用bodipy-tr-cadaverine置换反应来测量配合物与lta之间的键合力。bodipy-tr-cadaverine探针与lta结合之后荧光会淬灭,当其他分子取代探针与lta结合后,探针的荧光增强。bodipy-tr-cadaverine(最终浓度为5μm)与lta(终浓度为12.5μg/ml)混合置于96孔板中,15分钟后加入不同浓度的配合物(1
×
mic,2
×
mic,4
×
mic,8
×
mic),将混合物置于室温下孵育40分钟,然后用酶标仪测其荧光强度(激发波长580nm,发射波长620nm)。
[0044]
以上所述是发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1