一种多酶催化制备高纯度胆固醇的方法与流程
1.本发明属于胆固醇合成技术领域,具体涉及到一种多酶催化制备高纯度胆固醇的方法。
背景技术:
2.胆固醇是细胞膜最重要的结构成分之一。化学式为c
27h46
o,纯的胆固醇为白色结晶,胆固醇的结构是一种刚性平面分子,具有四个稠环(三个六元环和一个五元环)的类固醇骨架,化学名称是(3β)-胆甾-5-烯-3-醇,结构式见式(i):
[0003][0004]
胆固醇及其衍生物在药物递送系统(注射级药用辅料,脂质体)、活性药物或食品添加剂(如维生素d3)、液晶(胆固醇液晶)等不同研究领域中的应用广泛。
[0005]
胆固醇如用作注射级药用辅料、脂质体和胆固醇液晶制备的原材料,必须是高纯度的,以保障药物安全性或电子材料的高品质。现有的植物源胆固醇的合成方法存在过程复杂、使用多种有毒危险试剂或危险工艺、且成品中异构体杂质纯化困难等问题。
[0006]
专利文献cn105218610、cn105237603以豆甾醇或豆甾醇降解物为原料合成胆固醇,但仍存在合成路线长,起始原料来源受限的缺点。
[0007]
专利文献cn112608361以双降醇为原料,经过4步反应制备得到胆固醇,该路线短但是还原步骤存在异构体问题,且异构体精制较难除去,导致整体收率偏低。
[0008]
专利文献cn113943336以双降醇为原料,通过氧化、witting反应、酯化、加氢、钠硼氢还原制备侧链以及酯化还原制得胆固醇,但其中还原过程同样存在3α羟基异构体,高压加氢属于危险工艺,且存在加氢不完全和过渡加氢的情况可能产生多种杂质。
[0009]
因此,迫切需要开发一种植物来源的、安全、绿色、高纯度的胆固醇合成方法。
技术实现要素:
[0010]
本发明的目的是提供一种多酶催化制备高纯度胆固醇的方法,以解决背景技术中提出的现有的植物源胆固醇的合成方法存在过程复杂、使用多种有毒危险试剂或危险工艺、且成品中异构体杂质纯化困难等问题。
[0011]
本发明的技术方案是一种多酶催化制备高纯度胆固醇的方法,包括以下步骤:
[0012]
第一步为原料式(ii)与对甲苯磺酰氯反应,在二氯甲烷、三乙胺和4-二甲氨基吡啶催化条件下磺酰化得中间体1;
[0013]
中间体1再通过第一制备线路或第二制备线路制备胆固醇;
[0014]
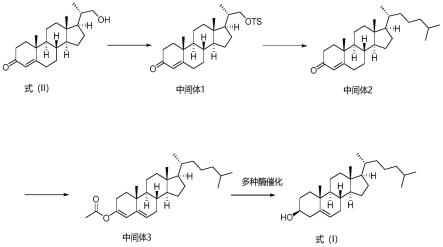
第一制备线路为:中间体1先与由溴代异戊烷制备的偶联试剂,在铜锂试剂催化下偶联反应得到中间体2;中间体2再与醋酐发生酯化反应,得到中间体3;最后中间体3在酯水解酶、3β-类固醇脱氢酶、葡萄糖脱氢酶和nad+催化作用下,发生酯水解和酮基还原反应,得到胆固醇式(i);
[0015]
第二制备线路为:中间体1先与醋酐发生酯化反应,得到中间体4;中间体4再在酯水解酶、3β-类固醇脱氢酶、葡萄糖脱氢酶和nad+催化作用下,发生酯水解和酮基还原反应,得到中间体5;最后中间体5与由溴代异戊烷制备的偶联试剂,在铜锂试剂催化下偶联反应,得到胆固醇式(i)。
[0016]
在一种具体的实施方式中,第一步中:
[0017]
先是在室温条件下,向反应容器加入化合物式(ii)、4-二甲氨基吡啶、三乙胺和二氯甲烷,并进行氮气置换;再升温至35~40℃加入对甲苯磺酰氯回流反应1~2小时;然后对应完的溶液进行精制得到中间体1。
[0018]
在一种具体的实施方式中,所述精制得到中间体1的过程包括:
[0019]
先将反应完的溶液降温至0~30℃,滴加甲醇水溶液搅拌分层并进行第一次分液;在第一次分液的水相中加入二氯甲烷萃取并进行第二次分液,再将第一次分液的有机层与第二次分液的有机层合并,合并后的有机层加入氯化钠溶液搅拌一段时间分层并进行第三次分液,第三次分液的有机层减压浓缩至稠状,加入甲醇减压浓缩置换,降温至10~30 度搅拌0.5~1小时,过滤,滤饼用甲醇洗涤,将洗涤后的滤饼装盘于50℃以下烘料,烘至干燥得中间体1;减压浓缩的温度为40~50℃;所述甲醇水溶液中的甲醇:水为1:1~3。
[0020]
在一种具体的实施方式中,所述铜锂试剂为四氯铜酸锂溶液;
[0021]
所述四氯铜酸锂溶液的制备过程为:在室温条件下,向反应容器加入氯化铜、氯化锂和四氢呋喃,控制温度在10~30℃反应1~2小时至溶清;
[0022]
所述由溴代异戊烷制备的偶联试剂的制备过程为:在室温条件下,向反应容器加入镁屑、溴代异戊烷和四氢呋喃,缓慢升温至30~42℃反应1~5小时,得到由溴代异戊烷制备的偶联试剂。
[0023]
在一种具体的实施方式中,所述第一制备线路中,得到中间体2的反应如下:
[0024]
由溴代异戊烷制备的偶联试剂降温至-20~-10℃,控温滴加四氯铜酸锂溶液;反应1 小时后,滴加中间体1的四氢呋喃溶液,滴加完毕后,缓慢升温至0~10℃,反应10~30 小时,控温在0~20℃,加入盐酸淬灭,再对盐酸淬灭后的溶液精制得中间体2;
[0025]
所述第二制备线路中,得到胆固醇的反应如下:
[0026]
由溴代异戊烷制备的偶联试剂降温至-30~-20℃,控温滴加四氯铜酸锂溶液;反应1 小时后,滴加中间体5的四氢呋喃溶液,滴加完毕后,缓慢升温至0~10℃,反应10~30 小时,控温在0~20℃,加入盐酸淬灭,再对盐酸淬灭后的溶液精制得胆固醇。
[0027]
在一种具体的实施方式中,所述中间体1的四氢呋喃溶液中的中间体1与四氢呋喃的配制比例为1g:10~14ml;
[0028]
对盐酸淬灭后的溶液精制得中间体2的过程包括:
[0029]
控温在40~45℃减压浓缩至无馏分;加入水和二氯甲烷,搅拌分层,有机层先用碳酸氢钠溶液洗涤分层;有机层再用水洗涤分层;
[0030]
有机层于40~45℃减压浓缩至无馏分;加入甲醇浓缩置换,降温搅拌,过滤,固体
于 70℃以下烘料,烘至干燥得中间体2;
[0031]
所述中间体5的四氢呋喃溶液中的中间体5与四氢呋喃的配制比例为1g:10~14ml;
[0032]
对盐酸淬灭后的溶液精制得胆固醇的过程包括:
[0033]
控温在40~45℃减压浓缩至无馏分;加入水和二氯甲烷,搅拌分层,有机层用碳酸氢钠溶液洗涤分层,接着将有机层于40~45℃减压浓缩至无馏分,加入甲醇浓缩置换,降温搅拌,过滤,固体于70℃以下烘料,制得胆固醇粗品,用乙酸乙酯重结晶后,得高纯度胆固醇。
[0034]
在一种具体的实施方式中,所述第一制备线路中酯化得到中间体3和第二制备线路中酯化得到中间体4的反应条件如下:
[0035]
将反应液升温反应3~4小时,反应完后降温至0-20℃,将反应液缓慢加至纯水中,搅拌1~3小时后过滤,固体烘料烘至干燥。
[0036]
在一种具体的实施方式中,所述第一制备线路中酯化得到中间体3时,反应液升温反应的温度为48~53℃,反应液中包括中间体2、醋酐和对甲苯磺酸,固体烘料的温度控制在60℃以下;
[0037]
所述第二制备线路中酯化得到中间体4时,反应液升温反应的温度为60~65℃,反应液中包括中间体1、醋酐和pts,固体烘料的温度控制在50℃以下。
[0038]
在一种具体的实施方式中,所述第一制备线路中酯水解和酮基还原反应得到胆固醇的反应如下:
[0039]
室温条件下,在反应容器中依次加入中间体3、纯水、葡萄糖脱氢酶、3β-类固醇脱氢酶、酯水解酶和辅酶nad+,控制温度28~32℃,使用na2co3调ph值为6.8~7.5;搅拌反应一段时间,tlc检测无底物残留时停止反应;反应结束后将反应体系升温至38~42℃搅拌一段时间,再降温至18~22℃,过滤,用纯水洗涤滤饼,于热风循环烘箱中干燥,烘干后的滤饼加入无水乙醇升温至48~52℃搅拌一段时间后趁热过滤,滤饼用乙醇淋洗;将滤液负压浓缩,浓缩后冷却析晶,过滤,热风循环烘箱中干燥,烘干后得白色晶体,即高纯度胆固醇。
[0040]
在一种具体的实施方式中,所述第二制备线路中酯水解和酮基还原反应得到中间体5 的反应如下:
[0041]
室温条件下,在反应容器中依次加入中间体4、纯水、葡萄糖脱氢酶、3β-类固醇脱氢酶、酯水解酶、辅酶nad+和乙酸乙酯,控制温度28℃-32℃,使用na2co3调ph值为 6.8~7.5;搅拌反应一段时间,tlc检测无底物残留时停止反应;反应结束后将反应体系升温至38~42℃搅拌一段时间,负压浓缩,补加水,再降温至18~22℃,过滤,用纯水洗涤滤饼,于热风循环烘箱中干燥,烘干后的滤饼加入二氯甲烷,搅拌溶解,过滤,滤饼用二氯甲烷淋洗,将滤液负压浓缩,然后用乙醇置换,置换后冷却析晶,过滤,热风循环烘箱中干燥,烘干后得到白色晶体,即中间体5。
[0042]
本发明的有益效果包括:
[0043]
本发明是一种简便的由双降醇制备胆固醇的方法,为快速获得高质量植物源的胆固醇提供了理想途径,同时原材料的来源不受限制。关键步骤使用酶催化替代钠硼氢还原,实验条件温和,制备过程绿色环保,污染小,可操作性强,所得胆固醇纯度高达 99.9%,能够有效控制由于还原产生的异构体,避免其他路线的危险反应,因此整体路线在收率和质
量方面都有明显优势。
[0044]
除了上面所描述的目的、特征和优点之外,本发明还有其它的目的、特征和优点。下面将参照图,对本发明作进一步详细的说明。
附图说明
[0045]
构成本技术的一部分的附图用来提供对本发明的进一步理解,本发明的示意性实施例及其说明用于解释本发明,并不构成对本发明的不当限定。在附图中:
[0046]
图1为本发明中第一种制备胆固醇的线路图。
[0047]
图2为本发明中第二种制备胆固醇的线路图。
[0048]
图3为本发明中实施例4制得的胆固醇的hplc图谱。
[0049]
图4为本发明中实施例7制得的胆固醇的hplc图谱。
[0050]
图5为本发明中制得的胆固醇的氢谱图。
[0051]
图6为本发明中制得的胆固醇的碳谱图。
具体实施方式
[0052]
以下结合附图对本发明的实施例进行详细说明,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0053]
实施例1
[0054]
磺酰化反应制备中间体1
[0055]
在室温10~30℃条件下,向2l反应瓶加入150g化合物式(ii)、5.5g 4-二甲氨基吡啶(即dmap)、400ml三乙胺和1000ml二氯甲烷,氮气置换,搅拌溶清。升温至 35~40℃回流反应。分五次加入109.1g对甲苯磺酰氯。添加完后,控制温度在35~40℃回流反应1~2小时。取样点板,控制原料基本消失。将反应完的溶液降温至0~30℃。控制温度为0~30℃,滴加50ml甲醇:水为1:2的溶液,搅拌30分钟,分层。水相加入100ml 二氯甲烷萃取,有机层合并。有机层加入70ml的10%氯化钠溶液搅拌30分钟,分层。有机层于40~50℃减压浓缩至稠状,分2次加入50ml甲醇于40~50℃减压浓缩置换。降温至10~30度搅拌0.5~1小时,过滤,滤饼用37.5ml甲醇洗涤。将洗涤后的滤饼装盘于 50℃以下烘料。烘至干燥得中间体1,共213.7g,收率142.5%。
[0056]
实施例2
[0057]
偶联反应制备中间体2
[0058]
在室温10~30℃条件下,向250ml干燥的反应瓶加入2.41g氯化铜、1.52g氯化锂和 100ml四氢呋喃,控制温度在10~30℃反应1~2小时至溶清,得到四氯铜酸锂溶液。室温 10~30℃,向1l干燥的反应瓶加入9.68g镁屑、60.9g溴代异戊烷和500ml四氢呋喃。缓慢升温至37~42℃反应约4小时,得到格式试剂反应液2。反应液2降温至-20~-10℃,控温滴加四氯铜酸锂溶液,约1小时滴完。反应1小时后,滴加中间体1的四氢呋喃溶液 (25g中间体1溶于300ml四氢呋喃),约1小时滴完。滴加完毕,缓慢升温至0~10℃,反应过夜,约20小时,原料基本消失,控温t=0~20℃,加入200ml的5%盐酸淬灭,搅拌30分钟。控温在40~45℃减压浓缩至基本无馏分。加入100ml水和200ml二氯甲烷,搅拌1小时,分层,有机层用5%碳酸氢钠溶液洗涤,洗涤两次,每次50ml,分层。有机层用50ml水,洗涤一次,分层。
[0059]
有机层于40~45℃减压浓缩至基本无馏分。加入25ml甲醇浓缩置换2次,降温至 10℃度搅拌1小时,过滤,固体于70℃以下烘料。烘至干燥得中间体2,共12.9g,收率 51.6%。气相检测纯度98.6%。
[0060]
实施例3
[0061]
酯化反应制备中间体3
[0062]
在室温10~30℃条件下,向250ml反应瓶加入10.3g中间体2、65ml醋酐和3.5g对甲苯磺酸搅拌。升温至48~53℃,控温在48~53℃,反应3~4小时。取样点板,无原料剩余。将反应完体系降温0~20℃,将反应液缓慢加至200ml水中,搅拌2小时,过滤,固体于60℃以下烘料。烘至干燥得中间体3共10.5g,收率102%。
[0063]
实施例4
[0064]
酶催化制备胆固醇(式i)
[0065]
在室温25℃条件下,在洁净的500ml四口反应瓶中依次加入10.0g中间体3、140ml 纯化水、10ml葡萄糖脱氢酶(菌液,400g/l)、10ml的3β-类固醇脱氢酶(菌液, 400g/l)、10ml酯水解酶(菌液,400g/l)、0.2g辅酶nad+和20ml乙酸乙酯,控制温度28℃~32℃,使用10%的na2co3调ph=6.8~7.5。搅拌反应14小时,tlc检测无底物残留时停止反应(≤0.5%)。反应结束后将反应体系升温至40℃搅拌0.5小时,负压浓缩至无明显乙酸乙酯残留,补加50ml水,再将体系降温至20℃,过滤,用20ml纯水洗涤滤饼,于50℃热风循环烘箱中干燥,烘干后的滤饼重10.2g。滤饼加入20ml二氯甲烷室温25℃,搅拌溶解,过滤,滤饼用少量二氯甲烷淋洗。将滤液在30℃,0.1mpa负压浓缩,至有固体析出后,用95%的乙醇置换,得到大量白色固体,将体系于0~5℃冷却析晶,过滤,45℃热风循环烘箱中干燥,烘干后得白色晶体9.2g,重量收率92.0%。制得胆固粗品醇,先用甲醇,再用乙酸乙酯重结晶后,即得高纯度胆固醇,液相色谱纯度: 99.93%,单项杂质<0.05%。具体液相色谱结果如下表:
[0066]
峰结果
[0067][0068]
实施例5
[0069]
酯化反应制备中间体4
[0070]
在室温10~30℃条件下,向2l反应瓶加入213g中间体1、865ml醋酐和25.5g的 pts搅拌。升温至60~65℃。控温反应3~4小时。取样点板,控制原料基本消失,将反应完体系降温至0~20℃,将反应液缓慢加至2l水中,搅拌2小时。过滤,滤饼水洗至中性。固体装盘于50℃以下烘料。烘至干燥得中间体4共223.7g,收率105%。
[0071]
实施例6
[0072]
酶催化制备中间体5
[0073]
在室温25℃条件下,在洁净的500ml四口反应瓶中依次加入10.0g中间体4、140ml 纯水、10ml葡萄糖脱氢酶(菌液,400g/l)、10ml的3β-类固醇脱氢酶(菌液, 400g/l)、10ml酯水解酶(菌液,400g/l)、0.2g辅酶nad+和20ml乙酸乙酯,控制温度28℃~32℃,使用10%的na2co3调ph=6.8~7.5。搅拌反应14小时,tlc检测无底物残留时停止反应(≤0.5%)。反应
结束后将反应体系升温至40℃搅拌0.5小时,负压浓缩至无明显乙酸乙酯残留,补加50ml水,再将体系降温至20℃,过滤,用20ml纯水洗涤滤饼,于50℃热风循环烘箱中干燥,烘干后的滤饼重10.2g。滤饼加入20ml二氯甲烷室温25℃,搅拌溶解,过滤,滤饼用少量二氯甲烷淋洗。将滤液在30℃,0.1mpa负压浓缩,至有固体析出后,用95%的乙醇置换,得到大量白色固体,将体系于0~5℃冷却析晶,过滤,45℃热风循环烘箱中干燥,烘干后得白色晶体9.2g,即中间体5,重量收率 92.0%。
[0074]
实施例7
[0075]
偶联反应制备胆固醇(式i)
[0076]
在室温条件下,向250ml干燥的反应瓶加入1.0g氯化铜、0.6g氯化锂和40ml四氢呋喃,反应1~2小时至溶清,得到四氯铜酸锂溶液。室温,向1l干燥的反应瓶加入5.3g 镁屑、40.9g溴代异戊烷和250ml四氢呋喃。缓慢升温至30~35℃反应约2小时,得到格式试剂反应液。反应液降温至-30~-20℃,控温滴加四氯铜酸锂溶液。随后滴加中间体5 的四氢呋喃溶液(7.5g中间体5溶于80ml四氢呋喃)。滴加完毕,缓慢升温至0~10℃,反应过夜,约15小时,原料基本消失,控温t=0-20℃,加入60ml的5%盐酸淬灭。控温在40~45℃减压浓缩至基本无馏分。加入50ml水和80ml二氯甲烷,搅拌1小时,分层,有机层用5%碳酸氢钠溶液洗涤,洗涤两次,每次20ml,分层。有机层于40~45℃减压浓缩至基本无馏分。加入20ml甲醇浓缩置换2次,降温至5℃搅拌1小时,过滤,固体于 70℃以下烘料。制得胆固醇粗品,用25ml乙酸乙酯重结晶后,得5.3g高纯度胆固醇,液相色谱纯度:99.93%,单项杂质<0.05%。具体液相色谱结果如下表:
[0077]
峰结果
[0078][0079]
本发明操作简单,反应条件温和,试剂毒性小,污染小,生产成本低,可操作性强,专一性强,能够有效控制还原反应的异构体杂质,收率高。
[0080]
本发明中,葡萄糖脱氢酶,购自上海麦克林生化科技有限公司。辅酶(nad+):氧化型烟酰胺腺嘌呤二核苷酸,购自上海跃腾生物技术有限公司。其他试剂均为市售。
[0081]
为简便起见,本发明中的反应投料比经常以重量体积比来表示反应比例,如无特别说明,该重量体积比是指反应原料的重量与反应试剂的重量或体积的比例。
[0082]
以上内容是结合具体的优选实施方式对本发明作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干简单推演和替换,都应当视为属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1