一种体外培养人次级卵泡的培养液及其应用
1.本发明涉及细胞培养技术领域,尤其是涉及一种体外培养人次级卵泡的培养液及其应用。
背景技术:
2.人体内卵泡发育阶段是从始基卵泡激活至初级卵泡,生长至次级卵泡,最终形成窦卵泡,窦卵泡中的卵母细胞-卵丘细胞复合物(coc)成熟后形成成熟卵母细胞。而人次级卵泡体外培养技术是从人卵巢中分离出次级卵泡,在体外培养至窦卵泡阶段,再将窦卵泡中coc行体外成熟培养以获得成熟卵母细胞的过程。该技术是肿瘤患者生育力保存技术的重要发展方向,目前处于实验研究阶段,有望为儿童及青春期前患者、患雌激素敏感肿瘤、卵巢肿瘤的患者提供更高效、安全的生育力保存选择。
3.目前,有研究报道人卵泡培养体系可获得成熟卵母细胞,但是大部分研究未能将卵泡培养至成熟阶段即发育停滞,国内也尚未有成功报道。xu j等(文献1)从体外培养3周的卵巢组织中分离出次级卵泡,应用低粘度锥底96孔板体外培养6周,最终卵泡直径可达到617~676μm,成熟卵母细胞直径达119.4
±
3.3μm,形态正常,每存活卵泡的成熟率为21%(3/14)。mclaughlin,m等(文献2)从体外培养8天的卵巢组织中分离出次级卵泡,应用v底96孔板体外培养8天,最终卵泡直径达248
±
4.5μm(第8天较第6天无明显增长),成熟卵母细胞出现第一极体体积异常增大,每存活卵泡的成熟率为10.3%(9/87)。xiao,s等(文献3)从卵巢碎片组织中分离出次级卵泡,结合凝胶及低粘度培养板体外培养30~40天,最终卵泡直径可达到400~500μm,每存活卵泡的成熟率为20%(4/20)。
4.上述3篇文献中提到的培养液支持卵泡体外发育可达到的窦卵泡直径(248~676μm)远小于体内发育的早期窦卵泡(890~4000μm);并且培养液体外培养卵泡最终达到的卵母细胞体外成熟率(10.3%~21%)远低于体内发育卵泡的卵母细胞体外成熟率(50%),其中1篇报道获得的成熟卵母细胞形态异常,因此,亟需一种提高人次级卵泡体外培养获得的窦卵泡发育水平及卵母细胞的成熟率的体外培养人次级卵泡的培养液。
5.参考文献:
6.文献1.xu f,lawson ms,bean y,et al.matrix-free 3d culture supports human follicular development from the unilaminar to the antral stage in vitro yielding morphologically normal metaphase ii oocytes.hum reprod.2021;36(5):1326-1338.
7.文献2.mclaughlin m,albertini df,wallace w,anderson ra,telfer ee.metaphase ii oocytes from human unilaminar follicles grown in a multi-step culture system.mol hum reprod.2018;24(3):135-142.
8.文献3.xiao s,zhang j,romero mm,smith kn,shea ld,woodruff tk.in vitro follicle growth supports human oocyte meiotic maturation.sci rep.2015;5:17323.
技术实现要素:
9.本发明的目的在于克服上述现有技术的不足之处而提供一种体外培养人次级卵泡的培养液及其应用。本发明的体外培养人次级卵泡的培养液可提高人次级卵泡体外培养获得的窦卵泡直径及体积,提高其发育水平;还可以提高人次级卵泡体外培养获得卵母细胞的体外成熟率,应用于临床后有望为患者保存更多成熟卵母细胞。
10.为实现上述目的,本发明采取的技术方案为:
11.第一目的,本发明提供了一种体外培养人次级卵泡的培养液,所述培养液含有以下浓度的组分:
12.胎球蛋白0.5~2mg/ml、胰岛素-转铁蛋白-硒混合液0.1~1%、血清蛋白替代物5~10%、人神经营养因子4 10~200ng/ml和人重组卵泡刺激素1~20miu/ml。
13.在本技术中,将人神经营养因子4添加至体外培养人次级卵泡的培养液配方中,使得培养液可以促进卵泡发育、提高卵母细胞成熟率。在本技术培养液的配方中还含有胎球蛋白、胰岛素-转铁蛋白-硒混合液、血清蛋白替代物和人重组卵泡刺激素,其中胎球蛋白可以促进细胞生长和分化;胰岛素-转铁蛋白-硒混合液中的胰岛素可以促进葡萄糖和氨基酸吸收、胞内运输及蛋白和核酸的合成,转铁蛋白降低氧自由基和过氧化物的毒性水平,硒用作抗氧化剂;血清蛋白替代物可以维持和促进细胞生长;人重组卵泡刺激素可以促进卵泡发育(颗粒细胞甾体激素合成功能等),采用上述组分组成的培养液可以有针对性弥补体外卵泡培养环境较体内卵泡发育调控的不足,也实现了国内无可获得成熟卵母细胞的人卵泡体外培养体系的突破。
14.其中培养液中胰岛素-转铁蛋白-硒混合液的配比为胰岛素10mg/l、转铁蛋白5.5mg/l、硒5μg/l;
15.作为本发明所述体外培养人次级卵泡的培养液的优选实施方式,所述培养液还包括αmem培养基为基础培养基。
16.本技术的培养液还含有αmem培养基为基础培养基,αmem培养基提供细胞培养所需的氨基酸、维生素、无机盐等,有利于人次级卵泡的培养。
17.作为本发明所述体外培养人次级卵泡的培养液的优选实施方式,所述培养液含有以下质量浓度的组分:
18.胎球蛋白0.8~1.2mg/ml、胰岛素-转铁蛋白-硒混合液0.1~0.5%、血清蛋白替代物5~8%、人神经营养因子4 50~150ng/ml和人重组卵泡刺激素5~10miu/ml。
19.当体外培养人次级卵泡的培养液优选为上述浓度的组分时,组分之间相互协同,使得制备的培养液可提高人次级卵泡体外培养获得的窦卵泡直径及体积,提高其发育水平,还可以提高人次级卵泡体外培养获得卵母细胞的体外成熟率,应用于临床后有望为患者保存更多成熟卵母细胞。
20.作为本发明所述体外培养人次级卵泡的培养液的优选实施方式,所述培养液含有以下质量浓度的组分:
21.胎球蛋白1mg/ml、胰岛素-转铁蛋白-硒混合液0.1%、血清蛋白替代物6%、人神经营养因子4 100ng/ml和人重组卵泡刺激素10miu/ml。
22.当培养液的组分选择上述浓度时,可以更好地促进窦卵泡发育水平和促进卵母细胞体外成熟。人次级卵泡在该培养液的体系下可以持续生长,最长可保持存活6周,存活率
为33.3%(15/45);卵泡直径逐渐增大,每存活卵泡的窦腔形成率达100%,窦腔开始形成的时间平均为培养第2周,分离得到的次级卵泡平均直径为253.00
±
46.0μm。
23.在本技术的培养液中体外培养4周过程中,直径呈线性增长,卵泡每周平均直径的增长差异均有统计学意义,体外培养4周平均直径为967.00
±
41.1μm,较文献报道的可达到的直径(248~676μm)大。每存活卵泡的卵母细胞成熟率为46.7%(7/15),较文献报道(10.3%~21%)的成熟率高。
24.第二目的,本发明提供了上述体外培养人次级卵泡的培养液的制备方法,包括以下步骤:
25.1)按照上述浓度将胎球蛋白、胰岛素-转铁蛋白-硒混合液、血清蛋白替代物加入至αmem培养基中,摇匀,离心,过滤,获得过滤后的培养液;
26.2)向过滤后的培养液加入人重组卵泡刺激素及人神经营养因子4混合,获得体外培养人次级卵泡的培养液。
27.作为本发明所述制备方法的优选实施方式,步骤1)中,离心的速度为1500rpm/min,离心时间为3-5min。
28.第三目的,本发明提供了上述体外培养人次级卵泡的培养液在体外培养人次级卵泡中的应用。
29.上述培养液可提高人次级卵泡体外培养获得的窦卵泡直径及体积,提高其发育水平,还可以提高人次级卵泡体外培养获得卵母细胞的体外成熟率,应用于临床后有望为患者保存更多成熟卵母细胞。
30.与现有技术相比,本发明具有以下有益效果:
31.本发明提供了一种体外培养人次级卵泡的培养液及其应用;该培养液添加胎球蛋白、胰岛素-转铁蛋白-硒混合液、血清蛋白替代物、人神经营养因子4和人重组卵泡刺激素,上述组分之间相互协同,使得制备的培养液可提高人次级卵泡体外培养获得的窦卵泡直径及体积,提高其发育水平,还可以提高人次级卵泡体外培养获得卵母细胞的体外成熟率,应用于临床后有望为患者保存更多成熟卵母细胞。培养液中加入的人神经营养因子4,可以针对性弥补体外卵泡培养环境较体内卵泡发育调控的不足,也实现了国内无可获得成熟卵母细胞的人卵泡体外培养体系的突破。
附图说明
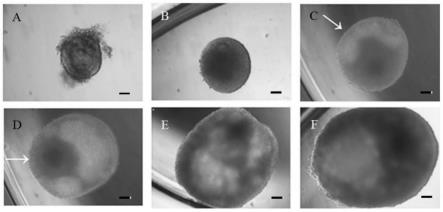
32.图1为人卵巢次级卵泡体外生长过程图;
33.图2为人卵巢次级卵泡体外生长直径变化图(*:p<0.05,**:p<0.01);
34.图3为采用实施例1的培养基在人体外培养获得的卵泡的amh、雌二醇、孕酮分泌水平图;
35.图4为采用实施例1的培养基在人体外培养卵泡获得的卵母细胞体外成熟情况图。
具体实施方式
36.为更好的说明本发明的目的、技术方案和优点,下面将结合附图和具体实施例对本发明作进一步说明。
37.在以下实施例中,所使用的实验方法如无特殊说明,均为常规方法,所用的材料、
试剂等,如无特殊说明,均可从商业途径得到。
38.胰岛素-转铁蛋白-硒混合液(its)的配比为胰岛素10mg/l;转铁蛋白5.5mg/l;硒5μg/l,厂家均为sigma;
39.血清蛋白替代物(serum protein substitute,sps)的厂家为sage;
40.人神经营养因子4(人nt4)的厂家为peprotech;
41.人重组卵泡刺激素(rhfsh)的厂家为merck。
42.实施例1、一种体外培养人次级卵泡的培养液及其制备方法
43.一种体外培养人次级卵泡的培养液,含有以下质量浓度的组分:
44.αmem培养基、胎球蛋白1mg/ml、胰岛素-转铁蛋白-硒混合液0.1%、血清蛋白替代物6%、人神经营养因子4 100ng/ml和人重组卵泡刺激素10miu/ml。
45.上述体外培养人次级卵泡的培养液的制备方法,包括以下步骤:
46.1)按照上述浓度将胎球蛋白、胰岛素-转铁蛋白-硒混合液、血清蛋白替代物加入至αmem培养基中,摇匀(3-5分钟),离心3-5分钟(1500rpm),用0.22μm过滤器除菌,获得过滤后的培养液;
47.2)向过滤后的培养液加入人重组卵泡刺激素(rhfsh)及人神经营养因子4(人nt4)混合,4℃保存,获得体外培养人次级卵泡的培养液,使用前一天需置于培养箱中(37℃,5%co2)提前平衡。
48.实施例2、一种体外培养人次级卵泡的培养液及其制备方法
49.一种体外培养人次级卵泡的培养液,含有以下质量浓度的组分:
50.αmem培养基、胎球蛋白0.5mg/ml、胰岛素-转铁蛋白-硒混合液(its)0.1%、血清蛋白替代物(serum protein substitute,sps)5%、人神经营养因子4(人nt4)10ng/ml和人重组卵泡刺激素(rhfsh)1miu/ml。
51.本实施例的体外培养人次级卵泡的培养液的制备方法与实施例1相似。
52.实施例3、一种体外培养人次级卵泡的培养液及其制备方法
53.一种体外培养人次级卵泡的培养液,含有以下质量浓度的组分:
54.αmem培养基、胎球蛋白2mg/ml、胰岛素-转铁蛋白-硒混合液(its)1%、血清蛋白替代物(serum protein substitute,sps)10%、人神经营养因子4(人nt4)200ng/ml和人重组卵泡刺激素(rhfsh)20miu/ml。
55.本实施例的体外培养人次级卵泡的培养液的制备方法与实施例1相似。
56.实施例4、一种体外培养人次级卵泡的培养液及其制备方法
57.一种体外培养人次级卵泡的培养液,含有以下质量浓度的组分:
58.αmem培养基、胎球蛋白1.2mg/ml、胰岛素-转铁蛋白-硒混合液(its)0.5%、血清蛋白替代物(serum protein substitute,sps)8%、人神经营养因子4(人nt4)150ng/ml和人重组卵泡刺激素(rhfsh)9miu/ml。
59.本实施例的体外培养人次级卵泡的培养液的制备方法与实施例1相似。
60.实施例5、一种体外培养人次级卵泡的培养液及其制备方法
61.一种体外培养人次级卵泡的培养液,含有以下质量浓度的组分:
62.αmem培养基、胎球蛋白0.8mg/ml、胰岛素-转铁蛋白-硒混合液(its)0.1%、血清蛋白替代物(serum protein substitute,sps)5%、人神经营养因子4(人nt4)50ng/ml和人重
组卵泡刺激素(rhfsh)5miu/ml。
63.本实施例的体外培养人次级卵泡的培养液的制备方法与实施例1相似。
64.对比例1
65.与实施例1相比,区别仅在于,体外培养人次级卵泡的培养液不含有人神经营养因子4,其余组分及制备方法与实施例1相同。
66.对比例2
67.与实施例1相比,区别仅在于,体外培养人次级卵泡的培养液中的人神经营养因子4的浓度为300ng/ml,其余组分及制备方法与实施例1相同。
68.对比例3
69.与实施例1相比,区别仅在于,体外培养人次级卵泡的培养液中的人重组卵泡刺激素的浓度为30miu/ml,其余组分及制备方法与实施例1相同。
70.对比例4
71.与实施例1相比,区别仅在于,使用人神经营养因子3替换人神经营养因子4,其余组分及制备方法与实施例1相同。
72.实施例6、一种提高卵母细胞成熟率的人次级卵泡体外培养方法
73.本实施例提供了一种提高卵母细胞成熟率的人次级卵泡体外培养方法,包括以下步骤:
74.1)卵巢组织消化及卵泡分离培养:
75.在无菌条件下,37℃恒温操作台上,在l-15培养基中将卵巢组织剪成大小约0.3~0.5mm3,在恒温培养箱(37℃)中放置60分钟,后用等体积的l-15培养液(含5% sps)终止反应。后将次级卵泡分离出来,选取基底膜完整,形态正常的卵泡,用平衡后的体外培养人次级卵泡的培养液(使用实施例1制备的体外培养人次级卵泡的培养液)清洗3次。每个卵泡单独置于96孔板中培养(37℃,5% co2),每个孔含200μl培养液,每隔一天更换一半培养液,直至终点事件出现则停止培养。
76.2)监测与检测:
77.每隔一天于显微镜观察卵泡形态变化,测量卵泡相互垂直的两个最大直径,取其平均值作为卵泡直径;每隔一天更换一半培养液,储存于-80℃冰箱中待测激素浓度。
78.3)终点事件定义:
79.卵母细胞从卵泡中孵出、卵母细胞萎缩退化、卵泡直径连续1周无增长;卵泡直径达到800μm;coc(卵丘细胞-卵母细胞复合物)从窦腔中孵出;体外培养达6周。
80.4)卵母细胞体外成熟培养(ivm):
81.当卵泡直径达到800μm或coc从窦腔中孵出时,将coc置于商用的体外成熟培养液(市场上的培养液均可)中进行体外成熟培养,分别在24、36、48小时后观察第一极体排出情况,排出第一极体者为成熟卵母细胞。
82.实验结果:
83.1、人体外培养卵泡生长情况:
84.如图1所示,人次级卵泡在实施例1制备的体外培养人次级卵泡的培养液体系中持续生长,最长可保持存活6周,存活率为33.3%(15/45);卵泡直径逐渐增大,每存活卵泡的窦腔形成率达100%,窦腔开始形成的时间平均为培养第2周。从图1-a至图1-f分别为体外
培养第1~6周,卵泡直径逐渐增大,图1-c图中可见窦腔(透亮处、白色箭头),窦腔体积逐渐增大,形成卵丘细胞-卵母细胞复合体(图1-d图白色箭头)。放大倍数100x,图右下角黑色标尺代表100μm。
85.如图2所示,分离得到的次级卵泡平均直径为253.00
±
46.0μm,次级卵泡在本发明实施例1制备的体外培养人次级卵泡的培养液中体外培养4周过程中,直径呈线性增长,卵泡每周平均直径的增长差异均有统计学意义,体外培养4周平均直径为967.00
±
41.1μm,较文献报道的可达到的直径(248~676μm)大。
86.2、体外培养人卵泡可正常分泌甾体激素:
87.如图3所示,在本发明实施例1制备的培养液中体外培养的人卵泡可正常分泌amh、雌二醇、孕酮。
88.3、人体外培养卵泡的卵母细胞体外成熟情况:
89.将窦卵泡中的coc进行体外成熟培养(采用实施例6的方法),可获得成熟卵母细胞(如图4所示,平均直径120
±
2.1μm),可见第一极体排出(黑色箭头),每存活卵泡的卵母细胞成熟率为46.7%(7/15),较文献报道(10.3%~21%)的成熟率高。
90.当实施例6培养方法中分别采用实施例2-5及对比例1-4制备的体外培养人次级卵泡的培养液时,人体外培养卵泡生长情况及人体外培养卵泡的卵母细胞体外成熟情况如表1所示。
91.表1
[0092][0093]
结论:本发明配制的体外培养人次级卵泡的培养液均能达到较文献报道更高的卵母细胞成熟率,其中实施例1的成熟率最高;如不添加神经营养因子4、或添加其他有相似结构的神经营养因子并不能达到类似的效果;当体外培养人次级卵泡的培养液中的组分超出或低于限定含量时,其卵母细胞成熟率也较低。
[0094]
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1