一种新型脂滴、溶酶体双靶向可变色荧光探针的制备及其应用
1.本发明涉及脂滴溶酶体双靶向荧光探针技术领域,尤其涉及一种新型脂滴、溶酶体双靶向可变色荧光探针的制备及其应用。
背景技术:
2.脂滴(ld)是由含有特殊组分的磷脂单分子层包裹中性的脂质核所形成的富含脂质的细胞器,存在于大多数物种和细胞类型中。脂滴的大小和生长与肥胖密切相关,具备很强的储脂能力,其生长的分子机制尚不明确。近些年的研究表明,脂滴在细胞中承担着与其他细胞器相互作用调节新陈代谢和维持能量平衡等很重要的作用。在细胞生长的过程中,当细胞膜需要膨胀时,脂滴内核中的甘油三酯会通过脂解作用或噬脂作用产生脂肪酸从而供给膜的生物合成;脂滴储存容量的增加会引起未折叠蛋白响应(upr)机制的上调从而缓解内质网应激反应而胞内脂滴的异常是各种疾病的标志,例如脂肪肝病,高脂血症和ii型糖尿病。另一个重要的细胞器是溶酶体,它是一种酸性细胞器,用于消化和去除细胞中的内源性和内吞性物质。事实上,脂滴和溶酶体在某些生物过程中也相互关联,并且脂滴中的组分可被溶酶体酶降解。此外,脂滴和溶酶体之间的相互作用与溶酶体贮积病和慢性炎症有很大关系。因此,监测脂滴和溶酶体之间的动态过程对其相关疾病的治疗具有重要意义。总的来说,一方面脂滴作为一种动态细胞器,它不但参与生物体内脂质体的新陈代谢,也调节膜的转移,参与蛋白质降解与信号传导过程。另一方面,脂滴与溶酶体协同作用对于细胞能量代谢起到关键性作用。
3.因此,开发出一种脂滴与溶酶体双靶向可探索脂滴与溶酶体相互作用的荧光探针,对于研究脂滴与溶酶体的功能与作用机理来说是非常具有实际应用意义的。
技术实现要素:
4.本发明的目的是为了解决现有技术中没有针对脂滴与溶酶体双靶向的探针的技术问题。
5.为了实现上述目的,本发明采用了如下技术方案:
6.一种基于hbi的席夫碱类化合物(dpabp-bi),其特征在于:所述化合物dpabp-bi的结构式如下(i):
[0007][0008]
上述结构式中,r为甲基,羟甲基,溴乙基结构单元。
[0009]
本技术还提供了化合物dpabp-bi的应用包括:化合物dpabp-bi在脂滴识别中的应用。
[0010]
化合物dpabp-bi在线粒体识别中的应用。
[0011]
化合物dpabp-bi在区分线粒体和脂滴中的应用。
[0012]
化合物dpabp-bi在识别斑马鱼体内脂肪类化合物中的应用。
[0013]
一种化合物dpabp-bi的制备方法,其特征在于:合成路线为:
[0014][0015]
优选的,包含以下步骤:
[0016]
i)1,3偶极环加成反应制备(ii)所示的hbi衍生物;
[0017]
2)通过式(ii)所示的硝基hbi化合物在钯碳催化下与氢气发生氢化反应制备式(iii)所示的化合物;
[0018]
3)通过(iii)所示的化合物与三(4-甲酰苯基)胺发生醛胺缩合反应制备(i)所示的基于hbi的席夫碱类化合物;
[0019]
[0020]
优选的,包含以下具体步骤:
[0021]
将1当量的对硝基苯甲醛、1.2当量的乙胺溶液以及50ml乙醇加入100ml圆底烧瓶中,开启搅拌,在室温下搅拌过夜,反应结束后旋蒸移去溶剂,油泵抽干得到淡黄色固体1;
[0022]
向50ml圆底烧瓶中加入1.5当量的2-((1-乙氧基亚乙基)氨基)乙酸甲酯、1当量的化合物1和15ml甲醇,室温反应20h,反应结束后过滤,沉淀用少量甲醇洗涤,滤液浓缩后静置使其析出沉淀,反复进行结晶洗涤浓缩的操作直至没有沉淀析出,收集得到淡黄色固体2;
[0023]
向250ml双颈烧瓶中加入1当量的化合物2、10%的pd/c和20ml乙醇,抽真空/充氢气3次,室温下反应30min,反应完全后,快速滤去pd/c,滤液浓缩抽干并进行ar气保护得化合物3,然后直接投入下一步反应,向25ml双颈烧瓶中加入1当量的三(4-甲酰基苯基)胺和1.2当量的化合物3,抽真空/充ar气三次,向反应体系中加入20ml乙醇,在30℃下反应2天,反应结束后快速柱层析分离,得红色固体dpabp-bi。
[0024]
本技术的化合物dpabp-bi以hbi单元为中心,通过与三(4-甲酰苯基)胺醛胺缩合得到席夫碱类化合物,具有大斯托克位移,红光发射,双光子激发,低自发光的特点。
附图说明
[0025]
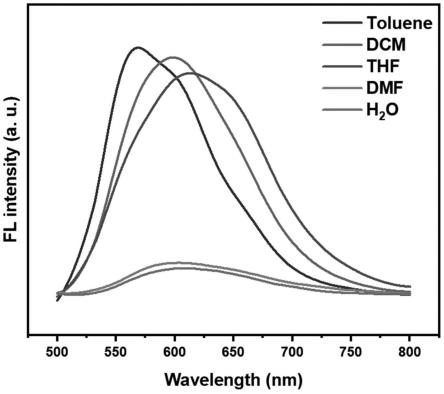
图1为本发明一实施方式中化合物dpabp-bi在不同溶剂中的荧光发射谱图;
[0026]
图2为本发明一实施方式中化合物dpabp-bi对脂滴的靶向识别结果图;
[0027]
图3为本发明一实施方式中化合物dpabp-bi和商业化脂滴成像试剂bodipy 493/503共定位分析图;
[0028]
图4为本发明一实施方式中化合物dpabp-bi对溶酶体的靶向识别结果图;
[0029]
图5为本发明一实施方式中化合物dpabp-bi和商业化溶酶体成像试剂lsyobrite blue共定位分析图;
[0030]
图6为本发明一实施方式中化合物dpabp-bi对脂滴和溶酶体同时成像图;
[0031]
图7为本发明一实施方式中化合物dpabp-bi对斑马鱼体内脂肪类物质的成像图。
具体实施方式
[0032]
为使本发明的目的、技术方案和优点更加清楚,以下结合具体实施例,对本发明作进一步地详细说明。
[0033]
在下面的描述中阐述了很多具体细节以便于充分理解本发明,但是,本发明还可以采用不同于在此描述的其他方式来实施,因此,本发明并不限于下面公开说明书的具体实施例的限制。
[0034]
实施例1:
[0035]
本技术提供了一种基于hbi(绿色荧光蛋白生色团)的席夫碱类化合物dpabp-bi,所述dpabp-bi的结构是如下(ⅰ):
[0036][0037]
上述结构式(ⅰ)中,r为甲基,羟甲基,溴乙基结构单元。
[0038]
实施例2:
[0039]
本技术还提供了所述dpabp-bi的制备方法,合成路径如下:
[0040][0041]
所述制备方法包含以下步骤:
[0042]
s1:制备化合物1:使用乙醇、乙胺及对硝基苯甲醛在室温下反应得到化合物1。
[0043]
具体的,在一实施方式中,将1当量的对硝基苯甲醛、1.2当量的乙胺溶液以及50ml乙醇加入100ml圆底烧瓶中,开启搅拌。在室温下搅拌过夜,反应结束后旋蒸移去溶剂,油泵抽干得到淡黄色固体1,产率90%;
[0044]
化合物1:1h nmr(600mhz,cdcl3):δ8.38(s,1h),8.27(d,j=9.0hz,2h),7.90(d,j=9.0hz,2h),3.72(q,j=7.2hz,2h),1.34(t,j=7.2hz,3h)
13
c nmr(100mhz,cdcl3).δ158.0,148.8,141.8,128.6,123.7,56.0,15.9。
[0045]
s2:制备化合物2:
[0046]
使用化合物1、2-((1-乙氧基亚乙基)氨基)乙酸甲酯及甲醇进行反应获得化合物2。
[0047]
具体的,在一实施方式中,向50ml圆底烧瓶中加入1.5当量的2-((1-乙氧基亚乙基)氨基)乙酸甲酯、1当量的化合物1和15ml甲醇,室温反应20h。反应结束后过滤,沉淀用少量甲醇洗涤,滤液浓缩后静置使其析出沉淀,反复进行结晶洗涤浓缩的操作直至没有沉淀析出。收集得到淡黄色固体2,产率75%;
[0048]
化合物2:1h nmr(600mhz,cdcl3)δ8.28(d,j=9.0hz,2h),8.24(d,j=9.0hz,2h),7.05(s,1h),3.68(q,j=6.6hz,2h),2.43(s,3h),1.27(t,j=6.6hz,3h).
13
c nmr(100mhz,cdcl3)δ170.1,165.2,147.6,141.4,140.4,132.4,123.6,123.0,35.5,15.7,14.5。
[0049]
s3:制备化合物3:
[0050]
使用化合物2、pd/c及h2进行反应获得化合物3.
[0051]
具体的,在一实施方式中,向250ml双颈烧瓶中加入1当量的化合物2、10%的pd/c和20ml乙醇,抽真空/充氢气3次,室温下反应30min。反应完全后,快速滤去pd/c,滤液浓缩抽干并进行ar气保护得化合物3
[0052]
s4:制备化合物dpabp-bi:
[0053]
使用化合物3、三(4-甲酰基苯)胺及乙醇行反应获得化合物dpabp-bi。
[0054]
具体的,在一实施方式中,向25ml双颈烧瓶中加入1当量的三(4-甲酰基苯基)胺和1.2当量的化合物3,抽真空/充ar气三次。向反应体系中加入20ml乙醇,在30℃下反应2天。反应结束后快速柱层析分离,得红色固体dpabp-bi。产率:60%。
[0055]
化合物dpabp-bi:1h nmr(400mhz,cdcl3)δ7.93(d,j=8.4hz,2h),7.73(d,j=8.3hz,2h),7.55-7.51(m,3h),7.32-7.28(m,5h),7.15(d,j=7.4hz,8h),7.08(t,j=7.3hz,4h),4.12-4.10(m,2h),1.26(s,3h),0.88(t,j=6.8hz,3h).
13
c nmr(100mhz,cdcl3)δ158.3,154.2,149.0,148.4,147.3,146.6,134.6,132.7,130.3,129.4,128.0,127.0,126.9,124.9,124.4,124.0,123.5,123.1,119.0,34.5,31.4,30.2.
[0056]
实施例3:
[0057]
请参阅图1,将实施例2中制备的化合物dpabp-bi溶解在不同溶剂(toluene、dcm、thf、dmf及h2o)中,并对其荧光发射进行测试;可以看出该化合物dpabp-bi具有红色荧光发射。
[0058]
实施例4:
[0059]
向hepg2细胞中加入20μl的bodipy(1mm dmso溶液),再分别加入4μl的dpabp-bi(1mm dmso溶液),在培养箱中孵育30min,然后使用共聚焦显微镜进行拍摄。
[0060]
请参阅图2,图2中fitc通道为商业化脂滴成像试剂bodipy 493/503、tritc通道为实施例2化合物dpabp-bi通道。通过merge通道定性的表明dpabp-bi可靶向脂滴成像。
[0061]
实施例5:
[0062]
请参阅图3,将实施例4中的结果进行分析,可计算出化合物dpabp-bi对脂滴的共定位系数,图3中可以看出化合物dpabp-bi的共定位系数为0.98,并表明dpabp-bi对脂滴具有非常优异的靶向性。
[0063]
实施例6:
[0064]
请参阅图4,向hepg2细胞中加入5μl的lysoblue(1mm in dmso)溶液,再分别加入4μl的dpabp-bi(1mm in dmso)溶液,分别在培养箱中孵育2-24h,然后使用共聚焦显微镜进行拍摄。
[0065]
图4中dapi通道为商业化溶酶体成像试剂lysoblue;fitc通道为化合物dpabp-bi通道,通过merge通道定性的表明dpabp-bi可靶向溶酶体成像。
[0066]
实施例7:
[0067]
请参阅图5,对实施例6中的结果进行分析,计算出化合物dpabp-bi对溶酶体的共定位系数;
[0068]
其中图5中a-c分别为化合物dpabp-bi对溶酶体不同时间的共定位图,并且dpabp-bi的共定位系数分别为0.35、0.69、0.83,表明dpabp-bi对溶酶体具有优异的靶向性。
[0069]
实施例8,:
[0070]
请参阅图6,向hela细胞中加入4μl的dpabp-bi(1mm in dmso)溶液,在培养箱中孵育30min,然后使用共聚焦显微镜进行拍摄;
[0071]
图6中tritc通道为脂滴显像、fitc通道为溶酶体显像;化合物dpabp-bi在溶酶体中的绿色荧光和脂滴中的红色荧光存在部分位置的重叠,这可能是由于溶酶体和脂滴形态相似,在空间位置上的重叠所导致的。同时,红色和绿色存在大量的非重叠区域,说明目标分子的确可以对溶酶体和脂滴同时染色。
[0072]
实施例9
[0073]
请参阅图7,向斑马鱼中加入4μl的dpabp-bi(1mm in dmso)溶液,在室温下孵育2h,然后使用共聚焦显微镜进行拍摄。
[0074]
图7中,tritc通道为斑马鱼体内脂肪类物质的显像;fitc通道为dpabp-bi分解过程的显像。表明,本发明可以有效的对斑马鱼体内的脂肪类物质经行检测,同时可以观察到dpabp-bi探针本身的分解代谢过程。
[0075]
本技术的化合物dpabp-bi以hbi单元为中心,通过与三(4-甲酰苯基)胺醛胺缩合得到席夫碱类化合物,具有大斯托克位移,红光发射,双光子激发,低自发光的特点。
[0076]
以上所述仅为本发明的实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的权利要求范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1