一种检测卵巢癌的环状RNA生物标志物、特异性引物对、试剂盒及其应用的制作方法
一种检测卵巢癌的环状rna生物标志物、特异性引物对、试剂盒及其应用
技术领域
1.本发明属于基因检测技术领域,具体地说,涉及一种检测卵巢癌的环状rna生物标志物、特异性引物对、试剂盒及其应用。
背景技术:
2.卵巢癌作为卵巢肿瘤的一种恶性肿瘤,是威胁妇女健康的最大疾患之一。虽然卵巢癌的发病率比宫颈癌和子宫内膜癌低,在妇科恶性肿瘤中位居第三位,但其死亡率却排在妇科癌症首位,甚至大于宫颈癌及子宫内膜癌的死亡率之和。这可能与卵巢处于腹部比较深的地方有关,往往造成卵巢癌发现的时候往往是晚期,而此时癌细胞扩散到了腹部其他器官,治愈起来比较困难。因此,非常有必要开发一种检测灵敏度和特异性理想的用于卵巢癌诊断的生物标志物和试剂盒,为卵巢癌患者的确诊及治疗方案选择提供辅助参考。
3.环状rna是一种具有闭合环状结构的rna,不可依赖于5端的帽子结构来翻译蛋白。与此同时,环状rna可以抵抗rna酶的水解作用,具有比线性rna更强的稳定性。换句话说,环状rna具有保守性,并具有时间和组织表达特异性是一种潜在的疾病诊断分子生物标志物。已有研究表明,肿瘤的发生、发展与环状rna的表达异常与有关。譬如, hsa_circrna_0047905,hsa_circrna_0138960和has_ circrna_7690-15与胃癌的形成息息相关。此外,hsa_circrna_0001785与乳腺癌的发生、发展有关。
4.有鉴于此,为了更好的服务卵巢癌患者的诊断,本发明申请人公开了一种检测卵巢癌的环状rna生物标志物、特异性引物对、试剂盒及其应用,用于卵巢癌的诊断,为卵巢癌患者的确诊和治疗方案选择提供辅助参考。
技术实现要素:
5.本发明要解决的技术问题在于克服卵巢癌诊断现有技术的不足,提供一种可以克服上述问题或者部分地解决上述问题的一种检测灵敏度和特异性理想的用于卵巢癌诊断的生物标志物和试剂盒,为卵巢癌患者的确诊及治疗方案选择提供辅助参考。
6.为了达到上述目的,本发明的技术方案是:本发明提供一组用于卵巢癌诊断的环状rna生物标志物,包括seq id no. 1所示的hsa_circrna_0007132和seq id no.2所示的hsa_circrna_0078217两种环状rna。
7.上述生物标志物在制备诊断卵巢癌患者的试剂盒或试剂中的应用。
8.上述生物标志物在诊断肺癌的环状rna芯片中的应用。
9.上述生物标志物在制备或筛选卵巢癌靶向药物中的应用。
10.本发明还提供一组用于卵巢癌诊断的环状rna生物标志物的引物组合,所述引物组合包括针对hsa_circrna_0007132的特异性引物和针对hsa_circrna_0078217的特异性引物。
11.进一步地,上述针对hsa_circrna_0007132的特异性引物包括seq id no. 3所示
的上游引物和seqidno.4所示的下游引物。
12.进一步地,上述针对hsa_circrna_0078217的特异性引物包括seqidno.5所示的上游引物和seqidno.6所示的下游引物。
13.进一步地,上述环状rna生物标志物的引物组合在制备诊断卵巢癌的试剂盒或试剂中的应用。
14.进一步地,制备诊断卵巢癌的试剂盒包括trizol裂解液、氯仿、异丙醇、75%乙醇、depc水和qrt-pcr反应液。
15.进一步地,所述诊断卵巢癌的试剂盒中的qrt-pcr反应液包括:pcr缓冲液、mg
2+
、dntps、sybr、taqdna聚合酶、模板和ddh2o。
16.进一步地,上述环状rna生物标志物的引物组合在制备或筛选卵巢癌靶向药物的应用。
17.本发明还提供一种诊断卵巢癌的试剂盒,其中包括上述的环状rna生物标志物的引物的任意一种或两种。
18.采用上述技术方案后,本发明与现有技术相比具有以下有益效果:(1)本发明通过基因芯片技术和rt-qpcr技术,筛选出用于检测卵巢癌的环状rna生物标志物,通过上述两种方法联合筛选的生物标志物,在卵巢癌发生时表达量变化差异性大,利于应用于临床检测;(2)针对两种筛选出的环状rna生物标志物的特异性引物,其具有特异性强和敏感性高等优点,通过rt-qpcr技术,可以准确地检测出所筛选的生物标志物的含量;(3)两种筛选出的环状rna生物标志物在卵巢癌发生时表达量发生显著的变化,在制备或筛选卵巢癌靶向药物中具有应用价值;(4)两种筛选出的环状rna生物标志物在制备诊断卵巢癌患者的试剂盒或试剂方面具有应用价值。
附图说明
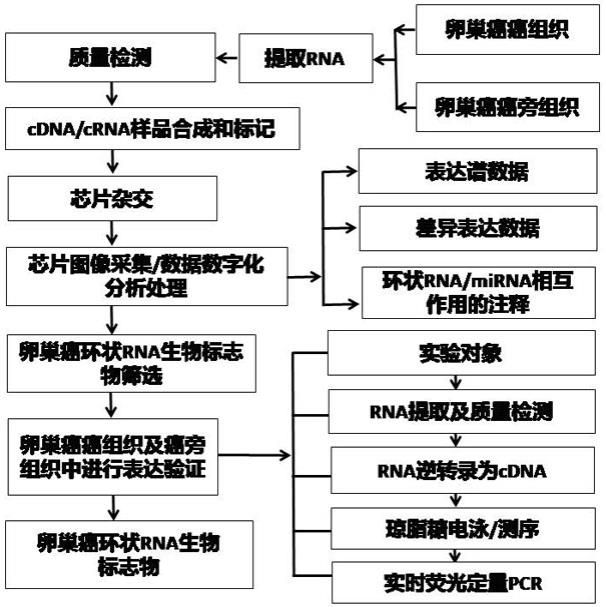
19.图1为卵巢癌环状rna生物标志物的筛选流程图。
具体实施方式
20.为使本发明实施例的目的、技术方案和优点更加清楚,下面将结合本发明的实施例,对本发明实施例中的技术方案进行清楚、完整地描述。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。图1为卵巢癌环状rna生物标志物的筛选流程图。
21.实施例一卵巢癌环状rna生物标志物的初步筛选第一步,对样本中的rna进行抽提及对所抽提的rna进行质量检测:首先收集符合伦理要求的术前未接受过化疗和放疗的病理学诊断为卵巢癌的患者的癌组织及癌旁组织,然后用trizol法对样本中的rna进行提取,随后保存在-80摄氏度。所提取rna的质量通过紫外吸收法和凝胶电泳法来检测。与此同时,将总体rna分为等量2份,1份采用rnaser处理,另一份不作处理,在经过纯化和反转录后,用荧光定量pcr检测gapdh和环状rna的ct值表达来评估线性转录本去除效率。所提取rna的完整性采用琼脂糖凝胶电泳来评估。结果表明,
所提取的rna都达到检测纯度和浓度等方面的要求,且较为完整,可用于后续实验;第二步,采用商用试剂盒将rnaser处理后的rna用随机引物反转录为带有t7promoter的cdna序列,再将cdna转录为荧光标记的 crna序列;第三步,按照卵巢癌分期(ⅰ期:80/200;ⅱ期:72/200;ⅲ期:48/200)及组织来源(癌和癌旁),将从200个样本提取的rna分为6组,每组内各rna样本混合后利用arraystarhumancircrnaarrayv2比较不同环状rna的表达情况。与此同时,按照标准条件的要求,对标记好的探针和高密度基因组芯片进行杂交;第四步,对第三步中所制成芯片的荧光强度采用芯片扫描仪进行扫描,并将实验结果转换成相应的数字型数据并进行分析;箱图分析结果表明6组环状rna检测结果具有良好的均一性;由差异倍数和p值所得火山图给出显示差异倍数与p存在显著差异表达的环状rna为hsa_circrna_0007132、hsa_circrna_0078217、hsa_circrna_0000039、hsa_circrna_0088865、hsa_circrna_0095226、hsa_circrna_0008702、hsa_circrna_0002501 和hsa_circrna_00035341;第五步,对第四步获得的原始数据分析及靶mirna预测:s1.在对表达谱数据使用r软件中的limma包进行标准化处理后,再进行低强度滤波,保留6个样本中至少有3个样本的标志为“p”或“m
”ꢀ
(所有目标值),以做进一步分析;本发明针对人类环状rna设计探针,3组样本共检测到9765个环状rna,包括8389个外显子类型环状rna、564个内含子类型环状rna、480个正义链重叠类型环状rna、232个反义链类型环状rna、100个基因间类型环状rna;s2.对每组环状rna表达谱差异采用差异倍数进行比较,并采用t检验进行显著性差异评估。通过差异倍数和p值等来筛选显著差异表达的环状rna。当环状rna的差异倍数大于等于2.0且p小于等于0.05时,该环状rna被认为存在显著差异表达。结果表明:各期样本检测到的差异表达的环状rna上调的数量分别为:656(i期),437(ii期),182(iii期);各期样本检测到的差异表达的环状rna下调的数量分别为:994(i期),780(ii期),363(iii期)。可以看出,从i到iii期样本检测到的差异表达的环状rna数量下调的比上调的多。与此同时,检测到的环状rna数量从i到iii期越来越少;s3. 环状rna/mirna相互作用的注释:采用 t a r g e t s c a n和m i r a n d a为基础的 a r r a y s t a r 's h o m e-mademirnatarget预测软件来预测环状rna/mirna之间的作用,并对存在显著差异表达的环状rna的预测相应的靶mirna进行详细注释;s4. 筛选候选卵巢癌环状rna生物标志物:卵巢癌环状rna生物标志物根据以下原则进行筛选:差异倍数大于等于2,rawintensity大于等于200,及环状rna长度在200-2000bp之间,p值小于等于0.05,预测靶mirnas或宿主基因与卵巢癌存在相关性。结果表明,样本检测到的从i到iii期共有的显著差异表达的环状rna有369个,其中87个上调,282个下调。随后,按差异倍数值大小,再结合环状rna的rawintensity值大小进行进一步筛选,得到175个卵巢癌环状rna生物标志物,其中54个上调,121个下调。结合p值及预测的mirna或宿主基因与卵巢癌相关性,筛选出hsa_circrna_0007132、hsa_circrna_0078217、hsa_circrna_0000039、hsa_circrna_0088865、hsa_circrna_0095226进行进一步验证;
no.7);反向引物:tttgcccattcataatttgt(seq id no.8))、hsa_circrna_0055190(正向引物: tgggatagagggagcccagc(seq id no.9);反向引物:tgagtaacggacagcggaac(seq id no.10))、hsa_circrna_00035341 (正向引物: ttggcagagacatatgtcagg(seq id no.11);反向引物:ctatgtaaccttgtgatcagt(seq id no.12));s2. 实时荧光定量pcr (rt-qpcr)检测:首先,按照rt-qpcr试剂盒说明书配制pcr反应液,并进行分装,在每个分装有pcr反应液的pcr管中依次加入cdna模板,并配置成20微升体系的反应液。与此同时,采用无rnase水作为阴性对照;其次,将pcr管置于实时荧光定量pcr仪中进行实时荧光定量pcr反应;然后,分析卵巢癌癌组织和癌旁组织hsa_circrna_0007132、hsa_circrna_0078217、hsa_circrna_0002501、hsa_circrna_0055190和hsa_circrna_00035341的表达量。结合分析熔解曲线是否为单峰、琼脂糖凝胶电泳的结果来确定产物的唯一性,再进一步用测序的方法确定产物是否为目的产物,然后计算各样本的δct(ct目的基因-ct内参基因)、δδct(δct癌-δct癌旁)、2
–
δct及2
–
δδct的值。以2
–
δct代表目的环状rna在组织中的相对表达量,2
–
δδct代表目的环状rna的差异表达倍数;在退火延伸阶段45-95摄氏度收集卵巢癌癌组织和癌旁组织中所提取的hsa_circrna_0007132、hsa_circrna_0078217、hsa_circrna_0002501、hsa_circrna_ 0055190和hsa_circrna_00035341的rt-qpcr反应的熔解曲线,获取相应环状rna的特异性熔解曲线,结果显示,各环状rna的产物特异性熔解曲线均为单峰,说明各环状rna的产物是唯一的。各环状rna产物的琼脂糖凝胶电泳结果进一步确定其产物唯一。而进一步的测序结果显示可比对上各环状rna原始序列首尾相接后的拼接序列,且各环状rna产物均跨各自的剪接位点,进一步确定各环状rna产物不仅唯一,而且均为目的产物;s3. 统计学分析对卵巢癌组织和癌旁组织目的环状rna的相对表达量进行统计分析,通过k-s检验数据是否满足正态分布,若符合正态分布,则选用配对t检验,若不符合正态分布,则用非参数检验中的wilcoxon秩和检验,对环状rna的表达与临床资料的相关性分析,采用卡方检验的方法。采用kaplan-meier生存分析法评估环状rna的表达与卵巢癌癌预后的关系。p<0.05表示差异具有统计学意义;rt-qpcr的结果结合统计学分析进行正态性检验。结果表明,所有数据均不符合正态分布。故,采用非参数检验中的wilcoxon秩和检验来统计分析和比较卵巢癌和卵巢癌癌旁的目的环状rna的相对表达量。其中,hsa_circrna_0007132在癌组织的相对表达量的中位数为5.3612
×
10-5
,在癌旁组织的相对表达量的中位数为2.2238
×
10-5
,p值为0.0024,上调比例为70%(140/200); hsa_circrna_0078217在癌组织的相对表达量的中位数为7.6185
×
10-5
,在癌旁组织的相对表达量的中位数为3.5764
×
10-5
,p值为0.0005,上调比例为75%(150/200);hsa_circrna_0002501在癌组织的相对表达量的中位数为1.8036
×
10-5
,在癌旁组织的相对表达量的中位数为1.8179
×
10-5
,p值为0.3058,上调比例为32%(64/200);hsa_circrna_00035341在癌组织的相对表达量的中位数为2.9823
×
10-5
,在癌旁组织的相对表达量的中位数为6.3048
×
10-5
,p值为0.0001,下调比例为87%(174/200)。可以看出,hsa_circrna_0007132、hsa_circrna_0078217、hsa_circrna_00035341在卵巢癌和卵巢癌中的
表达差异有意义,而hsa_circrna_0002501则无差异,但hsa_circrna_0055190的rt-qpcr结果与芯片结果相反;s4.差异表达的环状rna与临床资料的相关分析:采用卡方检验的统计方式对hsa_circrna_0007132、hsa_circrna_0078217、hsa_circrna_00035341的相对表达与临床资料进行相关性分析,发现只有hsa_circrna_0007132和hsa_circrna_0078217的表达上调与肿瘤大小具有相关性,p值分别为0.008和0.011;s5.差异表达的环状rna的预测靶mirna功能查阅采用arraystarshome-mademirnatarget预测软件来预测hsa_circrna_0007132和hsa_circrna_0078217的靶mirnas,并对hsa_circrna_0007132和hsa_circrna_0078217的预测靶mirnas进行了详细注释。研究表明hsa_circrna_0007132的预测靶mirnahas_mir_1273g_3p是潜在的卵巢癌诊断生物标志物(archgynecolobstet.298(6)(2018)1173-1180)。而在hsa_circrna_0078217的预测靶mirna为has_mir_542_5p。一些证据表明mir-542-5p可能在卵巢癌中发挥着潜在的抑癌作用(现代肿瘤医学,23(9)(2015)1180-1184)。
23.本发明进一步分析了卵巢癌的环状rna表达谱,发现hsa_circrna_0007132和hsa_circrna_0078217在卵巢癌中存在差异表达,且hsa_circrna_0007132和hsa_circrna_0078217的预测mirna参与卵巢癌进展调控。由此可见,hsa_circrna_0007132和hsa_circrna_0078217可作为卵巢癌的潜在生物标志物。
24.应理解,在阅读了本发明的上述内容后,本领域技术人员可以对本发明进行各种修改和润色,然而均是以检测本发明所述的环状rna相关,或者是本发明所述的环状rna的各种形式的应用,这些修改或润色均属于本发明的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1