用于制备的制作方法
用于制备e-选择素抑制剂中间体的方法
1.本技术根据
35 u.s.c.
§
119(e)
要求于
2021
年2月
18
日提交的第
63/150,940
号美国临时申请的权益,所述美国临时申请据此通过援引整体并入
。
2.提供了用于合成中间体的方法,所述中间体可用于合成
e-选择素抑制剂
。
还提供了由所述方法获得的有用中间体
。
这类化合物描述于例如第
9,796,745
号和第
9,867,841
号美国专利,第
15/025,730
号
、
第
15/531,951
号
、
第
16/081,275
号
、
第
16/323,685
号和第
16/303,852
号美国专利申请以及第
pct/us2018/067961
号
pct
国际申请
。
3.选择素是一组结构相似的对于介导白细胞与内皮细胞的结合重要的细胞表面受体
。
这些蛋白是1型膜蛋白,并且由氨基末端凝集素结构域
、
表皮生长因子
(egf)
样结构域
、
可变数目的补体受体相关重复
、
疏水结构域跨越区和细胞质结构域组成
。
结合相互作用似乎是通过选择素的凝集素结构域和各种碳水化合物配体的接触介导的
。
4.有三种已知的选择素:
e-选择素
、p-选择素和
l-选择素
。e-选择素存在于活化的内皮细胞表面,其排列在毛细血管的内壁上
。e-选择素结合碳水化合物唾液酸化-路易斯
x
(sle
x
)
,其作为某些白细胞
(
单核细胞和嗜中性粒细胞
)
的表面上的糖蛋白或糖脂呈现,并且帮助这些细胞粘附在周围组织被感染或损伤的区域中的毛细管壁;并且
e-选择素还结合在许多肿瘤细胞上表达的唾液酸化-路易斯a(slea)。p-选择素在发炎的内皮和血小板上表达,并且还识别
sle
x
和
slea,但还含有与硫酸化酪氨酸相互作用的第二位点
。
当毛细血管附近的组织被感染或损伤时,
e-选择素和
p-选择素的表达通常增加
。l-选择素在白细胞上表达
。
选择素介导的细胞间粘附是选择素介导的功能的实例
。
5.尽管需要选择素介导的细胞粘附来抵抗感染和破坏外来物质,但存在这样的情况,其中此类细胞粘附是不希望的或过度的,导致组织损伤而非修复
。
例如,许多病状
(
例如,自身免疫性疾病和炎性疾病
、
休克和再灌注损伤
)
涉及白细胞的异常粘附
。
此类异常的细胞粘附也可能在移植和移植排斥中起作用
。
此外,一些循环癌细胞似乎利用炎性机制结合活化的内皮
。
在这种情况下,可能需要调节选择素介导的细胞间粘附
。
6.本文提供了用于制备化合物
16(
可用于合成
e-选择素抑制剂的中间体
)
的新方法
。
7.附图说明
8.图
1a、
图
1b
和图
1c
例示出化合物
16
的合成
。
9.在一些实施方案中,提供了用于制备化合物
16
的方法,其中所述方法包括化合物
15
的氢化
。
[0010][0011]
在一些实施方案中,化合物
15
的氢化包括使用
h2和
pd/c。
在一些实施方案中,化合物
15
的氢化在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂选自醇
。
在一些实施方案中,所述至少一种溶剂是
2-丙醇
。
在一些实施方案中,所述至少一种溶剂选自酯和醚
。
在一些实施方案中,所述至少一种溶剂是
thf。
在一些实施方案中,所述至少一种溶剂是水
。
在一些实施方案中,化合物
15
的氢化在至少两种溶剂的存在下进行
。
在一些实施方案中,所述至少两种溶剂是
2-丙醇和
thf。
在一些实施方案中,化合物
15
的氢化在至少三种溶剂的存在下进行
。
在一些实施方案中,所述至少三种溶剂是
2-丙醇
、thf
和水
。
[0012]
在一些实施方案中,用于制备化合物
16
的方法包括化合物
14
的
meo-三苯甲基裂解以提供化合物
15。
[0013][0014]
在一些实施方案中,化合物
14
的
meo-三苯甲基裂解包括使用至少一种酸
。
在一些实施方案中,所述至少一种酸选自无机酸
。
在一些实施方案中,所述至少一种酸选自有机酸
。
在一些实施方案中,所述至少一种酸是盐酸
。
在一些实施方案中,所述至少一种酸选自三氟乙酸
、
三氯乙酸
、
甲酸
、
对甲苯磺酸和甲磺酸
。
在一些实施方案中,所述至少一种酸是三氯乙酸
。
[0015]
在一些实施方案中,化合物
14
的
meo-三苯甲基裂解在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂选自醇
。
在一些实施方案中,所述至少一种溶剂是甲醇
。
在一些实施方案中,所述至少一种溶剂是水
。
在一些实施方案中,所述至少一种溶剂是二氯甲烷
。
在一些实施方案中,化合物
14
的
meo-三苯甲基裂解在至少两种溶剂的存在下进行
。
在一些实施方案中,所述至少两种溶剂是二氯甲烷和甲醇
。
[0016]
在一些实施方案中,用于制备化合物
16
的方法包括化合物
13
的烯丙氧羰基裂解和酰化以提供化合物
14。
[0017]
[0018]
在一些实施方案中,化合物
13
的烯丙氧羰基裂解
/
酰化包括使用至少一种碱
。
在一些实施方案中,所述至少一种碱是
4-甲基吗啉
。
在一些实施方案中,化合物
13
的烯丙氧羰基裂解
/
酰化包括使用至少一种酸
。
在一些实施方案中,所述至少一种酸是乙酸
。
在一些实施方案中,化合物
13
的烯丙氧羰基裂解
/
酰化包括使用至少一种酸酐
。
在一些实施方案中,所述至少一种酸酐是乙酸酐
。
[0019]
在一些实施方案中,化合物
13
的烯丙氧羰基裂解
/
酰化包括使用至少一种膦
。
在一些实施方案中,所述至少一种膦是三苯基膦
。
在一些实施方案中,化合物
13
的烯丙氧羰基裂解
/
酰化包括使用至少一种催化剂
。
在一些实施方案中,所述至少一种催化剂是
pd[(c6h5)3p]4。
[0020]
在一些实施方案中,化合物
13
的烯丙氧羰基裂解
/
酰化在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是二氯甲烷
。
在一些实施方案中,所述至少一种溶剂是甲苯
。
[0021]
在一些实施方案中,用于制备化合物
16
的方法包括化合物
11
与化合物
12
的
o-烷基化以提供化合物
13。
[0022][0023]
在一些实施方案中,化合物
11
的
o-烷基化包括使用至少一种烷基锡
。
在一些实施方案中,所述至少一种烷基锡是氧化二丁基锡
(iv)。
在一些实施方案中,化合物
11
的
o-烷基化在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是乙腈
。
在一些实施方案中,所述至少一种溶剂是甲醇
。
在一些实施方案中,所述至少一种溶剂是甲苯
。
在一些实施方案中,化合物
11
的
o-烷基化在至少两种溶剂的存在下进行
。
在一些实施方案中,所述至少两种溶剂是甲苯和乙腈
。
在一些实施方案中,化合物
11
的
o-烷基化包括至少一种氟化物
。
在一些实施方案中,所述至少一种氟化物是氟化铯
。
[0024]
在一些实施方案中,用于制备化合物
16
的方法包括化合物
10
的甲氧基-三苯甲基化以提供化合物
11。
[0025]
[0026]
在一些实施方案中,化合物
10
的甲氧基-三苯甲基化包括使用
4-meo-三苯甲基-cl。
在一些实施方案中,化合物
10
的甲氧基-三苯甲基化包括使用至少一种碱
。
在一些实施方案中,所述至少一种碱选自
dabco、
吡啶和
2,6-二甲基吡啶
。
在一些实施方案中,化合物
10
的甲氧基-三苯甲基化在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是二氯甲烷
。
在一些实施方案中,所述至少一种溶剂是
me-thf。
在一些实施方案中,化合物
10
的甲氧基-三苯甲基化在至少两种溶剂的存在下进行
。
在一些实施方案中,所述至少两种溶剂是
methf
和二氯甲烷
。
[0027]
在一些实施方案中,用于制备化合物
16
的方法包括化合物9的脱乙酰化以提供化合物
10。
[0028][0029]
在一些实施方案中,化合物9的脱乙酰化包括使用至少一种碱
。
在一些实施方案中,所述至少一种碱选自醇盐
。
在一些实施方案中,所述至少一种碱是
naome。
在一些实施方案中,化合物9的脱乙酰化在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是甲醇
。
在一些实施方案中,所述至少一种溶剂是乙酸甲酯
。
在一些实施方案中,化合物9的脱乙酰化在至少两种溶剂的存在下进行
。
在一些实施方案中,所述至少两种溶剂是甲醇和乙酸甲酯
。
[0030]
在一些实施方案中,化合物
10
作为乙醇溶剂化物结晶
。
在一些实施方案中,化合物
10
在至少一种溶剂的存在下作为乙醇溶剂化物结晶
。
在一些实施方案中,所述至少一种溶剂是乙醇
。
在一些实施方案中,化合物
10
在至少两种溶剂的存在下作为乙醇溶剂化物结晶
。
在一些实施方案中,所述至少两种溶剂是乙醇和水
。
在一些实施方案中,结晶化合物
10
是乙醇溶剂化物
。
在一些实施方案中,结晶化合物
10
乙醇溶剂化物的特征在于棒状晶体
。
[0031]
在一些实施方案中,用于制备化合物
16
的方法包括化合物6与化合物8的糖基化以提供化合物
9。
[0032][0033]
在一些实施方案中,化合物6的糖基化在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是甲苯
。
在一些实施方案中,所述至少一种溶剂是二氯甲烷
。
在一些实施方案中,化合物6的糖基化在至少两种溶剂的存在下进行
。
在一些实施方案中,所
述至少两种溶剂是甲苯和二氯甲烷
。
在一些实施方案中,化合物6的糖基化包括使用至少一种酸
。
在一些实施方案中,所述至少一种酸是三氟甲磺酸
。
[0034]
在一些实施方案中,用于制备化合物8的方法包括化合物7的活化
。
[0035][0036]
在一些实施方案中,化合物7的活化包括使用至少一种亚磷酸酯
。
在一些实施方案中,所述至少一种亚磷酸酯选自氯亚磷酸酯
。
在一些实施方案中,所述至少一种亚磷酸酯是氯亚磷酸二乙酯
。
在一些实施方案中,化合物7的活化在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是甲苯
。
在一些实施方案中,化合物7的活化在至少一种有机碱的存在下进行
。
在一些实施方案中,所述至少一种有机碱是三乙胺
。
[0037]
在一些实施方案中,用于制备化合物
16
的方法包括化合物5的
tbdms-去保护以提供化合物
6。
[0038][0039]
在一些实施方案中,化合物5的
tbdms-去保护包括使用至少一种氟化物
。
在一些实施方案中,所述至少一种氟化物是
tbaf。
在一些实施方案中,化合物5的
tbdms-去保护在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是
thf。
在一些实施方案中,所述至少一种溶剂是
acn。
在一些实施方案中,化合物5的
tbdms-去保护在至少两种溶剂的存在下进行
。
在一些实施方案中,所述至少两种溶剂是
thf
和
acn。
[0040]
在一些实施方案中,化合物6是结晶的
。
在一些实施方案中,化合物6在至少一种溶剂的存在下结晶
。
在一些实施方案中,所述至少一种溶剂是二氯甲烷
。
在一些实施方案中,所述至少一种溶剂是甲醇
。
在一些实施方案中,所述至少一种溶剂是水
。
在一些实施方案中,化合物6在至少两种溶剂的存在下结晶
。
在一些实施方案中,所述至少两种溶剂是水和甲醇
。
[0041]
在一些实施方案中,用于制备化合物
16
的方法包括化合物3与化合物
4b
的岩藻糖基化以提供化合物
5。
[0042][0043]
在一些实施方案中,化合物3的岩藻糖基化包括使用
tbabr。
在一些实施方案中,化合物3的岩藻糖基化包括使用至少一种碱
。
在一些实施方案中,所述至少一种碱是
dipea。
在一些实施方案中,化合物3的岩藻糖基化在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是
methf。
在一些实施方案中,所述至少一种溶剂是二氯甲烷
。
在一些实施方案中,化合物3的岩藻糖基化在至少两种溶剂的存在下进行
。
在一些实施方案中,所述至少两种溶剂是
methf
和二氯甲烷
。
[0044]
在一些实施方案中,制备化合物
4b
的方法包括使化合物
4a
与
br2反应
。
在一些实施方案中,化合物
4a
与
br2的反应在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是环己烷
。
[0045]
在一些实施方案中,用于制备化合物
16
的方法包括化合物
2a
的环氧开环以提供化合物
3。
[0046][0047]
在一些实施方案中,化合物
2a
的环氧开环包括使用至少一种有机格氏试剂
。
在一些实施方案中,所述至少一种有机格氏试剂选自卤化乙基镁
。
在一些实施方案中,卤化乙基镁是溴化乙基镁
。
在一些实施方案中,卤化乙基镁是氯化乙基镁
。
在一些实施方案中,使用
0.5
当量或更多
(
相对于化合物
2a)
的氯化乙基镁,例如1当量或更多
、2
当量或更多
、3
当量或更多
、5
当量或更多
、7
当量或更多
、9
当量或更多
、11
当量或更多
、13
当量或更多以及
15
当量或更多,并且可以是
0.5
当量至
25
当量
、3
当量至
20
当量
、5
当量至
20
当量
、5
当量至
15
当量或
10
当量至
20
当量
。
[0048]
在一些实施方案中,化合物
2a
的环氧开环包括使用至少一种路易斯酸
。
在一些实施方案中,所述至少一种路易斯酸选自三卤化硼和三氟甲磺酸铝
。
在一些实施方案中,三卤化硼选自三氟化硼
、
三氯化硼和三溴化硼
。
在一些实施方案中,三卤化硼是三氟化硼
。
在一些实施方案中,三卤化硼是三氯化硼
。
在一些实施方案中,三卤化硼是三溴化硼
。
在一些实施方案中,三氟化硼是三氟化硼乙醚
。
在一些实施方案中,至少一种路易斯酸是三氟甲磺酸铝
。
[0049]
在一些实施方案中,使用
0.5
当量或更多
(
相对于化合物
2a)
的路易斯酸
(
例如,三氟化硼乙醚
)
,例如1当量或更多
、2
当量或更多
、3
当量或更多
、4
当量或更多
、5
当量或更多
、10
当量或更多,并且可以是
0.5
当量至
15
当量
、1
当量至
10
当量
、1
当量至8当量
、1
当量至6当量
、1
当量至4当量
、1
当量至3当量
、2
当量至8当量
、2
当量至6当量
、2
当量至4当量
、3
当量至
10
100℃
至
10℃、-100℃
至
0℃、-100℃
至-20℃、-100℃
至-40℃、-100℃
至-60℃、-20℃
至
30℃、-20℃
至
20℃、-20℃
至
10℃.-20℃
至
0℃、-10℃
至
25℃、-10℃
至
15℃、-10℃
至
5℃。
在一些实施方案中,化合物
2a
的环氧开环在约-78℃
下进行
。
[0056]
在一些实施方案中,化合物
2a
的环氧开环在化合物
2b
的存在下进行
。
在一些实施方案中,在环氧开环之前化合物
2a
与化合物
2b
的摩尔比是大于7比1,例如大于
7.5
比
1、
大于8比
1、
大于9比
1、
大于
10
比
1、
大于
11
比
1、
大于
15
比
1、
大于
25
比1或大于
50
比
1。
[0057]
在一些实施方案中,化合物
2a
的环氧开环包括在没有色谱的情况下使用通过化合物1的氧化制备的化合物
2a。
[0058][0059]
在一些实施方案中,用于制备化合物
16
的方法包括化合物1的环氧化以提供化合物
2a。
[0060][0061]
在一些实施方案中,化合物1的环氧化
(wo2013/096926)
包括使用过氧单硫酸钾
(
例如,
oxone)。
在一些实施方案中,使用
0.5
当量或更多
(
相对于化合物
1)
的过氧单硫酸钾,例如1当量或更多
、2
当量或更多
、3
当量或更多
、4
当量或更多
、5
当量或更多,并且可以是
0.5
当量至
10
当量
、1
当量至8当量
、1
当量至6当量
、1.5
当量至5当量或2当量至4当量
。
[0062]
在一些实施方案中,化合物1的环氧化包括使用至少一种碱
。
在一些实施方案中,所述至少一种碱选自金属碳酸盐
。
在一些实施方案中,金属碳酸盐是
nahco3。
在一些实施方案中,使用1当量或更多
(
相对于化合物
1)
的
nahco3,例如2当量或更多
、3
当量或更多
、4
当量或更多
、5
当量或更多
、8
当量或更多
、10
当量或更多,并且可以是1当量至
20
当量
、1
当量至
10
当量
、1
当量至7当量
、1
当量至5当量
、3
当量至
15
当量
、3
当量至9当量
、3
当量至6当量
、4
当量至
12
当量
、4
当量至8当量或4当量至6当量
。
[0063]
在一些实施方案中,化合物1的环氧化包括使用过氧单硫酸钾
(
例如,
oxone)
和使用至少一种碱
。
在一些实施方案中,化合物1的环氧化包括使用过氧单硫酸钾
(
例如,
oxone)
和
nahco3。
在一些实施方案中,使用约
2.5
当量
(
相对于化合物
1)
的过氧单硫酸钾
(
例如,
oxone)
和约
4.5
当量
(
相对于化合物
1)
的
nahco3。
[0064]
在一些实施方案中,化合物1的环氧化在至少一种溶剂的存在下进行
。
在一些实施方案中,所述至少一种溶剂是丙酮
。
在一些实施方案中,所述至少一种溶剂是水
。
在一些实施方案中,化合物1的环氧化在至少两种溶剂的存在下进行
。
在一些实施方案中,所述至少两种溶剂是丙酮和水
。
[0065]
在一些实施方案中,化合物1的环氧化在-10℃
至
50℃
的温度下进行,例如-10℃
至
40℃、-10℃
至
30℃、-10℃
至
20℃、-10℃
至
10℃、-5℃
至
45℃、-5℃
至
35℃、-5℃
至
25℃、-5℃
至
15℃、-5℃
至
10℃、
[0066]-5℃
至
5℃。
在一些实施方案中,化合物1的环氧化在约
0℃
下进行
。
[0067]
在一些实施方案中,化合物1的环氧化导致化合物
2a
和化合物
2b
的形成
。
在一些实施方案中,由环氧化形成的化合物
2a
与化合物
2b
的摩尔比是大于7比1,例如大于
7.5
比
1、
大于8比
1、
大于9比
1、
大于
10
比
1、
大于
11
比
1、
大于
15
比
1、
大于
25
比1或大于
50
至
1。
[0068]
在一些实施方案中,用于制备化合物
16
的方法包括以下步骤中的至少一个:
[0069]
(a)
化合物
15
的氢化;
[0070]
(b)
化合物
14
的
meo-三苯甲基裂解;
[0071]
(c)
化合物
13
的烯丙氧羰基裂解
/
酰化;
[0072]
(d)
化合物
11
的
o-烷基化;
[0073]
(e)
化合物
10
的甲氧基-三苯甲基化;
[0074]
(f)
化合物9的脱乙酰化;
[0075]
(g)
化合物6的糖基化;
[0076]
(h)
化合物5的
tbdms-去保护;以及
[0077](i)化合物3的岩藻糖基化;
[0078]
(j)
化合物
2a
的环氧开环;
[0079]
(k)
化合物1的环氧化
。
[0080]
在一些实施方案中,以上步骤d包括化合物
11
与化合物
12
的
o-烷基化以形成化合物
13。
在一些实施方案中,以上步骤g包括化合物6与化合物8的糖基化以形成化合物
9。
[0081]
在一些实施方案中,用于制备化合物
16
的方法包括选自以上步骤
(a)-(k)
中的至少两个步骤
。
在一些实施方案中,用于制备化合物
16
的方法包括选自以上步骤
(a)-(k)
中的至少三个步骤
。
在一些实施方案中,用于制备化合物
16
的方法包括选自以上步骤
(a)-(k)
中的至少四个步骤
。
在一些实施方案中,用于制备化合物
16
的方法包括选自以上步骤
(a)-(k)
中的至少五个步骤
。
在一些实施方案中,用于制备化合物
16
的方法包括选自以上步骤
(a)-(k)
中的至少六个步骤
。
在一些实施方案中,用于制备化合物
16
的方法包括选自以上步骤
(a)-(k)
中的至少七个步骤
。
在一些实施方案中,用于制备化合物
16
的方法包括选自以上步骤
(a)-(k)
中的至少八个步骤
。
在一些实施方案中,用于制备化合物
16
的方法包括选自以上步骤
(a)-(k)
中的至少九个步骤
。
在一些实施方案中,用于制备化合物
16
的方法包括选自以上步骤
(a)-(k)
中的至少十个步骤
。
在一些实施方案中,用于制备化合物
16
的方法包括以上步骤
(a)-(k)
中的每一个
。
[0082]
在一些实施方案中,用于制备化合物
16
的方法包括至少以上步骤
(j)。
在一些实施方案中,用于制备化合物
16
的方法包括至少以上步骤
(k)。
在一些实施方案中,用于制备化合物
16
的方法包括至少以上步骤
(j)
和
(k)。
[0083]
化合物
16
可以根据图
1a、
图
1b
和图
1c
中所示的一般反应方案制备
。
应理解,本领域普通技术人员能够通过类似方法或通过组合本领域普通技术人员已知的其它方法制备这些化合物
。
通常,起始组分可以从诸如
sigma aldrich、lancaster synthesis,inc.、maybridge、matrix scientific、tci
和
fluorochem usa
等来源获得和
/
或根据本领域普通
[0088][0089]
化合物
2a/2b:
在室温下将烯烃
1(
描述于
magnani
等人的
wo2013/096926
,
8.1g
,
0.03mol)
溶解在丙酮
(90ml)
中
。
添加固体
nahco3(12.0g
,
0.14mol)。
将混合物冷却至
0℃。
逐滴添加溶解在
150ml
水中的
oxone(24g
,
0.08mmol)(1ml/min)。
将反应混合物在
0℃
下剧烈搅拌直至
tlc
指示烯烃1消耗
。
将反应混合物转移到分液漏斗中并用
mtbe
萃取3次
。
将合并的有机相用水萃取2次
。
将有机相经
mgso4干燥,过滤并浓缩,得到环氧化物
2a/2b
的混合物
(8.0g
,
93
%产率
)。lcms
分析表明约
11
%的不希望的环氧化物
2b。lc-ms m/z
=
287.2(m+1)。
[0090]
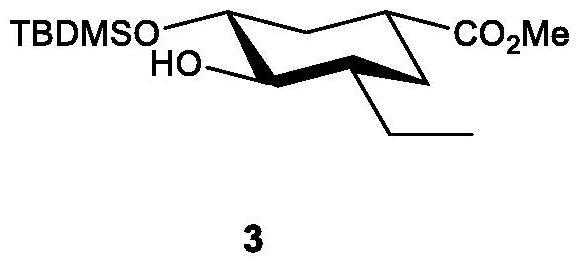
步骤2[0091][0092]
化合物
3:
向
cubr
.
dms(10.8g
,
0.052mol
,
5.0
当量
)
在冷却至-78℃
的无水
thf(240ml)
中的搅拌悬浮液中逐滴添加
(
历时
20
分钟的时间段
)etmgcl(acros organics 2.7m
在
thf
中,
58.2ml
,
0.157mol
,
15.0
当量
)。
将混合物在-78℃
下搅拌
90
分钟以形成铜酸盐
。
添加溶解在无水
thf(30ml)
中的环氧化物
2a(3.0g,0.01mmol,1.0
当量
)
,随后逐滴添加
bf
3.
et2o(6.46ml,0.052mol,5.0
当量
)
,同时将混合物保持在-78℃
下
。
将反应混合物在该温度下搅拌
30
分钟
。
在-78℃
下通过逐滴添加甲醇
(30ml)
和三乙胺
(12ml)
的混合物淬灭反应并且使其升温至室温
。
将反应混合物用饱和
nh4cl
水溶液
(200ml)
和
nh4oh(30ml)
稀释,剧烈搅拌
10
分钟
。
分离各层,将有机层用
mtbe(2
×
)
萃取,用盐水洗涤,干燥
(na2so4)
,通过硅藻土过滤且真空浓缩,获得所需产物
3(3.03g
,
92
%产率
)。
醇3不经进一步纯化即用于下一步
。lc-ms m/z
=
317.2(m+1)。
[0093]
化合物
3(
使用催化
cubr.dms)
:向
cubr
.
dms(576mg
,
2.8mmol
,
0.1
当量
)
在冷却至-78℃
的无水
thf(200ml)
中的搅拌悬浮液中逐滴添加
(
历时
20-30
分钟的时间段
)etmgcl(acros organics 2.7m
在
thf
中,
93ml
,
252mol
,
9.0
当量
)。
将混合物在-78℃
下搅拌
60
分钟以形成铜酸盐
。
添加溶解在无水
thf(60ml)
中的粗品环氧化物
2a/2b(8.0g,28mmol,1.0
当量
)
,随后在-78℃
下逐滴添加
bf
3.
et2o(10.4ml,84mmol,3.0
当量
)。
将反应混合物在该温度下搅拌
45
分钟
。
在-78℃
下通过逐滴添加甲醇
(80.0ml)
和三乙胺
(35ml)
的混合物淬灭反应,然后使其升温至室温
。
将反应混合物用饱和
nh4cl
水溶液
(300ml)
和
nh4oh(80ml)
稀释,剧烈搅拌
10
分钟
。
分离各层,将有机层用
mtbe(2
×
)
萃取,用盐水洗涤,干燥
(na2so4)
,通过硅藻土过滤且真空浓缩,获得粗品
3(7.9g
,
89
%产率
)。
[0094]
化合物
3(
使用环戊基甲基醚作为溶剂
)
:向
cubr
.
dms(216mg
,
1.05mmol
,
3.0
当量
)
在冷却至-78℃
的无水
cpme(
环戊基甲基醚,
5ml)
中的搅拌悬浮液中逐滴添加
(
历时5分钟的时间段
)etmgcl(2.7m
在
thf
中,
1.17ml
,
3.15mol
,
9.0
当量
)。
将混合物在-78℃
下搅拌
60
分钟
以制备铜酸盐
。
添加溶解在无水
cpme(1.0ml)
中的环氧化物
2a(100mg,0.35mmol,1.0
当量
)
,随后在-78℃
下逐滴添加
bf
3.
et2o(0.13ml,1.05mmol,3.0
当量
)。
将混合物在-78℃
下搅拌
30
分钟
。
在-78℃
下通过逐滴添加甲醇
(1.0ml)
和三乙胺
(0.4ml)
的混合物淬灭反应并且使其升温至室温
。
将反应混合物用饱和
nh4cl
水溶液
(7ml)
和
nh4oh(1ml)
稀释,剧烈搅拌
10
分钟
。
分离各层,将有机层用
mtbe(2
×
)
萃取,用盐水洗涤,干燥
(na2so4)
,通过硅藻土过滤且真空浓缩,获得化合物
3(106mg
,
96
%,纯度:
100
%
)。
[0095]
步骤3[0096][0097]
化合物
5:
将
5.7g
的化合物
4a(1.20
当量
)
溶解在无水环己烷
(50ml)
中并且浓缩
。
添加无水环己烷
(50ml)
并再次汽提,并将残余物真空干燥
30
分钟
。
历经
10
分钟向干燥的硫苷在无水
ch2cl2(13ml)
中的冷却
(0℃)
溶液中添加溴
(0.59ml
,
0.01mol
,
1.15
当量
)
在无水
ch2cl2(1.5ml)
中的溶液,并且将混合物在
0℃
下搅拌
60
分钟,然后历经5分钟添加环己烯
(2.9ml
,
0.03mol
,
3.0
当量
)。
将混合物在
0℃
下再搅拌
30
分钟以得到供体溶液
。
[0098]
将醇
3(3.03g,0.01mol,1.0
当量
)
和
tbabr(3.09g
,
0.01mol
,
1.0
当量
)
溶解在无水环己烷
(20ml)
中,然后浓缩
。
添加无水环己烷
(20ml)
并再次蒸馏出,将混合物真空干燥1小时
。
向新活化的分子筛
(
粉末状,
4a
,
9.0g)
中添加
3.0ml
无水
ch2cl2,随后添加醇3和
tbabr
的干燥混合物在无水
ch2cl2(9ml)
和
n,n-二异丙基乙胺
(5.0ml,0.03mol,3.0
当量
)
中的溶液
。
使悬浮液在室温下搅拌2小时,得到受体溶液
。
[0099]
在
0℃
下将受体溶液添加到供体溶液中,并使反应在室温下搅拌2天,然后将混合物通过硅藻土过滤以去除分子筛
。
将滤液依次用水
、15
%的柠檬酸水溶液
、10
%的
nahco3水溶液和最终再次用水洗涤,经
na2so4干燥并浓缩,得到呈黄色油状物的粗品5,其不经进一步纯化用于下一步
。
[0100]
步骤4[0101][0102]
化合物
6:
向粗品5中添加
tbaf(1.0m
在
thf
中,
30ml
,
0.03mol
,
3.0
当量
)
的溶液,并且将混合物在
55℃
下加热
18
小时,然后真空浓缩
。
将残余物溶解在
ch2cl2(50ml)
中,转移至分液漏斗,并用水
(50ml)
洗涤
。
分离各相,并且用
ch2cl2(2x 30ml)
萃取水相
。
将合并的有机萃取物经
na2so4干燥
、
过滤和浓缩
。
将残余物从甲醇和水中结晶,得到呈灰白色固体的产物
6。
由于重结晶不完全,因此将母液进行快速色谱法分离剩余的产物
6(
总共
4.4g,71
%产
[0118][0119]
化合物
11:
将化合物
10(25.00g)
溶解在
dcm(6
体积
)
中
。
在
tj
=
50℃/
真空下蒸馏掉溶剂
(4
体积
)。
添加
dcm(6
体积
)
并蒸馏掉相同体积的溶剂
。
添加
dcm(6
体积
)
并蒸馏掉相同体积的溶剂
。
将澄清的淡黄色浓缩物用
dcm(4
体积
)
稀释并在氮气下冷却至环境温度
。
添加
2,6-二甲基吡啶
(1.8
当量
)。
添加
4-meo-三苯甲基氯
(1.03
当量
)
且分三份,用
dcm(0.5
体积
)
漂洗至反应混合物中,并在环境温度下搅拌1小时
。
[0120]
装入水
(3
体积
)
,随后装入
me-thf(6
体积
)
,并蒸馏掉6体积的溶剂
。
添加
me-thf(6
体积
)
并蒸馏掉相同量的溶剂
。
添加
15
%
w/w
柠檬酸
(3
体积
)
,并剧烈搅拌混合物
。
分离各相,并用水
(3
体积
)、
盐水
(3
体积
)
和饱和
nahco3水溶液
(1
体积
)
的混合物洗涤有机相
。
分离各相,并测量水相的
ph
为
7。
将有机相用半浓缩
nacl
水溶液
(6
体积
)
洗涤,得到
140ml
的有机相
。
[0121]
通过在
tj
=
45℃/250mbar
下蒸馏去除约
50ml
的溶剂而将产物溶液浓缩至4体积
。
将浓缩物升温至
ti
=
40℃
,并在相同温度下历经
30
分钟添加正庚烷
(12
体积
)。
将所得悬浮液加热至
ti
=
60℃
以溶解来自烧瓶壁的硬皮
(crust)
并在该温度下保持
25
分钟
。
历经2小时将悬浮液冷却至
20℃
,并在该温度下搅拌过夜
。
将固体经
250ml
翻转玻璃质
p3(turn over fritt p3)
过滤
。
用母液和正庚烷
(2.3
体积
)
漂洗滤饼,在氮气流下在真空中干燥5小时,并进一步在旋转蒸发仪上在
tj
=
33℃
下干燥过夜
。30.03g n.
校正
/29.89g lod
校正
(y 93.8
%校正
)。
[0122]1h nmr(
氯仿-d)
δ
1h nmr(
氯仿-d)
位移
:7.09-7.47(m,28h),6.76-6.82(m,2h),5.83-5.99(m,1h),5.32(dd,j
=
17.2,1.5hz,1h),5.24(dd,j
=
10.3,1.4hz,1h),4.77-5.00(m,4h),4.44-4.75(m,7h),4.10-4.21(m,2h),3.98-4.09(m,2h),3.75-3.95(m,4h),3.61-3.70(m,6h),3.54-3.60(m,1h),3.37-3.50(m,2h),3.27-3.37(m,2h),2.15-2.37(m,2h),1.93-2.14(m,2h),1.36-1.56(m,2h),1.05-1.29(m,5h),0.73-0.86(m,3h)。ms:c
67h77
no
15
的计算值=
1136.33
,实测值
m/z
=
1158.5(m+na
+
)。
[0123]
步骤8[0124]
[0125]
化合物
13:
将化合物
11(20.45g,1wt.)、
二丁基氧化锡
(iv)(0.37wt./1.7
当量
)、
甲醇
(4
体积
)
和甲苯
(2
体积
)
在
tj
=
82℃
下加热回流,并在回流下搅拌2小时
。
经由在
tj
=
65℃/320mbar
下蒸馏去除溶剂
(3
体积
)。
添加甲苯
(3
体积
)
,并将溶液在
tj
=
82℃
下回流搅拌
75
分钟
。
通过在
tj
=
65℃/400-140mbar
下蒸馏去除溶剂
(4
体积
)。
添加甲苯
(3
体积
)
并经由在
tj
=
65℃/130mbar
下蒸馏去除溶剂
(3
体积
)。
添加甲苯
(3
体积
)
并经由在
tj
=
65℃/105mbar
下蒸馏去除溶剂
(3
体积
)。
[0126]
在
ti
=
20℃
下将乙腈
(5
体积
)
添加到浓缩物中
。
添加含化合物
12
的甲苯
(2.25
当量;
ca18-0119)、
氟化铯
(3.0
当量;
f17-04152)
和甲醇
(1.0
当量
)。
制备水
(0.5
当量
)
和乙腈
(0.5
当量
)
的混合物
。
将
1/4
的制备的
acn
溶液添加到反应混合物中,随后在
ti
=
20℃
下搅拌1小时
。
添加第二部分的
acn
溶液,并将混合物再搅拌一小时
。
将此再重复两次
。
在添加最后的
acn/
水部分之后,将反应混合物在
ti
=
20℃
下搅拌
180
分钟
。
[0127]
通过添加
7.4
% nahco3水溶液
(4
体积
)
淬灭混合物并在
ti
=
20℃
下搅拌
50
分钟
。
将双相混合物经硅藻土床
(2wt
;预先用
12
体积甲苯调节
)
过滤
。
用甲苯
(3
体积
)
漂洗滤饼
。
分离各相并用甲苯
(3
体积
)
萃取水层
。
将合并的有机层用半饱和
nahco3水溶液
(5
体积
)
洗涤
。
将有机层经
na2so4(2.0wt)
干燥,过滤
na2so4,并用甲苯
(2
体积
)
漂洗滤饼
。
将
4-甲基吗啉
(1.0
当量;
f17-03830)
添加到产物溶液中
。
将溶液在
4℃
下储存过夜
。
[0128]
步骤9[0129][0130]
化合物
14:
将包含化合物
13
的有机相在旋转蒸发仪上在
ta
=
55℃/200-90mbar
下浓缩至5体积
。
装入
4-甲基吗啉
(20
当量
)
和
dcm(8
体积
)。
在
ti
=
20℃
下添加乙酸酐
(8
当量
)
和乙酸
(2
当量;
f16-04758)。
将烧瓶抽空并用氮气吹扫三次
。
添加三苯基膦
(0.05
当量
)
和
pd[(c6h5)3p]4(0.05
当量
)
,然后进行另一次抽空
/
氮气吹扫循环
。
将反应混合物在
ti
=
20℃
下搅拌
18
小时
。
[0131]
通过在环境温度下历经
20
分钟添加水
(5
体积
)
来淬灭反应
。
分离各相,并用柠檬酸
15
%
w/w
水溶液
(5
体积
)
洗涤有机层
。
向有机相中添加饱和
nahco3(5
体积
)
和甲醇
(0.5
体积
)。
将混合物在环境温度下剧烈搅拌
45
分钟
。
分离各相,将有机相用水洗涤两次
(
每次5体积
)
,并在旋转蒸发仪上在
tj
=
50℃/600mbar
下浓缩至7体积
。
[0132]
步骤
10
[0133][0134]
化合物
15:
向包含化合物
14
的浓缩物
(140ml)
中添加甲醇
(0.2
体积
)
和水
(0.5
体积
)
,并冷却至
ti
=
0-5℃。
制备
tca(3.0
当量
)
和
dcm(1
体积
)
的混合物,并在
ti
=
1-2℃
下历经
20
分钟将其加料到浓缩物中
。
将反应混合物在该温度下搅拌
3.5
小时
。
[0135]
在
ti
=
1-3℃
下在
25
分钟内将饱和
nahco3水溶液
(5
体积
)
加料到反应混合物中,并使混合物升温直至室温
。
分离各相并用
dcm(2
体积
)
萃取水相
。
将合并的有机层用水
(5
体积
)
洗涤并经
na2so4(1.5wt)
干燥
。
过滤
na2so2并用
dcm(2
体积
)
漂洗
。
[0136]
纯化:向色谱柱中装入
1548g(10wts)
硅胶
(
直径
15cm
,床高
22cm)
并用
1:1
的乙酸乙酯
/
庚烷调节
。
将来自步骤
6/7/8
镜管
(telescope)
的
582g
产物溶液
(
原材料:
157.63g)
装入柱的顶部并用
15ml
的
dcm
预洗脱
。
首先应用
60
体积
(9.5l)
的洗脱液
1(1:1
的乙酸乙酯
/
庚烷
)
洗脱柱:在收集
1l
的洗涤级分之后,收集
19
个级分
1#1
至
1#19(
每个
0.5l
体积
)。
之后,将洗脱液更换为洗脱液
2(3:1
的乙酸乙酯
/
庚烷
)
,收集另外的级分
1#20
至
1#33(
每个
1.0l
体积
)。
通过
tlc
分析级分:汇集物1:汇集级分
1#18
至
1#29
并将其浓缩,提供了
80.88g
固体残余物的化合物
15(98.15
%
a/a)。
收集级分
1#15
至
1#17
作为第二汇集物
ii
,提供了
9.98g
固体残余物的第二批化合物
15(67.1
%
a/a)。
[0137]1h nmr(
氯仿-d)
δ
7.20-7.45(m,24h),5.66(d,j
=
6.8hz,1h),5.14-5.25(m,2h),5.05(d,j
=
8.4hz,1h),4.69-5.01(m,7h),4.61(d,j
=
11.4hz,1h),4.35(dd,j
=
10.6,3.0hz,1h),3.95-4.12(m,3h),3.76-3.87(m,2h),3.59-3.74(m,7h),3.41(t,j
=
4.7hz,1h),3.29(t,j
=
9.6hz,1h),3.08-3.21(m,1h),2.66(dd,j
=
9.5,2.2hz,1h),2.29(tt,j
=
12.6,3.1hz,1h),2.13(d,j
=
12.7hz,1h),1.91-2.08(m,5h),1.36-1.81(m,13h),0.99-1.31(m,9h),0.72-0.98(m,5h)。ms:c
61h79
no
15
的计算值=
1066.28
,实测值
m/z
=
1088.5(m+na)。
[0138]
步骤
11
[0139][0140]
化合物
16:
向化合物
15(5.03g
;
1wt
;
ca18-0480)
中添加
2-丙醇
(15
体积
)、
水
(0.5
体积
)
和
thf(2.5
体积
)。
将悬浮液升温至
ti
=
30℃
以获得溶液
。
添加
pd/c 10
%
0.2wt
;
f15-01378)
和
2-丙醇
(3
体积
)
,并将混合物在氢气气氛下在大气压下和
tj
=
37℃
下搅拌7小时
。
将脱气的水
(1.5
体积
)
添加到反应混合物中,并在
tj
=
37℃/1
巴下继续氢化
17
小时
。
添加脱气的水
(2
体积
)
,并在以上给定的条件下再继续氢化7小时
。
将反应混合物在氢气气氛下在
tj
=
37℃/1
巴下搅拌过夜
。
[0141]
将氢气气氛更换为氮气并添加固体
nahco3(0.05
当量
)
和水
(2
体积
)。
将反应混合物在
30℃
下经
0.45
μm尼龙膜上过滤,并将滤饼用
2-丙醇
(3
体积
)
和水
(1
体积
)
的混合物漂洗
。
将合并的滤液在
tj
=
35℃/
真空下浓缩至干,得到
4.80g
的固体材料
。
将固体溶解在水
(0.2
体积
)
和
thf(3
体积
)
的混合物中,得到澄清溶液
。
[0142]
将乙酸异丙酯
(25.5
体积
)
冷却至
ti
=
0℃
,并在
ti
=
0℃
下历经
55
分钟经由滴液漏斗添加产物溶液
。
用水
(0.1
体积
)
和
thf(0.3
体积
)
的混合物漂洗滴液漏斗
。
将悬浮液在
ti
=
0℃
下搅拌
80
分钟后过滤
。
将滤饼用
mtbe(3
体积
)
漂洗,并将产物在真空和氮气流下干燥过夜
。3.10g n.
校正
/3.08g lod
校正
(y lod
校正
92.66
%
)。
[0143]1h nmr(400mhz,dmso-d6)
δ
4.61-4.83(m,2h),4.08-4.26(m,3h),3.98(d,j
=
8.6hz,1h),3.80(s,1h),3.29-3.57(m,10h),3.19-3.28(m,1h),3.06(t,j
=
9.5hz,1h),2.34-2.47(m,1h),2.22(d,j
=
12.7hz,1h),1.91-2.04(m,1h),1.71-1.89(m,5h),1.34-1.69(m,8h),0.68-1.31(m,13h)。ms:c
33h55
no
15
的计算值=
705.79
,实测值
m/z
=
728.4(m+na)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1