治疗用重组II型胶原的制作方法
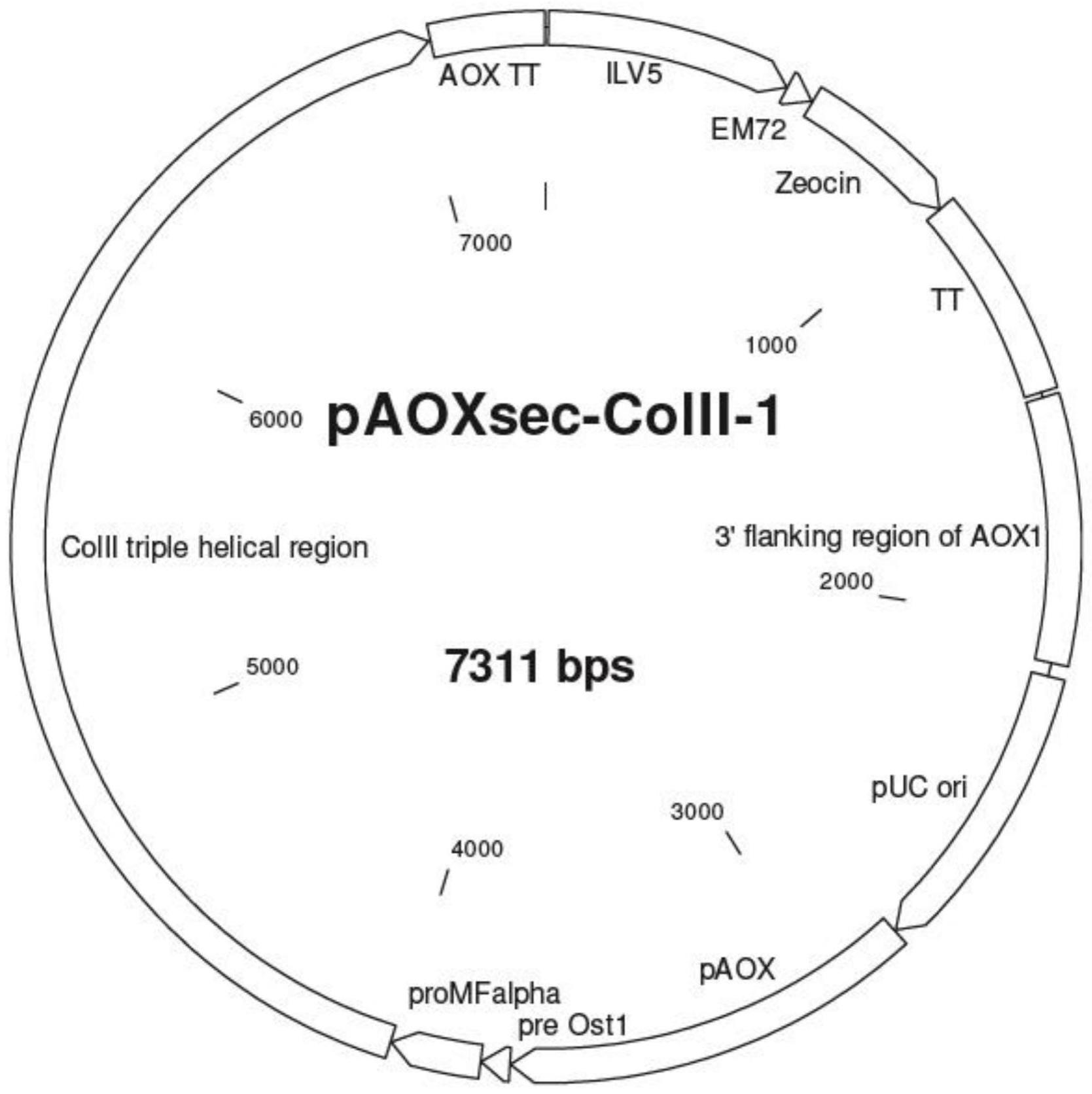
本发明涉及用于人体或动物体软骨疾病口服疗法的重组ii型胶原。
背景技术:
1、胶原是一种哺乳动物、鸟类和鱼类等动物体内的细胞外结构蛋白,一般存在于结缔组织中,特别是作为细胞外基质的组成部分。肌腱、韧带、软骨和骨骼富含胶原。植物和单细胞生物中却非天然存在胶原。
2、胶原呈现各种结构和功能不同的类型,在结构、功能和来源等方面存在差异。构成胶原的多肽链在细胞中呈较大前体分子的形式在内质网的核糖体上单独合成,并具有大范围的重复(gly-x-y)n序列,其中x和y可以是任何氨基酸,但一般是脯氨酸和4-羟脯氨酸。
3、这些前体多肽链在内质网中翻译后羟基化为多肽链的脯氨酸残基和赖氨酸残基,形成羟脯氨酸残基和羟赖氨酸残基。羟基化用于稳定细胞中各由三条前体多肽链(前胶原)形成的右旋三螺旋的相邻胶原多肽链。
4、这样形成的前胶原在细胞内糖基化,由细胞以糖基化三螺旋形式(前胶原)分泌,然后通过肽酶介导的末端残基裂解形成成熟胶原。这种胶原在原纤维形成过程中装配成胶原原纤维,然后共价交联形成胶原纤维。
5、胶原常以变性形式使用(有时称为明胶)或以其水解物的形式使用。
6、如果对明胶或胶原进行水解过程(特别是酶解)来获得胶原肽,则可根据所用胶原的类型及其来源以及酶促条件来生产具有多种组成和应用概况的胶原水解物。然而,此类胶原水解物是肽混合物,其分子量分布在一定的大小范围内。这种胶原水解物的用途早已为人所知,例如用作营养补充剂或作为美容辅助剂,包括用于预防和/或治疗骨骼、关节或结缔组织相关病症。
7、专利文献wo 2012/065782描述了获自猪皮明胶的胶原水解物,用于刺激皮肤细胞的细胞外基质蛋白的生物合成,特别适合美容目的。专利文献wo 2012/117012公开了来自牛裂解物的平均分子量为1500-8000da的酶解胶原,可以与益生元合用来预防和/或治疗骨质疏松症。
8、尽管采用获自动物材料的胶原或胶原水解物有益于许多应用和消费者群体,但对于某些消费者群体和应用概况而言,采用这种方式获得的胶原水解物也可能不太理想。某些消费者群体根本对获自动物材料的原材料持批评或消极态度,原因是担心沾染危害健康的微生物或制剂(例如加工添加剂)或不良的免疫反应,或者出于宗教或道德因素。此外,用于获得来自动物材料的胶原水解物的制造过程通常涉及复杂又昂贵的消化、纯化和再加工步骤。
9、在此背景下,开发出利用重组基因技术通过生物技术手段生产明胶、胶原、胶原水解物和单独胶原肽的工艺也不足为奇。
10、专利文献wo 2006/052451a2公开了在同样表达人源脯氨酰羟化酶的pichiapastoris(毕赤酵母)菌株中生产重组iii型胶原。专利文献wo 2005/012356a2公开了从人源i型胶原以及单独的50kda、65kda和100kda胶原肽种生产明胶(各呈完全羟基化、部分羟基化和非羟基化形式)。olsen等人(protein expression and purification,2005年第40期第346-357页)公开了在pichiapastoris中从人源胶原的α1链重组产生8.5kda胶原肽种。专利文献wo 01/34646a2还公开了生产由重组生产途径产生、具有高达350kda的限定分子量的重组明胶个体种,可以呈非羟基化、部分羟基化或完全羟基化的形式。
11、ii型胶原是一种专门存在于软骨组织中的胶原,一般呈α1链同源三聚体的形式。例如,专利文献us 5,593,859描述了重组ii型胶原肽的生产、借助脯氨酰-4-羟化酶将其羟基化并将其氢化形成前胶原以及相关的三螺旋形成。
12、专利文献us5,399,347描述了口服天然来源的高度纯化水溶性ii型胶原来治疗关节炎。然而,这种胶原的生产极其困难又耗时,而且容易受到污染,尤其是微生物污染。
13、专利文献us5,750,144、us5,645,851、us5,529,786和us5,637,321揭示了提供含有ii型胶原的含动物组织的组合物,口服施用来治疗类风湿性关节炎。这些文献尤其公开了采用含有获自天然动物来源的软骨组织材料,以便借助各种化学/物理工艺步骤获得含ii型胶原的组合物。这样获得的含ii型胶原的组合物的特征在于,既存在非变性的ii型胶原,又存在若干源自原料和分离工艺的次要组分,特别是蛋白质、抗原和盐。尽管提供此类组合物所需的工艺步骤要比从天然来源生产高度纯化ii型胶原所需的工艺步骤更为简单,但由于其来自天然来源,所生产的制剂因原料而异。此外,在整个生产加工过程中必须确保组合物中所含的ii型胶原不变性并避免病原体污染。
14、专利文献us7,083,820和ep1435906公开了采用获得含动物组织的组合物的方法,所述组合物含有非变性的ii型胶原,其中通过特殊的工艺步骤消除了微生物污染物,但要同时保留ii型胶原的原始非变性形式。
15、即使考虑到大部分人口(尤其是老年人)对健康、活动和健身的需求日益增长,仍然亟需食品、营养补充剂和药品组合物来改善和/或维持软骨健康和治疗软骨疾病。
技术实现思路
1、有鉴于此,本发明面临提供ii型胶原的技术问题,克服了前述缺点,特别是能够采取标准、可靠、明确的形式生产,甚至能以更大的高效益工业规模生产,又因其生物有效性而适用于口服治疗人体或动物体软骨疾病和/或维持软骨健康的方法。
2、为了解决根本技术问题,本发明提出了独立权利要求的教导,特别是说明书和从属权利要求中优选实施方案的教导。
3、本发明涉及一种用于人类或动物患者软骨疾病口服疗法的重组ii型胶原,特别是非变性重组ii型胶原。
4、本发明是基于如下出乎预料的教导:重组生成、尤其是分离形式的ii型胶原在口服施用后能够治疗软骨疾病。尽管并未采用或执行现有技术中生产治疗效用的ii型胶原组合物所必需的材料和工艺步骤,特别是利用天然动物软骨组织和采用某些工艺步骤来维持该起始组织中所含胶原的天然性,此外,原料中所含的次要组分不会存在于本发明提供的重组生成的ii型胶原中,可以证实根据本发明方法重组产生的ii型胶原的生物有效性,特别是出乎预料的高生物有效性。出乎预料地,本发明提出的重组ii型胶原、特别是重组ii型胶原肽能够表现出生物有效性,特别是与获自天然来源的ii型胶原至少相同的生物有效性,尤其是提高了生物有效性。优选实施方案中,由于重组ii型胶原、特别是ii型胶原肽在极低剂量下(即低浓度ii型胶原、特别是ii型胶原肽)表现出高生物有效性,本发明能够治疗人类或动物患者的软骨疾病。
5、特优选实施方案中,本发明提出的重组ii型胶原、特别是ii型胶原肽能够治疗免疫调节类软骨疾病,特别是自身免疫性疾病,尤其是多发性软骨炎或类风湿性关节炎。
6、特优选实施方案中,免疫调节类软骨疾病是免疫不耐受特点的疾病。
7、本发明还涉及用于治疗软骨疾病的重组ii型胶原,特别是重组ii型胶原肽,上述软骨疾病可能是软骨炎症和/或软骨退变,特别是类风湿性关节炎或关节病。
8、本发明又涉及用于诱导口服耐受性、特别是诱导内源性胶原(特别是内源性ii型胶原,尤其是存在于软骨组织内的内源性ii型胶原)口服耐受性的重组ii型胶原,特别是重组ii型胶原肽。
9、本发明具体涉及重组ii型胶原(特别是重组ii型胶原肽)以及包含重组ii型胶原(特别是重组ii型胶原肽)的组合物,用于治疗性处置或治疗性预防ii型胶原免疫不耐受、特别是通过诱导ii型胶原免疫耐受性的方法。
10、本发明还涉及用于ii型胶原免疫耐受性诱导方法的重组ii型胶原,特别是重组ii型胶原肽,尤其是涉及施用导致诱导ii型胶原口服耐受性的组合物。
11、本发明教导有利地提供了一种用于口服治疗软骨疾病的可用生物技术生产的可复制重组ii型胶原,这种重组ii型胶原能够采取标准化方式生产,能够以工业规模进行生产,不受天然原料的限制,可生产出无污染的高纯度高产量产品,尤其因其高生物有效性而呈现可低剂量使用的特点。
12、本发明采用的重组ii型胶原、特别是重组ii型胶原肽的特征在于,在人体或动物体内口服施用后发挥的生物有效性,特别是调节免疫和/或调节炎症的生物有效性。特优选实施方案中,这种生物有效性尤其发生在呈非变性形式(即天然形式)的全长重组ii型胶原上,但优选实施方案中,也发生在呈重组ii型胶原肽形式的缩短胶原肽上。
13、优选地,本发明提出的ii型胶原、特别是ii型胶原肽能够实现免疫调节和/或诱导口服耐受,特别是在所治疗的人体或动物体中引起免疫应答和/或诱导口服耐受。
14、本发明提出的重组ii型胶原优选地表现出抑制免疫球蛋白合成的生物有效性和/或抗炎生物有效性。因此,根据本发明可以减少促炎细胞因子,刺激抗炎细胞因子。不受理论束缚,本发明提出的重组ii型胶原、特别是重组ii型胶原肽口服施用后可在胃肠道中完全或基本无损地存活,在免疫调节细胞、特别是免疫抑制细胞、尤其是派尔斑细胞中触发免疫调节反应和/或细胞因子调节反应和/或信号级联,从而减少或完全防止软骨区域(特别是关节软骨)的不良免疫反应和炎症过程。
15、众所周知,存在于受损或退变软骨组织之中或之上的内源性ii型胶原或其片段可以诱导自身免疫反应,导致软骨中出现炎症、形成免疫球蛋白以及退变和破坏过程,从而造成进一步软骨破坏和退变,最终出现骨关节炎、类风湿性关节炎和类似疾病。本发明提出的口服施用重组ii型胶原、特别是ii型胶原肽貌似带来了针对引发此类不良反应的内源性ii型胶原的口服耐受性,从而能够治疗软骨疾病。
16、本发明提出的重组ii型胶原、特别是重组ii型胶原肽优选地具备与所治疗人或动物患者的细胞、特别是与派尔斑细胞相互作用的能力,尤其是刺激抗炎并抑制促炎细胞因子和抑制免疫球蛋白。
17、本发明提出的重组ii型胶原、特别是重组ii型胶原肽优选地对外周血单核细胞分化成免疫抑制性m2巨噬细胞表现出诱导作用。
18、更优选实施方案中,本发明提出的重组ii型胶原、特别是重组ii型胶原肽会减少炎症细胞因子(特别是tnfα和ifnτ)的合成并且/或者诱导抗炎细胞因子(特别是il-10)的合成。
19、根据本发明优选实施方案,本发明提出的重组ii型胶原、特别是重组ii型胶原肽会刺激/诱导原初cd4+t前体细胞分化成t抑制细胞。特别优选地,刺激/诱导原初cd4+t前体细胞分化成t抑制细胞会增强抗炎细胞因子(优选il-10、il-4和/或tgf-β)的释放。
20、本发明优选实施方案中,本发明提出的重组ii型胶原、特别是重组ii型胶原肽会减少软骨细胞、特别是关节软骨细胞表达促炎细胞因子(优选il-1β、tnfα和/或il-6)。
21、本发明特优选实施方案中,所述重组ii型胶原呈非变性形式,即天然形式。
22、本发明特优选实施方案中,所述重组ii型胶原呈三螺旋形式。
23、优选实施方案中,本发明提出了一种重组ii型胶原,可呈ii型胶原肽形式(即单链形式)或例如二链形式或三链形式(又称螺旋形式)等多链形式,特别是ii型前胶原或ii型成熟胶原形式,尤其是ii型α1链同源三聚体形式。
24、如果根据本发明的重组ii型胶原不呈单链ii型胶原肽,而是例如呈三螺旋形式,则根据本发明可以体现出构成重组ii型胶原三螺旋形式的某个或所有个体胶原肽。具体而言,本发明教导中公开的关于重组ii型胶原肽的陈述也适用于具有一条、两条或三条这种单链ii型胶原肽的ii型胶原,特别是完全由这些单链胶原肽构建的ii型胶原,尤其是由根据本发明的重组型ii胶原肽组成。
25、特优选实施方案中,所述重组ii型胶原可以是ii型牛胶原(iib型胶原)。
26、另一特优选实施方案中,所述重组ii型胶原可以呈ii型前胶原或ii型成熟胶原形式。
27、又一特优选实施方案中,所述重组ii型胶原可以呈三螺旋形式,特别是三条ii型α1链的同源三聚体形式。
28、特优选实施方案中,所述重组ii型胶原呈非变性形式,又称天然形式,即具有天然存在的蛋白质三级结构和蛋白质四级结构。
29、特优选实施方案中,所述重组ii型胶原可以呈交联或非交联原纤维形式。
30、特优选实施方案中,所述重组ii型胶原、特别是ii型胶原肽可以是全长胶原肽,即具有天然存在ii型胶原肽的完整氨基酸序列。
31、另一特优选实施方案中,所述重组ii型胶原呈ii型胶原肽形式。
32、特优选实施方案中,所述重组ii型胶原、特别是ii型胶原肽可以是分子量范围为5-400kda、特别是10-390kda、特别是10-350kda、特别是10-300kda、特别是10-110kda、特别是40-110kda、特别是40-100kda、特别是11-105kda、特别是15-100kda、特别是20-99kda、特别是25-95kda、特别是30-95kda、特别是35-95kda的ii型胶原肽。优选地,所述重组ii型胶原、特别是ii型胶原肽的分子量范围为40-50kda,特别是45kda。
33、特优选实施方案中,所述重组ii型胶原肽可以呈三螺旋形式。
34、特优选实施方案中,本发明的重组ii型胶原、特别是重组ii型胶原肽呈完全或部分羟基化、完全或部分糖基化或者完全或部分羟基化且糖基化。
35、特优选实施方案中,根据本发明的重组ii型胶原、特别是重组ii型胶原肽是非羟基化的ii型胶原、特别是ii型胶原肽。
36、更优选实施方案中,根据本发明的重组ii型胶原、特别是重组ii型胶原肽是羟基化的ii型胶原、特别是ii型胶原肽。
37、优选地,所述重组ii型胶原、特别是重组产生的ii型胶原肽具有羟基化脯氨酸和/或羟基化赖氨酸。
38、优选地,所述重组ii型胶原、特别是重组ii型胶原肽是非羟基化、部分羟基化或完全羟基化的ii型胶原、特别是ii型胶原肽。
39、根据本发明优选实施方案,所述重组ii型胶原、特别是重组ii型胶原肽呈糖基化。优选地,所述重组ii型胶原、特别是重组ii型胶原肽在至少一个羟基化赖氨酸上糖基化。优选地,所述重组ii型胶原、特别是重组ii型胶原肽的每个羟基化赖氨酸呈糖基化。
40、本发明优选实施方案中,所述重组ii型胶原、特别是重组ii型胶原肽无氨基酸修饰,特别是无羟基化。特别优选地,所述重组ii型胶原、特别是ii型胶原肽不具有任何羟基化和/或糖基化的氨基酸。
41、优选地,根据本发明的ii型胶原、特别是ii型胶原肽具有来自脊椎动物(特别是鱼类、两栖动物、爬行动物、鸟类和哺乳动物,特别是猪、羊、牛、啮齿动物、袋鼠、马)或来自无脊椎动物(特别是水母)的ii型胶原中出现的氨基酸序列,特别是来自牛的ii型胶原中出现的氨基酸序列。
42、特别优选地,所述ii型胶原、特别是ii型胶原肽包含seq id no.2所示的氨基酸序列。优选地,所述ii型胶原、特别是ii型胶原肽由seq id no.2所示的氨基酸序列组成。
43、本发明更优选实施方案中,所述ii型胶原、特别是ii型胶原与seq id no.2所示的氨基酸序列具有至少80%、优选至少85%、优选至少90%、优选至少95%、优选至少96有%、优选至少97%、优选至少98%、优选至少99%的序列一致性。
44、根据本发明更优选实施方案,所述ii型胶原、特别是ii型胶原肽包含seq id no.4所示的氨基酸序列。优选地,所述ii型胶原、特别是ii型胶原肽由seq id no.4所示的氨基酸序列组成。
45、本发明更优选实施方案中,所述ii型胶原、特别是ii型胶原肽与seq id no.4所示的氨基酸序列具有至少80%、优选至少85%、优选至少90%、优选至少95%、优选至少96%、优选至少97%、优选至少98%、优选至少99%的序列一致性。
46、优选地,所述重组ii型胶原、特别是ii型胶原肽的氨基酸序列是天然存在的ii型胶原、特别是ii型胶原肽的氨基酸序列。优选地,所述重组ii型胶原、特别是ii型胶原肽的氨基酸序列是非天然存在的ii型胶原、特别是ii型胶原肽的氨基酸序列。优选地,所述重组ii型胶原、特别是ii型胶原肽的氨基酸序列是基因修饰的ii型胶原、特别是ii型胶原肽的氨基酸序列。
47、特别优选地,根据本发明的ii型胶原、特别是ii型胶原肽具有非人胶原,特别是非人ii型胶原肽,优选地存在于非人ii型胶原的α1链中的氨基酸序列,特别是存在于牛、猪、马、羊、鱼类或禽类胶原中的氨基酸序列,特别是存在于牛胶原中的氨基酸序列。
48、本发明优选实施方案中,所述重组ii型胶原、特别是重组ii型胶原肽抗胶原酶,特别是抗人胶原酶消化。
49、根据本发明更优选实施方案,所述重组ii型胶原、特别是ii型胶原肽能够诱导口服耐受性,特别是针对内源性胶原,特别是内源性ii型胶原,特别是软骨组织中内源性ii型胶原。
50、根据本发明更优选实施方案,所述重组ii型胶原、特别是ii型胶原肽能够抑制免疫球蛋白的合成。
51、根据本发明更优选实施方案,所述重组ii型胶原、特别是ii型胶原肽能够抑制促炎细胞因子的合成。
52、根据本发明更优选实施方案,所述重组ii型胶原、特别是ii型胶原肽能够刺激抗炎细胞因子的合成。
53、根据本发明更优选实施方案,所述重组ii型胶原、特别是ii型胶原肽能够抑制免疫球蛋白的合成、抑制促炎细胞因子的合成并抑制抗炎细胞因子的合成。根据本发明优选实施方案,所述用于人类或动物患者软骨疾病口服疗法的重组ii型胶原、特别是ii型胶原肽的分子量范围为5-400kda,特别是10-390kda,特别是10-350kda,特别是10-300kda,特别是10-110kda,特别是40-110kda,特别是40-100kda,特别是11-105kda,特别是15-100kda,特别是20-99kda,特别是25-95kda,特别是30-95kda,特别是35-95kda。重组ii型胶原的分子量优选为40-50kda范围内,特别是45kda。
54、本发明优选实施方案中,根据本发明的重组ii型胶原、特别是ii型胶原肽在本发明用途中单独使用,即采取分离形式,即不含其他物质。
55、本发明优选实施方案中,根据本发明的重组ii型胶原、特别是ii型胶原肽作为分子量均匀的均质制剂,特别是作为单一重组ii型胶原、特别是ii型胶原肽的均质制剂。
56、本发明另一实施方案中,根据本发明的重组ii型胶原、特别是ii型胶原肽在本发明用途中用作唯一具有生物有效性的物质。
57、特优选实施方案中,本发明涉及包含至少一种重组ii型胶原、特别是至少一种重组ii型胶原肽的组合物,该组合物除了至少一种重组ii型胶原、特别是至少一种重组ii型胶原肽以及任选地可药用和/或可食用的载体之外,不含任何其他物质。
58、特优选实施方案中,所述包含至少一种重组ii型胶原、特别是至少一种重组ii型胶原肽的组合物是一种适合人体或动物体内口服施用的剂型。
59、本发明还涉及一种组合物,包含根据本发明的至少一种重组ii型胶原、特别是至少一种重组ii型胶原肽和至少一种可药用和/或可食用载体以及任选地至少一种用于软骨疾病口服疗法的添加剂或赋形剂。
60、有鉴于此,本发明还涉及一种组合物,用于通过诱导ii型胶原、特别是内源型ii型胶原的口服耐受性来治疗性预防或治疗性处置ii型胶原、特别是内源性ii型胶原的免疫不耐受反应的方法。
61、本发明还涉及一种组合物,用于诱导ii型胶原、特别是内源性ii型胶原的口服耐受性的方法,该组合物促使在人体或动物体内诱导口服耐受性。
62、本发明还涉及一种包含重组ii型胶原、特别是重组ii型胶原肽、特别是药物组合物或营养补充剂或者食品或嗜好品的组合物,用于诱导ii型胶原、特别是内源性ii型胶原的口服耐受性。
63、根据本发明用于口服施用的组合物尤其可以是药物组合物、营养补充剂或食品和嗜好品。特别地,根据本发明的组合物是药物组合物。特别地,根据本发明的组合物是营养补充剂。
64、本发明特别是涉及一种包含根据本发明的ii型胶原、特别是ii型胶原肽和至少一种可药用载体的药物组合物以及用于治疗性处置人体或动物体软骨疾病的方法的药物组合物。这便提出,根据本发明采取药物组合物形式施用的ii型胶原,特别是ii型胶原肽。特别有利地,本发明的药物组合物例如采取片剂、含片、咀嚼片、粉末、颗粒、硬胶囊、软胶囊、胶囊、咬胶囊、糖衣丸、锭剂、挤出物、液剂、混悬剂、凝胶或软膏的形式施用。
65、本发明特优选实施方案中,根据本发明使用的ii型胶原、特别是ii型胶原肽是能够延缓肠道释放的剂型,特别是缓释胶囊。
66、特优选实施方案中,根据本发明的组合物呈适合口服施用的形式,特别是按1-60mg/天、特别是5-50mg/天剂量的重组ii型胶原。
67、本发明还涉及一种包含根据本发明的ii型胶原、特别是ii型胶原肽和至少一种可食用载体的营养补充剂以及用于治疗性处置人体或动物体软骨疾病的方法的营养补充剂。这便提出,根据本发明的ii型胶原、特别是ii型胶原肽采取营养补充剂的形式施用。特别有利地,根据本发明的营养补充剂作为硬胶囊、软胶囊、胶囊、咬胶囊、片剂、糖衣丸、锭剂、药包、挤出物、溶液、混悬剂或凝胶,例如在安瓿中,作为颗粒或粉末。
68、本发明还涉及一种包含根据本发明的ii型胶原、特别是ii型胶原肽的食品或嗜好品以及用于治疗人体或动物体软骨疾病的方法的食品或嗜好品。根据优选实施方案,所述食品或嗜好品是巧克力棒、蛋白棒、谷物棒、用于制备饮品的速溶粉、牛奶、乳制品(例如酸奶、乳清或凝乳)以及代乳品(例如豆奶、米浆、杏仁奶和椰奶)、功能性食品或饮品(例如清凉饮料或健身饮料)。
69、如果根据本发明优选实施方案的重组ii型胶原、特别是ii型胶原肽不用作组合物、特别是药物组合物、营养补充剂或者食品或嗜好品的唯一生物有效性成分,它可以与一种或多种其他添加剂或赋形剂组合,特别是那些对一般健康、特别是软骨健康和/或耐力表现具有积极影响的添加剂或赋形剂。根据本发明优选的赋形剂选自下组:维生素c、b、d、e和k系维生素、omega-3脂肪酸、omega-6脂肪酸、共轭亚麻酸、咖啡因及其衍生物、瓜拉那提取物、玫瑰果提取物、绿茶提取物、表没食子儿茶素没食子酸酯(epigallocatechingallate)、肌酸、l-肉碱、α-硫辛酸、n-乙酰半胱氨酸、nadh、d-核糖、天冬氨酸镁、抗氧化剂(如花青素、类胡萝卜素、类黄酮、白藜芦醇、谷胱甘肽和超氧化物歧化酶)、矿物质(如铁、镁、钙、锌、硒和磷)以及其他蛋白质、水解物和肽(如大豆蛋白、小麦蛋白和乳清蛋白)。
70、特优选实施方案可以提出,根据本发明的组合物、特别是药物组合物、营养补充剂或者食品或嗜好品具有赋形剂,例如软骨素、硫酸软骨素、透明质酸、aflapin、univestin、5-glocsin、葡萄糖胺、硫酸葡萄糖胺和/或甲磺酰甲烷(msm)。
71、更优选实施方案可以提出,根据本发明的组合物、特别是药物组合物、营养补充剂或者食品或嗜好品具有添加剂,该添加剂是重组生成的胶原水解物、源自天然来源的胶原水解物、重组生成的i型胶原、天然来源的i型胶原或其组合。
72、本发明更优选实施方案中,本发明的产品、特别是药物组合物、营养补充剂或者食品或嗜好品除了本发明的ii型胶原之外还特别是包含ii型胶原肽,不含其他蛋白质或肽,特别是不含其他胶原肽。
73、本发明还涉及一种治疗、特别是预防和/或处置软骨疾病的方法,根据该方法,向人体或动物体施予足以达到治疗目的用量的至少一种根据本发明的重组ii型胶原、特别是ii型胶原肽来,必要时与载体和任选的赋形剂或添加剂一起口服施用。
74、本发明还涉及一种在人体或动物体内诱导ii型胶原、特别是内源性ii型胶原的口服耐受性的方法,包括施用足以达到治疗目的用量的至少一种根据本发明的重组ii型胶原、特别是重组ii型胶原肽,必要时借助载体和任选地赋形剂或添加剂,其中进行口服施用。
75、本发明还涉及一种用于治疗性处置或治疗性预防ii型胶原、特别是ii型胶原肽的免疫不耐受的方法,包括口服施用足以达到治疗目的用量的至少一种根据本发明的重组ii型胶原、特别是重组ii型胶原肽,必要时借助载体和任选地赋形剂或添加剂。
76、本发明还涉及重组ii型胶原、特别是重组ii型胶原肽在维持人类或动物软骨健康的非治疗性方法中的用途,根据该方法,向人体或动物体口服施用足以维持软骨健康用量的至少一种根据本发明的重组ii型胶原、特别是ii型胶原肽,必要时借助载体和任选地赋形剂或添加剂。这个本发明特优选实施方案中,人类或动物未患有任何软骨疾病。特优选实施方案中,可以向未患有软骨疾病的人类或动物提供重组ii型胶原、特别是重组ii型胶原肽的口服施用,并且通过施用重组ii型胶原、特别是重组ii型胶原肽,维持软骨健康。
77、另外,本发明涉及一种用于生产根据本发明可用的重组ii型胶原、特别是ii型胶原肽的方法,包括以下方法步骤:
78、a)提供具有至少一个表达盒的表达系统,该表达盒具有至少一个编码ii型胶原、特别是ii型胶原肽的核苷酸序列;
79、b)在能够表达ii型胶原、特别是ii型胶原肽的条件下培养表达系统;
80、c)获得根据本发明的ii型胶原、特别是ii型胶原肽。
81、本发明提出的用于产生根据本发明可用的重组ii型胶原、特别是ii型胶原肽的方法,其特征尤其在于:获得了一种精确定义、重组产生的ii型胶原,特定是ii型胶原肽,尤因其生物有效性而适合用于治疗人体或动物体软骨疾病或维持软骨健康的方法。
82、相较于从天然来源水解获得的ii型胶原、特别是ii型胶原肽,本发明提出的ii型胶原、特别是ii型胶原肽因其重组制法而具有极高的纯度。根据本发明的ii型胶原、特别是ii型胶原肽可以在各种表达系统中提供,甚至可按工业规模提供,而不会产生不良污染,同时具有生物有效性的优势。
83、重组ii型胶原及其生产例如可参阅专利文献us 5,593,859。该文献公开了获得重组ii型胶原肽以及在重组细胞培养物中获得前胶原的羟基化和原纤维形成,本公开内容完全涵盖关于重组ii型胶原和重组ii型胶原肽(尤其是羟基化和三螺旋形式)的生产过程。
84、优选实施方案中,根据本发明的方法直接获得的ii型胶原、特别是ii型胶原肽无需进一步加工步骤,就已有利地赋予根据本发明的ii型胶原、特别是ii型胶原肽的生物有效性以及与之相关的生物有效性或用于治疗人体或动物体软骨疾病的方法的适用性。根据本发明,优选实施方案中,羟基化和非羟基化ii型胶原、特别是ii型胶原肽皆具生物有效性,特别是与获自天然来源的ii型胶原至少相同的生物有效性,特别优选地与获自天然来源的ii型胶原相比更佳的生物有效性。
85、这里特别有利地,根据本发明的ii型胶原、特别是ii型胶原肽即使在非羟基化形式下也会出乎预料地具有生物有效性,优选地与获自天然来源的ii型胶原相同的生物有效性,特别优选地与获自天然来源的ii型胶原相比更佳的生物功效。
86、根据本发明,羟基化和非羟基化ii型胶原、特别是ii型胶原肽优选地展现生物有效性,优选地至少与获自天然来源的ii型胶原相同的生物有效性,特别优选地与获自天然来源的ii型胶原相比更佳的生物有效性。
87、步骤a)中提供的表达系统优选为宿主细胞,特别是原核或真核细胞。
88、优选地,表达系统是选自下组的宿主细胞:细菌细胞、酵母细胞、真菌细胞、哺乳动物细胞、昆虫细胞和植物细胞。
89、优选地,表达系统、特别是宿主细胞是细菌细胞,特别是escherichia coli(大肠杆菌)或bacillus subtilis(枯草芽孢杆菌)种的细菌细胞。
90、更优选实施方案中,表达系统、特别是宿主细胞是酵母细胞,特别是saccharomyces cerevisiae(酿酒酵母)、pichia pastoris(巴斯德毕赤酵母)或ogataeaangusta(hansenulapolymorpha)种的酵母细胞,特别是pichiapastoris(巴斯德毕赤酵母)。
91、优选地,表达系统、特别是宿主细胞是真菌细胞,特别是aspergillus niger(黑曲霉)种的真菌细胞。
92、本发明更优选实施方案中,表达系统、特别是宿主细胞是哺乳动物细胞,特别是cho细胞、hela细胞或hek293细胞。
93、优选地,表达系统、特别是宿主细胞是昆虫细胞,特别是sf-9细胞、sf-21细胞或tn-5细胞。
94、优选地,表达系统、特别是宿主细胞是植物细胞,特别是玉米细胞或烟草细胞。
95、本发明更优选实施方案中,步骤a)中提供的表达系统是能够使表达胶原肽的脯氨酸、赖氨酸或脯氨酸残基和赖氨酸残基羟基化的宿主细胞。优选地,步骤a)中提供的表达系统是不能使表达胶原肽的脯氨酸、赖氨酸或脯氨酸残基和赖氨酸残基羟基化的宿主细胞。
96、优选地,步骤a)中提供的表达系统是具有脯氨酰羟化酶活性和/或赖氨酰羟化酶活性的表达系统。优选地,步骤a)中提供的表达系统是具有脯氨酰羟化酶活性和/或赖氨酰羟化酶活性的宿主细胞。
97、优选实施方案中,步骤a)中提供的表达系统是具有至少一个包含脯氨酰-4-羟化酶编码多核苷酸序列的表达盒的宿主细胞。特别优选地,步骤a)中提供的表达系统是具有至少一个包含脯氨酰-4-羟化酶编码多核苷酸序列的表达盒的宿主细胞,从而步骤c)中获得体内羟基化ii型胶原,特别是体内羟基化ii型胶原肽。
98、优选实施方案中,步骤a)中提供的表达系统是具有至少一个包含赖氨酰羟化酶编码多核苷酸序列的表达盒的宿主细胞。特别优选地,步骤a)中提供的表达系统是具有至少一个包含赖氨酰羟化酶编码多核苷酸序列的表达盒的宿主细胞,从而步骤c)中获得体内羟基化的ii型胶原,特别是体内羟基化ii型胶原肽。
99、本发明更优选实施方案中,步骤a)中提供的表达系统是宿主细胞,其具有至少一个包含脯氨酰-4-羟化酶编码多核苷酸序列的表达盒和至少一个包含赖氨酰-4-羟化酶编码多核苷酸序列的表达盒。特别优选地,步骤a)中提供的表达系统是宿主细胞,其具有至少一个包含脯氨酰-4-羟化酶编码多核苷酸序列的表达盒和至少一个包含赖氨酰羟化酶编码多核苷酸序列的表达盒,从而步骤c)中获得体内羟基化的ii型胶原,特别是体内羟基化ii型胶原肽。
100、本发明优选实施方案中,脯氨酰-4-羟化酶编码多核苷酸序列包含seq id no.5所示的核苷酸序列。特别优选地,脯氨酰-4-羟化酶编码多核苷酸序列编码单体脯氨酰-4-羟化酶,特别是具有seq id no.6所示氨基酸序列的脯氨酰-4-羟化酶,优选地由seq id no.6所示氨基酸序列组成。
101、就此,本发明还涉及一种用于生产可根据本发明使用的重组ii型胶原、特别是ii型胶原肽、特别是体内羟基化ii型胶原、特别是体内羟基化ii型胶原肽的方法,包括以下方法步骤:
102、a)提供具有至少一个表达盒的表达系统,该表达盒具有至少一种编码ii型胶原、特别是ii型胶原肽的核苷酸序列,该表达系统能够使表达胶原肽的脯氨酸、赖氨酸或脯氨酸残基和赖氨酸残基羟基化;
103、b)在能够表达和羟基化ii型胶原、特别是ii型胶原肽的条件下培养表达系统;
104、c)获得根据本发明的ii型胶原,特别是ii型胶原肽,特别是体内羟基化ii型胶原,特别是体内羟基化ii型胶原肽。
105、就此,借助上述方法,能够有利地获得体内羟基化重组产生的ii型胶原,特别是ii型胶原肽,取决于所用的基于细胞的表达系统,其特征在于特定模式翻译后修饰,特别是羟基化和糖基化。这样就能有利地、特别是直接地(即无需后续修饰)即可获得具有预期生物有效性的ii型胶原,特别是重组产生的ii型胶原肽,可应用于治疗性处置人体或动物体软骨疾病的方法。
106、优选实施方案中,根据本发明产生的重组体内羟基化胶原肽具备生物有效性。根据本发明另一实施方案,步骤a)中提供的表达系统是不能引起表达胶原肽的脯氨酸、赖氨酸或脯氨酸残基和赖氨酸残基羟基化的表达系统,特别是步骤a)中提供的表达系统不具有脯氨酰羟化酶活性和赖氨酰羟化酶活性。
107、就此,本发明包括一种生产可根据本发明使用的重组胶原肽、特别是非羟基化胶原肽的方法,包括以下方法步骤:
108、a)提供具有至少一个表达盒的表达系统,该表达盒具有至少一种编码ii型胶原、特别是ii型胶原肽的核苷酸序列,该表达系统不能使所表达ii型胶原、特别是ii型胶原肽的脯氨酸、赖氨酸或脯氨酸残基和赖氨酸残基羟基化;
109、b)在能够表达ii型胶原、特别是ii型胶原肽的条件下培养表达系统;
110、c)获得根据本发明的ii型胶原,特别是ii型胶原肽,特别是非羟基化ii型胶原,特别是非羟基化ii型胶原肽。
111、根据本发明优选实施方案,所述至少一个表达盒的至少一个核苷酸序列经过密码子优化,即,核苷酸序列中不供所提供表达系统的翻译系统、特别是所提供基于细胞的表达系统的翻译系统、特别是所提供宿主细胞的翻译系统使用或优选使用的那些密码子取代为供所提供表达系统的翻译系统、特别是所提供基于细胞的表达系统的翻译系统、特别是所提供宿主细胞的翻译系统优选使用的那些密码子,而不改变所编码肽或蛋白质的氨基酸序列。
112、本发明优选实施方案中,由核苷酸序列编码的ii型胶原、特别是ii型胶原肽是脊椎动物、特别是哺乳动物(例如人类或非人类哺乳动物,例如马、袋鼠、啮齿动物、猪、羊或牛)、鸟类(例如鸡)、鱼类、两栖动物、爬行动物或无脊椎动物(例如水母)的ii型胶原、特别是ii型胶原肽。
113、本发明优选实施方案中,步骤a)中提供的表达盒包含至少一种seq id no.1所示的核苷酸序列。
114、特别优选地,步骤a)中提供的表达盒所含的至少一种核苷酸序列与seq id no.1所示核苷酸序列的序列一致性达至少90%、优选至少95%、优选至少96%、优选至少97%、优选至少98%、优选至少99%。
115、特别优选地,由核苷酸序列编码的ii型胶原、特别是ii型胶原肽是一种包含seqid no.2所示氨基酸序列的ii型胶原,特别是ii型胶原肽。由核苷酸序列编码的ii型胶原、特别是ii型胶原肽优选地由seq id no.2所示的氨基酸序列组成。
116、本发明更优选实施方案中,由核苷酸序列编码的ii型胶原、特别是ii型胶原肽与seq id no.2所示氨基酸序列的序列一致性达至少80%,优选至少85%,优选至少90%,优选至少95%,优选至少96%,优选至少97%,优选至少98%,优选至少99%。
117、根据本发明优选实施方案,步骤a)中提供的表达盒包含至少一种seq id no.3所示的核苷酸序列。
118、特别优选地,步骤a)中提供的表达盒所含的至少一种核苷酸序列与seq id no.3所示核苷酸序列的序列一致性达至少90%、优选至少95%、优选至少96%、优选至少97%、优选至少98%、优选至少99%。
119、特别优选地,由核苷酸序列编码的ii型胶原、特别是ii型胶原肽是一种包含seqid no.4所示氨基酸序列的ii型胶原,特别是ii型胶原肽。由核苷酸序列编码的ii型胶原、特别是ii型胶原肽优选地由seq id no.4所示的氨基酸序列组成。
120、本发明更优选实施方案中,由核苷酸序列编码的ii型胶原、特别是ii型胶原肽与seq id no.4所示氨基酸序列的序列一致性达至少80%,优选至少85%,优选至少90%,优选至少95%,优选至少96%,优选至少97%,优选至少98%,优选至少99%。
121、优选地,由核苷酸序列编码的ii型胶原、特别是ii型胶原肽是天然存在的ii型胶原、特别是ii型胶原肽。本发明更优选实施方案中,由核苷酸序列编码的ii型胶原、特别是ii型胶原肽不是天然存在的ii型胶原、特别是ii型胶原肽。优选地,由核苷酸序列编码的ii型胶原、特别是ii型胶原肽是基因修饰的胶原肽。
122、根据本发明优选实施方案,所述至少一种核苷酸序列编码的ii型胶原肽的分子量范围为5-400kda、特别是10-390kda、特别是10-350kda、特别是10-300kda,特别是10-110kda、特别是40-110kda、特别是40-100kda、特别是11-105kda、特别是15-100kda、特别是20-99kda、特别是25-95kda、特别是30-95kda、特别是35-95kda、特别是40-50kda、特别是45kda。
123、本发明特优选实施方案中,本发明方法的特征在于,在步骤b)中,选取能够形成非变性(即天然)ii型胶原、特别是ii型胶原肽的条件。
124、本发明特优选实施方案中,本发明方法的特征在于,在步骤b)中,选取能够形成ii型胶原、特别是ii型胶原肽的三螺旋形式的条件。
125、特优选实施方案中,根据本发明的方法能够产生分子量均一的特殊ii型胶原肽的均质分离制剂。
126、特优选实施方案中,本发明还提供以此方式制备的ii型胶原肽的均质分离制剂混合物,每种制剂的分子量均一。
127、本发明还提出了通过裂解、特别是水解从根据本发明的方法生产的分子量均一、均质分离的ii型胶原肽制备重组的胶原肽水解物。本发明特别是提供了本发明提出的用于口服治疗人体或动物体软骨疾病的分子量均一、均质分离的ii型胶原肽、它们的混合物或它们的水解物。
128、根据本发明,本发明方法的特征在于,继步骤b)或c)之后,在步骤d)中通过裂解、特别是水解所表达的ii型胶原、特别是ii型胶原肽,获得重组的ii型胶原肽水解物。
129、根据本发明通过步骤d)获得的ii型胶原肽水解物可以呈该ii型胶原水解物的形式或者在分离一种或多种、优选地均质分离的ii型胶原肽,用作根据本发明的重组ii型胶原肽。
130、本发明特优选实施方案中,还可以提出将均质分离的ii型胶原肽彼此混合,即代表重组ii型胶原肽的混合物。
131、因此,特优选实施方案中,本发明还涉及一种重组ii型胶原肽,其呈均质分离的均一分子量形式或作为重组ii型胶原肽存在于与重组或天然、特别是重组的ii型胶原肽的混合物中或存在于重组ii型胶原、特别是重组ii型胶原肽的水解物中。
132、编码可根据本发明使用的重组ii型胶原肽的核苷酸序列可以通过本领域常规方式获得,例如参阅专利文献wo 93/07889、us2006/0147501、us 5,593,859或us2008/0081353。
133、本发明优选实施方案中,可根据本发明使用、优选地通过上述本发明方法之一产生的ii型胶原,特别是ii型胶原肽是非羟基化、部分羟基化或完全羟基化ii型胶原肽,优选是非羟基化ii型胶原肽,优选是部分羟基化ii型胶原肽,优选是完全羟基化ii型胶原肽。
134、本发明优选实施方案中,可根据本发明使用、优选地通过上述方法之一产生的ii型胶原、特别是重组ii型胶原肽是糖基化胶原肽,用于治疗性处置人体或动物体软骨疾病的方法。所述ii型胶原、特别是ii型胶原肽优选为体内糖基化,优选为离体糖基化。
135、本发明更优选实施方案中,可根据本发明使用、优选地通过上述本发明方法之一产生的ii型胶原、特别是ii型胶原肽是非糖基化ii型胶原、特别是ii型胶原肽。
136、根据本发明,术语“生物有效性”优选意指可根据本发明使用的ii型胶原、特别是ii型胶原肽用于免疫调节、特别是抑制免疫球蛋白(特别是ige、iga、igm和/或igg)合成的能力。
137、根据本发明,术语“生物有效性”还优选意指可根据本发明使用的ii型胶原、特别是ii型胶原肽用于抑制促炎细胞因子(特别是tnfα、il-6和ifnγ)的形成和活性或者刺激抗炎细胞因子(特别是il-4、il-10和tgf-β1)的合成和活性、特别是二者兼备的能力。
138、根据本发明,术语“生物有效性”优选意指可根据本发明使用的ii型胶原、特别是ii型胶原肽用于免疫调节、特别是抑制免疫球蛋白(特别是ige、iga、igm和/或igg)合成、抑制促炎细胞因子(特别是tnfα、il-6和ifnγ)形成以及刺激抗炎细胞因子(特别是il-4、il-10和tgf-β1)合成的能力。
139、特优选实施方案中,生物有效性特别是通过本领域技术人员关于免疫调节、特别是刺激和抑制物质活性以及抗炎细胞因子和促炎细胞因子活性熟知的检测方法来测定。具体而言,通过根据例2、例3、例4和/或例5的方法来测定本发明意义上的生物有效性。根据本发明,术语“生物有效性”还优选意指可根据本发明使用的ii型胶原、特别是ii型胶原肽诱导口服耐受性的能力。特优选实施方案中,存在口服耐受性是通过本领域技术人员关于测定物质口服耐受性诱导能力熟知的检测方法、特别是通过根据例2、例3、例4和/或例5的方法来测定。
140、本发明上下文中,促炎细胞因子特别是tnfα、il-6和ifn-γ。
141、本发明上下文中,抗炎细胞因子特别是il-4、il-10和tgf-β1。
142、本发明上下文中,术语“抑制”应意指部分或完全阻止蛋白质合成,可具体表示为减少或抑制蛋白质合成或者减少或抑制蛋白质相关的mrna合成。
143、本发明上下文中,术语“胶原”采取广义理解,特别是例如wo 01/34646中的定义。更优选实施方案中,术语“胶原”应意指具有甘氨酸-脯氨酸、甘氨酸-4-羟脯氨酸或甘氨酸-x-4-羟脯氨酸序列,优选地重复基序(gly-xy)n的胶原蛋白或肽,其中x和y可以是任何氨基酸,优选为脯氨酸和4-羟基脯氨酸。术语“胶原”特别优选意指具有重复基序(gly-pro-y)n和/或(gly-x-hyp)m的肽,其中x和y可以是任何氨基酸。
144、根据本发明的“ii型胶原”是根据上述内容广义理解的胶原,其中ii型胶原具有天然存在的ii型胶原的氨基酸序列,特别是脊椎动物(特别是猪、羊、牛、啮齿动物、马、鸟、鱼、爬行动物或两栖动物)或无脊椎动物(特别是水母)的ii型胶原的氨基酸序列。
145、所述ii型胶原可以呈单体胶原肽(这里又称单链胶原肽)或者包含至少两个、特别是三个胶原肽、特别是三聚体的二聚体或三聚体,特别是由相同的单链胶原肽组成。特别地,所述ii型胶原可以呈三螺旋ii型胶原肽、特别是天然ii型胶原。
146、本发明上下文中,术语“ii型胶原肽”应意指单链ii型胶原肽,其具有如上定义的ii型胶原中存在的氨基酸序列,该肽是寡肽或多肽。所述ii型胶原肽特别是可呈化学修饰的形式,特别是羟基化和/或糖基化形式,也可以未修饰。
147、优选地,根据本发明使用的重组ii型胶原、特别是ii型胶原肽可以具有天然存在的ii型胶原、特别是ii型胶原肽的序列修饰、特别是功能保留序列修饰。
148、据此,“ii型胶原”也意指天然存在的ii型胶原、特别是ii型胶原肽的功能保留序列修饰,特别是若在氨基酸水平上,其与天然存在的ii型胶原的氨基酸序列的氨基酸序列一致性达至少80%,特别是至少85%,特别是至少90%,特别是至少95%,特别是至少96%,特别是在至少97%、特别是至少98%、特别是至少99%。根据本发明,ii型胶原的存在条件是:重组ii型胶原精确地具有天然存在的ii型胶原中存在的氨基酸序列,或者存在功能保留序列修饰,与天然存在的ii型胶原相比、特别是与来自脊椎动物(特别是猪、羊、牛、啮齿动物、袋鼠、马、鸟、爬行动物、两栖动物或鱼)或无脊椎动物(特别是水母)的天然存在的ii型胶原相比的氨基酸序列一致性达至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98、至少99%,特别是该氨基酸一致性与来自牛的天然存在的ii型胶原氨基酸序列相比。
149、本发明上下文中,利用smith-waterman算法(sse2,michael farrar,2006,7.2,2010年11月)用参数bl50矩阵(15:-5),open/ext:-12/-2确定氨基酸序列一致性。
150、根据本发明,术语“功能保留序列修饰”应意指既定、特别是天然存在的氨基酸序列的修饰,特别是单个或几个氨基酸的交换、添加和/或删除,这会导致氨基酸序列偏离既定的氨基酸序列,修饰的氨基酸序列则保留了既定氨基酸序列的功能特征,特别是其生物有效性。
151、“功能保留序列修饰”优选意指既定、特别是天然存在的氨基酸序列的修饰,其中作为既定氨基酸序列的特征性功能、特别是生物有效性保留至少50%、优选至少60%、优选至少70%、优选至少80%、优选至少90%、优选至少95%、优选100%。更优选地,根据本发明,“功能保留序列修饰”应意指既定氨基酸序列的修饰,其中修饰的氨基酸序列与既定氨基酸序列的序列一致性达至少50%、优选至少55%、优选至少55%、优选至少60%、优选至少65%、优选至少70%、优选至少75%、优选至少80%、优选至少85%、优选至少90%。
152、特别优选地,序列修饰、特别是本发明上下文中的“功能保留序列修饰”是对既定、特别是天然存在的氨基酸序列的修饰,其中一个或多个某些化学物理属性的氨基酸被一种或多种相同或相似化学物理属性的氨基酸取代,例如,一种非极性侧链氨基酸(例如ala、val、met、leu、ile、pro、trp、phe)被另一种非极性侧链氨基酸(例如ala、val、met、leu、ile、pro、trp、phe)取代,一种极性神经侧链氨基酸(例如tyr、thr、gln、gly、ser、cys、asn)被另一种极性神经侧链氨基酸(例如tyr、thr、gln、gly、ser、cys、asn)取代,一种酸性侧链氨基酸(例如,glu、asp)被另一种酸性侧链氨基酸(例如,glu、asp)取代,且/或碱性侧链氨基酸(例如,lys、arg、his)被另一种碱性侧链氨基酸(例如lys、arg、his)取代。根据该实施方案,“功能保留序列修饰”中既定氨基酸序列的化学物理属性得以保留或仅轻微改变。
153、另一实施方案中可以提出,序列修饰、特别是“功能保留序列修饰”包括将既定氨基酸序列、特别是天然存在的氨基酸序列的至少一种氨基酸、优选地既定氨基酸序列、特别是天然存在的氨基酸序列的至少一种非必需氨基酸(特别是ala、asn、asp、glu、ser)取代为至少一种极特定的氨基酸,特别是至少一种必需氨基酸,特别是ile、leu、lys、met、phe、thr、trp、val、his、cys、tyr,特别优选trp,其中,既定氨基酸序列、特别是天然存在的氨基酸序列保留了特征性功能,特别是生物有效性,特别是根据本发明的生物有效性,特别是根据例2、例3、例4和/或例5中所示检定的生物有效性。
154、根据本发明,序列修饰、特别是“功能保留序列修饰”还应意指对既定氨基酸序列、特别是天然存在的氨基酸序列的修饰,即:既定氨基酸序列、特别是天然存在的氨基酸序列添加有至少一种氨基酸,优选地至少一种必需氨基酸,特别是ile、leu、lys、met、phe、thr、trp、val、his、cys、tyr,特别优选是trp,其中,既定氨基酸序列、特别是天然存在的氨基酸序列保留特征性功能,特别是本发明的生物有效性,特别是根据例2、例3、例4和/或例5中所示检定的生物有效性。根据本发明可以提出,在n端、c端和/或氨基酸序列内添加至少一种氨基酸,优选地至少一种必需氨基酸,特别是ile、leu、lys、met、phe、thr、trp、val、his、cys、tyr,特别优选是trp。
155、本发明上下文中,术语“氨基酸修饰”是指可能发生在重组ii型胶原、特别是ii型胶原肽的合成之前、之后或期间的一种或多种氨基酸的化学变化,同时保留了ii型胶原肽的原始氨基酸骨架,特别是一种或多种蛋白氨基酸。就此,该术语既包括使用化学修饰的氨基酸来合成根据本发明的ii型胶原、特别是ii型胶原肽,又包括在合成ii型胶原、特别是ii型胶原肽之后或期间的氨基酸化学变化。胶原肽典型的氨基酸修饰特别是脯氨酸残基和赖氨酸残基的羟基化以及羟基化赖氨酸残基的糖基化。但根据本发明,该术语还包括氨基酸的其他化学变化,例如磷酸化、n-糖基化、乙酰化、甲基化或肉豆蔻酰化。
156、本发明上下文中,所述重组ii型胶原、特别是ii型胶原肽或重组产生的ii型胶原、特别是ii型胶原肽是借助表达系统通过生物技术重组生产获得的ii型胶原、特别是ii型胶原肽。根据本发明,所述重组ii型胶原、特别是ii型胶原肽或重组产生的ii型胶原、特别是ii型胶原肽的共同点是它们不是获自天然来源。
157、本发明特优选实施方案中,所述重组ii型胶原、特别是ii型胶原肽呈该ii型胶原或ii型胶原肽的均质制剂形式,特别是这样的制剂包含至少90wt.%、优选至少95wt.%、特别是至少98wt.%、特别是至少99wt.%、优选100wt.%的ii型胶原或ii型胶原肽。优选实施方案中,均质制剂中仅存特定大小(即特定分子量,即单一分子种)的ii型胶原或ii型胶原肽。本发明优选实施方案中,所述重组ii型胶原或ii型胶原肽呈分离形式。本发明特优选实施方案中,所述重组ii型胶原或ii型胶原肽不含其他蛋白质或肽,特别是不含其他物质,例如杂质,特别是不含非蛋白质材料、不含盐和/或不含其他蛋白质或肽。
158、本发明上下文中,术语“明胶”采取广义理解,特别是例如wo01/34646中的定义。
159、本发明上下文中,术语“重组dna”意指借助基因工程方法在体外产生的人工产生或操作的dna分子。优选实施方案中,重组dna由不同来源生物体的组分组成。
160、本发明上下文中,术语“表达盒”应意指dna片段,负责将该片段中编码的信息转录成rna、特别是转录成mrna,并含有至少一个启动子和蛋白质编码核苷酸序列,一般含有至少一个启动子、至少一个蛋白质编码核苷酸序列和任选的终止子。
161、本发明上下文中,“核苷酸序列”应意指核酸、特别是核酸链、特别是dna链或rna链的核苷酸序列。因此,“核苷酸序列”应意指信息单元和物理上表现该信息的dna链或rna链。
162、本发明上下文中,“表达系统”应意指可发生靶向和受控的蛋白质生物合成的系统。根据本发明,术语“表达系统”包括无细胞表达系统(其中蛋白质生物合成所需的组分不存在于细胞内,即蛋白质生物合成发生在细胞外)和基于细胞的表达系统(其中蛋白质生物合成发生在活细胞内)。本发明上下文中,无细胞表达系统优选是来自e.coli(大肠杆菌)、昆虫细胞、麦芽、烟草细胞或哺乳动物细胞,特别是来自兔的cho细胞或网织红细胞的裂解物或提取物,其包含蛋白质生物合成所必需的组分,特别是翻译系统和转录系统。在本发明方法之一使用无细胞表达系统的情况下,术语“培养”与“孵育”同义。
163、本发明上下文中,“宿主细胞”应意指能够表达外源dna、特别是重组dna中编码的肽或蛋白质的活细胞。
164、根据本发明,根据步骤c)的术语“获得ii型胶原、特别是ii型胶原肽”是本领域技术人员公知的方法,用于通过公知的分离法,例如离心法(特别是差速离心和/或密度梯度离心)、色谱法(特别是凝胶过滤、离子交换、亲和和/或高效液相色谱)、电泳法、过滤法和/或提取法,从含多种组分的组合物中分离ii型胶原或ii型胶原肽,其中从含多种组分的组合物中富集和纯化相关组分可以优选地通过连续应用几种分离法来实现。视需要,可以在提取之前、之后或期间裂解c端和/或n端前胶原片段来获得胶原。
165、在步骤b)的条件背景下,还可以优选地发生原纤维形成、化学修饰和表达ii型胶原肽分泌。
166、根据本发明,“能够表达ii型胶原、特别是ii型胶原肽的条件”应意指激活或增强ii型胶原、特别是ii型胶原肽表达的条件,例如特别是温度、压力、时间、光以及是否存在诱导物和/或阻遏物。优选实施方案中,ii型胶原、特别是ii型胶原肽的表达发生在高细胞密度发酵的背景下,特别是在高压下,优选是在高气压下。能够表达ii型胶原、特别是ii型胶原肽的具体条件为本领域技术人员公知,取决于所用的表达系统和所用的表达盒,特别是其中所含的启动子。ii型胶原、特别是ii型胶原肽的表达可以是组成型或诱导型表达,取决于表达盒的结构。
167、本发明上下文中,“软骨疾病口服疗法”应意指用于预防和/或处置软骨疾病、特别是用于处置软骨疾病的方法,其中重组ii型胶原为口服给药。
168、本发明上下文中,“软骨疾病”特别是炎症性、退变性和/或由自身免疫作用、特别是过度免疫反应引起的软骨疾病,特别是骨关节炎和/或类风湿性关节炎。本发明上下文中,“软骨疾病”特别是关节软骨疾病,特别是脚、膝盖、手指、手腕、臀部和脊柱中关节的软骨疾病。
169、根据本发明,“软骨疾病口服疗法”还优选意指诱导针对内源性胶原、特别是内源性ii型胶原、特别是存在于软骨组织之中或之上的内源性ii型胶原的口服耐受性的方法。
170、本发明上下文中,术语“包含”和“具有”是指除了这些术语明确涵盖的元素外还可能出现未明确提及的其他元素。本发明上下文中,这些术语也可指仅涵盖明确提及的元素而不存在其他元素。在本特定实施方案中,术语“包含”和“具有”与术语“由……组成”同义。另外,术语“包含”和“具有”还涵盖除了明确提及的元素外还包括虽未提及但在功能和定性上从属性的其他元素的组合物。在本实施方案中,术语“包含”和“具有”与术语“基本上由……组成”同义。
171、本发明上下文中,若数字中指定第一和第二小数位或者第二小数位,则将其设置为零。
172、本发明上下文中,术语“和/或”是指表示通过术语“和/或”连接的一组所有成员既可互为替代,又可相互之间任意组合。对于表述“a、b和/或c”,这应理解为:(a)a或b或c;或(b)a和b;或(c)a和c;或(d)b和c;或(e)a和b和c。
173、更多优选实施方案请参阅从属权利要求。
- 还没有人留言评论。精彩留言会获得点赞!