一种双膦配体衍生物的合成及其催化应用的制作方法
本发明属于精细化工和香精香料领域,具体涉及一种双膦配体衍生物的合成及其在催化不对称氢化中的应用。
背景技术:
1、香茅醛是天然香茅油和柠檬桉油的重要组分,具有强烈、新鲜的青柑橘气息。由于其分子结构中有一个手性碳,香茅醛有两种光学异构体—(r)-香茅醛和(s)-香茅醛;由于(r)-香茅醛可以用于清凉剂l-薄荷醇的合成,因而具有更高的经济价值,(s)-香茅醛附加值相对较低。
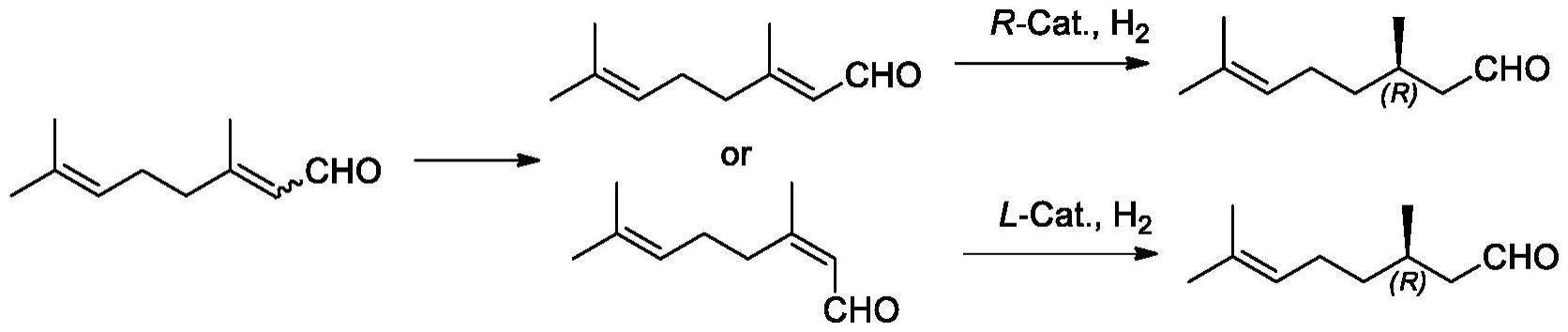
2、目前,在已有文献报道中,(r)-香茅醛的合成方法主要有以下3种,分别是橙花醛或香叶醛的不对称氢化法、月桂烯法、手性香茅醇脱氢法。橙花醛或香叶醛是一对双键异构体,由柠檬醛精馏分离得到,采用手性催化剂对柠檬醛进行加氢可以非常方便的合成手性香茅醛(j.mol.cat.1982,16,51;helv.chim.acta.2001,84,230.)。采用同一构型的催化剂,橙花醛和香叶醛加氢分别得到(r)-香茅醛和(s)-香茅醛;因此,要想选择性的得到(r)-香茅醛,必须首先分离得到纯净的橙花醛或香叶醛,二者的沸点十分相近,分离较困难(ep0000315,cn101039894a,cn101675020a,cn101932543a)。目前在已有的文献报道中,橙花醛或香叶醛的不对称氢化也仅能取得最高91-92%的ee值,由于ee值较低,造成收率较低,后续还需要通过重结晶除去相反构型的产物,进一步降低了收率,增加了成本。
3、
4、月桂烯法由日本高砂发明(j.chem.soc.chem.comn.,1982,11,600;topics incatalysis,1997,4,271.),以松节油衍生的月桂烯为原料,和二乙基胺基锂反应得到烯丙胺,烯丙胺在手性铑催化下,发生异构得到手性烯胺,最后水解得到(r)-香茅醛(us4605750a,cn101602651a,cn102935384a,cn103254047a)。虽然该路线已经实现千吨级放大,但是,该方法第1步反用到胺基锂,价格昂贵,对水、氧敏感,生产中存在较大的安全风险。
5、
6、综上所述,手性香茅醛具有重要的经济价值。目前已知的手性香茅醛合成方法中,橙花醛或香叶醛不对称氢化法是目前成本最低的手性香茅醛合成方法,但是现在不对称氢化法ee值较低,最高也仅有91-92%,影响该路线的经济性。因此,目前亟待发展新型的双膦配体,可以提高橙花醛或香叶醛不对称氢化法的对映选择性,提升反应收率,从而促进手性香茅醛的放大生产。
技术实现思路
1、本发明的目的在于提供一种双膦配体衍生物的合成方法及其在催化不对称氢化中的应用:首先是2,3-二苯基膦氧基-1,3-丁二烯和格氏试剂发生加成反应,得到消旋膦氧中间体,随后采用化学拆分法得到手性膦氧中间体,最后通过硅氢还原得到手性双膦配体;采用上述方法得到的手性双膦配体,实现了橙花醛、香叶醛的等底物的不对称氢化,高立体选择性地获得了手性产品。
2、为实现上述目的和达到上述技术效果,本发明采用如下技术方案:
3、一种双膦配体衍生物的合成方法,所述方法包括以下步骤:
4、s1:格氏试剂rmgx和2,3-二苯基膦氧基-1,3-丁二烯发生加成反应,得到消旋膦氧中间体a;
5、s2:化学拆分法拆分消旋膦氧中间体a,得到手性膦氧中间体b;
6、s3:硅氢还原手性膦氧中间体b,得到目标双膦配体c。
7、相比于chiraphos配体,本发明所述双膦配体手性碳的取代基位阻更大,可以在磷原子周围形成更大的手性空腔,因而手性识别效果更好,可以诱导产生更高的产物ee值。
8、在一种实施方案中,所述合成路线示意如下:
9、
10、本发明中,s1所述格氏试剂rmgx中,r是饱和烷基、不饱和烷基、芳香环及含取代基的芳香环、杂芳香环及含取代基的杂芳香环中的一种或多种,优选乙基、异丙基、异丁基、苯环中的一种或多种;x是卤族元素,优选氯、溴、碘中的一种或多种,更优选氯和/或溴;优选地,所述格氏试剂用量为2,3-二苯基膦氧基-1,3-丁二烯摩尔量的200.0~400.0mol%,优选220.0~250.0mol%。
11、本发明中,s1所述加成反应在催化剂和配体存在下进行;优选地,所述催化剂是具有催化迈克尔加成反应活性的金属,优选铜、镍、铁、锰、钯中的一种或多种,更优选催化剂是但不限于氯化铜、氯化亚铜、溴化铜、溴化亚铜、碘化铜、碘化亚铜、醋酸铜、乙酰丙酮铜、乙酰丙酮铁、醋酸镍、氯化钯、醋酸钯中的一种或多种,最优选碘化亚铜;优选地,所述催化剂的用量为2,3-二苯基膦氧基-1,3-丁二烯摩尔量的1.0~5.0mol%,优选2.0~5.0mol%。
12、本发明中,s1中配体是邻菲罗啉、联吡啶、异喹啉中的一种或多种;优选地,配体用量为2,3-二苯基膦氧基-1,3-丁二烯摩尔量的2.0~10.0mol%。
13、本发明中,s1所述加成反应在溶剂中进行;优选地,所述溶剂为非质子型溶剂,优选乙醚、甲基叔丁醚、四氢呋喃、2-甲基四氢呋喃、甲苯、苯、二甲苯中的一种或多种,更优选四氢呋喃。
14、本发明中,s1所述反应的温度为0~40℃,优选25~30℃,反应压力为常压,反应时间1~2小时。
15、本发明中,s2所述化学拆分法采用的拆分试剂为手性的有机酸,优选磺酸和/或羧酸,更优选樟脑磺酸、扁桃酸、酒石酸、酒石酸衍生物中的一种或多种,最优选二苯甲酰酒石酸、二对甲苯甲酰酒石酸、二对甲氧基苯甲酰酒石酸中的一种或多种;优选地,所述拆分试剂的用量为消旋膦氧中间体a摩尔量的90.0-120.0mol%,优选100.0-110.0mol%。
16、本发明中,s2所述化学拆分法采用的拆分溶剂是非质子型溶剂,优选乙酸乙酯、乙酸甲酯、二氯甲烷、二氯乙烷、氯仿、四氢呋喃中的一种或多种,更优选乙酸乙酯。
17、本发明中,s2所述化学拆分的温度为25-120℃。
18、本发明中,s3所述硅氢还原采用的还原试剂为氯硅烷试剂,优选三氯硅烷和/或二氯硅烷;优选地,所述还原试剂用量为手性膦氧中间体b摩尔量的3-6倍。
19、本发明中,s3所述硅氢还原的温度为120-150℃。
20、本发明中,s3采用溶剂,优选烷烃溶剂,更优选甲苯和/或二甲苯。
21、本发明中,s3反应结束后采用碱金属氢氧化钠水溶液淬灭过量硅氢试剂。
22、本发明的另一目的在于提供一种chiraphos型双膦配体。
23、一种chiraphos型双膦配体,采用上述合成方法制备得到,所述双膦配体具有偕二手性中心,手性碳原子取代基大小可调。
24、本发明的又一目的在于提供一种不对称氢化的方法。
25、一种不对称氢化的方法,所述方法采用上述合成方法制备的chiraphos型双膦配体,或采用上述的chiraphos型双膦配体;所述不对称氢化反应中金属催化剂为铑;优选地,所述金属催化剂用量为底物的0.05~0.5mol%;优选地,所述配体用量为底物的0.06~0.6mol%。
26、本发明中,所述不对称氢化反应的底物是醛或酮,优选橙花醛、香叶醇、3-甲基-2-丁烯醛、异佛尔酮、e,e-金合欢醛中的一种或多种,更优选橙花醛和/或香叶醛。
27、本发明中,所述不对称氢化反应中氢气压力是4.0~6.0mpag,反应温度为60~80℃,反应时间4~12小时。
28、本发明中,所述不对称氢化的反应在非质子型溶剂中进行;优选地,非质子型溶剂选自甲基叔丁醚、四氢呋喃、甲苯、苯、二甲苯、乙酸乙酯、乙酸丙酯、二氯甲烷、二氯乙烷中的一种或多种。
29、本发明采用上述技术方案,具有如下积极效果:
30、1、所述双膦配体制备原料易得、价格低廉,合成路线新颖,收率高且易于放大合成和制备。
31、2、制备过程中催化剂催化的迈克尔加成反应,可高效得到加成产物。
32、3、所述双膦配体在不对称氢化中可以更高的ee值。
- 还没有人留言评论。精彩留言会获得点赞!