一种基于KFERQ序列的药物控制系统及其构建方法和应用
本发明属于生物医药,具体涉及一种基于kferq序列的药物控制系统及其构建方法和应用。
背景技术:
1、dna敲除和rna干扰这两种在基因组和mrna水平上调节蛋白质表达水平的技术现已被广泛应用,其无疑是现阶段改变蛋白质表达含量和功能的有力工具。然而,这两种方法对蛋白质的调控都是间接的,在特异性、速度和可逆性方面受到限制,例如由crispr/cas9(clustered regulatory interspaced short palindromic repeats/crispr-associatedprotein 9)技术引起的脱靶现象;长寿命的蛋白质需要更多的时间来消耗它甚至可能完全抵抗dna和rna靶向消耗方法,并且在去除外部影响后受损的基因组可能很难在不逆转目标蛋白质表达的情况下恢复。这些缺陷使得这些方法作为研究工具和临床治疗收到限制。
2、目前,已发现的细胞内蛋白质的降解途径主要包括溶酶体途径、泛素-蛋白酶体途径、自噬途径等。泛素-蛋白酶体系统主要降解可溶性、短寿命和单体错误折叠的蛋白质,而溶酶体系统主要降解长寿命的蛋白质、蛋白质聚集体和受损的细胞器。自噬和泛素-蛋白酶体系统都可以通过泛素化降解底物。为了克服dna敲除和rna干扰所带来的限制,目前已有几种基于细胞自身降解方法靶向特定蛋白质降解的方法,主要有protac(proteolysis-targeting chimeras)、lytac(lysosome-targeting chimaeras)和autac(autophagy-targeting chimeras)。尽管这些用于快速靶向降解蛋白质的新技术具有许多优势,但这些降解系统缺乏一定的调控开关能力。因此,研发出一套能广泛应用的实现内源性蛋白降解开关效果的药物控制系统具有重大意义。
技术实现思路
1、针对现有技术的不足,本发明的目的是提供一种基于kferq序列的药物控制系统及其构建方法和应用,该药物控制系统通过将kferq序列与hcv-ns3序列及内源性蛋白靶向序列重组,并利用hcv-ns3蛋白酶自切割的特性药物调控内源性蛋白的降解,提供一种内源性蛋白降解的新策略。
2、伴侣介导的自噬(cma,chaperon mediated autophagy)是一种针对含有与kferq生化相关的五肽基序的蛋白质的自噬。这种cma靶向基序存在于作为cma底物的所有已知蛋白质中。有研究表明,只要kferq序列暴露,kferq序列附着(融合)的非cma底物也能服从cma。因此,发明人利用cma作为我们的降解途径来降解内源蛋白质。
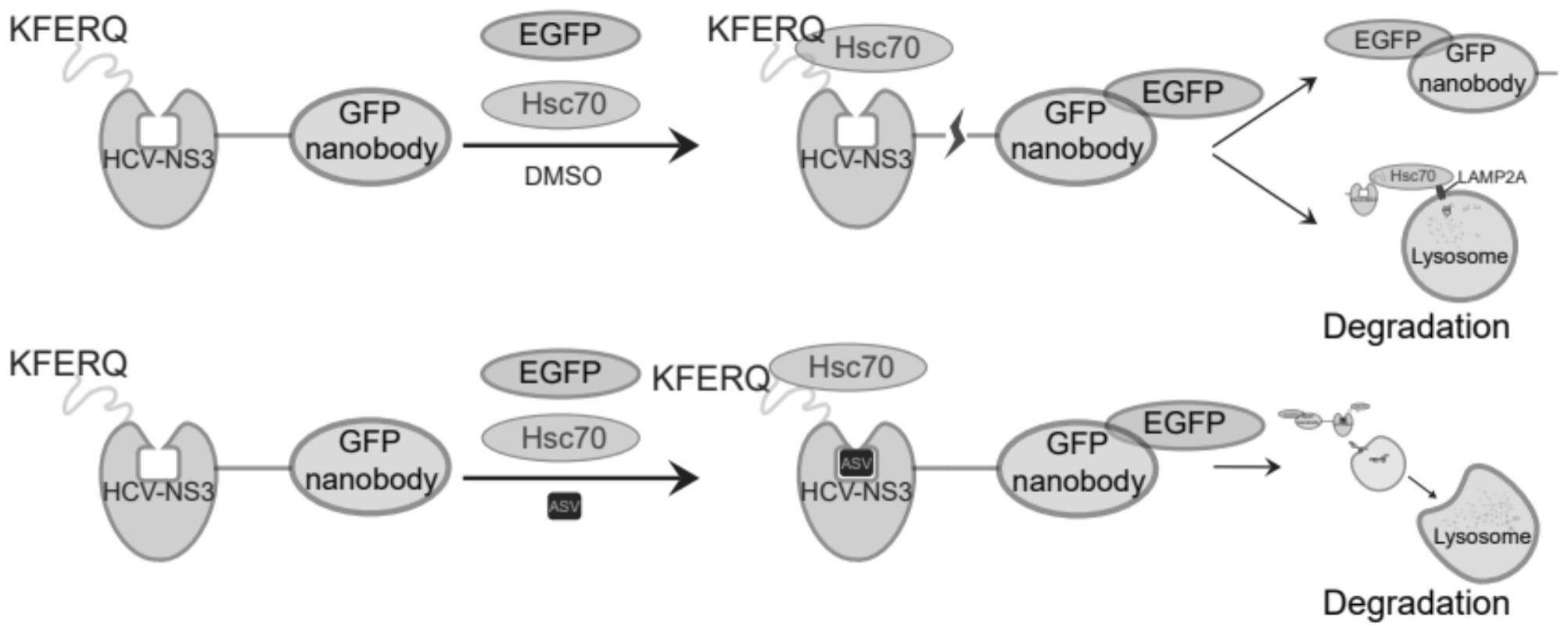
3、丙型肝炎病毒(hepatitis c virus,hcv)是黄病毒科病毒家族的成员,具有9.6kb正链rna基因组,该基因组编码约3000个氨基酸的长多蛋白前体,在被细胞和病毒蛋白酶翻译成至少10种单独的蛋白质后被蛋白水解加工,包括四种结构蛋白(c、e1、e2和p7)和六种非结构(ns)蛋白(ns2、ns3、ns4a、ns4b、ns5a和ns5b)。ns3蛋白是一种多功能蛋白,在其n端三分之一处具有丝氨酸蛋白酶结构域,在c端三分之一处具有解旋酶结构域。ns3-4a丝氨酸蛋白酶是一种非共价异二聚体复合物,由两种hcv编码蛋白、ns3的n末端丝氨酸蛋白酶结构域(催化亚基)和ns4a辅因子(活化亚基)形成。ns3-4a丝氨酸蛋白酶负责在hcv多蛋白前体的四个连接处进行蛋白水解切割:ns3/ns4a(自切割)、ns4a/ns4b、ns4b/ns5a和ns5a/ns5b。无特殊处理时,蛋白酶会从蛋白质中切除自身,但可以通过应用细胞可渗透的hcv-ns3蛋白酶抑制剂来阻止在规定时间后合成的蛋白质,如simeprevir、danoprevir、asunaprevir(asv)和ciluprevir。
4、同时,丙型肝炎病毒ns3蛋白酶由于其蛋白酶结构域很小(19kda)且是单体,表现出不寻常但特征明确的底物特异性,并且可以被无毒的细胞渗透性抑制剂很好地抑制。而kferq序列附着(融合)的非cma底物在kferq暴露时能服从cma,从而快速靶向降解蛋白质。
5、因此,为实现上述目的,本发明提供一种基于kferq序列的药物控制系统,所述药物控制系统由kferq序列、hcv-ns3序列(cleavage site与hcv-ns3相邻并组成一个元件)和蛋白靶向序列重组而成,其中,三者重组时,蛋白靶向序列在重组序列的n端或c端。
6、进一步的,上述技术方案中,所述hcv-ns3序列为由cleavage site与相邻hcv-ns3组成的一个元件。
7、hcv-ns3是一个切割cleavage site的酶,其活性位点会随着序列的顺序而改变,在一般条件下,cleavage site是在hcv-ns3的n端以获得稳定的被切割效率;而kferq序列在重组序列的n端时,hcv-ns3被调整序列顺序(即循环排列)在cleavage site的n端也可获得稳定的切割效率,此时我们称之为mhcv-ns3(和hcv-ns3一样简写为h)。
8、进一步的,上述技术方案中,所述药物控制系统为kferq-mhcv-ns3(kh)序列和蛋白靶向序列重组而成。
9、进一步的,上述技术方案中,所述蛋白靶向序列是内源性蛋白序列,为细胞内过表达的egfp序列、内源性akt序列、内源性pakt序列中的任一种。
10、进一步的,上述技术方案中,所述药物为asv(阿那匹韦)。阿那匹韦是一种丙肝病毒ns3/ns4a蛋白酶抑制剂,可用于治疗丙肝。
11、本发明还提供一种基于kferq序列的药物控制系统的构建方法,包括以下步骤:以fv185为质粒载体,先将hcv-ns3序列序列与kefrq序列进行重组,得到kferq-mhcv-ns3(kh)或hcv-ns3-kferq(hk)重组序列,然后在所得重组序列的n端或c端插入蛋白靶向序列,即得重组质粒。
12、进一步的,上述技术方案中,所述蛋白靶向序列为内源性akt时,在c端插入gfpnanobody序列或2xaktin序列。
13、优选的,所述重组质粒包括kh-蛋白靶向序列。
14、本发明还提供一种上述药物控制系统在降解外源性过表达的egfp、降解内源性促癌蛋白中的应用。
15、进一步的,上述技术方案中,应用于降解细胞内过表达的egfp时,将含蛋白靶向序列为egfp的药物控制系统的质粒转染受体细胞6-8h后,加入asv药物进行处理,继续培养24h,检测egfp降解情况。
16、进一步的,上述技术方案中,应用于降解内源性促癌蛋白时,将蛋白靶向序列为2xaktin的药物控制系统的质粒转染受体细胞6-8h后,加入asv药物进行处理,继续培养24h,检测akt、pakt降解情况。
17、本发明具有的有益效果是:
18、本发明通过将kferq序列与hcv-ns3序列及内源性蛋白靶向序列进行重组,并利用hcv-ns3蛋白酶自切割的特性药物调控内源性蛋白的降解,可为内源性蛋白降解提供一种新策略。
19、本发明通过试验确定了kferq序列置于重组多肽n-末端拥有更高的伴侣蛋白hsc70识别结合效率,为其他调控元件的插入和替换提供了一种良好的模板。
20、本发明设计的含kefrq-mhcv-ns3(kh)的药物控制降解系统可以靶向内源性和外源性蛋白质,且可以显著降低细胞内过表达的egfp及内源性akt、pakt水平,实现对胞内egfp和内源性促癌蛋白的显著降解,同时能有效抑制细胞的增殖活性,为癌症治疗提供依据。
- 还没有人留言评论。精彩留言会获得点赞!