精氨酸代谢及DNA去甲基化相关基因作为标志物及治疗靶标在肿瘤诊断及治疗中的应用
本发明涉及医药,更具体地,涉及一种精氨酸代谢及dna去甲基化相关基因作为标志物及治疗靶标在肿瘤诊断及治疗中的应用。
背景技术:
1、肿瘤相关巨噬细胞(tams)是肿瘤微环境中主要的炎症细胞,大量研究显示tams在肿瘤的免疫逃逸及复发转移等恶性进展中发挥了重要的促进作用。目前,已有研究揭示了tams促肿瘤表型产生、维持的部分分子机制,但依旧有部分分子机制未得到深入研究或阐明。其中,就包括精氨酸代谢与tams促肿瘤表型之间的关系。大量研究已表明精氨酸代谢与tams极化密切相关,但其中具体的分子机制仍不清楚。为深入了解相关机制以获取新的治疗方式,进一步探索肿瘤微环境中精氨酸代谢及其与tams促肿瘤表型之间的分子机制显得尤为重要。有利于挖掘新的相关标志物,以用于检测tams或预测乳腺癌复发转移及恶性进展的可能性,提供新的肿瘤治疗靶标。对控制肿瘤的免疫逃逸及复发转移意义重大。
2、表观遗传学改变在巨噬细胞的极化及促肿瘤表型中也发挥着重要调控作用。dna甲基化是关键的表观遗传学机制之一,作为基因表达的关键开关,广泛影响细胞的生理功能。dna甲基化水平由甲基化和去甲基化动态平衡决定,dna甲基转移酶(dnmt3a,dnmt3b和dnmt1)负责建立和维持dna甲基化。dna去甲基化有两种基本机制:依赖于dna复制的被动dna去甲基化和不依赖于dna复制的主动dna去甲基化。在被动dna去甲基化过程中,甲基化dna通过dnmt1的失活而在连续的复制周期中被稀释。在主动dna去甲基化过程中,tets将dna中的5-甲基胞嘧啶(5mc)氧化为5-羟甲基胞嘧啶(5hmc)、5-甲酰胞嘧啶(5fc)和5-羧基胞嘧啶(5cac),随后5hmc、5-fc和5cac被dna糖苷酶tdg切除,dna主动去甲基化完成。tet/tdg复合物介导的dna主动去甲基化发生在不涉及dna复制的细胞中。tams受到肿瘤微环境信号的趋化及刺激后,极化成无dna复制能力的免疫细胞。尽管表观遗传学改变已被报道在巨噬细胞极化中起重要作用,但具体到tet/tdg复合物介导的dna主动去甲基化对tams极化及促肿瘤表型的影响尚未被清晰揭示。
3、具体到,精氨酸代谢与表观遗传学改变之间是否有关联(尤其是精氨酸代谢与dna去甲基化之间的关联),以及其是否相互关联而影响tams、肿瘤进展,目前也尚未有研究揭示。精氨酸代谢通路中起关键调控作用的代谢分子尚不明确,以及精氨酸代谢物是否通过影响dna去甲基化而发挥促肿瘤作用仍缺乏研究。
4、因此,筛选精氨酸代谢通路中起关键作用的代谢物分子,并揭示相关代谢物分子是否通过影响dna去甲基化而促进tams的促肿瘤功能非常必要。
技术实现思路
1、本发明旨在克服上述现有技术的至少一种不足,提供一种精氨酸代谢及dna去甲基化相关基因作为标志物及治疗靶标在肿瘤诊断及治疗中的应用,提供肿瘤中新的标志物和治疗靶标。
2、本发明的一个目的在于提供特异性检测肿瘤细胞中精氨酸合成通路基因表达水平、肿瘤相关巨噬细胞中精氨酸代谢通路基因表达水平、精胺合成通路基因表达水平、dna主动去甲基化通路基因表达水平、基因组去甲基化水平和/或精胺水平的检测产品在制备预后乳腺肿瘤患者的产品中的用途。
3、进一步地,精氨酸合成通路基因包括精氨酸合成限速酶基因ass1;精氨酸代谢通路基因包括精氨酸代谢限速酶基因arg1;精胺合成通路基因包括鸟氨酸脱羧酶1基因odc1、亚精胺合酶基因srm以及精胺合酶基因sms;dna主动去甲基化通路基因包括糖苷酶基因tdg和10-11易位酶基因tet。
4、更进一步地,精氨酸合成限速酶ass1可作为预测乳腺癌不良预后的诊断标志物;精氨酸代谢限速酶arg1可作为预测乳腺癌不良预后的诊断标志物;糖苷酶tdg可作为预测乳腺癌不良预后的诊断标志物;该标志物的诊断方式包括:基于以上三个基因的核酸水平及蛋白水平检测,检测方法包含qpcr、fish以及western blot、ihc/if、elisa等至少其中一种。更进一步地,精氨酸代谢物精胺可作为预测乳腺癌不良预后的诊断标志物。巨噬细胞基因组去甲基化水平增加可作为预测乳腺癌不良预后的诊断标志物,且检测方式可基于差异甲基化杂交(dmh)dna甲基化芯片技术。
5、在本发明的一个以上实施例中,发现前述通路基因表达水平与肿瘤相关巨噬细胞以及乳腺癌不良预后相关,其中通路基因可作为代表相应的标志物,通过检测标志物水平,有利于确认和诊断对应的细胞状态以及肿瘤进展、预后。具体地,分别利用western及免疫组化检测肿瘤细胞、tams体外模型细胞以及乳腺肿瘤组织中ass1、arg1及tdg的蛋白表达水平,western结果显示ass1在肿瘤细胞中高表达,arg1在tams中高表达;免疫组化结果显示ass1、arg1及tdg转移性乳腺癌患者组织高表达。利用网络已发表临床数据统计发现,ass1、arg1及tdg的高表达和乳腺癌不良预后显著相关。
6、提供多种用于预测乳腺癌恶性进展的诊断标志物,所述标志物为精氨酸合成限速酶ass1、精氨酸酶arg1、糖苷酶tdg、精氨酸代谢物精胺或肿瘤相关巨噬细胞基因组dna甲基化水平。其中肿瘤细胞中ass1升高、肿瘤相关巨噬细胞中arg1或tdg高表达或精胺水平升高或肿瘤相关巨噬细胞基因组dna甲基化水平降低可作为独立因素预测乳腺癌不良预后。
7、进一步地,检测产品通过qpcr、fish、western blot、ihc/if和/或elisa方式特异性检测基因的表达水平;和/或,检测产品通过差异甲基化杂交(dmh)dna甲基化芯片技术特异性检测基因组去甲基化水平。更进一步地,检测试剂特异性检测肿瘤细胞中精氨酸合成通路基因、肿瘤相关巨噬细胞中精氨酸代谢通路基因和dna主动去甲基化通路基因表达水平,且精氨酸合成通路基因包括ass1、精氨酸代谢通路基因包括arg1、dna主动去甲基化通路基因包括tdg。
8、前述标志物的检测方法包括基因的核酸水平及蛋白水平检测,检测方法包含qpcr、fish以及western blot、ihc/if、elisa等至少其中一种;精氨酸代谢物检测方法主要指基于质谱的代谢物检测方式;dna甲基化水平检测主要指基于差异甲基化杂交(dmh)的dna甲基化芯片技术。
9、本发明的再一目的在于提供肿瘤细胞精氨酸合成抑制剂、肿瘤相关巨噬细胞精氨酸代谢抑制剂、精胺合成抑制剂、精胺抑制剂和/或dna主动去甲基化抑制剂在制备抑制肿瘤相关巨噬细胞促肿瘤表型、减少肿瘤相关巨噬细胞免疫抑制性炎症因子和/或治疗肿瘤的药物中的用途。进一步地,肿瘤包括乳腺癌。
10、进一步地,肿瘤细胞精氨酸合成抑制剂靶向精氨酸合成通路基因及基因对应蛋白中间体、蛋白;其中,精氨酸合成通路基因包括精氨酸合成限速酶基因ass1;肿瘤相关巨噬细胞精氨酸代谢抑制剂靶向精氨酸代谢通路基因及基因对应蛋白中间体、蛋白;其中,精氨酸代谢通路基因包括精氨酸代谢限速酶基因arg1;精胺合成抑制剂靶向精胺合成通路基因及基因对应蛋白中间体、蛋白;其中,精胺合成通路基因包括鸟氨酸脱羧酶1基因odc1、亚精胺合酶基因srm以及精胺合酶基因sms;dna主动去甲基化抑制剂靶向dna主动去甲基化通路基因及基因对应蛋白中间体、蛋白;其中,dna主动去甲基化通路基因包括糖苷酶基因tdg和10-11易位酶基因tet。
11、在本发明的一个以上实施例中,发现肿瘤细胞来源的精氨酸可促进tams极化,体内外研究发现通过抑制肿瘤细胞精氨酸合成限速酶ass1抑制肿瘤细胞精氨酸合成后,可显著抑制tams的促肿瘤表型。
12、机制研究发现,精氨酸代谢产物精胺(spermine)是维持tams促肿瘤表型的关键代谢物分子,且精胺可通过上调dna去甲基化关键基因糖苷酶tdg促进tams主动去甲基化的发生,进而维持tams的促肿瘤表型。通过抑制精氨酸代谢通路相关基因arg1以及odc1等基因功能抑制精胺合成或通过抑制dna主动去甲基化关键基因tet及tdg功能后,可显著抑制tams的促肿瘤表型。
13、进一步地,肿瘤细胞精氨酸合成抑制剂、肿瘤相关巨噬细胞精氨酸代谢抑制剂、精胺合成抑制剂和/或dna主动去甲基化抑制剂包括小分子干扰rna;肿瘤细胞精氨酸合成抑制剂、肿瘤相关巨噬细胞精氨酸代谢抑制剂、精胺合成抑制剂、精胺抑制剂和/或dna主动去甲基化抑制剂包括阻断对应通路功能的结合抗体。
14、本发明提供了多种可用于设计生产抗肿瘤药物的靶标,所述靶标包括ass1、arg1、odc1、tets及tdg等;所述药物包括以上基因的sirna、抑制以上基因表达的小分子化合物、结合以上蛋白抑制其功能的小分子抑制剂或结合抗体等可以抑制基因功能的物质中的至少一种。在本技术的一个以上实施例中,通过ass1、arg1、tdg对应的sirna沉默、敲低对应的基因表达。其中,至少包括ass1 sirna:5’-gcctgaattctacaaccggtt-3’;arg1 sirna:5’-gggcggagaccacaguuug-3’;tdg sirna:5’-cuccaguaaagaauuucgutt-3’。
15、进一步地,肿瘤细胞精氨酸合成抑制剂包括ass1抑制剂;巨噬细胞精氨酸代谢抑制剂包括arg1抑制剂、dfmo抑制剂;精胺合成抑制剂包括arg1抑制剂;dna主动去甲基化抑制剂包括tdg抑制剂。进一步地,ass1抑制剂包括ass1 sirna;tdg抑制剂包括tdg sirna;arg1抑制剂包括arg1 sirna。
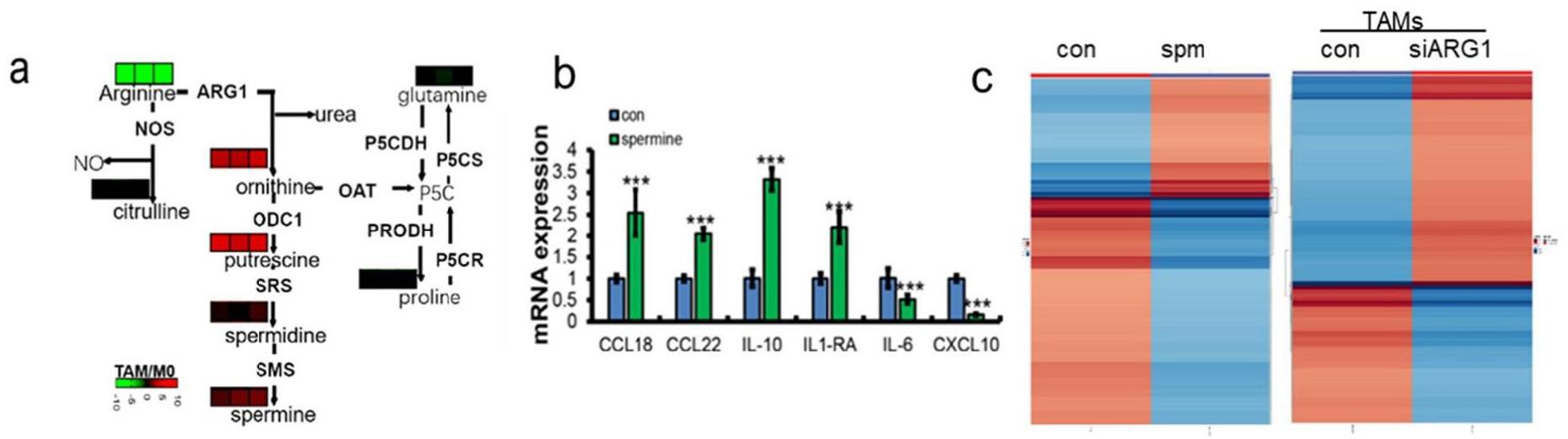
16、在本发明的一个以上实施例中,发明人利用dna甲基化芯片技术检测了肿瘤相关巨噬细胞dna甲基化状态改变、精氨酸代谢物精胺对dna甲基化状态影响以及抑制arg1介导的精氨酸代谢后dna甲基化状态的改变,结果表明肿瘤相关巨噬细胞极化后更多的基因发生了去甲基化,精氨酸代谢物精胺处理巨噬细胞直接导致dna去甲基化水平增加,利用sirna干扰arg1表达抑制精氨酸代谢后,tams去甲基化状态被显著抑制。
17、具体操作中,包括利用rna干扰技术抑制肿瘤细胞中ass1的表达,ass1表达降低直接导致发现肿瘤细胞分泌的精氨酸水平降低,与未敲除ass1肿瘤细胞培养上清相比,ass1敲低的肿瘤细胞培养上清刺激的巨噬细胞,其促肿瘤表型比如炎症抑制因子的表达、m2型表面标志物显著被抑制,而在补充足量精氨酸后,敲除ass1导致的抑制效果可部分被恢复。
18、本发明人还利用乳腺癌细胞系mda-mb-231构建了敲低ass1表达的稳转株细胞,将对照细胞与敲低了ass1的稳转株细胞皮下植入重度免疫缺陷小鼠,通过鼠尾静脉给与人源pbmc细胞。结果显示,无论低精氨酸喂食或正常精氨酸水平喂食,敲低ass1组小鼠移植瘤体积及重量明显低于对照组小鼠。利用免疫组化技术分析移植瘤标本发现,敲低ass1组肿瘤组织中浸润的cd163及精氨酸代谢限速酶arg1阳性免疫抑制型巨噬细胞明显减少。这说明肿瘤细胞来源的精氨酸通过维持巨噬细胞arg1介导的精氨酸代谢促进肿瘤相关巨噬细胞的促肿瘤作用。
19、在肿瘤相关巨噬细胞体外模型中分别利用arg1 sirna及arg1介导的精氨酸代谢通路抑制剂dfmo抑制多胺合成后,肿瘤相关巨噬细胞炎症抑制因子的表达被显著抑制,抑制精氨酸代谢后的巨噬细胞对t细胞的激活抑制程度显著降低。
20、在肿瘤相关巨噬细胞体外模型中分别利用tdg sirna降低tdg的表达以及利用dna去甲基化抑制剂bcat抑制肿瘤相关巨噬细胞去甲基化后,肿瘤相关巨噬细胞炎症抑制因子的表达被显著抑制,抑制dna去甲基化后的巨噬细胞对t细胞的激活抑制程度显著降低。
21、发明人还将未处理人外周血巨噬细胞以及分别敲低了arg1或tdg表达的巨噬细胞与乳腺肿瘤细胞系mda-mb-231经皮下共注射入重度免疫缺陷小鼠,后续分别分成两组,其中一组给予每周两次的精胺腹腔注射。结果显示,精胺单独处理组小鼠乳腺细胞移植瘤体积及质量明显高于对照组,敲低arg1或tdg组小鼠移植瘤体积及重量明显低于对照组小鼠,给与精胺处理的arg1敲低组小鼠移植瘤体积及重量有明显恢复,而精胺处理的tdg敲低组小鼠移植瘤体积及重量却未有明显改变。利用免疫组化技术分析移植瘤标本发现,敲低arg1或tdg组肿瘤组织中浸润的cd163阳性免疫抑制型巨噬细胞明显减少及浸润cd3阳性的t淋巴细胞显著增加。这说明精氨酸代谢产物精胺通过上调tdg促进巨噬细胞去甲基化进而促进肿瘤相关巨噬细胞的促肿瘤作用。
22、本发明的再一目的在于提供精胺在制备上调基因tdg表达水平、增强dna去甲基化的药物中的用途。进一步地,在制备上调肿瘤相关巨噬细胞中基因tdg表达水平、增强肿瘤相关巨噬细胞中dna去甲基化的药物中的用途。在本发明的一个以上实施例中发现,精胺上调肿瘤相关巨噬细胞基因tdg表达水平,进而增强其基因组dna去甲基化。
23、本发明的再一目的在于提供一种cd163阳性巨噬细胞标志物,包括表达水平特异性上调的arg1和/或表达水平特异性下调的ass1。在本发明的一个以上实施例中发现,在乳腺肿瘤组织中,精氨酸代谢关键酶arg1特异性的在cd163阳性的巨噬细胞表达;精氨酸合成限速酶ass1在cd163阳性的巨噬细胞中表达极低。
24、本发明的再一目的在于提供一种肿瘤相关巨噬细胞标志物,包括:
25、特异性下调的精氨酸和特异性上调的鸟氨酸;
26、激活的精氨酸代谢;
27、基因组甲基化水平、基因组去甲基化水平或基因组基因甲基化比例;
28、和/或,特异性上调的精胺。
29、在本发明的一个以上实施例中,发现肿瘤相关巨噬细胞中特异性的精氨酸下调、鸟氨酸上调;且arg1介导的精氨酸被激活;基因组dna去甲基化增强;精胺水平增多。
30、与现有技术相比,本发明的有益效果为:发现了肿瘤细胞来源精氨酸与肿瘤相关巨噬细胞精氨酸代谢、dna去甲基化之间的关系,不仅提供了多个与肿瘤预后、肿瘤相关细胞巨噬细胞相关的标志物,更基于该类标志物提供了治疗靶点。在本发明的一个以上实施例中,通过抑制精氨酸至dna去甲基化中的相关通路,发现能有效抑制肿瘤相关巨噬细胞的促肿瘤表型,并能有效减小肿瘤体积,起到治疗作用。为包括乳腺癌在内的肿瘤提供新的预后标志物和治疗策略。更为具体地,涉及精氨酸代谢相关基因ass1、arg1、糖苷酶tdg以及精氨酸代谢产物精胺作为标志物诊断肿瘤不良进展以及在筛选和/或制备用于治疗和/或诊断肿瘤不良进展的药物中的用途。其中,本发明所述的基因ass1在肿瘤细胞中特异性高表达,arg1及tdg在肿瘤相关巨噬细胞中特异性高表达,精胺在巨噬细胞中特异性升高,以上四个因素可独立预测肿瘤的不良预后;抑制肿瘤细胞ass1或抑制肿瘤相关巨噬细胞arg1或tdg的表达或抑制巨噬细胞精胺合成后,均可显著抑制肿瘤细胞的增殖。通过不同方式抑制ass1、tdg的表达或功能,以及抑制精胺合成可作为恶性肿瘤治疗的有效策略。
- 还没有人留言评论。精彩留言会获得点赞!