一种生物气溶胶发生用标准物质及其制备方法与定值方法与流程
本发明涉及一种生物气溶胶发生用标准物质及其制备方法与定值方法。
背景技术:
1、近些年,关于气溶胶感染的报道屡见不鲜,通过气溶胶传播的细菌包括鼠疫、炭疽等致病微生物,其致死率高,对社会危害极大。同时,气溶胶监测的技术发展迅猛,各种气溶胶监测的设备层出不穷,如何评价其监测的有效性,成为亟待解决的问题。气溶胶模拟试验是目前公认的可以用来测试仪器的性能,验证消毒剂及器械的消杀效率和质量的方法。根据卫生部制定的消毒技术规范,用于消毒及灭菌的器械都需要进行模拟试验。将标准物质菌均匀分散到实验舱里,用采样设备采样记录生长菌落数,进行试验对照。3次同条件试验结果的杀灭率≥99.90%,可认为消杀合格。
2、病原微生物感染严重威胁人类健康。微生物标准物质的研究与研制较少,此类标准物质匮乏。直至2018年国家标准物质库才出现了细菌相关的一级标准物质。近几年对于食品安全领域的常见食品微生物研究和研制较多,例如单核细胞增生李斯特氏菌、金黄色葡萄球菌、大肠杆菌、沙门氏菌等。
3、对于气溶胶模拟实验相关的标准物质研究较少。现在常用的气溶胶发生物质为粉尘、聚苯乙烯微球等模拟微生物的粒径,却不具有微生物真正的生物活性,从而使得其结果与真实的微生物气溶胶发生不同,并且不能通过监测生物荧光本底来进行定量。
4、冷冻干燥法是长期稳定保存微生物菌株的有效方法之一,针对各类菌株的生存条件差异,冻干保护剂不尽相同。糖类(蔗糖、海藻糖、乳糖)、氨基酸类、脱脂乳、明胶等是用的比较多的冻干保护剂成分。已有对于冻干保护剂的研究中,其与细菌混合后保存时间可以达到6个月,12个月甚至18个月,细菌存活率基本可维持在70%以上,甚至可以达到90%以上。
5、针对实验室安全保障和仪器效率类的细菌标准物质研究较少且售卖有限,为满足实验室检测需要,研制稳定性良好的细菌标准物质是有必要的。
技术实现思路
1、本发明的目的是提供一种生物气溶胶发生用标准物质及其制备方法与定值方法。本发明标准物质具有良好的均匀性,复水性和稳定性,标准物质可用于空气微生物监测的各种模拟气溶胶实验,其中活菌定值和总菌的定值可用于微生物采样器的微生物存活率的计算;颗粒总量定值可用于微生物采样器的采样效率计算。
2、本发明提供了一种生物气溶胶发生用标准物质,包括细菌菌体和菌体冻干保护剂的冻干物;
3、所述菌体冻干保护剂的冻干物包括蔗糖、谷氨酸钠、peg8000和pvp。
4、本发明所述生物气溶胶发生用标准物质具有生物活性与颗粒特性,用于活体细菌定值、总菌定值或总颗粒定值。
5、上述的标准物质中,所述细菌菌体选自革兰氏阳性菌、革兰氏阳性菌芽孢、革兰氏阴性菌中的至少一种。
6、上述的标准物质中,所述革兰氏阳性菌选自白色葡萄球菌;
7、所述革兰氏阳性菌芽孢选自萎缩芽胞杆菌;
8、所述革兰氏阴性菌选自大肠埃希氏菌或粘质沙雷氏菌;
9、上述的标准物质中,所述细菌标准物质由纯水复水后,菌液浓度不低于1×108cfu/ml;
10、所述标准物质还包括磷酸盐缓冲液,用于将所述菌体冻干保护剂的冻干物溶解为所述菌体冻干保护剂。
11、上述的标准物质中,所述冻干物优选为饼状或球状。
12、上述的标准物质中,所述菌体冻干保护剂包括如下质量份的组份:
13、蔗糖1~4份;谷氨酸钠1~10份;peg8000 1~3份;pvp 0.5~1份;溶剂为磷酸盐缓冲液。
14、本发明还提供了一种上述的标准物质的制备方法,包括如下步骤:1)用无菌生理盐水将所述细菌菌体稀释到109级,成菌悬液状;
15、所述菌体冻干保护剂的冻干物用磷酸盐缓冲液溶解成所述菌体冻干保护剂;
16、2)所述菌悬液状与所述菌体冻干保护剂进行混合,然后在-80~-60℃预冻4h~8h后冻干,即得到所述标准物质。
17、上述的制备方法中,步骤1)中,所述生理盐水的质量百分浓度为0.85%;
18、步骤2)中,所述菌悬液状与所述冻干保护剂溶液混合的体积比可为1:10~20。
19、上述的制备方法中,步骤2)中,所述冻干的条件如下:冷阱-50℃,冻干温度-40℃,隔板最终温度25℃,冻干压力0.037mbar。
20、上述的制备方法中,当所述细菌菌体选自革兰氏阳性菌或革兰氏阴性菌时,培养方法如下:挑取单克隆菌落于灭菌的lb培养基中,培养方案是37±1℃下,1200rpm摇床培养12h;
21、当所述细菌菌体为选自革兰氏阳性菌芽孢,所述芽孢的培养方法如下:将液体菌液接种到罗氏瓶固体培养基中培养芽孢,选择芽孢培养基为胰蛋白胨、酵母粉、nacl、kcl、mgso4、ca(no3)、mncl2、feso4、琼脂粉,培养7~10天,然后染色,显微镜观察芽孢比例大于90%时用l棒刮取菌液收集,收集菌落用0.85%生理盐水保存。
22、本发明中,制备得到标准物质于-20℃保存,稳定性大于6个月。
23、本发明进一步提供了一种上述的标准物质的定值方法,
24、当用于活体细菌定值时,包括如下(1)-(3)的步骤:
25、(1)用纯水复水溶解所述气溶胶发生用标准物质,复水后充分混匀定为s0溶液;
26、(2)用0.85%的生理盐水对所述s0溶液进行10倍列稀释,根据估算浓度选取三个稀释度在lb培养基的平板中进行平板涂布,涂布后静置10min,然后放于37℃±2℃培养12h以上;
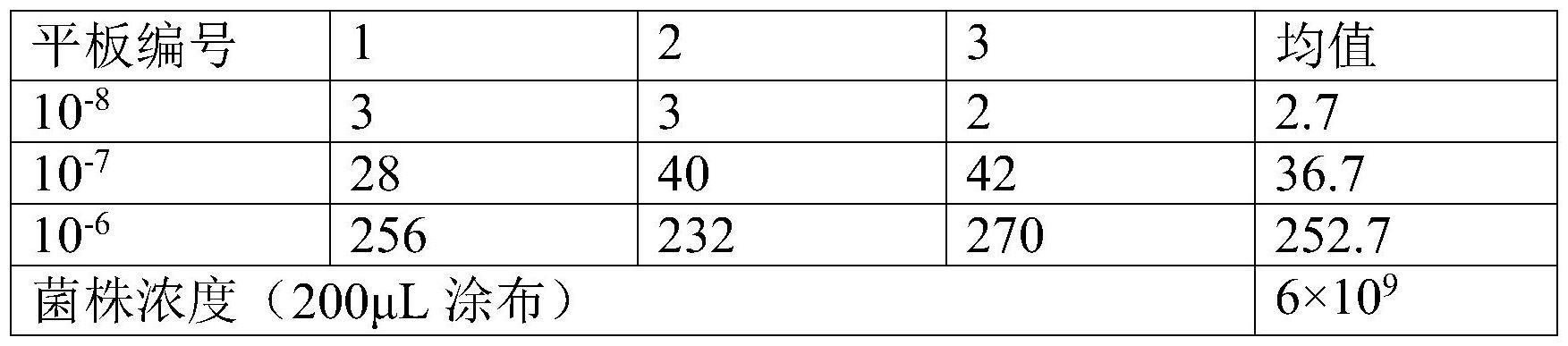
27、(3)选择步骤(2)中菌落数在3cfu~300cfu之间的平板,菌落计数以菌落形成单位cfu表示,实验结果以活菌浓度表示,计数该稀释度平板上的典型菌落,按照如下式ⅰ计算标准值,即为所述活体细菌的定值;活体菌定值结果表示为:所述活体细菌标准值±拓展不确定度;
28、式ⅰ:
29、式ⅰ中,
30、c为菌落浓度,cfu/ml;
31、n为平板上典型菌落的总数,cfu;
32、d为稀释因子,无量纲;
33、v为平板上菌液接种体积,单位ml;
34、当用于总菌定值时,包括如下(4)-(6)的步骤:
35、(4)用纯水复水溶解所述气溶胶发生用标准物质,复水后充分混匀定为s0溶液;
36、(5)通过核酸取试剂盒提取s0溶液的总核酸;
37、(6)通过微量分光光度计测量所述总核酸浓度,即为所述总菌的定值;所述总菌定值结果表示为:总菌标准值±拓展不确定度;
38、当用于总颗粒定值时,包括如下(7)-(8)的步骤:
39、(7)用纯水复水溶解所述气溶胶发生用标准物质,复水后充分混匀定为s0溶液;
40、(8)将上述溶液通过库尔特计数仪,得到总颗粒浓度,即为所述总颗粒的定值;所述总颗粒的定值结果表示为:总颗粒标准值±拓展不确定度。
41、本发明中,所述拓展不确定度的来源如下:a类不确定度主要为不同管间批件差引入的误差以及平板计数产生的随机误差;b类不确定度为仪器设备带来的不确定度,包括移液器、库尔特计数器、微量分光光度计;其计算方法按照本领域技术人员公知的方法即可。
42、本发明中,所述冻干保护剂用磷酸盐缓冲液溶解;且所述冻干保护剂和所述磷酸盐缓冲液均需要灭菌;灭菌方法为过滤除菌或高压灭菌;具体可:冷冻干燥保护剂经0.22μm滤膜过滤除菌,磷酸盐缓冲液采用高温高压灭菌121℃,20min。
43、冻干前活菌液浓度按照平板计数法进行计数,浓度为c1,取3份冻干后标准物质,复水后,每份体积同样200μl,采用相同平板涂布法测定其活菌浓度c2。冻干存活率(freeze-drying viability,fdv)计算公式如式ii所示:
44、式ⅱ:
45、式ⅱ中,
46、fdv1为冻干存活率;
47、c1冻干前细菌活菌浓度;
48、c2冻干后细菌活菌浓度。
49、总菌用总核酸浓度表示,用柱提法提取总核酸,然后用微量分光光度计测量其核酸总量,冻干前总菌核酸浓度为c3;冻干后总菌核酸浓度为c4;冻干总菌留存率计算公式如式ⅲ所示:
50、式ⅲ:
51、式ⅲ中,
52、fdv2为冻干总菌留存率;
53、c3冻干前细菌活菌浓度;
54、c4冻干后细菌活菌浓度。
55、用库尔特计数器测量菌液总颗粒浓度,冻干前总颗粒浓度为c5,冻干后总颗粒数为c6;冻干总颗粒维持率计算公式如式ⅳ所示:
56、式ⅳ:
57、式ⅳ中,
58、fdv3为冻干总菌维持率;
59、c5冻干前总颗粒浓度;
60、c6冻干后总颗粒浓度。
61、本发明具有以下有益效果:
62、1、本发明所有冻干保护剂配方不含产生生物荧光本底的物质,为了避免通过光学方法监测生物荧光变化预警微生物浓度的设备,其评价受到冻干配方中生物荧光物质的干扰,从而无法进行评价和准确定量。
63、2、通过优化冻干保护剂各组分比例可以有效降低菌体在冷冻干燥过程中的总核酸、总颗粒、和细菌死亡的比率。
64、3、冻干后的标准物质纯水即可复水,并且复水后菌液均匀,无结块等,具有良好的稳定性。
65、4、本标准物质使用的操作简单,只需按照说明书加入纯水,即可得到所需浓度的微生物。
66、5、本标准物质可以用于生物气溶胶发生的指示微生物。
67、6、本发明标准物质的定值采用三参数定值,适用于不少于三种气溶胶发生应用场景,结果准确。
- 还没有人留言评论。精彩留言会获得点赞!