马兜铃酸D的对照品的制备方法与流程
本发明涉及一种马兜铃酸d的制备方法,尤其涉及能够制备可以用于适用于工业化的马兜铃酸d的固体对照品的制备方法。
背景技术:
1、马兜铃酸类成分是一类硝基菲类羧酸,具有肾脏毒性和致癌性。已报道的大量马兜铃酸肾病病例中,有些马兜铃酸肾病患者后续发生尿路上皮癌和膀胱癌。泌尿系统致癌性的发现使马兜铃酸被列为ⅰ类致癌物。马兜铃酸类成分是一类植物次生代谢产物,广泛存在于马兜铃科植物中。马兜铃科植物共有500多种,在亚洲地区被作为传统药物用于治疗多种疾病。中国地区的马兜铃科植物主要有4属共70余种,其中大多数是药用植物,常作为中药材配伍使用,具有止咳平喘、祛风止痛和清热活血等功效。现在存于2020版药典中的马兜铃科植物仅有细辛一种,细辛临床应用广泛,主要用于治疗过敏性哮喘、鼻炎、咳嗽以及新型冠状病毒感染等症。除了入汤剂外,大量的中成药制剂中亦含有细辛。《中国药典》收载有50种含细辛品种。很多品种极为常用,如小青龙颗粒、儿童清肺口服液、小儿咳喘颗粒、痧气体丸、鼻渊舒口服液、小儿肺闭宁片、辛芩颗粒、九味羌活片、川芎茶调片、鼻炎片、胃炎宁冲剂、人参再造丸、正天丸、杜仲壮骨丸等,其中不乏儿童常用药。在含马兜铃、土木香、木通、防己、寻骨风等药材的中成药中均检测到了马兜铃酸成份。为了避免药物中的马兜铃酸类成分在实际应用中带来的毒性伤害,对马兜铃酸毒性进行早期诊断,对于其安全性监测极为重要。
2、常见的马兜铃酸类成分有马兜铃酸a、马兜铃酸b、马兜铃酸c、马兜铃酸d。目前国内外马兜铃酸a、马兜铃酸b、马兜铃酸c的相关研究很多,马兜铃酸d的研究报道很少,市场上也很少有现成的马兜铃酸d供应。然而,马兜铃酸d(aristolochic acid d)已经被列为《中华人民共和国药典》规定的毒性药材指标成分,其重要程度不容忽视。
3、
4、马兜铃酸d,分子式:c17h11no8
5、由于马兜铃酸d已被药典列为药典毒性指标成分,所以分离得到马兜铃酸d标准品能够极大的提高相关药材质量控制水平,显得十分必要,具有极高应用价值。
6、马兜铃酸d检测方面的专利文献较多,但是大量提取工艺方面的文献很少,大部分都是分离马兜铃酸d类似物。有文献报导通过醇提-碱溶酸沉-大孔树脂纯化-高压制备的方法,从关木通中分离获得马兜铃酸ⅰ和ii,纯度分别为96%和94.45%,没有得率数据。还有文献报导将马兜铃药材进行醇提,醇提物与硅胶拌样,烘干后依次用石油醚,氯仿,乙醇索氏提取,氯仿提取物经硅胶柱层析,重结晶获得马兜铃酸,从其它溶剂提取物中分离获得另外2中马兜铃酸类似物,未做结构鉴定,也没有纯度和得率数据。还有文献报导,通过醇提-浓缩析出-沉淀经酒精多次洗涤-硅胶柱层析-重结晶的方法,从朱砂莲中分离获得马兜铃酸,得率0.45%,没有纯度数据。
7、专利文献
8、[1]一种细辛中6种马兜铃酸类成分的含量测定方法cn113252810 a
9、非专利文献
10、[1]屈碧琼,刘洁,阳娇,杨晓芹,潘绮雪,刘明妍,刘璐璐,肖红斌.马兜铃酸ⅰ,ii的制备工艺研究[j].华西药学杂志,2022,37(3):245-248.
11、[2]李舒养,姚琪.广西马兜中马兜铃酸的分离与鉴定[j].中国药学杂质,1981,(02):15-18.
12、[3]邱运平,陈秀珍,全德健,文玲芳,巫燕妹.朱砂莲化学成分的研究ⅰ,马兜铃酸的分离[j].广西植物,1980,(01):24-27.
13、现状是植物来源的马兜铃酸d的植物来源的提取分离困难,没有现成的工艺,其总含量低,难以从混合物中结晶出来,因此已经公开的马兜铃酸d的现有提取制备方法非常有限,目前尚无高效的相关的马兜铃酸d工业化提取制备方法。作为一种重要的特征性成分,迫切需要研发一种高通量、能提供高纯度的纯度马兜铃酸d,且适合大量制备的马兜铃酸d对照品制备方法。
技术实现思路
1、本发明的目的在于提供一种高通量、能提供高纯度的纯度马兜铃酸d,且适合大量制备的马兜铃酸d对照品制备方法。本发明中,马兜铃酸d有时也称为分离目标物。本发明对马兜铃酸d的分离纯化做了很大的改进,引入了独特的ph调节手段,使整个提取方法适合于天仙藤药材化学成分的提取,再经过深入探索,找到了成本可控的提取分离手段,实现可以工业化的目标化合物提纯方法,在化合物的量和纯度上有了很大的提高,从而完成了本发明。
2、本发明通过简单高效的操作流程,能够分离得到纯度很高的马兜铃酸d。
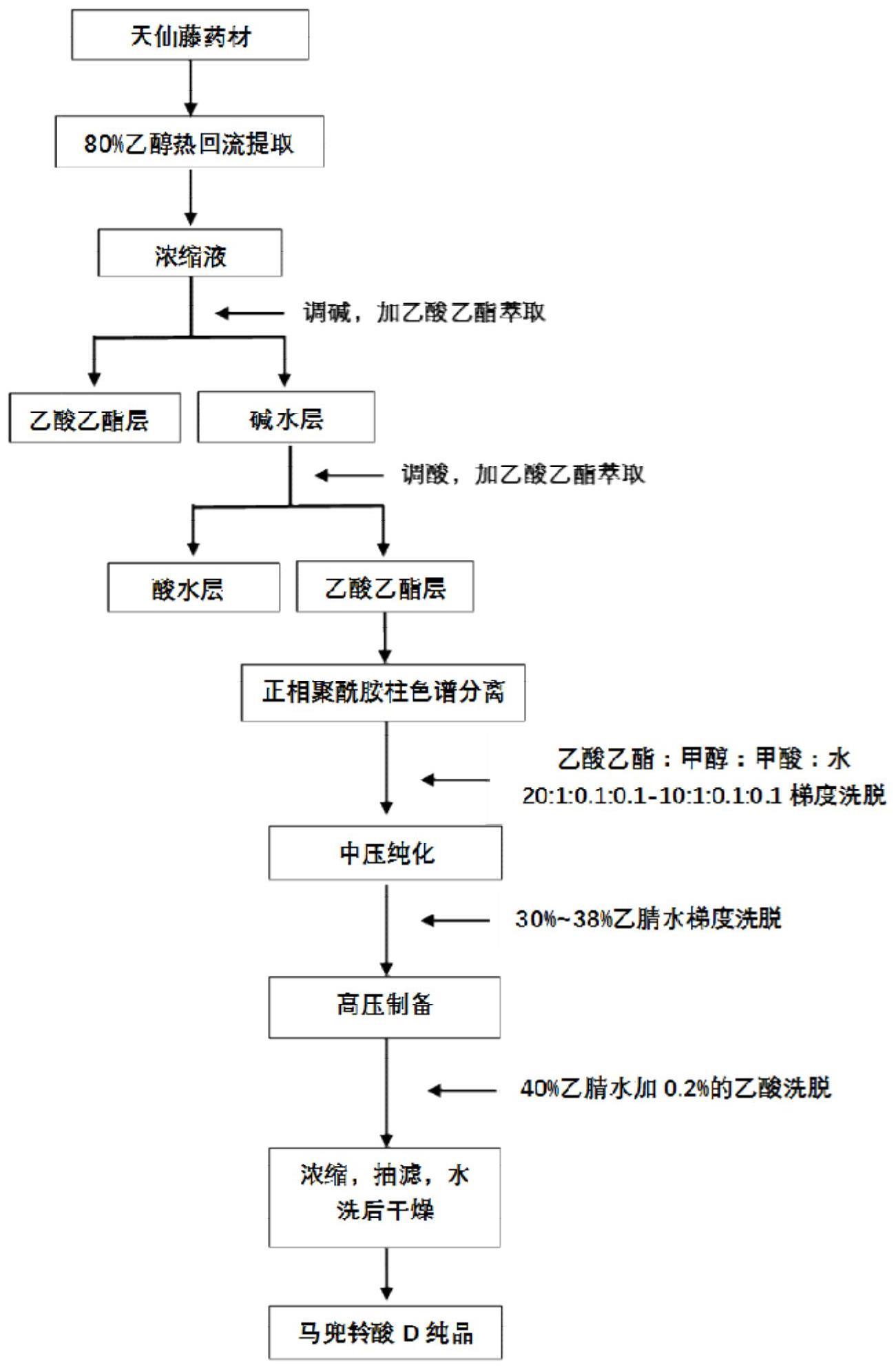
3、本发明的制备分离方法依次包括以下步骤:
4、酸碱处理工序,将天仙藤药材总提取物粉末或浸膏,以3~7倍重量的ph值8~9的碱化的水溶液混悬,静置0.5~1.5小时后,以再以0.8~4倍体积的有机溶剂萃取,回收水相,加入酸性水溶液,调节ph至3~4,用0.8~4倍体积的体积有机溶剂萃取,回收有机相,浓缩得到天仙藤总提取物ii,
5、聚酰胺纯化工序,将天仙藤总提取物ii上样于100~200目聚酰胺柱层析,以乙酸乙酯:甲醇=20:1~10:1洗脱液逐渐增加极性进行洗脱,根据tlc或者hplc检测收集洗脱液,将洗脱液浓缩、干燥,天仙藤粗提物i,其中,甲醇中含有8体积%~12体积%的甲酸以及8体积%~12体积%的水;
6、反相色谱纯化工序:天仙藤粗提物i上样至反相色谱柱,用乙腈水溶液或甲醇水溶液的混合洗脱剂,其中,乙腈或甲醇:水的比例以体积比计为0.4~0.7:1,根据tlc或者hplc检测收集洗脱液,将洗脱液在50℃以下的温度减压浓缩,干燥得到马兜铃酸d的粗品ii溶液,乙腈水溶液或甲醇水溶液的混合洗脱剂中可选地含有0.1%~0.3%乙酸;
7、溶剂处理工序,将反相色谱纯化工序中所得到马兜铃酸d的粗品ii溶液在50℃以下的温度浓缩,得到析出物,淋洗,干燥之后获得马兜铃酸d的对照品。
8、溶剂处理工序所得的马兜铃酸d的对照品,可以利用重结晶方法进行纯化,优选重复进行2次以上重结晶,例如在本发明优选的实施方式中,将反相色谱纯化工序中所得到马兜铃酸d粗品ii用醇系溶剂溶解,于-30℃~0℃结晶,过滤获得结晶,再进行2次以上重结晶。
9、在本发明优选的实施方式中,所述天仙藤药材总提取物溶液的制备方法如下,将天仙藤药材粉碎,加入5~20倍重量的醇系水溶液,室温浸泡或者热回流提取10~60小时,过滤,浓缩,得天仙藤药材总提取物溶液。
10、在本发明优选的实施方式中,反相色谱纯化工序可先进行中低压反相色谱纯化工序,再进行高压反相色谱纯化工序,其中例如,中低压反相色谱纯化工序:将天仙藤粗提物i上样至反相色谱柱,用乙腈水溶液或甲醇水溶液的混合洗脱剂,以0.5~1mpa压力进行洗脱,其中,乙腈或甲醇:水的比例以体积比计为0.4~0.6:1,根据tlc或者hplc检测收集洗脱液,将洗脱液在50℃以下的温度减压浓缩,去除其中的乙腈或甲醇,得到含有马兜铃酸d的粗品ii-1;高压反相色谱纯化工序:将马兜铃酸d的粗品ii-1上样至反相色谱柱,用可选地含有0.1%~0.3%乙酸的乙腈水溶液或甲醇水溶液的混合洗脱剂,以1~15mpa压力进行洗脱,其中,乙腈或甲醇:水的比例以体积比计为0.4~0.67:1,,根据tlc或者hplc检测收集洗脱液,得到马兜铃酸d的粗品ii溶液。
11、需要说明的是,中低压、高压并非基于本领域严格的定义,本发明中的中低压色谱只要没有特殊限定,都按照上述表述,代表0.5~1mpa的压力的色谱,高于1mpa的色谱,在本发明中称为高压色谱。
12、在本发明优选的实施方式中,醇系溶剂例如优选甲醇、乙醇、正丁醇等,醇系的水溶液为60%~90%的甲醇水溶液或者60%~90%的乙醇水溶液。
13、在本发明优选的实施方式中,反相色谱纯化工序中,以压力为0.1~0.3mpa进行洗脱,采用乙腈和水的混合液进行洗脱,选用40~60μm的十八烷基硅烷键合硅胶填料;在高压反相色谱纯化工序中,反相色谱柱的填料为粒径为5-10μm的十八烷基硅烷键合硅胶,使用乙腈:水洗脱液,溶液的比例以体积比计为0.5~0.7:1的洗脱剂进行洗脱。
14、在本发明优选的实施方式中,酸碱处理工序,酸化水溶液为8wt%~10wt%的盐酸,碱性溶液为碳酸氢钠溶液。
15、在本发明优选的实施方式中,酸碱处理工序中,用于萃取的有机溶剂为选自卤代烃溶剂、酯类溶剂中的一种,卤代烃溶剂选自二氯甲烷、三氯甲烷、四氯化碳、1,1-二氯乙烷、1,2-二氯乙烷、1,1,1-三氯乙烷、1,1,2-三氯乙烷、1,1,1,2-四氯乙烷、1,1,2,2-四氯乙烷、五氯乙烷、1,1-二氯乙烯、1,2-二氯乙烯、三氯乙烯及四氯乙烯中的一种或多种的组合,酯类溶剂为选自乙酸甲酯、乙酸乙酯、乙酸苯酯、苯甲酸甲酯、乙酸丁酯、丙烯酸辛酯中的一种或多种的组合。
16、本发明还提供一种纯度为99.5%以上的马兜铃酸d的固体对照品,其通过本发明的制备方法制备得到,本发明的方法制备的对照品hplc纯度高,成本优势明显。
17、本发明具有以下特点:
18、1.本发明操作简单高效,能够进行工艺放大,分离得到大量马兜铃酸d单体;
19、2.本发明经过生产实践从500kg天仙藤药材中分离获得60g马兜铃酸d,纯度99.8%,得率0.012%,纯度相对文献有了很大的提升,可作为对照品供检测使用,在文献专利报导中尚属首次。本发明分离到获得60g马兜铃酸d,根据需求,还可以放大至百克级,因此在针对制备方法、通量上都有较大改进。
20、3.酸碱处理组合结合聚酰胺,实现了大量目标物的快速富集,增加了最终的回收率。
- 还没有人留言评论。精彩留言会获得点赞!