基于微滴式数字PCR的大别班达病毒定量检测引物探针组合物及其应用
本发明属于病毒分子检测,具体涉及一种基于微滴式数字pcr的大别班达病毒定量检测引物探针组合物及其应用。
背景技术:
1、大别班达病毒(dabie bandavirus,dbv)属于布尼亚病毒目、白蛉纤细病毒科、班达病毒属,是一种具有包膜的单股负链rna病毒。病毒形态呈球形,由密集的二十面体糖蛋白gn/gc阵列覆盖,其基因组是分节段的,由大(l)、中(m)、小(s)三条片段组成。dbv感染后易引起发热伴血小板减少综合征(severe fever with thrombocytopenia syndrome,sfts),主要临床表现为高热和血小板减少,病死率高达10%-30%。近年来该病发病率逐年上升,地域分布广泛,人群对本病普遍易感。由于其高致死率和引起大流行传播的可能性,sfts已被who列为优先关注的十大突发传染病之一。
2、病毒血症是sfts发病最为显著的临床症状,大别班达病毒一旦侵入机体能迅速繁殖并随着血液循环扩散到各个器官。高病毒血症患者的病情可迅速发展为重型或危重型,造成因多脏器功能衰竭而死亡的结局。由于目前尚无治疗sfts的特效药物,提高重型或危重症患者的早期精准识别,并给予积极干预是该病救治的关键因素之一。此外,sfts属于自然疫源性疾病,病毒在蜱虫等媒介中的载量通常较低、维持时间较短,因此早期精准、灵敏的媒介病毒检测,对于dbv流行的监测与预警具有重要意义。
3、目前dbv实验室的检测手段主要为病毒分离鉴定、血清学检测以及核酸检测法。病毒分离鉴定存在耗时长、病变不明显、操作复杂等缺点。病毒血清学检测特异性较低,限制了其在临床上的应用。病毒核酸检测法包括常规pcr法和实时荧光定量pcr法,是实验室目前最常用的检测方法,但该技术只能得到定性结果,无法直接获得定量数据;需依赖参考标品、标准曲线和内标校正等复杂的操作间接得到病毒定量结果,且无法应用于低dbv载量的样本检测。因此亟需开发一种快速、精准、超敏的定量检测方法,为dvb的早期防控与治疗提供技术支持。
4、微滴式数字pcr(droplet digital pcr,ddpcr)是一种全新的核酸定量方法,通过将待测核酸在扩增前随机分配形成均一的纳升级微滴,每个微滴为一个独立的反应单元。经pcr扩增后,对每个微滴进行荧光信号判读,最后依据泊松分布原理以及阳性结果比例直接得出样本中靶分子的拷贝数或浓度。微滴式数字pcr单分子级的检测灵敏度高,无需依靠标准曲线、循环阈值就能得到准确性高、重复性好的病毒绝对定量结果。
技术实现思路
1、针对现有技术存在的上述不足,本发明提供了一种基于微滴式数字pcr的大别班达病毒定量检测引物探针组合物及其应用。从ncbi中下载不同年份、不同省份、不同国家及动物源(蜱虫、山羊等)的相关大别班达病毒s片段全基因序列。把上述基因序列导入dnaman软件,进行同源性比对分析,找出高度保守且通用的基因区域。在s片段全基因范围内设计广谱大别班达病毒检测的引物探针,同时与其他虫媒病毒如登革病毒(dengue virus,denv)、基孔肯雅病毒(chikungunya vius,chikv)、寨卡病毒(zika virus,zika)、日本脑炎病毒(japanese encephalitis virus,jev)等进行特异性验证,保证设计引物探针的保守性、通用性及特异性。
2、本发明的大别班达病毒微滴式数字pcr检测方法可以实现病毒拷贝数的绝对定量,对患者病程不同阶段进行实时、精确的监测,直接辨别病情轻重,为制订恰当的诊治方案提供科学依据;同时,对于含量极低的dbv感染潜伏期样本,本发明方法可提高检测阳性率,减少和避免漏诊的出现,并给予积极的早期治疗,阻止病情加重。另外,本发明方法对媒介宿主所携带的低载量病毒也具有良好的检测效果,能够对疫区传染源及传播媒介进行防控监测。
3、一种基于微滴式数字pcr的大别班达病毒定量检测引物探针组合物,序列分别为:
4、上游引物:5'-agaggrtccctgaaggagttgta-3’;
5、下游引物:5'-actctytrtggcaagatgccttca-3’;
6、荧光探针:5'-ttgctggctccdcgcatcttcacatt-3’,
7、其中,荧光探针的两端分别具有荧光报告基团和荧光淬灭基团。
8、优选的,荧光基团为fam、vic、rox、cy5、tet、hex、joe中的一种,淬灭基团为bhq-1、bhq-2、bhq-3、tamra、dabcyl中的一种。
9、本发明又提供了所述基于微滴式数字pcr的大别班达病毒定量检测引物探针组合物在以非疾病诊断为目的检测大别班达病毒中的应用。
10、本发明又提供了一种基于微滴式数字pcr的定量检测大别班达病毒的试剂盒,包括所述基于微滴式数字pcr的大别班达病毒定量检测引物探针组合物。优选的,所述用于检测大别班达病毒的试剂盒还包括用于微滴式数字pcr检测的试剂。进一步优选的,用于微滴式数字pcr检测的试剂包括:一步法微滴式数字pcr探针法预混液、探针法微滴式数字pcr微滴生成油;其中,一步法微滴式数字pcr探针法预混液包括:rna逆转录酶和dna聚合酶、权利要求1或2所述基于微滴式数字pcr的大别班达病毒定量检测引物探针组合物、无rna酶的蒸馏水。
11、本发明还提供了一种非疾病诊断为目的检测大别班达病毒的方法,使用所述基于微滴式数字pcr的大别班达病毒定量检测引物探针组合物进行扩增检测,并对扩增产物进行荧光检测,有荧光的为扩增阳性。本发明非疾病诊断为目的检测大别班达病毒的方法可以是对环境样本进行定量检测,也可以对疫区相关媒介宿主所携带的低载量病毒进行检测,能够对疫区传染源及传播媒介进行防控监测。
12、优选的,所述方法为微滴式数字pcr检测方法。所述的方法,包括以下步骤:
13、(1)提取待检测样品的总rna,
14、(2)以步骤(1)所得总rna作为扩增模板,配置微滴式数字pcr反应体系,
15、(3)将步骤(2)配置好的微滴式数字pcr反应体系制备微滴,
16、(4)使用微滴式数字pcr扩增仪对步骤(3)制备的微滴进行扩增,
17、(5)使用微滴分析仪对扩增后的微滴进行分析,获得待检测样品中大别班达病毒的拷贝数。
18、待检测样品可以是患者血清、蜱虫等。
19、本发明关键在于特异性引物和探针的设计,对不同年份、不同省份、不同国家及动物源(蜱虫、山羊等)的相关大别班达病毒s片段全基因序列进行同源性比对分析,在高度保守且通用的基因区域设计检测的引物探针。反应液内的其他组分,为本领域常规用于ddpcr的反应试剂,本领域普通技术人员可根据常识进行选择,可自行配制,也可选用市购商品。
20、优选的,按照20μl的反应体系计算,所述ddpcr的反应体系为:supermix 5μl、reverse transcriptase 2μl、dtt(300nm)1μl、10μm上游引物0.4μl、10μm下游引物0.4μl、10μm探针0.2μl、模板核酸1μl、dnase/rnase free water补至20μl。
21、制备微滴,把20μl样品反应体系加入至微滴生成芯片的样本孔中,一排8个,不足8个样品时用20μl 1×buffer control补足,向油相孔中加入70μl微滴生成油,盖上胶垫,接着把芯片放置在微滴生成仪中生成微滴;
22、微滴生成结束后取出芯片,取40μl生成的微滴按一一对应的方式全部转入96孔板,用热封仪进行封膜;
23、将封好膜的96孔板放置于pcr扩增仪进行扩增;
24、将完成ddpcr扩增的pcr板放入微滴分析仪中,使用微滴分析仪检测微滴进行读数,分析每管反应体系中发出荧光的微滴数,显示样品中大别班达病毒检测结果。检测结果依据一维图划定阈值区分阴性微滴和阳性微滴并计算拷贝数。若总微滴数<10000,则该结果无效,需重新生成微滴。
25、作为本发明所述应用的优选实施方式,扩增程序为:45℃逆转录60min,95℃预变性10min;95℃变性30s,然后55℃退火60s,在55℃进行fam荧光检测,共进行40个循环;98℃,10min,4℃恒温,结束反应,每步都设置2.5℃/sec的降温速度。
26、本发明与现有技术相比,具有以下优点和效果:
27、1.通用性好,适用于目前全球流行的dbv毒株序列,上下游引物及探针做了兼并。
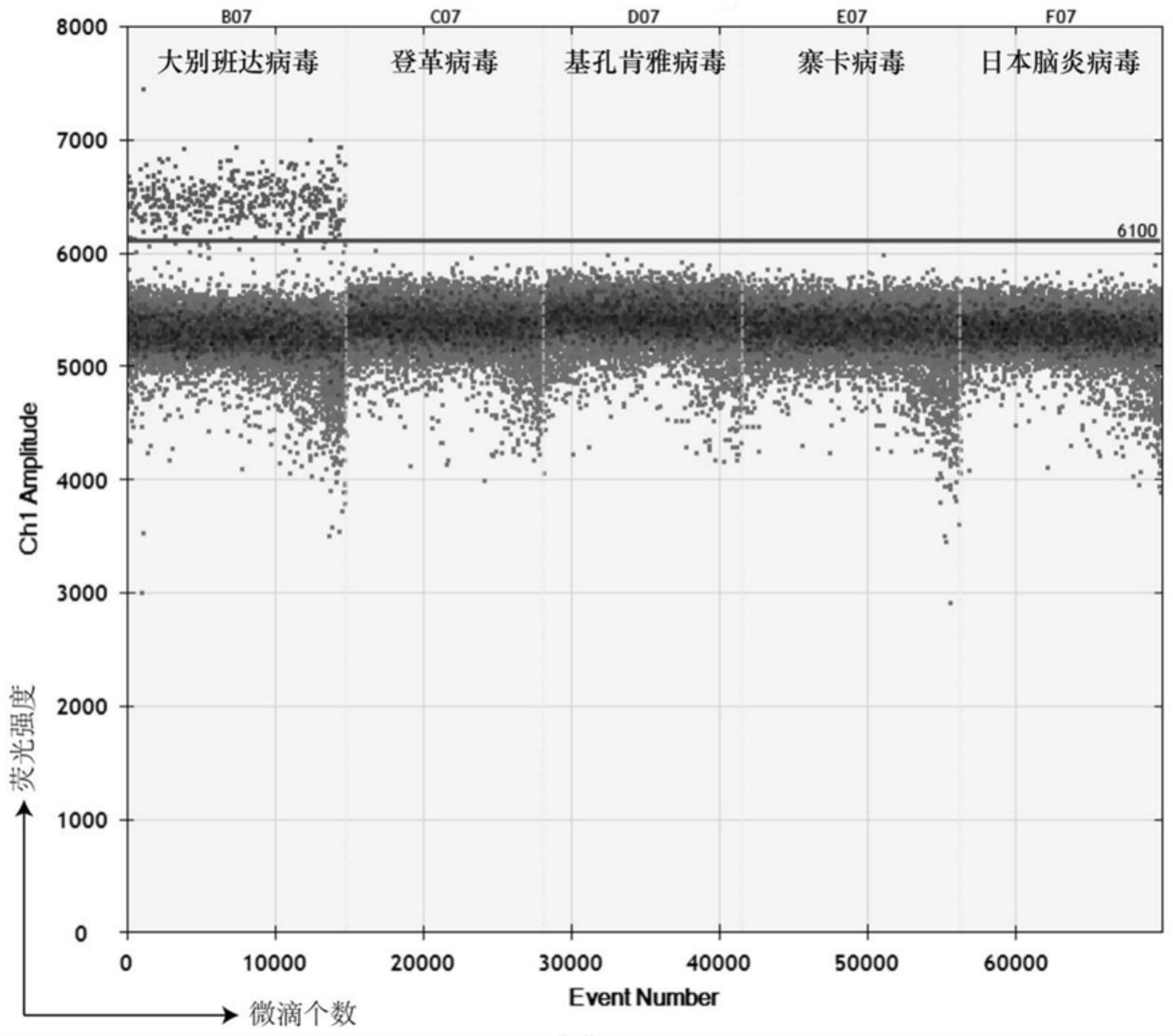
28、2.特异性好,与zika、chikv、denv、jev等虫媒病毒均无交叉反应。
29、3.灵敏度高,在20μl体系下,检出限可达6拷贝/反应。
30、4.绝对定量,无需设置标准曲线,可根据检测结果直接判读样本中大别班达病毒的拷贝数,极大的简化了操作步骤。
- 还没有人留言评论。精彩留言会获得点赞!