一种半乳糖化海藻酸钠衍生物凝胶微球及其制备方法与应用
本发明涉及高分子材料,更具体地,涉及一种半乳糖化海藻酸钠衍生物凝胶微球及其制备方法与应用。
背景技术:
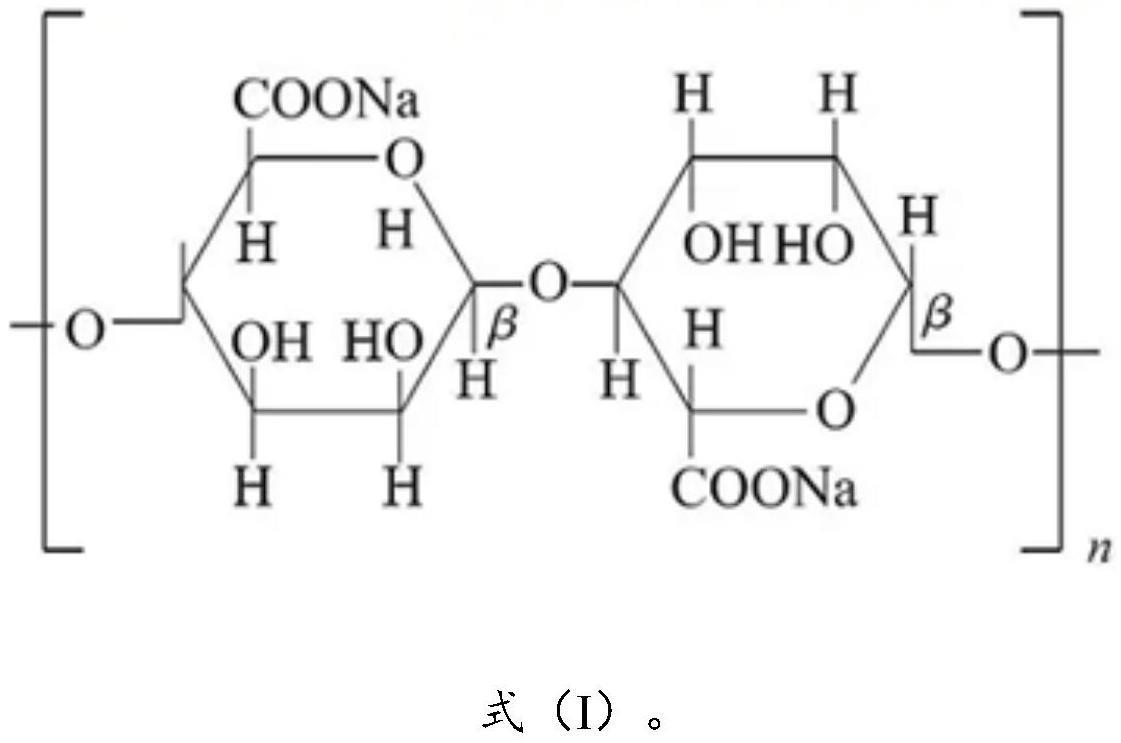
1、高分子水凝胶作为一种重要的软物质材料,已广泛用于各种抗生素、抗癌药物、生长因子、核酸等的负载和控释,以及细胞包埋、培养等。基于天然多糖的高分子水凝胶,具有良好的生物相容性。与常用的合成高分子相比,这些天然高分子具有高亲水性、可生物降解、来源丰富、无毒、可化学修饰等特点。海藻酸钠是由α-l-古洛糖醛酸(g)和β-d-甘露糖醛酸(m)按(1-4)键链接的一种线型无规共聚物,是从褐藻中提取的一种水溶性阴离子聚多糖,属于海藻酸衍生物中的一种,分子量在32000-400000g/mol之间,海藻酸钠的分子结构如下式(ⅰ)所示。海藻酸钠可生物降解,无毒,生物相容性好,在生物医用领域被用作药物载体、组织工程支架等。海藻酸钠凝胶微球是海藻酸钠水凝胶的形式之一,可通过钙离子交联法将海藻酸钠或其衍生物的水溶液用液滴法逐滴滴入到离子交联剂(氯化钙溶液)中进行制备,称为液滴法(或外部凝胶化法),该方法简单,反应条件温和,容易实现,是常用的制备方法。
2、
3、在细胞培养中,细胞在常用的培养基质表面通常会过度铺展,影响其正常表型或功能。因此,亟需开发一种能够负载药物,并且能够用于培养细胞的凝胶材料。
技术实现思路
1、本发明旨在至少解决上述现有技术中存在的技术问题之一。为此,本发明提出一种半乳糖化海藻酸钠衍生物凝胶微球及其制备方法与应用,本发明提供的半乳糖化海藻酸钠衍生物凝胶微球生物相容性好,可用于作为药物负载载体,还可以用作细胞培养材料,本发明采用的颜料可降解。
2、本发明的第一方面提供一种半乳糖化海藻酸钠衍生物凝胶微球的制备方法。
3、具体地,一种半乳糖化海藻酸钠衍生物凝胶微球的制备方法,包括如下步骤:
4、(1)将海藻酸钠溶于溶剂中,加入半乳糖胺盐酸盐混合,通过酰胺反应,制得半乳糖化海藻酸钠衍生物;
5、(2)将步骤(1)制得的半乳糖化海藻酸钠衍生物和海藻酸钠混合,加入水制得混合水溶液,然后加入交联剂,通过凝胶化反应,制得所述半乳糖化海藻酸钠衍生物凝胶微球。
6、本发明先合成半乳糖化海藻酸钠衍生物,再添加海藻酸钠,通过凝胶化反应制得半乳糖化海藻酸钠衍生物凝胶微球,凝胶微球含有海藻酸钠,表面含肝细胞表面受体的特异性配体半乳糖基团,可以作为肝细胞体外培养基质材料,使肝细胞相互聚集生长,不易铺展,能保持与体内相似的立体形态,长时间保持分化功能,还可以用作药物负载的载体,用于药物的控制释放。
7、优选地,步骤(1)中,所述半乳糖胺盐酸盐与海藻酸钠的糖单元的摩尔比为(0.5-2.5)∶1。
8、进一步优选地,步骤(1)中,所述半乳糖胺盐酸盐与海藻酸钠的糖单元的摩尔比为(1.5-2.5)∶1。
9、优选地,步骤(1)中,所述酰胺反应的温度为20-40℃,所述酰胺反应的时间为12-48小时。
10、进一步优选地,步骤(1)中,所述酰胺反应的温度为25-40℃,所述酰胺反应的时间为24-48小时。
11、优选地,步骤(1)中,所述溶剂为无水吗啉乙磺酸(mes)缓冲液。
12、优选地,所述无水吗啉乙磺酸缓冲液的浓度为0.1-0.5mol/l。
13、进一步优选地,所述无水吗啉乙磺酸缓冲液的浓度为0.2-0.5mol/l。
14、优选地,所述无水吗啉乙磺酸缓冲液的ph值为4-5。
15、优选地,所述海藻酸钠和无水吗啉乙磺酸缓冲液的质量体积比(w/v)为(0.01-0.3)∶(30-50)。
16、进一步优选地,所述海藻酸钠和无水吗啉乙磺酸缓冲液的质量体积比(w/v)为(0.15-0.3)∶(40-50)。
17、优选地,步骤(1)中,所述酰胺反应后,还包括纯化的步骤。
18、优选地,所述纯化为透析。
19、优选地,所述透析采用的透析袋截留分子量为90000-11000。
20、进一步优选地,所述透析采用的透析袋截留分子量为90000-10000。
21、优选地,所述透析的时间为1-5天。
22、进一步优选地,所述透析的时间为3-5天。
23、优选地,所述纯化后还包括干燥的步骤。
24、优选地,所述干燥为冷冻干燥。
25、优选地,步骤(1)中,所述将海藻酸钠和半乳糖胺盐酸盐混合后,还包括加入n-羟基琥珀酰亚胺(nhs)和1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(edc)。nhs和edc可活化羧基。
26、优选地,所述n-羟基琥珀酰亚胺(nhs)和1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(edc)的摩尔比为(0.1-0.3):1。
27、进一步优选地,所述n-羟基琥珀酰亚胺(nhs)和1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(edc)的摩尔比为(0.2-0.3):1。
28、优选地,所述1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(edc)和海藻酸钠的糖单元为(0.5-5)∶1或1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(edc)和海藻酸钠的酯基的摩尔比为(0.5-5)∶1。
29、进一步优选地,所述1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(edc)和海藻酸钠的糖单元的摩尔比为(2.5-5)∶1或1-乙基-(3-二甲基氨基丙基)碳二亚胺盐酸盐(edc)和海藻酸钠的酯基的摩尔比为(2.5-5)∶1。
30、优选地,将步骤(1)制得的半乳糖化海藻酸钠衍生物和海藻酸钠混合,采用滴加的方式加入到交联剂中。
31、更优选地,将步骤(1)制得的半乳糖化海藻酸钠衍生物和海藻酸钠混合,装入注射器中,采用滴加的方式加入到交联剂中。
32、优选地,所述滴加时保持滴加的速度和液滴下落的高度一致。目的是形成均匀的凝胶微球。
33、优选地,所述注射器的针头直径为0.1-1mm。
34、进一步优选地,所述注射器的针头直径为0.5-0.8mm。
35、优选地,步骤(2)中,所述半乳糖化海藻酸钠衍生物和海藻酸钠的质量比为(1-3):(1-3)。
36、进一步优选地,步骤(2)中,所述半乳糖化海藻酸钠衍生物和海藻酸钠的质量比为(1-2):(1-2)。
37、优选地,步骤(2)中,所述凝胶化反应的温度为20-40℃,所述凝胶化反应的时间为5-15min。
38、进一步优选地,步骤(2)中,所述凝胶化反应的温度为25-40℃,所述凝胶化反应的时间为10-15min。
39、优选地,所述交联剂为氯化钙。
40、优选地,所述交联剂的浓度为0.1-1mol/l。
41、进一步优选地,所述交联剂的浓度为0.5-1mol/l。
42、优选地,所述交联剂和海藻酸钠的糖单元的摩尔比为(10-30):1。
43、优选地,步骤(2)中,制得所述半乳糖化海藻酸钠衍生物凝胶微球后,还包括将半乳糖化海藻酸钠衍生物凝胶微球继续静置12-24h。继续在原反应体系中静置使得半乳糖化海藻酸钠衍生物的凝胶化过程不仅在表面进行,也深入到凝胶微球的内部。
44、优选地,步骤(2)中,所述半乳糖化海藻酸钠衍生物和水的质量体积比(w/v)为(0.005-0.015)∶1。
45、进一步优选地,步骤(2)中,所述半乳糖化海藻酸钠衍生物和水的质量体积比(w/v)为(0.01-0.015)∶1。
46、本发明的第二方面提供一种半乳糖化海藻酸钠衍生物凝胶微球。
47、一种半乳糖化海藻酸钠衍生物凝胶微球,所述半乳糖化海藻酸钠衍生物凝胶微球的粒径为1300-1500μm。
48、本发明的第三方面提供一种半乳糖化海藻酸钠衍生物凝胶微球的应用。
49、一种半乳糖化海藻酸钠衍生物凝胶微球在制备载体材料或制备细胞培养材料中的应用。
50、一种蛋白负载凝胶微球,包括载体和蛋白,所述载体为半乳糖化海藻酸钠衍生物凝胶微球。
51、优选地,所述蛋白负载凝胶微球还包括药物。
52、优选地,所述药物为降血脂药物、抗肿瘤药物、抗炎药物、抗氧化药物、抗菌药物中的一种或几种。
53、优选地,所述蛋白为牛血清白蛋白(bsa)。
54、优选地,所述蛋白负载凝胶微球的制备方法为先将半乳糖化海藻酸钠衍生物和海藻酸钠混合,加水溶解,再加入蛋白,制得混合溶液,然后加入到交联剂中,进行凝胶化反应,制得所述蛋白负载凝胶微球。
55、优选地,所述蛋白与半乳糖化海藻酸钠衍生物凝胶微球的质量体积比为(0.001-0.005)∶1。
56、一种细胞培养材料,包括所述半乳糖化海藻酸钠衍生物凝胶微球制得。
57、优选地,所述细胞培养材料为肝细胞培养材料。
58、优选地,所述半乳糖化海藻酸钠衍生物凝胶微球与肝细胞共培养。
59、优选地,所述共培养的时间为24-60min。
60、进一步优选地,所述共培养的时间为48-60min。
61、相对于现有技术,本发明的有益效果如下:
62、(1)本发明先利用海藻酸钠和半乳糖胺盐酸盐进行酰胺反应制得半乳糖化海藻酸钠衍生物,然后利用半乳糖化海藻酸钠衍生物和海藻酸钠通过凝胶化反应制得半乳糖化海藻酸钠衍生物凝胶微球,本发明采用的海藻酸钠原料来源丰富,具有较好的生物相容性和生物降解性,而且本发明的制备方法简便易操作,可方便半乳糖化海藻酸钠衍生物凝胶微球的生产和应用;
63、(2)本发明的凝胶化反应在20-40℃下进行,反应条件温和,容易实现;
64、(3)本发明提供的半乳糖化海藻酸钠衍生物凝胶微球可用作载体材料或者细胞培养材料,例如作为载体材料用于负载蛋白和药物,可实现对药物的控制释放;本发明的半乳糖化海藻酸钠衍生物凝胶微球还可以构筑一个三维的人造细胞外基质,用于细胞培养、固定和包埋,由于引入了半乳糖基团,半乳糖基团是肝细胞表面去唾液酸糖蛋白受体的特异性配体,因此用于细胞培养,尤其是肝细胞的培养,能够使肝细胞相互聚集生长,不易铺展,能保持与体内相似的立体形态,长时间保持分化功能,与二维的基材相比,三维支架所提供的细胞生长环境更加接近正常的组织环境。
- 还没有人留言评论。精彩留言会获得点赞!