一种用于检测反义寡核苷酸类药物的荧光探针及检测方法
本发明涉及一种荧光探针及检测方法,尤其涉及一种用于检测反义寡核苷酸类药物的荧光探针及检测方法。
背景技术:
1、脊髓性肌萎缩(spinal muscular atrophy,sma)是一种罕见的常染色体隐性遗传神经肌肉疾病,由于运动神经元存活基因1(survival motor neuron gene 1,smn1)致病性变异(纯合缺失或突变),修饰基因smn2产生的全长功能性smn蛋白不足,最终导致脊髓前角a-运动神经元变性而致病。家族中有sma患者的人群儿童、成人均可患病,发病率为万分之一,携带率为1/50~1/40。依照国际分型标准,按照发病年龄和可获得最大运动里程碑,将sma从重到轻分为5个类型(0~4),其中0型sma为出生前或出生时,无运动历程碑,仅存活数月。1型与2型sma通常导致患儿的寿命严重缩短甚至死亡,3型与4型sma虽然不致命,但会严重影响患者的运动功能,导致生活质量的急剧下降。诺西那生钠(nusinersen sodium,商品名spinraza)是全球首个sma精准靶向治疗药物,2016年由fda批准上市。诺西那生钠是一种改性的反义寡核苷酸(aso)药物,由18个核糖核苷酸残基组成的一段单链rna(5’-uca cuuuca uaa ugc ugg-3’),其中核呋喃糖基环的2'-羟基被2'-o-2-甲氧基乙基取代,磷酸键被硫代磷酸酯键取代,以降低诺西那生钠对体外环境与体内广泛存在的核酸酶的降解能力。研究显示,诺西那生钠可修饰smn2基因剪接,促进全长功能性smn蛋白产生,显著改善sma患者的生存以及运动、呼吸等重要功能,改变sma疾病进程,且安全性和依从性良好。临床上采用鞘内注射的方式进行多剂量给药,由于寡合苷酸药物的半衰期较短且极易在肝肾中蓄积,血浆与脑积液中的诺西那生钠含量非常低,给诺西那生钠的药代动力学研究以及临床治疗药物的监测带来了巨大的挑战。
2、目前,已被报道的诺西那生钠检测方法主要有酶联免疫吸附法(enzyme linkedimmunosorbent assay,elisa)与电化学发光法(electro chemiluminescenceimmunoassay,ecl)。其中,用于诺西那生钠检测的elisa技术是根据2002年rosie等人报道的一种非竞争性杂交-连接酶联免疫吸附试验技术加以改进开发而来。该方法首先使用固相载体上的模板链捕获诺西那生钠,利用t4连接酶催化诺西那生钠-模板杂交双链的粘末端与地高辛修饰的连接探针连接,最后以碱性磷酸酶标记的地高辛抗体进行elisa分析。该方法检测限约为1.5ng/m,涉及多重酶促反应,原理复杂,成本高昂,需要反复洗涤、孵育,重现性差,且实验周期长。诺西那生钠临床试验数据显示,诺西那生钠进入体内后绝大部分富集于肝、肾、脾等器官,血浆以及脑脊液中的浓度极低,且生物样品中的各种酶活物质及内源性物质对检测均有干扰。此外,与microrna以及其他的反义寡核苷酸药物相比,诺西那生钠的寡核苷酸链长度较短,仅含有18个核苷酸残基,这使得杂交酶联免疫吸附试验(helisa)以及一些信号放大策略难以应用于诺西那生钠的生物分析检测。电化学发光法是目前用于诺西那生钠检测的首选方法,灵敏度高(检测限低至0.015ng/ml),但是检测条件苛刻,仪器昂贵,且需要对电极进行复杂的改性,这严重限制了ecl法的应用。lc-ms/ms技术已经被广泛用于体内药物分析,寡核苷酸药物因极性较强且具有大量负电荷,通常需要在液相分离系统中加入离子对试剂以增强保留并改善色谱行为,然而离子对试剂的加入会导致显著的离子抑制效应,导致检测灵敏度较低,因此经典的lc-ms/ms技术并不适合于寡核苷酸药物的高灵敏检测。
技术实现思路
1、发明目的:本发明的目的是提供一种快速、灵敏、高通量的用于检测反义寡核苷酸类药物的荧光探针;本发明的另一目的是提供一种及检测反义寡核苷酸类药物的方法。
2、技术方案:本发明的一种用于检测反义寡核苷酸类药物的荧光探针,所述荧光探针包括mnps-ssb分散液和rqds-cp分散液,所述mnps-ssb由磁球和修饰在磁球上的单链dna结合蛋白构成;所述rqds-cp由红色荧光量子点和修饰在红色荧光量子点上的单链dna构成;所述单链dna的序列与待测反义寡核苷酸类药物的序列互补,所述单链dna结合蛋白可特异性结合所述单链dna。
3、优选的,所述红色荧光量子点为cdte@zns荧光量子点。
4、作为上述方案的进一步改进,所述cdte@zns荧光量子点由以下步骤制备所得:
5、(1)镉源和还原型谷胱甘肽加溶剂溶解,获得镉前体溶液;
6、(2)锌源和还原型谷胱甘肽加溶剂溶解,获得锌前体溶液;
7、(3)nahte溶液注入镉前体溶液中,回流一段时间,在反应沸腾状态下,注入锌前体溶液,继续回流一段时间,反应结束,得到cdte@zns荧光量子点。
8、作为上述方案的更进一步改进,所述rqds-cp由以下步骤制备所得:
9、(1)cdte@zns荧光量子点、1-乙基-(3-二甲基氨基丙基)碳酰二亚胺和单链dna结合蛋白在缓冲溶液中反应一段时间;
10、(2)反应结束后,收集红色沉淀,即为rqds-cp。
11、可选地,所述反义寡核苷酸类药物为诺西那生钠及其类似物;
12、优选的,所述反义寡核苷酸类药物为诺西那生钠,所述单链dna序列为
13、5’-h2n-(ch2)6-cca gca tta tga aag tga-3’
14、所述单链dna结合蛋白为t4 gene 32protein。
15、作为上述方案的更进一步改进,所述mnps-ssb由以下步骤制备所得:
16、(1)羧基化磁性纳米颗粒洗涤后,分散于偶联缓冲液中,得到羧基化磁性纳米颗粒分散液;
17、(2)所述羧基化磁性纳米颗粒分散液与1-乙基-(3-二甲基氨基丙基)碳酰二亚胺和单链结合蛋白混合,室温反应一段时间,反应结束后,进行磁分离,所得产物即为mnps-ssb。
18、另一方面,本发明提供一种利用上述的荧光探针检测反义寡核苷酸类药物的方法,所述方法包括以下步骤:
19、(1)若干份rqds-cp分散液中分别加入梯度浓度的反义寡核苷酸类药物,孵育一段时间后,加入mnps-ssb分散液,继续孵育一段时间;孵育结束后进行磁分离,得到若干份上清溶液;
20、(2)分别测定若干份上清溶液的荧光强度,得到反义寡核苷酸类药物浓度与对应荧光强度的标准曲线;
21、(3)rqds-cp分散液中加入待测样品,孵育一段时间后,加入mnps-ssb分散液,继续孵育一段时间;孵育结束后进行磁分离,得到上清溶液;
22、其中,步骤(3)中的rqds-cp分散液浓度、mnps-ssb分散液浓度、孵育条件与步骤(1)保持一致;
23、(4)测定步骤(3)中上清溶液的荧光强度,并与步骤(2)中得到的标准曲线比对,得到待测样品中反义寡核苷酸类药物的浓度。
24、优选的,步骤(1)和步骤(3)中,rqds-cp分散液中rqds-cp的浓度为0.1~0.8mg/ml。
25、优选的,步骤(1)和步骤(3)中,rqds-cp分散液与反义寡核苷酸类药物或待测样品的孵育温度为25~37℃。
26、优选的,步骤(1)和步骤(3)中,步骤(2)和步骤(4)中使用酶标仪测定荧光强度,测定条件为:在610nm处测定荧光强度,荧光光谱扫描范围500~700nm,激发波长为365nm。
27、优选的,所述方法对反义寡核苷酸类药物的线性检测范围为0.1~200nm。
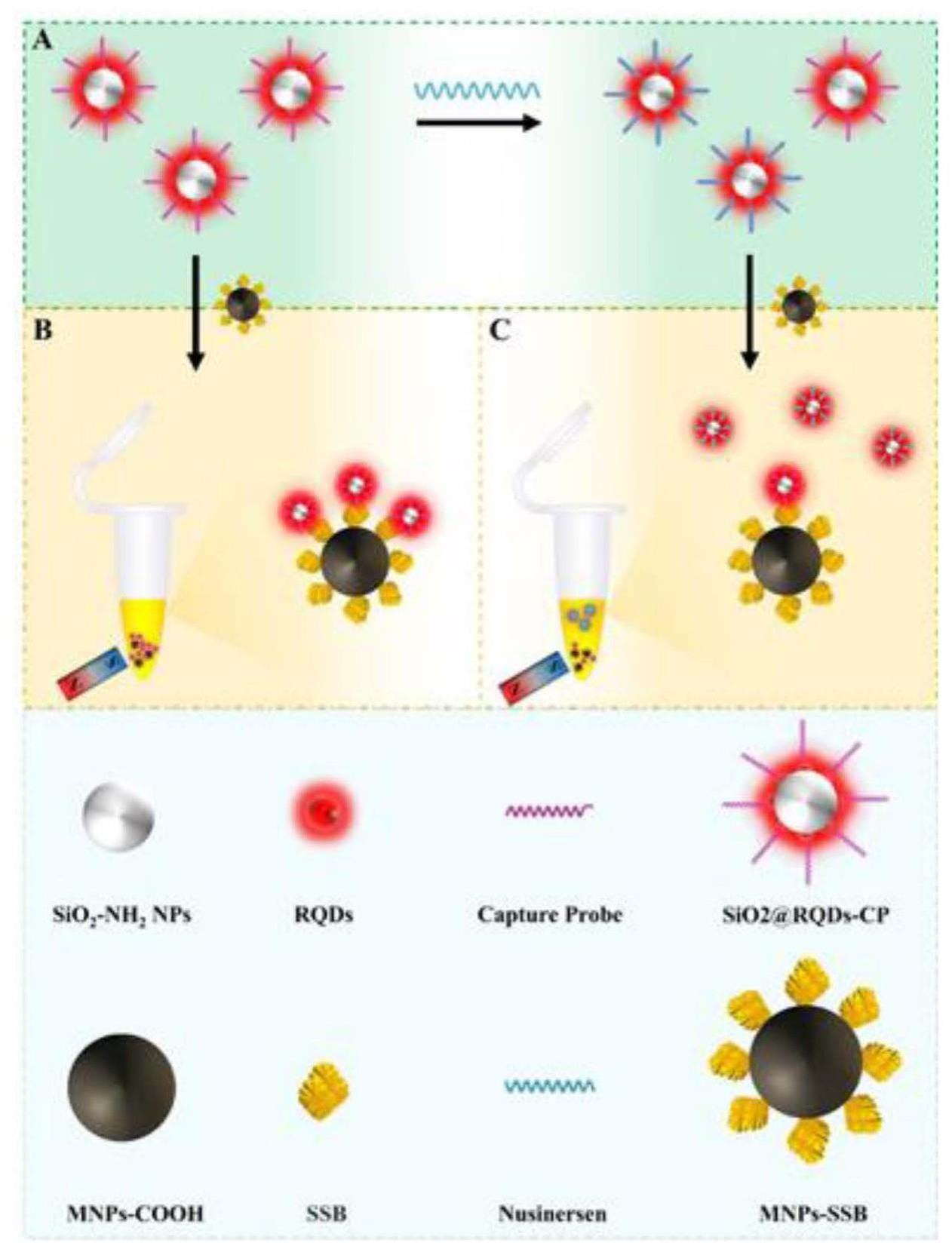
28、针对诺西那生钠药物在复杂生物基质中检测分析中的难点,本发明提出了一种基于单链dna结合蛋白特异性捕获寡核苷酸功能化荧光探针的分析策略,用于复杂生物样品中诺西那生钠的快速、灵敏、高通量的检测。首先,将单链dna结合蛋白(single-strandedbinding protein,ssb)通过酰胺键修饰在磁球(magnetic nanoparticles,mnps)表面,得到mnps-ssb。与诺西那生钠互补的单链dna(ssdna)通过酰胺键修饰在红色荧光量子点(rqds)表面,得到rqds-cp的捕获探针(capture probe,cp)。ssb能够特异性结合单链dna(ssdna),几乎不与双链dna(dsdna)、双链rna(dsrna)以及dna-rna杂交双链结合,即使与单链rna结合,但是亲和力较低(约为单链dna的1/10)。当样品中不存在诺西那生钠时,rqds-cp的捕获探针能够与mnps-ssb高效结合,经磁分离后上清液中的rqds-cp较少,上清液的红色荧光较弱。当样品中存在诺西那生钠时,rqds-cp的捕获探针与诺西那生钠形成dna-rna杂交双链,难以被mnps-ssb捕获,此时上清液中的rqds-cp含量增加,红色荧光增强。因此,上清液的红色荧光强度可反映样品中的诺西那生钠的浓度,通过建立荧光检测信号(f/f0)与诺西那生钠浓度的线性关系实现定量分析。
29、有益效果:与现有技术相比,本发明具有如下显著优点:本发明的荧光探针可用于复杂生物样品中诺西那生钠的快速、灵敏、高通量的检测;本发明在生物样品中的诺西那生钠在0.1~200nm的范围内,检测信号f/f0与诺西那生钠浓度之间具有良好的线性关系(r2=0.9152),常见小分子化合物以及诺西那生钠单碱基、二碱基、三碱基突变的相似序列的检测信号均明显低于诺西那生钠,表明此方法具有良好的特异性。此外,本方法无需洗涤、离心等复杂繁琐的前处理,且不需要额外添加酶或底物等酶促反应,分析周期短(仅为30min),能够实现高灵敏性、高特异性、快速简便的高通量分析检测。为诺西那生钠及类似反义寡核苷酸药物的药代动力学研究及临床用药监测提供了技术支持。
- 还没有人留言评论。精彩留言会获得点赞!