一种用于检测大熊猫三种致病菌的引物组合、试剂盒及其检测方法与流程
本发明属于基因工程,具体涉及一种用于检测大熊猫三种致病菌的引物组合、试剂盒及其检测方法。
背景技术:
1、大熊猫(ailuropoda melanoleuca)是我国特有的珍稀濒危动物,是世界生物多样性保护的旗舰种。随着近年来保护工作的不断加强深入,大熊猫种群数量和生活环境得到了巨大的改善。大熊猫疾病按病原分主要分为病毒性疾病、寄生虫性疾病、细菌性疾病,而细菌性疾病是引起大熊猫感染发病的重要因素。
2、大熊猫细菌性疾病是一类对大熊猫种群健康和生命安全具有极大威胁的疾病。近年来,细菌性疾病发病率呈上升趋势,奇异变形杆菌(proteus mirabilis,pm)、肺炎克雷伯杆菌(klebsiella pneumoniae,kpn)和大肠埃希菌(简称大肠杆菌,escherichia coli,e.coli)均是临床中引起大熊猫感染发病的常见病原菌。奇异变形杆菌可以导致大熊猫泌尿生殖道感染并引起血尿等症状;肺炎克雷伯菌可引起大熊猫腹泻、带黏液或血液的粪便、败血症和泌尿生殖系统感染;大肠杆菌感染可导致大熊猫出现腹泻、肠炎等症状。
3、目前在大熊猫细菌性疾病检测工作中,主要采用传统的病原菌分离检测方法,该方法存在周期长、步骤繁琐、检出率低等缺点,无法满足临床诊疗中对病原体快速、准确的检测需求。随着生物技术学的发展,采用pcr检测病原菌,可达到快速、准确的要求。
4、多重pcr是一种可以同时检测多个病原的检测方法,具有检测量大、准确和快速等优点,在食品病原菌检测和家畜疾病诊断中得到广泛应用。但传统的多重pcr方法通常需要设计多个引物对,并确保这些引物在反应条件下相互兼容。这涉及到引物之间的长度、gc含量、熔点以及互相之间的相互作用等因素。并且,如果引物之间存在互补性或二聚体的形成,可能会导致引物之间的竞争和干扰,从而影响pcr扩增的效率和特异性。这可能导致非特异性扩增产物的出现。引物设计的复杂性可能导致引物选择的困难,增加了实验的时间和成本。
5、其次,在传统多重pcr方法中,由于不同引物的特性和扩增条件的差异,不同目标片段的扩增效率可能存在差异。一些片段可能会被过度扩增,而其他片段可能会被低效扩增,导致结果的偏倚性。
6、另外,多重pcr方法通常需要在有限的反应体系中同时扩增多个目标片段,这可能限制了扩增的灵敏度。较低的灵敏度可能使检测低丰度目标或检测样本中稀有突变的能力受到限制。
技术实现思路
1、针对现有技术中的上述不足,本发明提供一种用于检测大熊猫三种细菌性病毒的引物组合、试剂盒及其检测方法,本发明建立的多重pcr检测方法具有良好特异性、灵敏性和抗干扰性,检出率优于病原分离鉴定法,极大的提高了检出效率,可为大熊猫种群三种细菌性疾病感染的快速诊断及流行病学调查提供技术支持,具有重要的临床意义。
2、为实现上述目的,本发明解决其技术问题所采用的技术方案是:
3、一种用于检测大熊猫三种致病菌的引物组合,包括以下引物序列:
4、phoe-f:5’-taatgatgatgggctttgtg-3’;(seq id no.1)
5、phoe-r:5’-cgaagaagtcggtgttgc-3’;(seq id no.2)
6、phoa-f:5’-cgtttctaccgcagagttg-3’;(seq id no.3)
7、phoa-r:5’-gtgactatgaccagcgtgtt-3’;(seq id no.4)
8、urer-f:5’-tacttcagcaatgtctaccgc-3’;(seq id no.5)
9、urer-r:5’-ccccattctgacatccaac-3’。(seq id no.6)
10、一种用于检测大熊猫三种致病菌的试剂盒,包括上述引物组合。
11、进一步地,还包括阳性对照、阴性对照、缓冲液、pcr酶和水中的至少一种。
12、进一步地,phoe、phoa和urer引物对的摩尔比为0.1~1:0.1~1:0.1~0.5。
13、进一步地,phoe、phoa和urer引物对的摩尔比为0.8:0.8:0.2。
14、一种以非诊断目的检测大熊猫三种致病菌的方法,包括以下步骤:
15、(1)提取待测样本dna;
16、(2)采用上述引物组合,或试剂盒对其进行多重pcr检测,然后将pcr产物进行电泳,根据电泳条带判断是否含有phoe、phoa或urer的细菌。
17、进一步地,该样本为至少含有phoe、phoa和urer序列的基因。
18、进一步地,多重pcr扩增体系为:2×taq pcr master mix 12.5μl、上下游引物(10μmol/l)各1μl、dna模板2μl、ddh2o 8.5μl
19、进一步地,多重pcr扩增程序为:95℃5min;95℃30s,60℃30s,72℃40s,共25个循环;72℃10min,4℃10min。
20、进一步地,根据电泳条带进行判断:
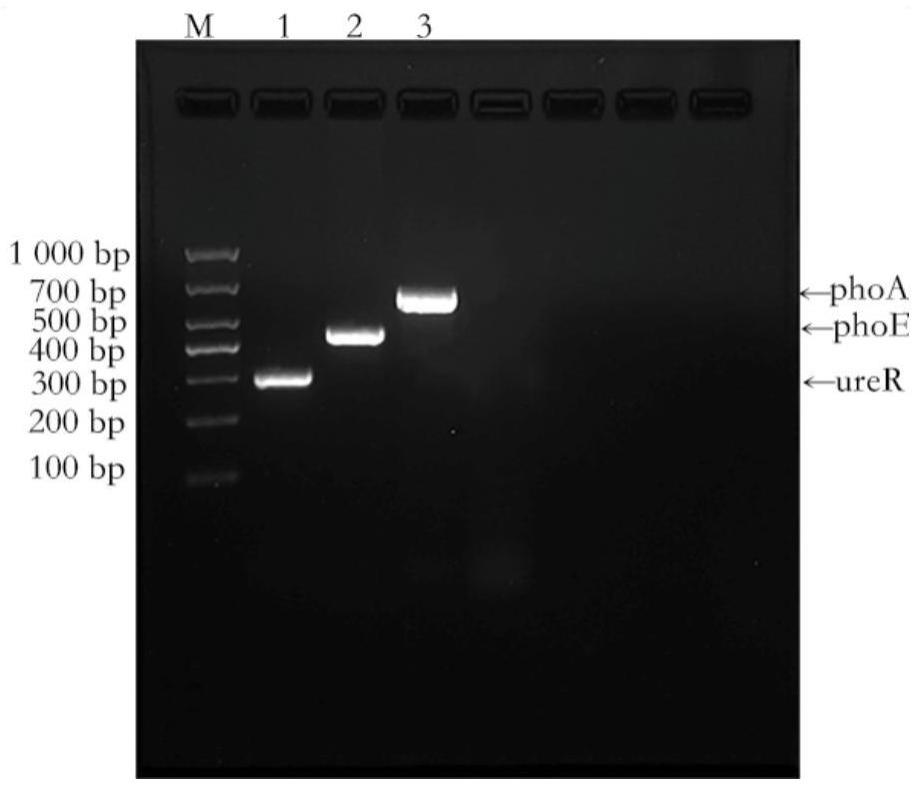
21、当目标片段产物为666bp时,可以判定为大肠杆菌感染;
22、当目标片段产物为456bp时,可以判定为肺炎克雷伯菌感染;
23、当目标片段产物为308bp时,可以判定为奇异变形杆菌感染;
24、当目标片段产物为308bp、和456bp时,可以判定为奇异变形杆菌和肺炎克雷伯菌混合感染;
25、当目标片段产物为308bp、和666bp时,可以判定为奇异变形杆菌和大肠杆菌混合感染;
26、当目标片段产物为456bp、和666bp时,可以判定为奇异变形杆菌和肺炎克雷伯菌混合感染
27、当目标片段产物同时出现在308bp、456bp、666bp时,可以判定为奇异变形杆菌、肺炎克雷伯菌、大肠杆菌混合感染。
28、本发明的有益效果:
29、本发明所建立的大熊猫泌尿生殖道三种细菌性疾病感染的诊断方法,分别针对大肠杆菌phoa、肺炎克雷伯菌phoe、奇异变形杆菌urer基因序列的保守区域设计引物,可分别扩增出666bp、456bp、和308bp、的基因片段,可以准确检测到大熊猫生殖泌尿道三种病原菌感染。该方法准确度高、操作简单、工作量较小、重复性好;能够为大熊猫生殖泌尿道细菌性疾病感染提供诊断,和临床用药提供依据,对促进大熊猫保护具有重要意义。
技术特征:
1.一种用于检测大熊猫三种致病菌的引物组合,其特征在于,包括以下引物序列:
2.一种用于检测大熊猫三种致病菌的试剂盒,其特征在于,包括权利要求1所述的引物组合。
3.根据权利要求2所述的试剂盒,其特征在于,还包括阳性对照、阴性对照、缓冲液、pcr酶和水中的至少一种。
4.根据权利要求2所述的试剂盒,其特征在于,phoe、phoa和urer引物对的摩尔比为0.1~1:0.1~1:0.1~0.5。
5.根据权利要求3所述的试剂盒,其特征在于,phoe、phoa和urer引物对的摩尔比为0.8:0.8:0.2。
6.一种以非诊断目的检测大熊猫三种致病菌的方法,其特征在于,包括以下步骤:
7.根据权利要求6所述的方法,其特征在于,该样本为至少含有phoe、phoa和urer序列的质粒,或相应的标准菌株。
8.根据权利要求6所述的方法,其特征在于,多重pcr扩增体系为:2×taq pcr mastermix 12.5μl,奇异变形杆菌、肺炎克雷伯杆菌、大肠杆菌上下游引物各1μl,基因组混合模板2μl,ddh2o 4.5μl。
9.根据权利要求6所述的方法,其特征在于,多重pcr扩增程序为:95℃5min;95℃30s,60℃30s,72℃40s,共25个循环;72℃10min,4℃10min。
10.根据权利要求6所述的方法,其特征在于,根据电泳条带进行判断:
技术总结
本发明公开了一种用于检测大熊猫三种致病菌的引物组合、试剂盒及其检测方法。其中,引物序列如SEQ ID NO.1~6所示。本发明建立的多重PCR检测方法具有良好特异性、灵敏性和抗干扰性,检出率优于病原分离鉴定法,极大的提高了检出效率,可为大熊猫种群三种细菌性疾病感染的快速诊断及流行病学调查提供技术支持,具有重要的临床意义。
技术研发人员:苏小艳,刘颂蕊,燕霞,刘圣,曹立亭,杨梅,岳婵娟,范雪阳,李运莉,张东升,李林,张洪文
受保护的技术使用者:成都大熊猫繁育研究基地
技术研发日:
技术公布日:2024/1/15
- 还没有人留言评论。精彩留言会获得点赞!