一种反式-1,3-二氧六环类液晶化合物的制备方法与流程
本发明涉及液晶化合物合成,尤其涉及一种反式-1,3-二氧六环类液晶化合物的制备方法。
背景技术:
1、反式-1,3-二氧六环类液晶化合物是一种重要的向列型液晶单体,主要应用于制备混合液晶,可有效提高液晶面板的响应值和清晰度。以其中较为常用的为例,目前文献报道的常见的合成路线如下。
2、
3、该路线的主要缺陷在于,其最后一步是转位反应,由于1,3-二氧六环类化合物的结构特殊性,这一步的收率很低,同时,工艺步骤较多,导致生产成本较高。因此,有必要研发一种操作简单、且产品收率和纯度均较高的反式-1,3-二氧六环类液晶化合物的制备方法。
技术实现思路
1、针对现有合成反式-1,3-二氧六环类液晶化合物方法存在的工艺步骤较多,及产品收率、纯度低的问题,本发明提供一种反式-1,3-二氧六环类液晶化合物的制备方法。
2、为解决上述技术问题,本发明提供的技术方案为:
3、一种反式-1,3-二氧六环类液晶化合物的制备方法,包括如下步骤:
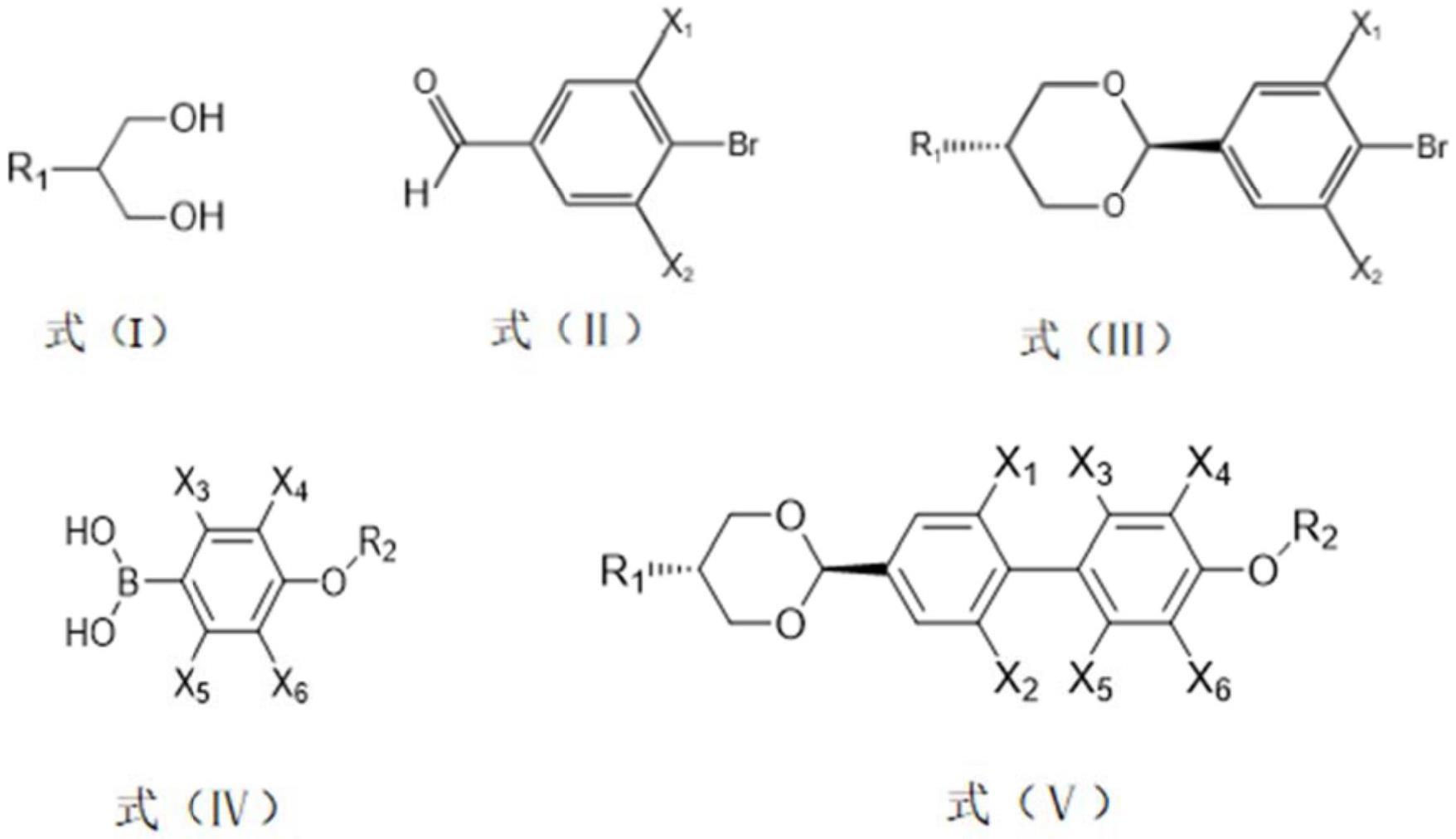
4、s1,以咪唑类三氟甲磺酸盐离子液体为催化剂,式(i)所示的二醇类化合物与式(ⅱ)所示的醛类化合物进行脱水、转位反应,得式(ⅲ)所示的化合物;
5、
6、s2,以碱金属盐和钯盐为催化剂,式(ⅲ)所示的化合物和式(ⅳ)所示的苯硼酸类化合物进行铃木反应,得式(ⅴ)所示的反式-1,3-二氧六环类液晶化合物;
7、
8、其中,r1为c1-c5烷基、c3-c5环烷基;r2为c1-c5直链烷基;
9、x1、x2、x3、x4、x5、x6为h或f;
10、若x1、x2至少一个为f时,则x3、x5均为h;
11、若x1、x2均为h,x3为f时,则x4为f;
12、若x1、x2均为h,x5为f时,则x6为f;
13、若x1、x2、x3、x5均为h时,则x4、x6至少有一个为f。
14、如下所示的式(x)所示的1,3-二氧六环类化合物具有顺反构型,反式构型可使分子呈线性结构,更易使分子呈现液晶态,而顺式构型分子呈弯曲态,较难有液晶态出现,因此,反式-1,3-二氧六环类化合物是本领域技术人员研究的重要液晶材料。但是,通过常规的脱水反应制备而得的产物中顺反比例较高,通常反应液中顺反式构型比例会高于7:3,再经过转位反应处理后,产品中反式目标化合物的收率只有40%~50%左右,造成该类化合物的生产成本居高不下。
15、
16、相对于现有技术,本发明创造性地以咪唑类三氟甲磺酸盐离子液体作为脱水反应的催化剂,一步完成了脱水和转位两步反应,在第一步反应就制备得到式(ⅲ)所示的化合物(反式构型),然后以制备得到的式(ⅲ)所示的化合物和式(ⅳ)所示的苯硼酸类化合物进行铃木反应,制备得到式(ⅴ)所示的反式-1,3-二氧六环类液晶化合物,不但有效简化了合成路线,将原来的三步反应简化为了两步,还有效提高了反式-1,3-二氧六环类液晶化合物的收率,目标化合物的收率可达90%以上,纯度可达99.9%以上;同时,将铃木反应后置,生产成本进一步降低。
17、本发明提供的反式-1,3-二氧六环类液晶化合物的制备方法,具有工艺路线短,生产成本低,产品收率高,操作安全,工艺实用性强,经济效益好等优点,易于实现工业化生产,对于提高企业市场竞争力具有十分重要的意义。
18、优选的,反式-1,3-二氧六环类液晶化合物的制备方法具体包括如下步骤:
19、s1,将式(i)所示的二醇类化合物、式(ⅱ)所示的醛类化合物和咪唑类三氟甲磺酸盐离子液体溶于第一溶剂中,于80℃~110℃进行脱水、转位反应,得式(ⅲ)所示的化合物;
20、s2,将式(ⅲ)所示的化合物、式(ⅳ)所示的苯硼酸类化合物、碱金属盐和钯盐溶于第二溶剂和水的混合溶液中,于75℃~120℃进行铃木反应,得式(ⅴ)所示的反式-1,3-二氧六环类液晶化合物。具体反应方程式如下:
21、
22、现有合成反式-1,3-二氧六环类液晶化合物的工艺一般为先进行铃木反应,再进行脱水反应和转位反应的三步合成法,工艺路线较长,且转位反应的目标产物的收率较低,限制了反式-1,3-二氧六环类液晶化合物的生产成本和生产效率。
23、发明人经过创造性思维改变了合成路线的反应顺序,先进行脱水反应,且以咪唑类三氟甲磺酸盐离子液体作为催化剂,在实现脱水反应高效进行的同时,还意外实现了转位反应的同时进行,获得了反式中间体,进而再以反式中间体为原料,与苯硼酸类化合物进行铃木反应,高收率地得到了反式目标产物,且将原来的三步反应简化为了两步,提高了生产效率,降低了能耗和生产成本,便于实现工业化规模生产。
24、优选的,所述咪唑类三氟甲磺酸盐离子液体为1-丁基-3-甲基咪唑三氟甲磺酸盐、1,3-二甲基咪唑三氟甲磺酸盐或1,3-二丁基咪唑三氟甲磺酸盐。
25、优选的离子液体不但可以作为脱水反应的催化剂,还能作为转位反应的催化剂,实现脱水反应和转位反应的同时进行,极大地简化了生产路线,提高了反式目标产物的收率。
26、本发明中所述咪唑类三氟甲磺酸盐离子液体可以采用市售产品,也可以采用本领域常规的合成该类离子液体的合成方法自行合成得到。
27、示例性的,1-丁基-3-甲基咪唑三氟甲磺酸盐、1,3-二甲基咪唑三氟甲磺酸盐可采用市售产品,cas号分别为174899-66-2、121091-30-3。
28、1,3-二丁基咪唑三氟甲磺酸盐可采用如下方法制备得到:
29、将1-丁基咪唑和溴丁烷加入甲苯中,混合均匀,回流反应2h~3h,反应结束后旋蒸去除甲苯,得1,3-二丁基咪唑氢溴酸盐粗品;将1,3-二丁基咪唑氢溴酸盐粗品溶于水中,加入三氟甲磺酸钾的水溶液,搅拌30min~40min,然后加入二氯甲烷萃取,将有机相进行水洗,旋蒸去除溶剂,得1,3-二丁基咪唑三氟甲磺酸盐。
30、优选的,所述咪唑类三氟甲磺酸盐离子液体的加入量为式(i)所示的二醇类化合物质量的3%~10%。
31、优选的,s1中,所述式(i)所示的二醇类化合物与式(ⅱ)所示的醛类化合物的摩尔比为1:1~1.2。
32、优选的,s1中,所述第一溶剂与式(i)所示的二醇类化合物的体积质量比为(3~5)ml:1g。
33、优选的,s1中,所述第一溶剂为甲苯或环己烷中至少一种。
34、优选的,s1中,所述脱水、转位反应的时间为1h~4h。
35、优选的反应条件可促进脱水反应和转位反应的充分进行,提高式(ⅲ)所示的化合物的收率。
36、优选的,所述式(i)所示的二醇类化合物与式(ⅱ)所示的醛类化合物的反应结束后具体包括如下后处理步骤:
37、向所述式(i)所示的二醇类化合物与式(ⅱ)所示的醛类化合物反应结束后的反应液中加入水,分液,去除水相,旋蒸去除溶剂,得式(ⅲ)所示的化合物。
38、优选的,s2中,所述碱金属盐为碳酸钾、碳酸钠、碳酸铯、氟化钾、碳酸氢钾或碳酸氢钠中至少一种。
39、优选的,s2中,所述钯盐为四(三苯基膦)钯、氯化钯或醋酸钯中至少一种。
40、优选的,s2中,所述第二溶剂为甲苯、n,n-二甲基甲酰胺或乙醇中至少一种。
41、优选的,s2中,所述钯盐与式(ⅳ)所示的苯硼酸类化合物的比例为(0.1~1)g:1mol。
42、优选的,s2中,所述碱金属盐与式(ⅳ)所示的苯硼酸类化合物的摩尔比为1~5:1。
43、优选的,s2中,所述第二溶剂与式(ⅳ)所示的苯硼酸类化合物的体积质量比为(3~10)ml:1g。
44、优选的,s2中,所述水与碱金属盐的质量比为1~3:1。
45、优选的,s2中,所述式(ⅲ)所示的化合物与式(ⅳ)所示的苯硼酸类化合物的摩尔比为1:1~1.2。
46、优选的,s2中,所述铃木反应的时间为2h~6h。
47、采用优选的反应条件,如反应温度、催化剂、溶剂以及各原料的加入量等,有利于提高原料的利用率,降低副反应的发生,从而提高反式-1,3-二氧六环类液晶化合物的收率和纯度,使收率达90%以上,纯度可达99.9%以上。
48、优选的,所述式(ⅲ)所示的化合物与式(ⅳ)所示的苯硼酸类化合物的反应结束后具体包括如下后处理步骤:
49、向所述式(ⅲ)所示的化合物与式(ⅳ)所示的苯硼酸类化合物反应结束后的反应液中加入水,分液,去除水相,旋蒸去除溶剂,得到粗品;将粗品溶于甲醇和甲苯的混合溶剂中,重结晶,干燥,得到式(ⅴ)所示的反式-1,3-二氧六环类液晶化合物。
50、进一步地,所述甲醇的加入量为粗品质量的4~6倍,甲苯的加入量为粗品质量的1~2倍。
51、进一步地,所述重结晶的温度为-8℃~-12℃,重结晶的时间为10h~14h。
52、本发明提供的反式-1,3-二氧六环类液晶化合物的制备方法,采用先进行脱水反应再进行铃木反应的工艺路线,在脱水反应中引入了咪唑类三氟甲磺酸盐离子液体作为催化剂,实现了脱水反应和转位反应的同时进行,极大地提高了反式-1,3-二氧六环类液晶化合物的收率和纯度,产品收率可达90%以上,纯度可达99.9%以上,且操作简单,生产效率高,生产成本低,适用于工业化生产应用,推广价值极高。
- 还没有人留言评论。精彩留言会获得点赞!