来自牦牛血的新型降血糖肽、发掘方法及应用
本发明涉及生物活性肽,特别涉及一种来自牦牛血的新型降血糖肽、发掘方法及应用。
背景技术:
1、糖尿病是一种血糖升高的慢性代谢疾病,通常与肥胖、心血管疾病、神经退行性疾病及慢性炎症有关。据估计,到2035年,全球糖尿病患者人数可能超过5.92亿。二肽基肽酶iv(dpp-iv)是一种糖蛋白,具有裂解肠降血糖素(如葡萄糖依赖性促胰岛素肽、胰高血糖素样肽-1)的活性,通过促进胰岛素分泌在血糖调节中起关键作用。因此,抑制dpp-iv的生物活性是改善糖尿病患者或高血糖人群健康状态的重要策略。目前,许多具有dpp-iv活性抑制能力的药物已经被开发出来并广泛用于糖尿病患者的血糖调节,但其中大多数都伴有不良反应。公开号为“cn107337674a”的专利文献,公开了用作dpp-iv抑制剂的四氢吡喃胺衍生物、其药物组合物和制剂以及用途;该药剂具有良好的dpp-iv抑制活性和优异的药效学性能,以及较低的毒性,但是人体服用后仍有比较大的不良反应。多肽是一种天然来源的低分子量生物活性物质,被认为是其潜在的安全替代物之一。国内外学者已经从骨胶原蛋白、卵清蛋白、油菜籽、鱼皮、牛皮等动植物蛋白及加工副产物中广泛地分离和鉴定出多种dpp-iv抑制肽,如el、er、ka等。这些多肽与dpp-iv之间的相互作用也被广泛研究,但其抑制机制尚不完全清楚。
2、牦牛(bos mutus)是主要生存在海拔>3000米的青藏高原地区的特色物种,被誉为“沙漠之舟”。近年来,牦牛肉因其高蛋白、低脂肪、高多不饱和脂肪酸等特性备受广大消费者的青睐。同时,牦牛骨、血、皮、内脏等主要加工副产物也被认为是一种低成本和可持续的天然资源,可广泛用于制备生物活性化合物或功能性食品(如生物活性肽和矿物质)。血红蛋白是加工副产物血中的主要蛋白质之一,由珠蛋白和血红素-铁复合物构成。珠蛋白具有产生dpp-iv抑制肽等多种生物活性肽的潜力,血红素-铁复合物则具有较高的铁生物利用率。然而,由于具有较高的铁含量,牦牛血多被用于铁补充剂的提取和制备,而牦牛血红蛋白作为前体物质产生dpp-iv抑制肽的潜力及方法尚未被挖掘和报道。
3、另一方面,发现新型生物活性肽的传统技术途径通常包括酶解、分离、纯化和鉴定,这是一个高耗时、高成本和低产量的过程。最近,随着生物信息学的发展,数据库辅助的计算机模拟方法已经成功地应用于预测和设计具有不同活性的生物活性肽,如dpp-iv抑制、ace抑制肽、抗氧化肽等。此外,分子对接也广泛用于模拟多肽-受体蛋白相互作用,并有助于进一步理解多肽的靶向作用机制。与传统策略相比,计算机辅助筛选和分子对接的应用可以大大节省挖掘新型生物活性肽的时间和成本。公开号为“cn113035291a”的专利文献,公开了一种计算机辅助药物设计dpp-iv抑制肽的方法、dpp-iv抑制肽及其应用;该方法包括建立数据库并划分成内部训练集和外部测试集;构建数据库中多肽的结构;多肽与dpp-iv进行分子对接以选出评分最高的构象;以三肽ipi作为模板分子并以肽键为公共骨架进行叠合;手动调节各个肽的键角提高模型拟合度;用训练集算出测试集中多肽的ic50,并与实验得出的ic50对比;然后导出训练集的等势图来指导设计dpp-iv抑制肽;最后得到新型dpp-iv抑制肽。但是,其筛选的准确性仍然不够好,在筛选过程中会存在遗漏问题。
技术实现思路
1、本发明为了解决现有针对糖尿病患者和高血糖人群的dpp-iv抑制物研究过程中所存在的上述技术问题,提供了一种来自牦牛血的新型降血糖肽、发掘方法及应用,它具有无不良反应、筛选准确性较好和节本增效的特点。
2、本发明的第一种技术方案:来自牦牛血的新型降血糖肽,所述降血糖肽为dev;所述降血糖肽的氨基酸序列如seq id no:1所示;所述降血糖肽的分子式为c14h23n3o8;所述降血糖肽的分子结构式为,
3、
4、本发明中的降血糖肽从牦牛血红蛋白中分离得到,牦牛血红蛋白是牦牛血液中的重要蛋白质资源和生物活性肽的优质来源;本发明中的降血糖肽与dpp-iv具有较高的亲和力,能形成稳定的配体-受体复合物,对dpp-iv具有良好的抑制作用;本发明中的降血糖肽分子量较低,<500da;具有较高的疏水性(14.71kcal/mol)和水溶性(17.78mol/ml),感官上呈鲜味、酸味;等电点为3.01,在ph=7的中性水溶液中带有2个净负电荷;人体肠道吸收概率(hia)接近100%,人体口服生物利用度(hob)为28%,表明具有较高的胃肠道吸收率和口服生物利用率;本发明中的降血糖肽对dpp-iv活性的半数最大抑制浓度(ic50值)为339.45μmol/l,能通过较强的氢键作用和静电引力与dpp-iv活性位点s2口袋的核心残基结合,结合力很强,对dpp-iv的生物活性具有很好的抑制性能,作为功能性食品或配料在控制血糖升高方面具有很好的应用前景。
5、本发明的第二种技术方案:从牦牛血中发掘新型降血糖肽的方法,包括以下步骤,
6、(a)获得牦牛血红蛋白序列,如seq id no:2所示;
7、(b)通过组合蛋白酶对步骤(a)中牦牛血红蛋白序列进行计算机虚拟酶解后得到多肽序列,如seq id no:3所示;
8、(c)将步骤(b)中的多肽序列逐个与多肽数据库中已知的降血糖肽和同行评审文献报道的降血糖肽进行序列比对,其中与两者序列均不同的多肽,即为潜在新型降血糖肽的筛选肽;
9、(d)选用dpp-iv晶体结构,并对dpp-iv晶体结构进行预处理;
10、(e)构建步骤(c)中所有筛选肽的3d结构,并对构建出的筛选肽3d结构进行预处理;
11、(f)将步骤(e)预处理后的筛选肽3d结构与步骤(d)预处理后的dpp-iv晶体结构进行分子对接,其中能与dpp-iv成功对接且非键结合能为负的筛选肽即为潜在新型降血糖肽的候选肽;
12、(g)将步骤(f)中的候选肽进行固相合成后,得候选新型降血糖肽的合成肽;
13、(i)测定步骤(g)中所有合成肽不同浓度下的dpp-iv抑制率,得到所有合成肽对dpp-iv的半数最大抑制浓度ic50值;
14、(j)选取步骤(i)中ic50值≤1mmol/l的合成肽,即为来自牦牛血的新型降血糖肽。
15、本发明首先获得牦牛血红蛋白序列,牦牛血红蛋白是牦牛血液中的主要蛋白质成分之一,同时也是一种优质的生物活性肽资源,增大了牦牛加工副产物血的应用范围;由于牦牛血红蛋白本身是无活性的,本发明通过组合蛋白酶对牦牛血红蛋白进行计算机虚拟酶解后得到多肽序列,与单一蛋白酶酶解相比,组合蛋白酶酶解能增加酶解产物的降血糖肽频率值,促使更多的生物活性多肽释放,从而使后续过程中能筛选到更多的具有潜在dpp-iv活性抑制能力的新型肽;本发明将酶解后得到的多肽序列逐个与多肽数据库中已知的降血糖肽序列和同行评审文献报道的中已知的降血糖肽序列进行比较,筛选出序列均不同的潜在新型降血糖肽,整个筛选过程全面,得到的筛选肽代表性强,准确性高;选用dpp-iv作为分子对接对象,将能更好地反映本发明降血糖肽对dpp-iv的抑制性能,更好地反映临床使用时的降血糖效果,对dpp-iv晶体结构进行预处理也是为了后续与筛选肽能更好地对接;构建所有筛选肽的3d结构,后续逐个与dpp-iv晶体结构进行分子对接,将能更准确地得出每个筛选肽对dpp-iv的抑制效果,从而遴选出效果更好的筛选肽,将每个筛选肽构建出的3d结构进行预处理,也是为了能与dpp-iv晶体结构更好地进行分子对接;本发明将预处理后的dpp-iv晶体结构分别与预处理后的筛选肽3d结构进行分子对接,通过比对获得所需的降血糖肽的候选肽,整个获得过程逻辑严密,结果直观,具有很好的准确性;本发明将降血糖肽的候选肽进行固相合成后,得到降血糖肽的合成肽,测定所有合成肽在不同浓度下的dpp-iv抑制率,dpp-iv抑制率能更准确和科学的反映合成肽对dpp-iv的抑制效果,并得到所有合成肽对dpp-iv的半数最大抑制浓度ic50值,最终选取ic50值≤1mmol/l的合成肽,作为来自牦牛血的新型降血糖肽,整个获得过程科学合理,准确性较好,应用性也较好。
16、作为优选,还包括步骤,(h)计算和分析步骤(g)中所有合成肽的理化特性和潜在生物可及性指标。计算和分析出所有合成肽的理化特性和潜在生物可及性指标,最终选取理化特性好、潜在生物可及性指标高的合成肽,能更准确和科学的反映合成肽对dpp-iv的抑制效果。
17、作为优选,所述多肽数据库为biopep-uwm数据库、pepbank数据库、信号肽数据库、dbaasp数据库、apd3数据库、cppsite 2.0数据库、tide antigen database、peptideatlas数据库、thpdb、tumorhope、plantpepdb数据库或neuropep数据库。
18、作为优选,所述同行评审文献报道的降血糖肽为专利文献公开的降血糖肽、论文文献公开的降血糖肽、期刊杂志公开的降血糖肽、展品展览公开的降血糖肽或电视广告公开的降血糖肽。
19、作为优选,选用的dpp-iv晶体结构为人dpp-iv晶体结构或动物dpp-iv晶体结构。
20、作为优选,所述步骤(a)中,通过uniprot knowledgebase数据库获得牦牛血红蛋白序列。
21、所述牦牛血红蛋白序列包括牦牛α1-珠蛋白序列、牦牛α2-珠蛋白序列、牦牛β-珠蛋白序列、牦牛ζ-珠蛋白序列、牦牛ε1-珠蛋白序列、牦牛ε2-珠蛋白序列和牦牛μ-珠蛋白序列;所述牦牛α1-珠蛋白序列、牦牛α2-珠蛋白序列、牦牛β-珠蛋白序列、牦牛ζ-珠蛋白序列、牦牛ε1-珠蛋白序列、牦牛ε2-珠蛋白序列和牦牛μ-珠蛋白序列在uniprot knowledgebase数据库中的登记号分别为p01967、p01968、p02072、a0a6b0qz80、l8hug2、l8hwl4和a0a8b9xkr7。整个获得过程方便快捷,省时省力,准确性也较好,具有准确、快速和具体的特点。
22、作为优选,所述组合蛋白酶的获得包括以下步骤,
23、(b01)用多种蛋白酶对步骤(a)选定牦牛血红蛋白序列进行计算机虚拟酶解;
24、(b02)待步骤(b01)酶解完成后,得出各蛋白酶对选定牦牛血红蛋白序列的降血糖肽频率值;
25、(b03)根据步骤(b02)降血糖肽频率值大小,选定降血糖肽频率值≥0.05的蛋白酶;
26、(b04)将步骤(b03)选定降血糖肽频率值≥0.05的蛋白酶组合后,再次对步骤(a)选定牦牛血红蛋白序列进行计算机虚拟组合酶解;
27、(b05)待步骤(b04)计算机虚拟组合酶解完成后,得出各组合蛋白酶对选定牦牛血红蛋白序列的降血糖肽频率值,其中对应降血糖肽频率值最高的组合蛋白酶,即为所需的组合蛋白酶。先使用单一蛋白酶对牦牛血红蛋白进行虚拟酶解,获得每种蛋白酶酶解完全后的降血糖肽频率值,根据降血糖肽频率值大小,选定降血糖肽频率值高的几种单一蛋白酶,再将选出的几种单一蛋白酶多种组合后再对牦牛血红蛋白进行酶解,并获得各组合蛋白酶酶解后的降血糖肽频率值,再根据降血糖肽频率值大小,获得最佳组合蛋白酶,整个组合蛋白酶的获得过程科学合理,逻辑周全,最终获得的组合蛋白酶对牦牛血红蛋白的酶解过程最好。
28、作为优选,所述步骤(b02)中,通过公式(1)获得降血糖肽频率值,
29、a=a/n (1)
30、其中,a表示降血糖肽频率值;a表示酶解后得到的降血糖肽的数目;n表示蛋白序列中的氨基酸残基数目。
31、作为优选,所述组合蛋白酶的获得过程中,通过biopep-uwm数据库中的profilesof potential biological activity工具和calculations工具,对不同蛋白酶的酶解结果使用公式(1)获得降血糖肽频率值。基于数据库辅助的计算机模拟方法获得降血糖肽频率值,省时省力,人力成本小,也快捷准确。
32、作为优选,所述步骤(b01)中,通过biopep-uwm数据库的enzyme(s)action工具或expasy在线平台的peptidecutter工具,用多种蛋白酶对步骤(a)选定牦牛血红蛋白序列进行计算机虚拟酶解。数据库辅助的计算机虚拟酶解过程,省时省力,快速高效。
33、作为优选,所述步骤(b01)中的蛋白酶种类包括19-胰凝乳蛋白酶c、组织蛋白酶g、糜蛋白酶、胰凝乳蛋白酶a、coccolysin、无花果蛋白酶、白细胞弹性蛋白酶、metridin、寡肽酶b、寡肽酶f、胰弹性蛋白酶ii、胰弹性蛋白酶、木瓜蛋白酶、胃蛋白酶、纤溶酶、蛋白酶k、蛋白酶p1、茎菠萝蛋白酶、枯草杆菌蛋白酶、嗜热菌蛋白酶和胰蛋白酶。种类合适,具有良好的代表性,使得最终得到的最佳组合蛋白酶结果具有良好的可信度。
34、作为优选,所述步骤(b03)中,选定降血糖肽频率值≥0.05的多种蛋白酶。降血糖肽频率值高的蛋白酶包括茎菠萝蛋白酶、胰弹性蛋白酶、钙蛋白酶2、无花果蛋白酶和木瓜蛋白酶等,对牦牛血红蛋白具有良好的酶解效果。
35、作为优选,所述步骤(b04)中的组合酶解为2~5种蛋白酶组合酶解。蛋白酶的组合种类可以为两种、三种、四种或五种组合,尽可能完全的组合试验,从而得到酶解程度最完全的组合蛋白酶。更优选,考虑到工作量,兼顾工作量和结果的完全性,可以进行两种或三种蛋白酶的组合酶解。
36、作为优选,所述步骤(b)中的组合蛋白酶为胰弹性蛋白酶和茎菠萝蛋白酶组合。经过逐个组合酶解后,根据降血糖肽频率值得出最佳的组合蛋白酶为胰弹性蛋白酶和茎菠萝蛋白酶的组合,具有很好的准确性和可信度。
37、作为优选,所述步骤(d)中,dpp-iv的晶体结构来自protein data bank数据库。从蛋白质数据库中直接获得,数据库辅助的方式,获得方便快捷;选用dpp-iv的晶体结构进行分子对接,分子对接的结果与直接作用于人体获得的结果类同,具有很好的可信度。先通过基于计算机模拟的分子对接得到数据,再通过体外试验作用于人体验证,相比于传统筛选、验证过程,更快捷,更准确。
38、作为优选,所述步骤(d)中的预处理为去除水分子、去除共结晶配体、添加氢原子和能量最小化。采用计算机中的prepare protein程序对dpp-iv晶体结构进行预处理,以去除水分子和共晶配体,添加氢原子,并最大限度地减少能量,使得后续的对接工作具有更准确的对接效果。
39、作为优选,所述步骤(e)中的预处理为添加氢原子、输入charmm力场和能量最小化。采用计算机discovery studio v2019(ds2019)软件中的build and edit protein工具构建所有筛选肽的晶体结构,计算机软件处理方式更快捷,更省力,所有筛选肽的三维晶体结构均能直观准确地构建出来;采用计算机ds2019软件中的smart minimizer算法工具对所有筛选肽晶体结构进行预处理,保证后续的对接工作更准确、更快速地进行。
40、作为优选,所述步骤(f)中,预处理后的dpp-iv晶体结构为受体,预处理后的筛选肽3d结构为配体。其中,将受体设定为刚性,将配体设定为柔性。预处理后的筛选肽晶体结构往预处理后的dpp-iv晶体结构上去配,和本发明中降血糖肽作用于人体后与人体的dpp-iv去结合类似,具有更准确的模拟效果,柔性的配体将进行灵活变动,最终良好地对接在刚性受体上。
41、作为优选,所述步骤(f)中,获得每个配体-受体最佳对接构象的非键结合能;其中能与dpp-iv成功对接且非键结合能为负的筛选肽,即为候选的新型降血糖肽的候选肽。配体与受体间的最小结合力用-cdocker interaction energy(-cie)表示;配体-受体复合物稳定性通过-cdocker energy(-ce)反映;较高的-cie和-ce通常与配体-受体相互作用中的高能量释放相关,意味着配体与受体之间具有较高的结合力,并能形成较为稳定的配体-受体复合物。通过-ce值和-cie值来选择候选的新型降血糖肽,具体选择-ce值和-cie值均较高的筛选肽作为所需的候选肽,具有更好的准确性,所选择的候选肽能与dpp-iv结合形成非常稳定的配体-受体复合物,对dpp-iv具有良好的抑制作用。
42、作为优选,所述步骤(g)中,将步骤(f)中的候选肽序列通过fmoc保护的氨基酸合成法进行固相合成后,得潜在新型降血糖肽的合成肽。通过fmoc保护的氨基酸合成法将候选肽进行固相合成,具有精准、稳定和高效的合成效果。
43、作为优选,所述步骤(g)中,固相合成条件为,
44、流动相a,0.1%tfa溶于100%乙腈;流动相b,0.1%tfa溶于100%;sinochromods-bp柱,5μm孔径,250mm×4.6mm;注射体积,5μl;检测波长,220nm;流速,1.0ml/min。限定固相合成条件下能将候选肽更稳定高效地合成为合成肽。
45、作为优选,所述步骤(g)固相合成后,对合成肽进行洗脱。洗脱后能使得最终得到的合成肽具有更高的纯度,减少固相合成过程中其他杂质对纯度的影响。
46、作为优选,所述洗脱流程是从10%的流动相a开始,梯度上升至35%的流动相a并保持20min~30min,然后梯度上升至100%的流动相a保持0.1min~0.5min完成。更优选,所述洗脱流程是从10%的流动相a开始,梯度上升至35%的流动相a并保持25min,然后梯度上升至100%的流动相a并保持0.3min完成。采用梯度洗脱流动相的方式,每个梯度具有相应时间的限定,在保证洗脱完全的同时,也使得整个洗脱时间不至于太久。
47、作为优选,所述步骤(g)中,通过高效液相色谱法(hplc)测定合成肽的纯度,通过质谱法(ms)测定合成肽的分子量。高效液相色谱法对降血糖肽的合成肽纯度测定,能保证测定结果更快速,也更准确;质谱法对合成肽分子量的测定,能保证测定结果更快速,也更精确。
48、作为优选,所述合成肽的纯度>95%。采用本发明条件进行固相合成和洗脱,能使得最终得到的合成肽具有较高的纯度。
49、作为优选,所述步骤(h)中的理化特性和潜在生物可及性指标,包括疏水性、净电荷、等电点、潜在毒性、水溶性、人体肠道吸收率、人体口服生物利用度和感官特性。对具体性能的测定,能综合评估候选肽或合成肽是否能作为功能性食品原料在血糖调节中应用。
50、作为优选,通过pepdraw服务器计算合成肽的疏水性、净电荷和等电点。采用计算机pepdraw服务器计算合成肽的疏水性、净电荷和等电点,省时省力,方便快捷,准确性也很好。
51、作为优选,通过toxinpred工具,基于支持向量机方法,获得合成肽的潜在毒性;其中支持向量机的阈值为0。基于支持向量机方法,采用计算机toxinpred工具获得合成肽的潜在毒性值,省时省力,方便快捷,准确性也很好。
52、作为优选,通过swissadme网络工具,基于esol模型的拓扑方法,获得合成肽的水溶性。基于esol模型的拓扑方法,采用计算机swissadme网络工具获得合成肽的水溶性,省时省力,方便快捷,准确性也很好。
53、作为优选,通过idrug平台获得合成肽的人体肠道吸收率(hia)和人体口服生物利用度(hob)。通过计算机idrug平台获得合成肽的hia和hob,省时省力,方便快捷,准确性也很好。
54、作为优选,通过biopep-uwm数据库的sensory peptides and amino acids工具和calculations工具,获得合成肽的感官特性。通过计算机biopep-uwm数据库的sensorypeptides and amino acids工具和calculations工具,获得合成肽的感官特性,省时省力,方便快捷,准确性也很好。
55、作为优选,所述步骤(i)中,对dpp-iv抑制率的测定方法为体外化学分析、细胞模型评价或动物模型评价。
56、作为优选,所述步骤(i)中,对dpp-iv抑制率的测定包括以下步骤,
57、(i01)使用适量tris-hcl缓冲液对合成肽进行稀释;
58、(i02)取适量步骤(i01)中稀释的合成肽与适量gly-pro-p-硝基苯胺在微孔板中混合,并进行温育;
59、(i03)将步骤(i02)温育后的混合物加入适量dpp-iv溶液中进行反应;
60、(i04)在步骤(i03)中的反应液中加入适量乙酸钠缓冲液使反应停止;
61、(i05)测定步骤(i02)和步骤(i04)溶液的吸光度;
62、(i06)通过公式(3)得到对dpp-iv的抑制率,
63、
64、其中,di表示对dpp-iv的抑制率,单位为%;as表示dpp-iv溶液、gly-pro-p-硝基苯胺和合成肽存在下的吸光度(样品反应组);asc表示仅有tris-hcl缓冲液、gly-pro-p-硝基苯胺和合成肽的吸光度(样品对照组);anr表示仅有dpp-iv溶液和gly-pro-p-硝基苯胺的吸光度(阴性反应组);anc表示仅有gly-pro-p-硝基苯胺的吸光度(阴性对照组)。tris-hcl缓冲液能将合成肽分散,创造一个较为缓和的反应环境;
65、gly-pro-p-硝基苯胺是dpp-iv的反应底物,能快速、精准地反映出dpp-iv的活性;乙酸钠缓冲液能让反应物失活,从而使反应停止;吸光度能准确反映不同物质存在下的dpp-iv活性存留情况;通过公式(3)能科学、准确的反映出合成肽对dpp-iv的具体抑制情况,相当于在体外将本发明合成肽对dpp-iv的具体抑制情况再次进行了评估,科学性严密,可信度较高,并节约了试验成本。
66、作为优选,所述步骤(i01)中,tris-hcl缓冲液的取用量为80mmol/l~120mmol/l。更优选,所述步骤(i01)中,tris-hcl缓冲液的取用量为90mmol/l~110mmol/l。更优选,所述步骤(i01)中,tris-hcl缓冲液的取用量为100mmol/l。在将合成肽充分分散的同时,不至于用量过多对后续的吸光度产生影响。
67、作为优选,所述步骤(i01)中,tris-hcl缓冲液的ph值为7.5~8.5。更优选,所述步骤(i01)中,tris-hcl缓冲液的ph值为8。限定ph值的tris-hcl缓冲液将对合成肽具有更好的分散效果。
68、作为优选,所述步骤(i01)中,将合成肽稀释至0.5μg/ml~10mg/ml。更优选,所述步骤(i01)中,将合成肽稀释至1μg/ml~4.5mg/ml。更优选,所述步骤(i01)中,将合成肽稀释1.5μg/ml~4.0mg/ml。更优选,所述步骤(i01)中,将合成肽稀释至2μg/ml~3.5mg/ml。更优选,所述步骤(i01)中,将合成肽稀释至2.5μg/ml~3.0mg/ml。更优选,所述步骤(i01)中,将合成肽稀释至3μg/ml~2.5mg/ml。更优选,所述步骤(i01)中,将合成肽分别稀释至3.125μg/ml、6.25μg/ml、12.5μg/ml、125μg/ml和1.25mg/ml。限定浓度范围的合成肽,将能被后续更好地处理,将能与dpp-iv溶液更充分地反应。
69、作为优选,所述步骤(i02)中,合成肽的取用量为20μl~30μl。更优选,所述步骤(i02)中,合成肽的取用量为22μl~28μl。更优选,所述步骤(i02)中,合成肽的取用量为25μl。此处限定取用量的合成肽将能与限定取用量的gly-pro-p-硝基苯胺良好地混合温育。
70、作为优选,所述步骤(i02)中,所述gly-pro-p-硝基苯胺的取用量为20μl~30μl。更优选,所述步骤(i02)中,所述gly-pro-p-硝基苯胺的取用量为22μl~28μl。更优选,所述步骤(i02)中,所述gly-pro-p-硝基苯胺的取用量为25μl。此处限定取用量的gly-pro-p-硝基苯胺将能与限定取用量的合成肽良好地混合温育。
71、作为优选,所述步骤(i02)中,所述gly-pro-p-硝基苯胺的浓度为0.15mmol/l~0.25mmol/l。更优选,所述步骤(i02)中,所述gly-pro-p-硝基苯胺的摩尔浓度为0.2mmol/l。此处限定浓度的gly-pro-p-硝基苯胺结合其限定取用量,将能与限定取用量的合成肽良好地混合温育。
72、作为优选,所述步骤(i02)中,所述微孔板为96孔微孔板。将合成肽与gly-pro-p-硝基苯胺在96孔微孔板上温育,能方便后续对溶液吸光度的测定。
73、作为优选,所述步骤(i02)中,所述温育时间为5min~15min。更优选,所述步骤(i02)中,所述温育时间为8min~12min。更优选,所述步骤(i02)中,所述温育时间为10min。此处对温育时间的限定,在保证温育充分的同时,兼顾时效性。
74、作为优选,所述步骤(i02)中,所述温育温度为36℃~38℃。更优选,所述步骤(i02)中,所述温育温度为36.2℃~37.5℃。作为优选,所述步骤(i02)中,所述温育温度为37℃。此处对温育温度的限定,近似于人体温度,能更好地模拟人类dpp-iv的化学反应环境。
75、作为优选,所述步骤(i03)中,dpp-iv溶液的取用量为45μl~55μl。作为优选,所述步骤(i03)中,dpp-iv溶液的取用量为48μl~52μl。作为优选,所述步骤(i03)中,dpp-iv溶液的取用量为50μl。此处对dpp-iv溶液取用量的限定与合成肽取用量相适应,以能够充分完全反应为准。
76、作为优选,所述步骤(i03)中,dpp-iv溶液的浓度为2.0u/l~3.0u/l。作为优选,所述步骤(i03)中,dpp-iv溶液的浓度为2.2u/l~2.7u/l。作为优选,所述步骤(i03)中,dpp-iv溶液的浓度为2.5u/l。此处对dpp-iv溶液浓度的限定与合成肽浓度相适应,以能够充分完全反应为准。
77、作为优选,所述步骤(i03)中,所述温育温度为36℃~38℃。更优选,所述步骤(i03)中,所述温育温度为36.2℃~37.5℃。作为优选,所述步骤(i03)中,所述温育温度为37℃。此处对温育温度的限定,近似于人体温度,能更好地模拟人类dpp-iv的化学反应环境。
78、作为优选,所述步骤(i03)中,反应时间为40min~80min。作为优选,所述步骤(i03)中,反应时间为50min~70min。作为优选,所述步骤(i03)中,反应时间为60min。此处对反应时间的限定,是在保证反应完全同时,兼顾时效性。
79、作为优选,所述步骤(i04)中,乙酸钠缓冲液的加入量为90μl~110μl。作为优选,所述步骤(i04)中,乙酸钠缓冲液的加入量为95μl~105μl。作为优选,所述步骤(i04)中,乙酸钠缓冲液的加入量为100μl。此处对乙酸钠缓冲液加入量的限定,是在保证让反应物快速失活,使反应快速停止的同时,不至于加入量过多对后续的吸光度测试造成影响。
80、作为优选,所述步骤(i04)中,乙酸钠缓冲液的浓度为0.8m~1.2m。作为优选,所述步骤(i04)中,乙酸钠缓冲液的浓度为0.9m~1.1m。作为优选,所述步骤(i04)中,乙酸钠缓冲液的浓度为1m。此处对乙酸钠缓冲液的浓度的限定,是结合乙酸钠缓冲液的加入量与需要灭活的反应物来定的,是在保证让反应物快速失活,使反应快速停止的同时,不至于加入量过多对后续的吸光度测试造成影响。
81、作为优选,所述步骤(i04)中,乙酸钠缓冲液的ph为3.5~4.5。作为优选,所述步骤(i04)中,乙酸钠缓冲液的ph为3.7~4.2。作为优选,所述步骤(i04)中,乙酸钠缓冲液的ph为4。此处对乙酸钠缓冲液ph的限定,是为了让反应物快速失活。
82、作为优选,所述步骤(i05)中,通过spectramax 190酶标仪在405nm处测定步骤(i04)反应后溶液的吸光度。通过spectramax190酶标仪在405nm处测定的溶液吸光度,具有更好的准确性。
83、作为优选,所述步骤(i)中,合成肽的浓度范围为0~10mg/ml。更优选,所述步骤(i)中,合成肽的浓度范围为1μg/ml~5mg/ml。更优选,所述步骤(i)中,合成肽的浓度范围为2.5μg/ml~2.5mg/ml。更优选,所述步骤(i)中,合成肽的浓度范围为3.125μg/ml~1.25mg/ml。
84、作为优选,所述步骤(i)中,通过s型量效关系方程(2),采用非线性回归分析法获得半数最大抑制浓度ic50值,
85、y=100/{10^[(lgic50-lgx)×hill slope]+1}(2)
86、式中,y表示多肽对dpp-iv的抑制率,单位为%;x表示多肽的检测浓度,单位为mg/ml;ic50为多肽的半数最大抑制浓度,单位为mg/ml。通过s型量效关系方程得到的半数最大抑制浓度具有更好的准确性。
87、作为优选,所述步骤(j)中,选取ic50值≤1mmol/l且无毒性和/或水溶性>0.1mol/l和/或人体口服生物利用度>10%的合成肽为来自牦牛血的新型降血糖肽。
88、本发明的第三种技术方案:从牦牛血中发掘新型降血糖肽作为原料在制备血糖调节功能性食品中的应用。本发明中的新型降血糖肽分子量<500da,较低;具有较高的疏水性(14.71kcal/mol);具有良好的水溶性(17.78mol/ml);具有鲜味、酸味,有可接受的感官特性;等电点为3.01,在ph=7的中性水溶液中带有2个净负电荷;人体肠道吸收概率hia接近100%,人体口服生物利用度(hob)为28%,表明具有较高的胃肠道吸收率和口服生物利用率,作为原料制备血糖调节功能性食品具有很好的应用前景。
89、本发明具有如下有益效果:
90、(1)降血糖肽从牦牛血红蛋白中分离得到,牦牛血红蛋白是牦牛血液中的重要蛋白质资源和生物活性肽的优质来源,将具有更广泛的应用;
91、(2)降血糖肽在抑制dpp-iv的过程中,与dpp-iv具有高结合亲和力,能形成非常稳定的配体受体复合物,对dpp-iv具有良好的抑制作用;
92、(3)降血糖肽分子量<500da,较低;具有较高的疏水性(14.71kcal/mol);具有良好的水溶性(17.78mol/ml);具有鲜味、酸味,有可接受的感官特性;等电点为3.01,在ph=7的中性水溶液中带有2个净负电荷;人体肠道吸收概率hia接近100%,人体口服生物利用度(hob)为28%,表明具有较高的胃肠道吸收率和口服生物利用率,作为原料制备血糖调节功能性食品具有很好的应用前景;
93、(4)降血糖肽对dpp-iv的半数最大抑制浓度ic50值为339.45μmol/l,表明对dpp-iv具有优良抑制性能;
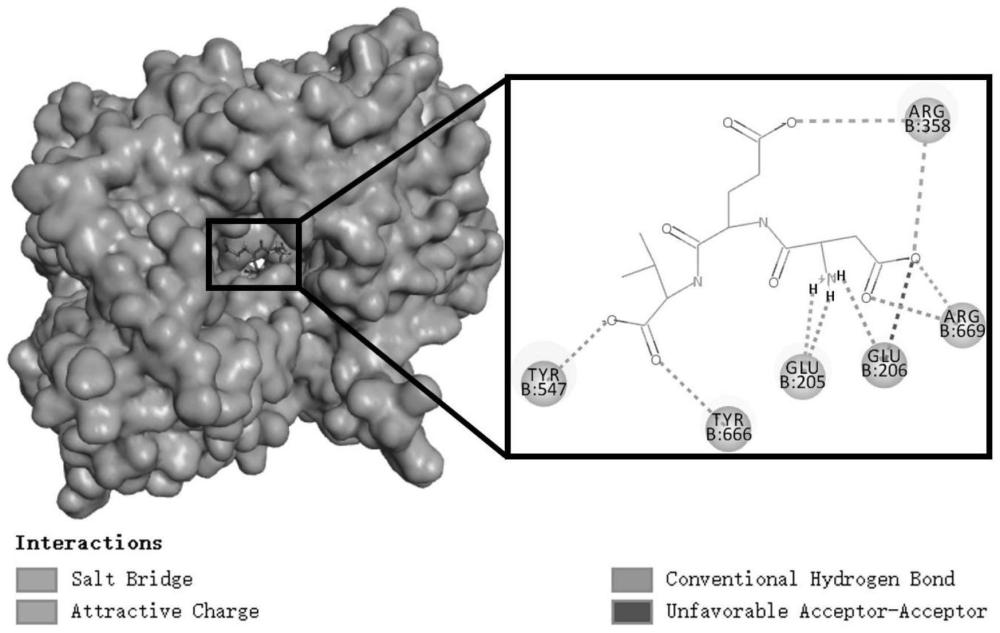
94、(5)降血糖肽通过较强的氢键作用和静电引力与dpp-iv活性位点s2口袋的核心残基结合,结合力很强,对dpp-iv具有很好的抑制性能,在控制血糖升高方面能发挥很好的作用。
- 还没有人留言评论。精彩留言会获得点赞!