一种两亲性聚多肽及其制备方法和应用
本发明涉及材料,尤其涉及一种两亲性聚多肽及其制备方法和应用。
背景技术:
1、近年来,纳米材料作为纳米药物被广泛应用于体内治疗和诊断应用。由于具有较高的表面自由能,这些纳米材料在静脉注射给药后与血液成分接触时,会自发地吸附生物分子。例如血清蛋白与纳米粒子表面结合形成生物分子涂层,称为蛋白质冠。蛋白质冠的形成显著改变了由此产生的纳米药物的生物物理化学性质,对细胞摄取、组织靶向、免疫反应以及单核吞噬细胞系统(mps)隔离等方面产生了深远的影响。在提高药物传递效率和最大限度地提高治疗效果的长期追求中,了解蛋白质冠形成机制以及通过调控纳米生物界面来利用蛋白质冠组分已成为研究热点。除了对纳米载体的物理化学参数进行工程设计,如化学成分、大小、形状和zeta电位,人们还广泛致力于用防污材料(包括聚乙二醇(peg)、两性离子聚合物、低声压蛋白等)对纳米药物进行表面功能化。由此产生的具有防污涂层的纳米药物增强了胶体稳定性,延长了血液循环时间,减少了mps清除率,从而优化了治疗效果,减少了副作用。尽管取得了很大的成就,但人们普遍认为这些防污聚合物并不能完全消除蛋白质冠的形成,这为通过减少血清蛋白吸附来调节纳米药物上的蛋白质冠提供了一种可行的手段。然而,是否可以通过主动调控吸附血清蛋白种类及含量来提高治疗性能仍然是一个悬而未决的问题,这为在纳米药物上设计蛋白质冠提供了一种独特的方法。
2、血清白蛋白是血液中含量最高的血浆蛋白(如人血清白蛋白为35-50g/l),参与许多关键的病理过程,如营养物质的运输,这一过程由其多个配体结合位点和细胞受体参与促进。血清白蛋白也被证明在许多类型的肿瘤中积累,常见的肿瘤过表达白蛋白结合受体如糖蛋白60(gp60)、分泌的酸性蛋白和半胱氨酸(sparc)。事实上,血清白蛋白已成功用于递送成像或治疗药物,如紫杉醇伊文思蓝(evans blue)、多肽和sirna,并显示出独特的优势,包括增加生物稳定性、扩大循环、靶向肿瘤等。阿霉素(dox)的马来酰亚胺基团功能化衍生物aldoxorubicin在静脉注射后立即与血清白蛋白上的半胱氨酸34(cys34)的巯基结合,与dox相比,显示出更好的治疗效果和较低的心脏毒性。我们推测血清白蛋白也可以用于纳米药物表面的功能化,以原位调节蛋白冠的组成,这可能会利用内源性白蛋白的长血液循环和肿瘤靶向能力提高治疗效果。
3、在用于诊断治疗的各种纳米药物中,多肽和多肽/合成聚合物复合物因其可规模化生产、易于功能化、可递送不同治疗药物、良好的生物相容性和独特的生物降解性而受到越来越多的关注。为了使基于多肽的纳米药物能够特异性响应病理微环境,人们引入了大量的刺激响应键,使得合成的纳米药物具有良好的血液循环稳定性,并在活性氧(ros)、酸性ph和酶过表达等病理微环境下触发药物释放。在这种情况下,肿瘤酸性已被认为是重要的癌症特征之一,ph响应性化学键如腙和缩氨基脲已通过利用细胞外肿瘤组织和细胞内酸性细胞器(例如,内涵体和溶酶体)中的酸性ph得到广泛研究。
技术实现思路
1、有鉴于此,本发明要解决的技术问题在于提供一种两亲性聚多肽及其制备方法和应用,制备的两亲性聚多肽可实现与含醛/酮衍生物高效动态可逆的共价结合。
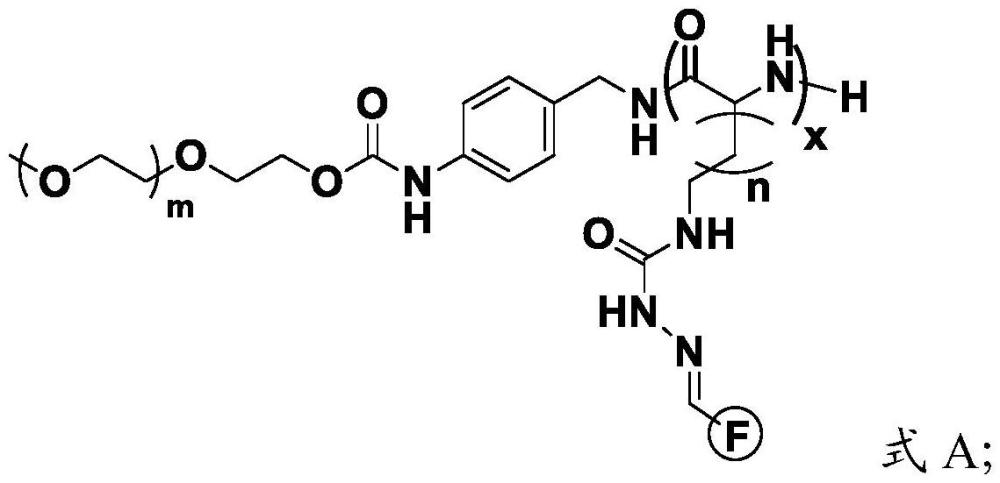
2、本发明提供了一种两亲性聚多肽,具有式a-d任一所示结构:
3、
4、
5、其中,n独立的选自1-3的整数;m独立的选自4-400的整数;x独立的选自5-100的整数;
6、r5选自以下任一结构:
7、
8、r6为h、c1~c5的烷基或卤素;优选为h、甲基、乙基、正丙基、异丙基、br或i。
9、上述m优选为45~112的整数。
10、上述x优选为5-80的整数。
11、上述n优选为2或3。
12、f表示键合的功能分子。包括但不限于键合的药物分子、造影剂、荧光探针等。上述f可以以化学键键合于式a-d结构中。所述化学键可以为脲酰腙、肟键中的任意一种。
13、可选的,所述f具有以下任一结构:
14、
15、r为h或c1~c5的烷基。优选为h、甲基、乙基、正丙基、异丙基、正丁基、异丁基或叔丁基。
16、上述f结构中,crgd表示具有靶向功能的五元环肽c(rgdfk)。
17、可选的,所述两亲性聚多肽的数均分子量为1000~500000。
18、本发明中,上述式a-d所示的两亲性聚多肽的单体如以下式a、式b所示:
19、
20、其中,r1为叔丁氧羰基(boc)或苄氧羰基(cbz),每个n独立地为1-3的任意整数。
21、本发明提供了上述式a-b所示两亲性聚多肽的制备方法,包括以下步骤:
22、s1)将式a所示单体或式b所示单体与式c1所示的链引发剂在溶剂中反应,得到中间体d1或中间体e1;
23、s2)脱去上述中间体d1的保护基r1,得到中间体f1;或脱去上述中间体e1的保护基r1,得到中间体g1;
24、s3)将中间体f1或中间体g1与含醛/酮基团的f衍生物进行反应,得到式a或式b所示的两亲性聚多肽;
25、
26、
27、其中r1为叔丁氧羰基(boc)或苄氧羰基(cbz),每个n独立地为1-3的整数,m为4-400的整数,x为5-100的整数。
28、上述m优选为45~112的整数。
29、上述x优选为5-80。
30、上述n优选为2或3。
31、上述含醛/酮基团的f衍生物为上述基团f中的连接位置被替换为醛基或酮基后得到的化合物。
32、可选的,上述步骤s1)中反应的溶剂为n,n-二甲基乙酰胺或二甲基亚砜。
33、可选的,上述步骤s1)中反应的温度为60~90℃。反应的时间为12h~2天。
34、可选的,上述步骤s2)中,当r1为叔丁氧羰基时,反应溶剂为三氟乙酸;当r1为苄氧羰基时,反应溶剂为甲醇。
35、可选的,上述步骤s2)中反应的温度为0~90℃,时间为12~24h。
36、可选的,上述步骤s3)中,反应的溶剂为二甲基亚砜。
37、可选的,上述步骤s3)中,反应的温度为25~40℃,反应的时间为5~24h。
38、上述聚合物接枝功能性小分子f效率较高,最高可达90%。
39、本发明提供了上述式c-d所示两亲性聚多肽的制备方法,包括以下步骤:
40、s11)将式a所示单体或式b所示单体与式c2所示的链引发剂在溶剂中反应,然后与苄基异氰酸酯反应,得到中间体d2或中间体e2;
41、s22)将上述中间体d2脱除保护基,得到中间体f2;或将上述中间体e2脱除保护基,得到中间体g2;
42、s33)将上述中间体f2或中间体g2和含醛/酮基团的f衍生物进行反应,得到式c或式d所示的两亲性聚多肽;
43、
44、
45、r5、r6范围同上。
46、r1为叔丁氧羰基(boc)或苄氧羰基(cbz),每个n独立地为1-3的整数,m为4-400的整数,x为5-100的整数。
47、上述m优选为45-112的整数。
48、上述x优选为5-80。
49、上述n优选为2或3。
50、上述含醛/酮基团的f衍生物为上述基团f中的连接位置被替换为醛基或酮基后得到的化合物。
51、可选的,上述步骤s11)中,式a所示单体或式b所示单体与式c2所示的链引发剂反应的溶剂选自n,n-二甲基乙酰胺或二甲基亚砜。反应的温度优选为60~90℃。反应的时间优选为12h~2天。
52、可选的,上述步骤s11)中,与苄基异氰酸酯反应的溶剂选自n,n-二甲基乙酰胺或二甲基亚砜。反应的温度优选为50~110℃。反应的时间优选为1~6h。
53、可选的,上述步骤s22)中,当r1为叔丁氧羰基时,反应溶剂为三氟乙酸;当r1为苄氧羰基时,反应溶剂为甲醇。
54、可选的,上述步骤s22)中反应的温度为0~90℃,时间为12~24h。
55、可选的,上述步骤s33)中,反应的溶剂为二甲基亚砜。
56、可选的,上述步骤s33)中,反应的温度为25~40℃,反应的时间为5~24h。
57、上述聚合物接枝功能性小分子f效率较高,最高可达90%。
58、本发明还提供了一种纳米粒子的制备方法,包括:
59、将上述两亲性聚多肽或上述制备方法制备的两亲性聚多肽溶解在有机溶剂中,采用共溶剂-加水法或闪沉法制备,得到纳米粒子。
60、上述共溶剂-加水法优选具体为:
61、将上述两亲性聚多肽溶解于有机溶剂中,搅拌过程中加入纯水,然后采用透析或减压蒸馏的方式除去有机溶剂,得到纳米粒子。
62、所述有机溶剂优选为二甲基亚砜、二氧六环或其以任意比例的混合物。
63、优选地,反应体系中,所述两亲性聚多肽的浓度为0.1-100mg/ml。
64、优选地,反应体系中,水的体积为所述有机溶剂体积的0.1~100倍。
65、优选地,体系中反应的温度为25-30℃。反应的时间为0.5~8h。
66、采用共溶剂-加水法制备的纳米粒子的粒径为几十到几百纳米,优选为100~400nm。
67、上述闪沉法优选具体为:
68、将上述两亲性聚多肽溶解于有机溶剂中,快速搅拌过程中将该溶有两亲性聚合物的有机溶液快速加入纯水,然后采用透析或减压蒸馏的方式除去有机溶剂,得到纳米粒子。
69、所述有机溶剂优选为二甲基亚砜、二氧六环或其以任意比例的混合物。
70、优选地,反应体系中,所述两亲性聚多肽的浓度为0.1-100mg/ml。
71、优选地,反应体系中,水的体积为所述有机溶剂体积的0.1~100倍。
72、优选地,体系中反应的温度为25-30℃。反应的时间为0.5~8h。
73、采用闪沉法制备的纳米粒子的粒径为几十到几百纳米,优选为70~150nm。
74、上述中间体f1、g1、f2、g2含有功能基元脲酰肼、羟胺,可以高效动态可逆共价结合含醛/酮衍生物,如药物或探针。
75、本发明提供了一种直接经单体聚合并经动态可逆共价结合含醛酮功能性小分子的方法,解决了之前含酰肼功能基元单体无法直接经α-氨基酸-n-羧酸酐(nca)开环聚合问题,实现了含醛酮药物、探针等小分子的高效可逆共价结合至聚多肽上。
76、具体地,用甲氧基/功能基团r5封端的peg大分子引发剂直接聚合npca单体,合成了侧链上含有氨基脲或羟胺基团的聚多肽。通过含醛酮功能性小分子形成酸性微环境响应脲酰腙或肟键得到聚多肽-药物缀合物。
77、在本发明的一些具体实施例中,上述含醛酮功能性小分子为含酮喜树碱(ketone-cpt)或含醛基乏氧探针(ir(btpna)(bpy)2)。
78、本发明还提供了上述制备方法制备的纳米粒子。
79、本发明还提供了上述纳米粒子在制备可控释放的负载型药物中的应用。
80、本发明还提供了上述纳米粒子在制备可控释放的抗肿瘤药物、抗炎药物中的应用。
81、本发明还提供了上述纳米粒子在肿瘤区域病灶诊断成像中的应用。
82、本发明提供了一系列具有式a-d结构的主链为聚多肽侧链悬挂功能性小分子f的两亲性聚合物,可以在酸性条件下释放功能性小分子f。肿瘤组织呈弱酸性且胞内存在溶酶体等酸性区域,在该酸性区域内,纳米粒子疏水区动态可逆共价结合键式i或式ii结构断裂,释放功能性小分子f药物或探针,释放药物进行化疗作用,探针则实现肿瘤区域成像。随着功能性小分子f释放,纳米粒子逐渐解组装最后形成亲水单链形式的嵌段聚合物,且主链为聚多肽生物相容性好。上述聚合物基于这一设计策略,实现了聚多肽侧链高效动态可逆的接枝含醛/酮衍生物,同时其纳米粒子中键合功能性小分子f可控释放。
83、
84、与现有技术相比,本发明提供了一种两亲性聚多肽,具有式a-d任一所示结构。本发明提供的两亲性聚多肽可以有效原位捕获功能性蛋白且在病理微环境响应以释放药物/探针。其中,式c或式d结构的两亲性聚多肽,亲水链端含有功能基团r5,自组装成胶束纳米粒子并经静脉注射后,胶束纳米粒子表面的功能基团r5原位捕获内源性血清蛋白,主动调节胶束纳米粒子上的蛋白质冠。胶束纳米粒子表面主动捕获功能性蛋白并对其表面蛋白质冠调节,极大的增加了血液循环时间,促进了肿瘤的积累,同时减少了肝脏和脾脏的隔离,并提高了肿瘤细胞的选择性摄取。进而实现调节纳米粒子表面蛋白质冠和病理微环境响应以释放药物/探针的功能。
- 还没有人留言评论。精彩留言会获得点赞!