具有经修饰的CH2-CH3序列的犬抗体的制作方法
本发明涉及具有特定属性的犬化抗体。本发明也涉及针对犬pd-1的犬化抗体,其具有特定序列并对犬pd-1具有高结合亲和力。本发明还涉及本发明的抗体在治疗狗(包括癌症治疗)上的用途。
背景技术:
1、犬抗体(也称为免疫球蛋白g或igg)是约150kd的大四聚体蛋白质。每个igg蛋白质由两条相同的、各约25kd的轻链和两条相同的、各约50kd的重链构成。犬igg有四个已知的igg重链亚类,且其分别被称为igga、iggb、iggc和iggd表示。轻链有两个类型:κ和λ链。每一条κ或λ轻链均由一个可变域(vl)和一个恒定域(cl)构成。两条重链中的每一条均由一个可变域(vh)和三个恒定域(称为ch-1、ch-2和ch-3)组成。ch-1域通过称为“铰链”或作为另一种叫法“铰链区”的氨基酸序列连接至ch-2域。在人类中,igg以四个被称为igg1、igg2、igg3和igg4的亚类中的一类而存在。igg的亚类很大程度上由铰链区的序列所确定,该序列在igg的四个亚类中彼此不同。两条重链通过二硫键彼此连接,并且每条重链也通过二硫键连接至轻链中的一条。
2、用木瓜蛋白酶消化igg抗体使抗体分子在铰链区断裂而导致形成三个片段。这些片段中的两个是相同的并且各自由与重链的vh和ch1域维系在一起的轻链组成。这些片段被称为“fab”片段,并且其含有抗体的抗原结合位点。用木瓜蛋白酶消化所得的第三个片段被称为“fc”,并且其含有通过二硫键维系在一起的两条重链的剩余部分。fc因而含有由两条重链各自的ch2和ch3域所组成的二聚体。fab使得抗体能够结合其同源表位,而fc使得抗体能够介导免疫效应器功能如抗体依赖性细胞毒性(adcc)、抗体依赖性吞噬作用(adcp)和补体依赖性细胞毒性(cdc)。
3、本领域熟知,igg抗体通过使其fc部分结合至一族被称为fcγ受体的蛋白质来介导效应器功能如adcc和adcp,而cdc则是通过使fc结合至补体的第一组分,c1q,来介导的。本领域还熟知,不同的igg亚类在其介导这些效应器功能的能力上有所不同。例如,人类igg1显示出强adcc和cdc,而igg4则显示出弱乃至无adcc和cdc。另外,用于识别哪个igg亚类显示出或缺乏效应器功能的方法是本领域熟知的。
4、用于治疗目的的依赖单克隆抗体的方法需要设计相称的抗体或抗体片段以实现所需的治疗响应。例如,一些癌症治疗方法需要治疗抗体具有增强的效应器功能,而其它的则需要显著减少或完全消除效应器功能。效应器功能的增强或消除可以通过如下实现:在抗体的fc部分引入一个或多个氨基酸突变(置换),从而增强或减少对fcγ受体以及补体的第一组分的结合。现有技术中有许多的报道描述了可被引入抗体分子从而调节其效应器功能的氨基酸置换。例如,shields等人,[j.ofbiol.chem.,276(9):6591-6604(2001)]公开了将天冬酰胺置换为丙氨酸(n297a),其导致非糖基化的抗体,显著减少了抗体对若干fcγ受体的结合。另外,shields等人公开了将天冬氨酸置换为丙氨酸(d265a)也显著减少了抗体对fcγ受体的结合。n297a和d265a置换也各自显示出显著地损害cdc。还有其它类似的报道也识别出了可能减少或消除抗体的效应器功能的置换[例如,sazinsky等人,proc.nat.acad.sci.,105:20167-20172(2008),alegre等人,transplantation,57:1537-1543(1994),hutchins等人,proc.nat.acad.sci.92:11980-11984(1994),mcearchem等人,blood,109:1185-1192(2007)]。
5、主要在活化的t和b细胞上表达的免疫抑制性受体(程序性细胞死亡受体1,也被称作程序性死亡受体(pd-1))是与cd28和ctla-4有关的免疫球蛋白超家族的一个成员。pd-1和类似的家族成员是含有细胞外ig可变型(v-型)结构域(其结合它的配体)和胞质尾区(其结合信号传递分子)的i型跨膜糖蛋白。pd-1的胞质尾区含有两个基于酪氨酸的信号传递基序:itim(基于免疫受体酪氨酸的抑制基序)和itsm(基于免疫受体酪氨酸的转换基序)。
6、pd-1当结合至程序性细胞死亡配体1(也被称作程序性死亡配体1(pd-l1))和/或程序性细胞死亡配体2(也被称作程序性死亡配体2(pd-l2))时减弱t-细胞应答。这些配体中的任一种与pd-1的结合会负调节抗原受体信号传递。阻断pd-l1与pd-1的结合会增强肿瘤特异性的cd8+t-细胞免疫,同时辅助免疫系统对肿瘤细胞的清除。已经报道了鼠pd-1的三维结构、以及小鼠pd-1与人pd-l1的共晶结构[zhang等人,immunity 20:337-347(2004);lin等人,proc.natl.acad.sci.usa 105:3011-3016(2008)]。
7、pd-l1和pd-l2是含有在细胞外区域中的igv-和igc-样结构域以及不具有已知信号传递基序的短细胞质区域的i型跨膜配体。pd-l1和pd-l2二者组成性地表达,或者可以在多种细胞类型(包括非造血组织以及多种肿瘤类型)中诱导。pd-l1不仅在b、t、骨髓和树突细胞(dc)上表达,而且在周围细胞(诸如微血管内皮细胞和非淋巴样器官例如心脏或肺)上表达。相反,pd-l2仅存在于巨噬细胞和dc上。pd-1配体的表达模式提示,pd-1在维持外周耐受中起作用,并且还可以用于调节外周中的自体反应性t-和b-细胞应答。
8、在任何情况下,现在非常清楚的是,pd-1在至少某些人癌症中起关键作用,可能是通过介导免疫逃避。因此,pd-l1已经被证实在许多小鼠和人肿瘤上表达,且在大多数pd-l1阴性的肿瘤细胞系中可被ifn-γ诱导[iwai等人,proc.natl.acad.sci.u.s.a.99:12293-12297(2002);strome等人,cancer res.,63:6501-6505(2003)]。此外,已经在许多原发性人肿瘤活组织检查中鉴别出pd-1在肿瘤浸润性淋巴细胞上的表达和/或pd-l1在肿瘤细胞上的表达。这样的肿瘤组织包括肺、肝、卵巢、子宫颈、皮肤、结肠、神经胶质瘤、膀胱、乳房、肾、食管、胃、口腔鳞状细胞、泌尿道上皮细胞和胰腺的癌症以及头和颈的肿瘤[brown等人,j.immunol.170:1257-1266(2003);dong等人,nat.med.8:793-800(2002);wintterle等人,cancer res.63:7462-7467(2003);strome等人,cancer res.,63:6501-6505(2003);thompson等人,cancer res.66:3381-5(2006);thompson等人,clin.cancer res.13:1757-1761(2007);nomi等人,clin.cancer res.13:2151-2157.(2007)]。更惊人的是,在肿瘤细胞上的pd-配体表达已经与跨多个肿瘤类型的人癌症患者的不良预后相关联[综述在okazaki和honjo,int.immunol.19:813-824(2007)]。
9、此外,nomi等人[clin.cancer res.13:2151-2157(2007)]证实了通过施用pd-1或pd-l1指导的抗体在侵袭性胰腺癌的鼠模型中阻断pd-l1与pd-1的结合的治疗效果。这些抗体会有效地促进肿瘤反应性的cd8+t细胞向肿瘤中的渗透,从而导致抗肿瘤效应物(包括ifn-γ、颗粒蛋白酶b和穿孔蛋白)的上调。类似地,抗体用于阻断pd-l1和pd-1的结合的用途,会在小鼠鳞状细胞癌模型中显著地抑制肿瘤生长[tsushima等人,oral oncol.42:268-274(2006)]。
10、在其它研究中,用pd-l1对鼠肥大细胞瘤系的转染导致当与肿瘤特异性的ctl克隆共培养时减少的肿瘤细胞裂解。当加入抗-pd-l1单克隆抗体时,裂解被恢复[iwai等人,proc.natl.acad.sci.u.s.a.99:12293-12297(2002)]。在体内,显示了阻断pd-1/pd-l1相互作用会增加继承性t细胞转移疗法在小鼠肿瘤模型中的效力[strome等人,cancerres.63:6501-6505(2003)]。关于pd-1在癌症治疗中的作用的其它证据来自用pd-1敲除的小鼠执行的实验,其中表达pd-l1的骨髓瘤细胞仅在野生型动物中生长(导致肿瘤生长和有关的动物死亡),但是不在pd-1缺陷型小鼠中生长[iwai y.等人,proc.natl.acad.sci.u.s.a.99:12293-12297(2002)]。近年来,针对pd-1的抗体(包括针对人pd-1的人源化鼠单克隆抗体)已经至少在人类的癌症治疗中显示了初步成功[参见例如,us 8,354,509 b2、us 8,008,449 b2和us 7,595,048b2]。
11、抗-pd-1抗体还可以用在慢性病毒感染中。在急性病毒感染以后产生的记忆性cd8+t细胞是高度功能性的,并且构成保护性免疫的一个重要组分。相反,慢性感染经常特征在于病毒特异性的t-细胞应答的不同程度的功能缺损(耗竭),并且该缺陷是宿主不能消除持久病原体的一个主要原因。尽管功能性的效应t细胞最初在感染的早期阶段产生,它们在慢性感染的进程中逐渐丧失功能。barber等人[nature 439:682-687(2006)]证实,用lcmv的实验室毒株感染的小鼠发展了慢性感染,导致血液和其它组织中的高病毒水平。这些小鼠最初形成了稳健的t细胞应答,但是最终在t细胞耗竭后屈服于感染。barber等人发现,通过注射阻断pd-1和pd-l1之间的相互作用的抗体,可以反转慢性感染的小鼠中效应t细胞的数目和功能的下降。
12、本文中对任何参考文献的引用不应解释为承认:这样的参考文献可作为本技术的“现有技术”得到。
技术实现思路
1、本发明提供了犬抗体的可结晶片段区(cfc区),其中所述cfc已经过基因修饰以增强、降低或消除一种或多种效应器功能。在本发明的一个方面,所述经过基因修饰的cfc降低或消除一种或多种效应器功能。在本发明的另一个方面,所述经过基因修饰的cfc增强一种或多种效应器功能。
2、在某些实施方案中,所述经过基因修饰的cfc区是经过基因修饰的犬iggb fc区。在另一个此类实施方案中,所述经过基因修饰的cfc区是经过基因修饰的犬iggc fc区。在具体的实施方案中,效应器功能是经增强、降低或消除的抗体依赖性细胞毒性(adcc)。在另一个实施方案中,效应器功能是经增强、降低或消除的补体依赖性细胞毒性(cdc)。在又另一个实施方案中,cfc区已经过基因修饰以同时增强、降低或消除adcc和cdc。
3、本发明还提供了包含经基因修饰的cfc区的犬框架和/或全长重链。因此,本发明提供了抗体的全长重链,其中所述全长重链包含本发明的经基因修饰的cfc区。此类全长重链也可以与对应的犬轻(κ或λ)链结合以形成完整的抗体。在这种具体的实施方案中,所得抗体特异性结合至特定的犬抗原。在某些此类实施方案中,犬抗原为犬pd-1。在又其它的实施方案中,犬抗原为犬pd-l1。在仍其它实施方案中,犬抗原为il-4受体α链。在又其它实施方案中,犬抗原为犬胸腺基质淋巴细胞生成素蛋白(ctslp)[参见u.s.7,718,772b2,其内容以引用方式全文并入本文中]。
4、在某些实施方案中,经基因修饰的cfc区包含seq id no:130(或seq id no:132)的氨基酸序列,其中下列氨基酸残基中的一至七个在所示位置由另一个氨基酸残基所取代:p4、d31、n63、g64、t65、a93或p95。用于置换p4、d31、n63、g64、t65、a93和/或p95的氨基酸单独地选自其它19种标准天然存在的氨基酸之一,如下表1中所列。本发明还提供了经基因修饰的cfc区的变体,其包含的氨基酸序列与该经基因修饰的cfc区的氨基酸序列具有90%、95%、98%或99%的同一性,并且保留了对adcc和/或cdc的增强、降低或消除,所述增强、降低或消除是包含seq id no:130(或seq id no:132)的氨基酸序列的经基因修饰的cfc区的至少50%、75%、90%、95%或更多,其中下列氨基酸残基中的一个或多个被取代:即,在p4、d31、n63、g64、t65、a93或p95处。
5、在其它的实施方案中,下列氨基酸残基中的二至五个在所示位置由另一个氨基酸残基所取代:p4、d31、n63、g64、t65、a93或p95。在这种具体的实施方案中,经基因修饰的cfc区包含seq id no:130或seq id no:132的氨基酸序列,并具有下列置换:p4a、d31a、n63a、a93g和p95a。在相关的实施方案中,经基因修饰的cfc区包含seq id no:130或seq id no:132的氨基酸序列,并具有下列置换:p4a、d31a、n63a和p95a。在其它实施方案中,经基因修饰的cfc区包含seq id no:130或seq id no:132的氨基酸序列,并在d31和n63处具有置换。在这种具体的实施方案中,位置31处的天冬氨酸被谷氨酸残基、天冬酰胺残基或丙氨酸残基所取代,而位置63处的天冬酰胺残基被谷氨酰胺残基、组氨酸残基或丙氨酸残基所取代。在这种更具体的实施方案中,经基因修饰的cfc区包含seq id no:130或seq id no:132的氨基酸序列,并具有下列置换:d31a和n63a。在具体的实施方案中,经基因修饰的cfc区由包含核苷酸变化的seq id no:129或seq id no:131的核苷酸序列编码,所述核苷酸变化对应于其所编码的氨基酸序列。
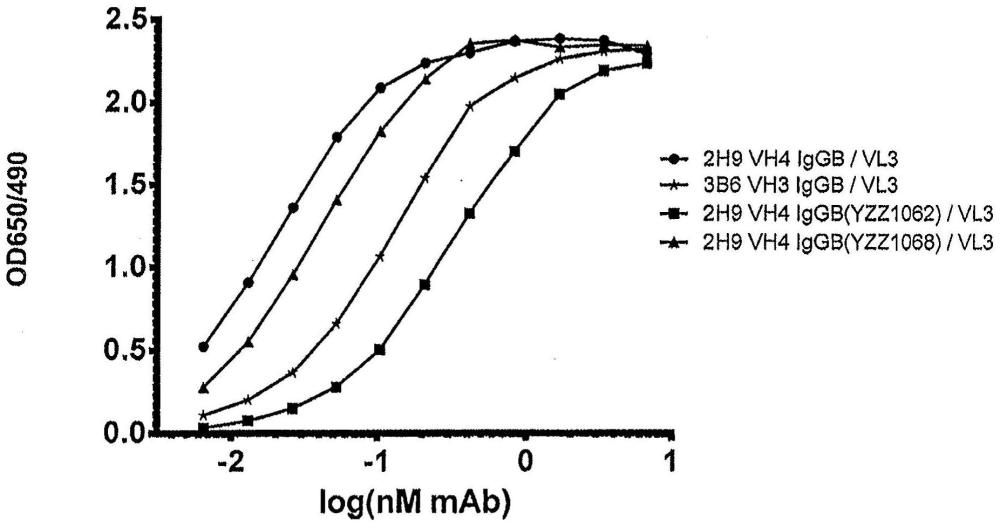
6、在另一个实施方案中,经基因修饰的cfc区包含seq id no:130或seq id no:132的氨基酸序列,并在a93处具有置换。在这种具体的实施方案中,所述置换为a93g。在相关的实施方案中,所述置换为a93s。如下文实施例4中所示,a93g的置换导致补体c1q结合的增强,表明了cdc活性升高。
7、在相关的实施方案中,经基因修饰的cfc区还包含铰链区,所述铰链区包含seq idno:109的氨基酸序列。在其它的实施方案中,经基因修饰的fc区还包含铰链区,所述铰链区包含seq id no:110的氨基酸序列。在仍其它的实施方案中,经基因修饰的fc区还包含铰链区,所述铰链区包含seq id no:111的氨基酸序列。在又其它的实施方案中,经基因修饰的fc区还包含经基因修饰的铰链区,所述经基因修饰的铰链区包含seq id no:112的氨基酸序列。
8、在可选的实施方案中,本发明提供了犬iggd fc区,其具有来自犬iggd抗体的经基因修饰的铰链区、来自犬igga抗体的铰链区、来自犬iggb抗体的铰链区或来自犬iggc抗体的铰链区。此外,本发明提供了抗体的全长重链,其中所述全长重链包含本发明的犬iggdfc区,所述犬iggd fc区具有来自犬iggd抗体的经基因修饰的铰链区、来自犬igga抗体的铰链区、来自犬iggb抗体的铰链区或来自犬iggc抗体的铰链区。此类全长重链也可以与对应的犬轻(κ或λ)链结合以形成完整的抗体。
9、因此,本发明提供了犬iggd fc区,其还包含来自犬iggd抗体的经基因修饰的铰链区。在这种具体的实施方案中,所述犬iggd fc区和经基因修饰的铰链区包含seq id no:6的氨基酸序列或与seq id no:6的氨基酸序列具有90%、95%、98%或99%同一性的氨基酸序列,其在位置10处包含脯氨酸残基(p10)。在更具体的实施方案中,所述犬iggd fc区和经基因修饰的铰链区由seq id no:5的氨基酸序列编码。在其它实施方案中,所述犬iggd fc区还包含来自犬igga抗体的铰链区。在这种具体的实施方案中,所述犬iggd fc区和铰链区包含seq id no:8的氨基酸序列或与seq id no:8的氨基酸序列具有90%、95%、98%或99%同一性的氨基酸序列。在更具体的实施方案中,所述犬iggd fc区和铰链区由seq idno:7的氨基酸序列编码。在仍其它实施方案中,所述犬iggd fc区还包含来自犬iggb抗体的铰链区。在这种具体的实施方案中,所述犬iggd fc区和铰链区包含seq id no:10的氨基酸序列或与seq id no:10的氨基酸序列具有90%、95%、98%或99%同一性的氨基酸序列。在更具体的实施方案中,所述犬iggd fc区和铰链区由seq id no:9的氨基酸序列编码。在又其它实施方案中,所述犬iggd fc区还包含来自犬iggc抗体的铰链区。在这种具体的实施方案中,所述犬iggd cfc区和铰链区包含seq id no:12的氨基酸序列或与seq id no:12的氨基酸序列具有90%、95%、98%或99%同一性的氨基酸序列。在更具体的实施方案中,所述犬iggd cfc区和铰链区由seq id no:11的氨基酸序列编码。本发明还提供了包含这些犬iggd fc区和铰链区的犬化抗体。在具体的实施方案中,所述犬化抗体或其抗原结合片段特异性结合犬程序性死亡受体1(犬pd-1)。
10、因此,本发明提供了对犬pd-1具有特异性和/或具有高结合亲和力的犬化抗犬pd-1抗体。在具体的实施方案中,所述犬化抗-犬pd-1抗体还有能力阻止犬pd-1结合至犬pd-l1。在特定的实施方案中,所述犬化抗-犬pd-1抗体对犬pd-1具有高结合亲和力,并且还有能力阻止犬pd-1结合至犬pd-l2。所述特异性结合犬pd-1的犬化抗体或其抗原结合片段可包含本发明的犬igg重链和犬κ或λ轻链。在具体的实施方案中,所述犬化抗-犬pd-1抗体为犬化鼠抗-犬pd-1抗体。本发明还涉及此类犬化抗体在治疗疾病(如癌症和/或由感染引起的那些)上的用途。
11、在具体的实施方案中,所述犬化抗-犬pd-1抗体包含本发明的经基因修饰的cfc区。在可供选择的实施方案中,所述犬化抗-犬pd-1抗体包含犬iggd fc区,其具有来自犬iggd抗体的经基因修饰的铰链区、来自犬igga抗体的铰链区、来自犬iggb抗体的铰链区或来自犬iggc抗体的铰链区。本发明还提供了此类犬化抗-犬pd-1抗体,其包含本发明的犬框架与cdr的组合,所述cdr得自小鼠抗-犬pd-1抗体,即,三个轻链cdr:cdr轻1(cdrl1)、cdr轻2(cdrl2)和cdr轻3(cdrl3),以及三个重链cdr:cdr重1(cdrh1)、cdr重2(cdrh2)和cdr重3(cdrh3)。
12、在具体的实施方案中,所述犬化鼠抗-犬pd-1抗体包含本发明的iggb或iggc的经基因修饰的cfc区,或者可选地,包含犬iggd fc区连同:来自犬iggd抗体的经基因修饰的铰链区、来自犬igga抗体的铰链区、来自犬iggb抗体的铰链区或来自犬iggc抗体的铰链区,与得自小鼠抗-犬pd-1抗体的cdr的组合。此外,本发明不仅提供了如本文所详述的具有特定cdr的犬化小鼠抗-犬pd-1抗体,还进一步提供了包含下述变体的犬化小鼠抗-犬pd-1抗体:这些cdr的经保守修饰的变体以及包含(例如,共享)相同规范结构的变体。
13、因此,在具体的实施方案中,所述犬化抗-犬pd-1抗体还包含互补决定区(cdr),其中所述cdr具有以下规范结构:分别对应于重链cdr1、cdr2和cdr3的h1-1、h2-1和h3-6,即,重链cdr1具有1类规范结构,重链cdr2具有1类规范结构,而重链cdr3具有6类规范结构。在甚至更具体的实施方案中,对应轻链的cdr具有以下规范结构:分别对应于轻链cdr1、cdr2和cdr3的l1-3、l2-1和l3-1。在其它实施方案中,所述犬化抗-犬pd-1抗体还包含互补决定区(cdr),其中所述cdr具有以下规范结构:分别对应于重链cdr1、cdr2和cdr3的h1-1、h2-1和h3-11。在这种甚至更具体的实施方案中,对应轻链的cdr具有以下规范结构:分别对应于轻链cdr1、cdr2和cdr3的l1-2a、l2-1和l3-1。在仍其它实施方案中,所述犬化抗-犬pd-1抗体还包含互补决定区(cdr),其中所述cdr具有以下规范结构:分别对应于重链cdr1、cdr2和cdr3的h1-1、h2-2a和h3-11。在这种甚至更具体的实施方案中,对应轻链的cdr具有以下规范结构:分别对应于轻链cdr1、cdr2和cdr3的l1-2a、l2-1和l3-1。在又其它实施方案中,所述犬化抗-犬pd-1抗体还包含互补决定区(cdr),其中所述cdr具有以下规范结构:分别对应于重链cdr1、cdr2和cdr3的h1-1、h2-2a和h3-13。在这种甚至更具体的实施方案中,对应轻链的cdr具有以下规范结构:分别对应于轻链cdr1、cdr2和cdr3的l1-4、l2-1和l3-1。
14、在更具体的实施方案中,本发明的犬化抗体或其抗原结合片段包含一个或多个重链互补决定区1(vh cdr1),所述重链互补决定区1具有seq id no:27、seq id no:28、seqid no:29或seq id no:30的氨基酸序列。在另一个实施方案中,重链互补决定区2(vhcdr2)包含seq id no:31、seq id no:32、seq id no:33、seq id no:34或seq id no:35的氨基酸序列。在仍另一个实施方案中,重链互补决定区3(vh cdr3)包含seq id no:36、seqid no:37、seq id no:38或seq id no:146的氨基酸序列。在这种具体的实施方案中,所述犬化抗体或抗原结合片段既包含vh cdr1,其包含seq id no:27、seq id no:28、seq idno:29或seq id no:30的氨基酸序列,又包含vh cdr2,其包含seq id no:31、seq id no:32、seq id no:33、seq id no:34或seq id no:35的氨基酸序列。在另一个此类实施方案中,所述犬化抗体或抗原结合片段既包含vh cdr1,其包含seq id no:27、seq id no:28、seq id no:29或seq id no:30的氨基酸序列,又包含vh cdr3,其包含seq id no:36、seqid no:37、seq id no:38或seq id no:146的氨基酸序列。在又另一个此类实施方案中,所述犬化抗体或抗原结合片段既包含vh cdr2,其包含seq id no:31、seq id no:32、seq idno:33、seq id no:34或seq id no:35的氨基酸序列,又包含vh cdr3,其包含seq id no:36、seq id no:37、seq id no:38或seq id no:146的氨基酸序列。在仍另一个此类实施方案中,所述犬化抗体或抗原结合片段既包含vh cdr1,其包含seq id no:27、seq id no:28、seq id no:29或seq id no:30的氨基酸序列,又包含vh cdr2,其包含seq id no:31、seqid no:32、seq id no:33、seq id no:34或seq id no:35的氨基酸序列,还包含vh cdr3,其包含seq id no:36、seq id no:37、seq id no:38或seq id no:146的氨基酸序列。
15、在具体的实施方案中,所述犬化抗体或抗原结合片段还包含轻链互补决定区1(vlcdr1),所述轻链互补决定区1包含seq id no:13、seq id no:14或seq id no:15的氨基酸序列。在相关的实施方案中,轻链互补决定区2(vl cdr2)包含seq id no:16、seq id no:17、seq id no:18、seq id no:19、seq id no:20或seq id no:21的氨基酸序列。在仍另一个实施方案中,轻链互补决定区3(vl cdr3)包含seq id no:22、seq id no:23、seq id no:24、seq id no:25或seq id no:26的氨基酸序列。在这种具体的实施方案中,所述犬化抗体或抗原结合片段既包含vl cdr1,其包含seq id no:13、seq id no:14或seq id no:15的氨基酸序列,又包含vl cdr2,其包含seq id no:16、seq id no:17、seq id no:18、seq idno:19、seq id no:20或seq id no:21的氨基酸序列。
16、在另一个此类实施方案中,所述犬化抗体或抗原结合片段既包含vl cdr1,其包含seq id no:13、seq id no:14或seq id no:15的氨基酸序列,又包含vl cdr3,其包含seqid no:22、seq id no:23、seq id no:24、seq id no:25或seq id no:26的氨基酸序列。在又另一个此类实施方案中,所述犬化抗体或抗原结合片段既包含vl cdr2,其包含seq idno:16、seq id no:17、seq id no:18、seq id no:19、seq id no:20或seq id no:21的氨基酸序列,又包含vl cdr3,其包含seq id no:22、seq id no:23、seq id no:24、seq id no:25或seq id no:26的氨基酸序列。在仍另一个此类实施方案中,所述犬化抗体或抗原结合片段既包含vl cdr1,其包含seq id no:13、seq id no:14或seq id no:15的氨基酸序列,又包含vl cdr2,其包含seq id no:16、seq id no:17、seq id no:18、seq id no:19、seqid no:20或seq id no:21的氨基酸序列,还包含vl cdr3,其包含seq id no:22、seq idno:23、seq id no:24、seq id no:25或seq id no:26的氨基酸序列。
17、本发明还提供了包含seq id no:40的氨基酸序列或与seq id no:40具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:42的氨基酸序列或与seq id no:42具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:44的氨基酸序列或与seq idno:44具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:46的氨基酸序列或与seq id no:46具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:48的氨基酸序列或与seq id no:48具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:50的氨基酸序列或与seq id no:50具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:52的氨基酸序列或与seq id no:52具有90%、95%、98%或99%同一性的氨基酸序列、seqid no:54的氨基酸序列或与seq id no:54具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:56的氨基酸序列或与seq id no:56具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:58的氨基酸序列或与seq id no:58具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:60的氨基酸序列或与seq id no:60具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:62的氨基酸序列或与seq id no:62具有90%、95%、98%或99%同一性的氨基酸序列、seq id no:64的氨基酸序列或与seq id no:64具有90%、95%、98%或99%同一性的氨基酸序列、或seq id no:66的氨基酸序列或与seq idno:66具有90%、95%、98%或99%同一性的氨基酸序列的犬化抗体或这些犬化抗体的抗原结合片段。
18、在具体的实施方案中,抗体重链包含seq id no:40、52、56或64的氨基酸序列(或与seq id no:40、52、56或64具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置239处包含p、a、g或s,(ii)在位置266处包含a、g或s,(iii)在位置298处包含a、g或s,(iv)在位置299处包含g、p或a,(v)在位置300处包含t、a、g或s,(vi)在位置328处包含a、g或s并且(vii)在位置330处包含p、a、g或s。在其它实施方案中,抗体重链包含seq id no:42、54、58或66的氨基酸序列(或与seq id no:42、54、58或66具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置237处包含p、a、g或s,(ii)在位置264处包含a、g或s,(iii)在位置296处包含a、g或s,(iv)在位置297处包含g、p或a,(v)在位置298处包含t、a、g或s,(vi)在位置326处包含a、g或s并且(vii)在位置328处包含p、a、g或s。在又其它实施方案中,抗体重链包含seq id no:44、50或60的氨基酸序列(或与seq id no:44、50或60具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置244处包含p、a、g或s,(ii)在位置271处包含a、g或s,(iii)在位置303处包含a、g或s,(iv)在位置304处包含g、p或a,(v)在位置305处包含t、a、g或s,(vi)在位置333处包含a、g或s并且(vii)在位置335处包含p、a、g或s。在仍其它实施方案中,抗体重链包含seq id no:46或62的氨基酸序列(或与seq id no:46或62具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置242处包含p、a、g或s,(ii)在位置269处包含a、g或s,(iii)在位置301处包含a、g或s,(iv)在位置302处包含g、p或a,(v)在位置303处包含t、a、g或s,(vi)在位置331处包含a、g或s并且(vii)在位置333处包含p、a、g或s。在又其它实施方案中,抗体重链包含seq id no:48的氨基酸序列(或与seq id no:48具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置246处包含p、a、g或s,(ii)在位置273处包含a、g或s,(iii)在位置305处包含a、g或s,(iv)在位置306处包含g、p或a,(v)在位置307处包含t、a、g或s,(vi)在位置335处包含a、g或s并且(vii)在位置337处包含p、a、g或s。
19、在仍其它实施方案中,抗体重链包含seq id no:40、52、56或64的氨基酸序列(或与seq id no:40、52、56或64具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置239处包含p、a、g或s,(ii)在位置266处包含a,(iii)在位置298处包含a,(iv)在位置299处包含g、p或a,(v)在位置300处包含t、a、g或s,(vi)在位置328处包含a、g或s并且(vii)在位置330处包含p、a、g或s。在其它实施方案中,抗体重链包含seq id no:42、54、58或66的氨基酸序列(或与seq id no:42、54、58或66具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置237处包含p、a、g或s,(ii)在位置264处包含a,(iii)在位置296处包含a,(iv)在位置297处包含g、p或a,(v)在位置298处包含t、a、g或s,(vi)在位置326处包含a、g或s并且(vii)在位置328处包含p、a、g或s。在又其它实施方案中,抗体重链包含seq id no:44、50或60的氨基酸序列(或与seq id no:44、50或60具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置244处包含p、a、g或s,(ii)在位置271处包含a,(iii)在位置303处包含a,(iv)在位置304处包含g、p或a,(v)在位置305处包含t、a、g或s,(vi)在位置333处包含a、g或s并且(vii)在位置335处包含p、a、g或s。在仍其它实施方案中,抗体重链包含seqid no:46或62的氨基酸序列(或与seq id no:46或62具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置242处包含p、a、g或s,(ii)在位置269处包含a,(iii)在位置301处包含a,(iv)在位置302处包含g、p或a,(v)在位置303处包含t、a、g或s,(vi)在位置331处包含a、g或s并且(vii)在位置333处包含p、a、g或s。在又其它实施方案中,抗体重链包含seqid no:48的氨基酸序列(或与seq id no:48具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置246处包含p、a、g或s,(ii)在位置273处包含a,(iii)在位置305处包含a,(iv)在位置306处包含g、p或a,(v)在位置307处包含t、a、g或s,(vi)在位置335处包含a、g或s并且(vii)在位置337处包含p、a、g或s。
20、在仍其它实施方案中,抗体重链包含seq id no:40、52、56或64的氨基酸序列(或与seq id no:40、52、56或64具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置239处包含a,(ii)在位置266处包含a,iii)在位置298处包含a,(iv)在位置299处包含p,(v)在位置300处包含a,(vi)在位置328处包含g并且(vii)在位置330处包含a。在其它实施方案中,抗体重链包含seq id no:42、54、58或66的氨基酸序列(或与seq id no:42、54、58或66具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置237处包含a,(ii)在位置264处包含a,iii)在位置296处包含a,(iv)在位置297处包含p,(v)在位置298处包含a,(vi)在位置326处包含g并且(vii)在位置328处包含a。在又其它实施方案中,抗体重链包含seq id no:44、50或60的氨基酸序列(或与seq id no:44、50或60具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置244处包含a,(ii)在位置271处包含a,iii)在位置303处包含a,(iv)在位置304处包含p,(v)在位置305处包含a,(vi)在位置333处包含g并且(vii)在位置335处包含a。在仍其它实施方案中,抗体重链包含seq id no:46或62的氨基酸序列(或与seq id no:46或62具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置242处包含a,(ii)在位置269处包含a,iii)在位置301处包含a,(iv)在位置302处包含p,(v)在位置303处包含a,(vi)在位置331处包含g并且(vii)在位置333处包含a。在又其它实施方案中,抗体重链包含seq id no:48的氨基酸序列(或与seq id no:48具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置246处包含a,(ii)在位置273处包含a,iii)在位置305处包含a,(iv)在位置306处包含p,(v)在位置307处包含a,(vi)在位置335处包含g并且(vii)在位置337处包含a。
21、在又其它实施方案中,抗体重链包含seq id no:40、52、56或64的氨基酸序列(或与seq id no:40、52、56或64具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置239处包含p,(ii)在位置266处包含a、g或s,(iii)在位置298处包含a、g或s,(iv)在位置299处包含g,(v)在位置300处包含t,(vi)在位置328处包含a并且(vii)在位置330处包含p。在其它实施方案中,抗体重链包含seq id no:42、54、58或66的氨基酸序列(或与seq idno:42、54、58或66具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置237处包含p,(ii)在位置264处包含a、g或s,(iii)在位置296处包含a、g或s,(iv)在位置297处包含g,(v)在位置298处包含t,(vi)在位置326处包含a并且(vii)在位置328处包含p。在又其它实施方案中,抗体重链包含seq id no:44、50或60的氨基酸序列(或与seq id no:44、50或60具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置244处包含p,(ii)在位置271处包含a、g或s,(iii)在位置303处包含a、g或s,(iv)在位置304处包含g,(v)在位置305处包含t,(vi)在位置333处包含a并且(vii)在位置335处包含p。在仍其它实施方案中,抗体重链包含seq id no:46或62的氨基酸序列(或与seq id no:46或62具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置242处包含p,(ii)在位置269处包含a、g或s,(iii)在位置301处包含a、g或s,(iv)在位置302处包含g,(v)在位置303处包含t,(vi)在位置331处包含a并且(vii)在位置333处包含p。在又其它实施方案中,抗体重链包含seq idno:48的氨基酸序列(或与seq id no:48具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置246处包含p,(ii)在位置273处包含a、g或s,(iii)在位置305处包含a、g或s,(iv)在位置306处包含g,(v)在位置307处包含t,(vi)在位置335处包含a并且(vii)在位置337处包含p。
22、在仍其它实施方案中,抗体重链包含seq id no:40、52、56或64的氨基酸序列(或与seq id no:40、52、56或64具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置239处包含p,(ii)在位置266处包含a,(iii)在位置298处包含a,(iv)在位置299处包含g,(v)在位置300处包含t,(vi)在位置328处包含a并且(vii)在位置330处包含p。在其它实施方案中,抗体重链包含seq id no:42、54、58或66的氨基酸序列(或与seq id no:42、54、58或66具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置237处包含p,(ii)在位置264处包含a,(iii)在位置296处包含a,(iv)在位置297处包含g,(v)在位置298处包含t,(vi)在位置326处包含a并且(vii)在位置328处包含p。在又其它实施方案中,抗体重链包含seq id no:44、50或60的氨基酸序列(或与seq id no:44、50或60具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置244处包含p,(ii)在位置271处包含a,(iii)在位置303处包含a,(iv)在位置304处包含g,(v)在位置305处包含t,(vi)在位置333处包含a并且(vii)在位置335处包含p。在仍其它实施方案中,抗体重链包含seq id no:46或62的氨基酸序列(或与seq id no:46或62具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置242处包含p,(ii)在位置269处包含a,(iii)在位置301处包含a,(iv)在位置302处包含g,(v)在位置303处包含t,(vi)在位置331处包含a并且(vii)在位置333处包含p。在又其它实施方案中,抗体重链包含seq id no:48的氨基酸序列(或与seq id no:48具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置246处包含p,(ii)在位置273处包含a,(iii)在位置305处包含a,(iv)在位置306处包含g,(v)在位置307处包含t,(vi)在位置335处包含a并且(vii)在位置337处包含p。
23、在其它实施方案中,抗体重链包含seq id no:40、52、56或64的氨基酸序列(或与seq id no:40、52、56或64具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置239处包含p、a、g或s,(ii)在位置266处包含a、g或s,(iii)在位置298处包含a、g或s,(iv)在位置299处包含g,(v)在位置300处包含t,(vi)在位置328处包含a、g或s并且(vii)在位置330处包含p、a、g或s。在其它此类实施方案中,抗体重链包含seq id no:42、54、58或66的氨基酸序列(或与seq id no:42、54、58或66具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置237处包含p、a、g或s,(ii)在位置264处包含a、g或s,(iii)在位置296处包含a、g或s,(iv)在位置297处包含g,(v)在位置298处包含t,(vi)在位置326处包含a、g或s并且(vii)在位置328处包含p、a、g或s。在又其它实施方案中,抗体重链包含seq id no:44、50或60的氨基酸序列(或与seq id no:44、50或60具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置244处包含p、a、g或s,(ii)在位置271处包含a、g或s,(iii)在位置303处包含a、g或s,(iv)在位置304处包含g,(v)在位置305处包含t,(vi)在位置333处包含a、g或s并且(vii)在位置335处包含p、a、g或s。在仍其它实施方案中,抗体重链包含seq id no:46或62的氨基酸序列(或与seq id no:46或62具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置242处包含p、a、g或s,(ii)在位置269处包含a、g或s,(iii)在位置301处包含a、g或s,(iv)在位置302处包含g,(v)在位置303处包含t,(vi)在位置331处包含a、g或s并且(vii)在位置333处包含p、a、g或s。在又其它实施方案中,抗体重链包含seq id no:48的氨基酸序列(或与seq id no:48具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置246处包含p、a、g或s,(ii)在位置273处包含a、g或s,(iii)在位置305处包含a、g或s,(iv)在位置306处包含g,(v)在位置307处包含t,(vi)在位置335处包含a、g或s并且(vii)在位置337处包含p、a、g或s。
24、在又其它实施方案中,抗体重链包含seq id no:40、52、56或64的氨基酸序列(或与seq id no:40、52、56或64具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置239处包含p、a、g或s,(ii)在位置266处包含a,(iii)在位置298处包含a,(iv)在位置299处包含g,(v)在位置300处包含t,(vi)在位置328处包含a、g或s并且(vii)在位置330处包含p、a、g或s。在其它此类实施方案中,抗体重链包含seq id no:42、54、58或66的氨基酸序列(或与seq id no:42、54、58或66具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置237处包含p、a、g或s,(ii)在位置264处包含a,(iii)在位置296处包含a,(iv)在位置297处包含g,(v)在位置298处包含t,(vi)在位置326处包含a、g或s并且(vii)在位置328处包含p、a、g或s。在又其它实施方案中,抗体重链包含seq id no:44、50或60的氨基酸序列(或与seq id no:44、50或60具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置244处包含p、a、g或s,(ii)在位置271处包含a,(iii)在位置303处包含a,(iv)在位置304处包含g,(v)在位置305处包含t,(vi)在位置333处包含a、g或s并且(vii)在位置335处包含p、a、g或s。在仍其它实施方案中,抗体重链包含seq id no:46或62的氨基酸序列(或与seqid no:46或62具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置242处包含p、a、g或s,(ii)在位置269处包含a,(iii)在位置301处包含a,(iv)在位置302处包含g,(v)在位置303处包含t,(vi)在位置331处包含a、g或s并且(vii)在位置333处包含p、a、g或s。在又其它实施方案中,抗体重链包含seq id no:48的氨基酸序列(或与seq id no:48具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置246处包含p、a、g或s,(ii)在位置273处包含a,(iii)在位置305处包含a,(iv)在位置306处包含g,(v)在位置307处包含t,(vi)在位置335处包含a、g或s并且(vii)在位置337处包含p、a、g或s。
25、在又其它实施方案中,抗体重链包含seq id no:40、52、56或64的氨基酸序列(或与seq id no:40、52、56或64具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置239处包含a,(ii)在位置266处包含a,iii)在位置298处包含a,(iv)在位置299处包含g,(v)在位置300处包含t,(vi)在位置328处包含g并且(vii)在位置330处包含a。在其它此类实施方案中,抗体重链包含seq id no:42、54、58或66的氨基酸序列(或与seq id no:42、54、58或66具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置237处包含a,(ii)在位置264处包含a,iii)在位置296处包含a,(iv)在位置297处包含g,(v)在位置298处包含t,(vi)在位置326处包含g并且(vii)在位置328处包含a。在又其它实施方案中,抗体重链包含seq id no:44、50或60的氨基酸序列(或与seq id no:44、50或60具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置244处包含a,(ii)在位置271处包含a,iii)在位置303处包含a,(iv)在位置304处包含g,(v)在位置305处包含t,(vi)在位置333处包含g并且(vii)在位置335处包含a。在仍其它实施方案中,抗体重链包含seq id no:46或62的氨基酸序列(或与seq id no:46或62具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置242处包含a,(ii)在位置269处包含a,iii)在位置301处包含a,(iv)在位置302处包含g,(v)在位置303处包含t,(vi)在位置331处包含g并且(vii)在位置333处包含a。在又其它实施方案中,抗体重链包含seq id no:48的氨基酸序列(或与seq id no:48具有90%、95%、98%或99%同一性的氨基酸序列),其(i)在位置246处包含a,(ii)在位置273处包含a,iii)在位置305处包含a,(iv)在位置306处包含g,(v)在位置307处包含t,(vi)在位置335处包含g并且(vii)在位置337处包含a。
26、此外,本发明提供了还包含犬轻链的犬化抗体或其抗原结合片段,所述犬轻链包含seq id no:72、seq id no:78、seq id no:84、seq id no:90、seq id no:96、seq id no:102或seq id no:108的氨基酸序列。
27、因此,本发明还提供了包含重链和轻链的犬化抗体或其抗原结合片段,所述重链包含seq id no:68的氨基酸序列,而所述轻链包含seq id no:72的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:70的氨基酸序列,而所述轻链包含seq id no:72的氨基酸序列。在另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:74的氨基酸序列,而所述轻链包含seq id no:78的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:76的氨基酸序列,而所述轻链包含seq id no:78的氨基酸序列。在又另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:80的氨基酸序列,而所述轻链包含seq id no:84的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:82的氨基酸序列,而所述轻链包含seq id no:84的氨基酸序列。在仍另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seqid no:86的氨基酸序列,而所述轻链包含seq id no:90的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:88的氨基酸序列,而所述轻链包含seq id no:90的氨基酸序列。在又另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:92的氨基酸序列,而所述轻链包含seq id no:96的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:94的氨基酸序列,而所述轻链包含seq idno:96的氨基酸序列。在仍另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:98的氨基酸序列,而所述轻链包含seq id no:102的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:100的氨基酸序列,而所述轻链包含seq id no:102的氨基酸序列。在又另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq idno:104的氨基酸序列,而所述轻链包含seq id no:108的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:106的氨基酸序列,而所述轻链包含seq id no:108的氨基酸序列。
28、本发明还提供了包含重链和轻链的犬化抗体或其抗原结合片段,所述重链包含seq id no:40的氨基酸序列,而所述轻链包含seq id no:72的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:42的氨基酸序列,而所述轻链包含seq id no:72的氨基酸序列。在另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:44的氨基酸序列,而所述轻链包含seq id no:78的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:46的氨基酸序列,而所述轻链包含seqid no:78的氨基酸序列。在又另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:48的氨基酸序列,而所述轻链包含seq id no:84的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:50的氨基酸序列,而所述轻链包含seq id no:84的氨基酸序列。在仍另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq idno:52的氨基酸序列,而所述轻链包含seq id no:90的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:54的氨基酸序列,而所述轻链包含seq id no:90的氨基酸序列。在又另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:56的氨基酸序列,而所述轻链包含seq id no:96的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:58的氨基酸序列,而所述轻链包含seq id no:96的氨基酸序列。
29、在仍另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:60的氨基酸序列,而所述轻链包含seq id no:102的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq idno:62的氨基酸序列,而所述轻链包含seq id no:102的氨基酸序列。在又另一个实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:64的氨基酸序列,而所述轻链包含seq id no:108的氨基酸序列。在相关的实施方案中,所述犬化抗体或其抗原结合片段包含重链和轻链,所述重链包含seq id no:66的氨基酸序列,而所述轻链包含seq id no:108的氨基酸序列。
30、本发明还提供了核酸,其编码本发明的任何氨基酸序列,包含本发明的犬化抗体的cdr、cfc区、具有铰链区的cfc区以及重链和轻链。本发明还提供了包含本发明的一种或多种核酸的表达载体。本发明还提供了宿主细胞,其包含本发明的一个或多个表达载体,并且提供了使用此类宿主细胞表达本发明的犬化抗体的cdr和/或cfc区和/或具有铰链区的cfc区和/或重链和/或轻链的方法。本发明还提供了宿主细胞,其已经过基因工程改造以在不存在此类载体的情况下表达本发明的犬化抗体的cdr和/或cfc区和/或具有铰链区的cfc区和/或重链和/或轻链。在具体的实施方案中,本发明的这些核酸、表达载体、多肽或宿主细胞可用于制造抗体的方法中。
31、在具体的实施方案中,所述抗体是重组抗体或其抗原结合片段。在相关的实施方案中,所述可变重链结构域和可变轻链结构域通过柔性接头连接以形成单链抗体。
32、在具体的实施方案中,所述抗体或抗原结合片段是fab片段。在其它实施方案中,所述抗体或抗原结合片段是fab'片段。在其它实施方案中,所述抗体或抗原结合片段是(fab')2片段。在仍其它实施方案中,所述抗体或抗原结合片段是双抗体。在具体的实施方案中,所述抗体或抗原结合片段是结构域抗体。在具体的实施方案中,所述抗体或抗原结合片段是骆驼源化的单结构域抗体。在具体的实施方案中,所述犬化鼠抗-犬pd-1抗体或抗原结合片段会增加正在接受治疗的犬个体的免疫应答。
33、在某些实施方案中,当结合至犬pd-1时,所述犬化抗体或其抗原结合片段结合至下列一个或多个氨基酸序列内的至少一个氨基酸残基:seq id no:138、seq id no:139、seq id no:140、seq id no:141、seq id no:142、seq id no:143、seq id no:144和/或seqid no:145。
34、此外,本发明还提供了针对犬pd-1的犬化抗体,其包含本发明的cdr的变体,所述变体具有本文中所提供的对应的规范结构,并且/或者结合至seq id no:144的氨基酸序列。在这种具体的实施方案中,犬化抗体-犬pd-1结合的解离常数(kd)为1x 10-5至1x 10-12m。在更具体的实施方案中,针对犬pd-1的犬化抗体包含本发明的cdr的变体,所述变体具有本文所提供的对应的规范结构并且结合至seq id no:145的氨基酸序列。本发明因此包括特异性结合犬pd-1的犬化抗体及其抗原结合片段,当其结合至犬pd-1时,所述抗体结合至seq id no:144内的至少一个氨基酸残基。在这种具体的实施方案中,所述抗体及其抗原结合片段结合犬pd-1并且阻止犬pd-1结合至犬程序性死亡配体1(pd-l1)。
35、因此,在具体的实施方案中,当结合至犬pd-1时,所述犬化抗体(包含具有一个或多个变体cdr的抗体,所述抗体变体包括例如经保守修饰的变体和/或包含限定的规范结构类别的变体)结合至下列一个或多个氨基酸序列内的至少一个氨基酸残基:seq id no:138、seq id no:139、seq id no:140、seq id no:141、seq id no:142、seq id no:143和/或seq id no:145。在甚至更具体的实施方案中,当结合至犬pd-1时,所述犬化抗体或其抗原结合片段结合至下列精氨酸残基中的一个或多个氨基酸残基:seq id no:114的r62、r69、r72、r75和r90。在特定的实施方案中,当结合至犬pd-1时,所述犬化抗体或其抗原结合片段结合至seq id no:145内的至少一个氨基酸残基。在更特定的实施方案中,当结合至犬pd-1时,所述抗体或其抗原结合片段结合至下列精氨酸残基中的一个或多个氨基酸残基:seqid no:114的r62、r69、r72和r75。在甚至更特定的实施方案中,当结合至犬pd-1时,所述抗体或其抗原结合片段结合至seq id no:114的r75。
36、本发明还提供了犬化抗体及其抗原结合片段,其以低于1x110-12m(例如,1x110-13m或更低)的解离常数(kd)结合至犬pd-1。在具体的实施方案中,所述犬化抗体及其抗原结合片段以1x110-5m至1x110-12m的解离常数结合至犬pd-1。在更具体的实施方案中,所述犬化抗体及其抗原结合片段以1x110-7m至1x110-11m的解离常数结合至犬pd-1。在仍更具体的实施方案中,所述犬化抗体及其抗原结合片段以1x110-8m至1x110-11m的解离常数结合至犬pd-1。在又更具体的实施方案中,所述犬化抗体及其抗原结合片段以1x110-8m至1x110-10m的解离常数结合至犬pd-1。
37、本发明还提供了犬化抗体或其抗原结合片段,其以大于1x1107m-1s-1的结合率(kon)结合至犬pd-1。在具体的实施方案中,所述犬化抗体或其抗原结合片段以1x102m-1s-1至1x1107m-1s-1的结合率结合至犬pd-1。在更具体的实施方案中,所述犬化抗体或其抗原结合片段以1x1103m-1s-1至1x1106m-1s-1的结合率结合至犬pd-1。在仍更具体的实施方案中,所述犬化抗体或其抗原结合片段以1x1103m-1s-1至1x1105m-1s-1的结合率结合至犬pd-1。在又更具体的实施方案中,所述犬化抗体或其抗原结合片段以1x1104m-1s-1至1x1105m-1s-1的结合率结合至犬pd-1。
38、本发明还提供了犬化抗体或其抗原结合片段,其以慢于1x110-7s-1的解离率(koff)结合至犬pd-1。在具体的实施方案中,所述犬化抗体或其抗原结合片段以1x110-3s-1至1x110-8s-1的解离率结合至犬pd-1。在更具体的实施方案中,所述犬化抗体或其抗原结合片段以1x110-4s-1至1x110-7s-1的解离率结合至犬pd-1。在仍更具体的实施方案中,所述犬化抗体或其抗原结合片段以1x110-5s-1至1x110-7s-1的解离率结合至犬pd-1。
39、在相关的实施方案中,所述犬化抗体或其抗原结合片段激发针对肿瘤或病原体的抗原特异性记忆应答。在具体的实施方案中,所述犬化抗体或其抗原结合片段激发体内抗体应答。在其它具体的实施方案中,所述犬化抗体或其抗原结合片段激发动物个体内的免疫应答。在更特定的实施方案中,所述动物个体为犬。在相关的实施方案中,所述动物个体为猫类。
40、因此,本发明的任何犬化抗体可具有一项、两项、三项、四项、五项或所有这些特性,即,前述与犬pd-1的解离常数、前述与犬pd-1结合的结合率、前述从所述犬化抗体-犬pd-1结合复合体解离的解离率、激发针对肿瘤或病原体的抗原特异性记忆应答、激发体内抗体应答和/或激发动物个体内的免疫应答。
41、在更具体的实施方案中,本发明的犬化抗体及其抗原结合片段结合犬pd-1并且还阻止犬pd-1结合至pd-l1。在甚至更具体的实施方案中,本发明的犬化抗体及其抗原结合片段结合犬pd-1、阻止犬pd-1结合至pd-l1并且还阻止犬pd-1结合至pd-l2。
42、本发明还提供了编码本发明的犬化鼠抗-犬pd-1抗体或其部分的核酸。在相关的实施方案中,此类抗体或抗原结合片段可用于制备药物以治疗犬个体的癌症。可选地,或共同地,本发明提供了本发明的任何抗体或抗体片段在诊断上的用途。在又另外的实施方案中,提供了包括本文公开的任何犬化抗体或抗原结合片段的试剂盒。
43、本发明还包括药物组合物,其包含抗-犬抗原抗体或其结合片段(例如,抗-犬pd-1抗体或其抗原结合片段)连同药学上可接受的载体或稀释剂。本发明还提供了提高免疫细胞活性的方法,包括向有此需求的个体(例如,犬)施用治疗有效量的本发明的药物组合物。在某些实施方案中,所述方法用于治疗癌症。在其它的实施方案中,所述方法用于治疗感染或传染病。在仍其它的实施方案中,本发明的犬化抗体或其抗原结合片段用作疫苗佐剂。在又另一个实施方案中,向犬施用犬化抗-tslp抗体以治疗过敏性皮炎。
44、通过参考以下附图说明和详细描述会更好地理解本发明的这些和其它方面。
- 还没有人留言评论。精彩留言会获得点赞!