一种4,6-二氯-3-羟基-2-硝基苯甲酸的合成方法与流程
本发明涉及一种4,6-二氯-3-羟基-2-硝基苯甲酸的合成方法。
背景技术:
1、加拿大专利ca215566c及欧州专利ep1737831b1提出了两种分子结构的化合物用以治疗如阿尔茨海默氏病、老年痴呆等脑部神经系统疾病。两篇专利分别给出了如下两个结构式:
2、
3、在合成上述两个分子结构化合物的过程中,均需要关键中间体4,6-二氯-3-羟基-2-硝基苯甲酸。4,6-二氯-3-羟基-2-硝基苯甲酸的分子结构式为:
4、
5、专利ca215566c给出了一种4,6-二氯-3-羟基-2-硝基苯甲酸合成方法。以4,6-二氯-3-羟基苯甲酸在硝基甲烷溶剂中以浓硝酸硝化得到粗品,再经层析以68%的摩尔收到得到4,6-二氯-3-羟基-2-硝基苯甲酸纯品。此合成方法所用原料4,6-二氯-3-羟基苯甲酸合成困难,供应稀少,价格昂贵。
6、专利ep1737831b1给出了一条4,6-二氯-3-羟基-2-硝基苯甲酸的合成路线。以2,4-二氯苯甲酸为起始原料,经硝化、还原、氨基保护、硝化、水解共5步反应得到4,6-二氯-3-羟基-2-硝基苯甲酸。反应式如下:
7、
8、专利ep1737831b1给出了后4步的合成实例。具体是以2,4-二氯-5-硝基苯甲酸为底物,先与氯化亚锡进行还原反应得到2,4-二氯-5-氨基苯甲酸,再与醋酐反应生成2,4-二氯-5-乙酰氨基苯甲酸,再经混酸硝化得到3-乙酰氨基-4,6-二氯-2-硝基苯甲酸,再分别在碱性、酸性条件下两次水解得到2-硝基-3-羟基-4,6-二氯苯甲酸。4步总摩尔收率为66%。
9、美国专利us2015/0025072a1给出了专利ep1737831b1所述第1步反应实例,即由2,4-二氯苯甲酸经硝化制得2,4-二氯-5-硝基苯甲酸。美国专利us2015/0025072a1指出有硝化异构体2,4-二氯-3-硝基苯甲酸生成。后处理要经两次碱溶、两次酸化才能得到纯品,硝化收率为72%,工艺繁琐、污水量大。结合美国专利us2015/0025072a1实例的收率数据,得出专利ep1737831b1合成路线5步反应总摩尔收率为47.52%。
10、综上所述,4,6-二氯-3-羟基-2-硝基苯甲酸是治疗脑部神经系统疾病新药的关键中间体。目前公开的工艺路线有的存在原料供应稀少,价格昂贵的缺点,有的反应路线长,包括两步硝化、一步还原等多步高危工艺,存在生产效率低、安全系数不高、总摩尔收率低等缺点。
技术实现思路
1、本发明的目的是提供一种新的4,6-二氯-3-羟基-2-硝基苯甲酸的合成方法,此方法采用价廉易得的原料,能够减少硝化高危工艺的次数,避免高危还原工艺。本发明工艺具有原材料成本低、转化率高、生产效率高等优点。
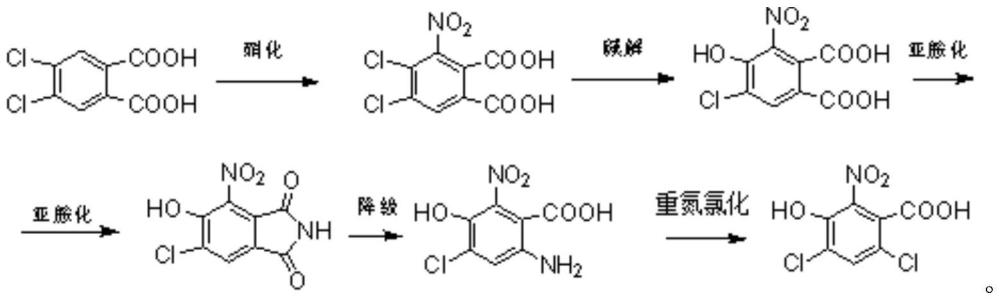
2、本发明的目的是通过以下技术方案实现的,一种4,6-二氯-3-羟基-2-硝基苯甲酸的合成方法,采用4,5-二氯邻苯二甲酸为反应底物,经硝化、碱解、亚胺化、降级和重氮氯化共5步高效反应,高收率得到4,6-二氯-3-羟基-2-硝基苯甲酸。
3、化学反应式如下:
4、
5、4,5-二氯邻苯二甲酸是生产4-氯邻苯二甲酸酐的副产物。4-氯邻苯二甲酸作为聚酰亚胺起始原料,我国已有多家企业规模化量产。作为副产物的4,5-二氯邻苯二甲酸供应充足。
6、在第一步硝化反应过程中,采用4,5-二氯邻苯二甲酸为反应原料,在苯环上引入硝基基团得到中间体4,5-二氯-3-硝基邻苯二甲酸。由于4,5-二氯邻苯二甲酸分子结构的对称性,硝基上到3号位和6号位所得的产物均为4,5-二氯-3-硝基邻苯二甲酸,故此反应没有一硝异构体。又由于4,5-二氯邻苯二甲酸分子结构中的氯及羧酸基团均使苯环钝化、当上了一个强吸电子硝基基团后,苯环活性进一步降低,很难再上一个硝基生成二硝化合物。本发明通过控制硝化温度、硝酸与4,5-二氯邻苯二甲酸的摩尔比,几乎定量生成4,5-二氯-3-硝基邻苯二甲酸。本发明实际选择的反应温度为55-60℃,反应时间1小时。硝酸与4,5-二氯邻苯二甲酸的摩尔比为(1-1.3)/1。反应结束后,将反应液倒入冰水中析出产品。经过滤可得4,5-二氯-3-硝基邻苯二甲酸。由于本发明第二步是在碱性溶液中进行水解。4,5-二氯-3-硝基邻苯二甲酸滤饼中带有的硫酸、硝酸会和下一步的碱液发生中和反应,所以本发明第一步硝化产物无需水洗和烘干。
7、在4,5-二氯-3-硝基邻苯二甲酸分子结构中,共有苯环4号位和苯环5号位的两个氯原子。4号位的氯原子其邻位有硝基,对位有吸电子的羧基,故4号位的氯原子极易水解成酚羟基。相反,5号位的邻位没有硝基。当4号位水解成羟基后,其做为5号位氯原子的邻位供电子基团,使得5号位氯原子更加难以水解。在第二步碱解反应过程中,只需要在氢氧化钠溶液中常压回流即可高收率的得到水解产物,即4-氯-5-羟基-6-硝基邻苯二甲酸。本发明的工艺是将4,5-二氯-3-硝基邻苯二甲酸与氢氧化钠水溶液混合后,以铜粉为催化剂加热至回流反应,反应结束过滤掉铜,滤液经酸化得到4-氯-5-羟基-6-硝基邻苯二甲酸。实际采用的氢氧化钠水溶液的质量浓度为40%,氢氧化钠与4,5-二氯-3-硝基邻苯二甲酸的摩尔比为(5-10)/1,铜粉质量是4,5-二氯-3-硝基邻苯二甲酸质量的1-5%,反应温度为100-105℃,反应时间为3-10小时。
8、第三步反应是4-氯-5-羟基-6-硝基邻苯二甲酸和尿素进行的亚胺化反应,其实际反应过程如下式:
9、
10、本发明参考邻苯二甲酰亚胺的合成方法,采用4-氯-5-羟基-6-硝基邻苯二甲酸和尿素无溶剂高温共熔得到产物。首先4-氯-5-羟基-6-硝基邻苯二甲酸在熔融状态时脱水生成4-氯-5-羟基-6-硝基邻苯二甲酸酐,生成的酸酐立即与尿素分解产生的氨生成开环酰胺。开环酰胺随即在高温条件下脱水关环得到产物4-氯-5-羟基-6-硝基邻苯二甲酰亚胺。本发明采取敞口操作以便生成的水及时蒸发出体系外。尿素分解产生的氨气也会有部分逸出,故本发明采取尿素与4-氯-5-羟基-6-硝基邻苯二甲酸的摩尔比为(2-3)/1。尿素在120-135℃之间开始分解并放出大量热能,体系温度最高会上升至180℃以上。随着体系内尿素的减少,放出的热能减少,需要额外使用电热套外部加热,并在160-180℃保温。本发明反应温度为160-180℃之间,反应时间为1-2小时。产物中有微量的未反应的4-氯-5-羟基-6-硝基邻苯二甲酸可用稀碳酸钠水溶液洗去。
11、第四步降级反应为经典霍夫曼降级反应。具体到本发明底物的反应来看,理论上有副反应生成。主反应的产物为本发明的目标中间体2-氨基-4-氯-5-羟基-6-硝基苯甲酸,副反应的产物为2-氨基-3-硝基-4-羟基-5-氯苯甲酸。主反应及副反应的反应式如下:
12、主反应:
13、
14、副反应:
15、
16、由上述反应式和霍夫曼降级反应的机理可知,控制4-氯-5-羟基-6-硝基邻苯二甲酰亚胺和氢氧化钠反应的开环方向是提高2-氨基-4-氯-5-硝基苯甲酸收率的关键。从结构上看由于硝基的吸电子效应,此步反应有利于主反应的发生。本发明采用等摩尔的氢氧化钠在水中低温下先开环,再与次氯酸钠溶液混合后滴加到浓碱中反应,这一操作可以得到90%以上的主反应转化率。实际采用质量浓度为5-10%的氢氧化钠溶液与4-氯-5-羟基-6-硝基邻苯二甲酰亚胺在5℃以下搅拌5-10小时进行开环反应,氢氧化钠与4-氯-5-羟基-6-硝基邻苯二甲酰亚胺的摩尔比为1/1。开环反应液与次氯酸钠混合后滴加到温度为50℃、质量浓度为50%、总重量为4-氯-5-羟基-6-硝基邻苯二甲酰亚胺20-50倍的氢氧化钠溶液中进行降级反应。次氯酸钠与4-氯-5-羟基-6-硝基邻苯二甲酰亚胺的摩尔比为(1-1.5)/1。滴加完成后在45-50℃之间保温反应2小时。再经酸化即得2-氨基-4-氯-5-羟基-6-硝基苯甲酸粗品。
17、反应液中过量的次氯酸钠可用30%的亚硫酸钠溶液淬灭。粗品中含有少量副反应生成的异构体2-氨基-3-硝基-4-羟基-5-氯苯甲酸,无需去除。它经过下一步反应后生成的杂质溶于水,可以轻松去除。
18、第五步重氮氯化反应是重氮盐sandmeyer取代反应,从反应机理上来说分为生成重氮盐、氯化两步反应,反应过程和机理如下式:
19、
20、实际操作时将先生成重氮盐溶液,再将重氮盐溶液滴加到氯化亚铜盐酸溶液中进行氯代反应。根据反应机理可知亚硝酸钠和氯化亚铜的用量均至少与2-氨基-4-氯-5-羟基-6-硝基苯甲酸等摩尔。本发明亚硝酸钠与2-氨基-4-氯-5-羟基-6-硝基苯甲酸的摩尔比为(1-1.2)/1,氯化亚铜与2-氨基-4-氯-5-羟基-6-硝基苯甲酸的摩尔比为(1-2)/1,所用盐酸均为质量浓度为36-38%。重氮盐工艺步骤中,盐酸与2-氨基-4-氯-5-羟基-6-硝基苯甲酸的质量比为(2-4)/1;氯化步骤所需的氯化亚铜盐酸溶液中,盐酸与氯化亚铜的质量比为(3-7)/1。重氮化反应温度0-5℃,氯化反应温度分为三个梯度:首先,将重氮盐溶液滴加到0-5℃的氯化亚铜盐酸溶液中,滴加完成后在0-5℃保温反应1-2小时;其次,将体系温度升至室温,搅拌3-5小时;最后,将体系温度升至50-60℃之间保温反应3-5小时。
21、三个阶段保温完成后,直接趁热过滤,再用20%的盐酸洗去滤饼中的氯化亚铜、再用50-60℃的自来水洗洗至中性后,烘干后即为本发明最终产物4,6-二氯-3-羟基-2-硝基苯甲酸。第四步带入的异构体2-氨基-3-硝基-4-羟基-5-氯苯甲酸经重氮氯化后生成的2,5-二氯-3-硝基-4-羟基苯甲酸杂质随温水除去。
22、本发明试验操作按以下方式进行:①,将计量好的4,5-二氯邻苯二甲酸、浓硫酸和一定量的发烟硝酸在55-60℃反应1小时。反应结束后,将反应液倒入冰水中析出产品。经过滤、烘干得到4,5-二氯-3-硝基邻苯二甲酸;②,将计量好的4,5-二氯-3-硝基邻苯二甲酸加入到一定量的40%氢氧化钠水溶液中,再加入一定数量的铜粉,升温回流3-10小时后过滤铜,滤液用盐酸酸化,经过滤、烘干得到4-氯-5-羟基-6-硝基邻苯二甲酸;③,将计量好的4-氯-5-羟基-6-硝基邻苯二甲酸和尿素加入到反应瓶中,升温到160-180℃保温并保温反应1-2小时,加水打浆,过滤、烘干得到4-氯-5-羟基-6-硝基邻苯二甲酰亚胺;④,将计量好的4-氯-5-羟基-6-硝基邻苯二甲酰亚胺加到一定量的5-10%的氢氧化钠溶液,在5℃以下搅拌5-10小时,再滴加次氯酸钠溶液。再将此混合液滴加到温度为50℃、质量浓度为50%的氢氧化钠溶液中进行降级反应。滴加完成后在45-50℃之间保温反应2小时。反应液经酸化、过滤、烘干得到2-氨基-4-氯-5-羟基-6-硝基苯甲酸粗品;⑤,将计量好的亚硝酸钠分批加入到一定量的2-氨基-4-氯-5-羟基-6-硝基苯甲酸和盐酸的混合体系中,再将此混合液滴加到氯化亚铜盐酸溶液,并在0-5℃、室温,50-60℃三个温度区间分别保温反应一段时间。过滤、盐酸洗、水洗、烘干得到4,6-二氯-3-羟基-2-硝基苯甲酸。
23、相比于现有公开技术,本发明采用了价廉易得的原料,减少了硝化高危工艺的次数,避免了高危还原工艺。本发明工艺具有转化率高、生产效率高、全程都不使用有机溶剂等优点,避免了回收溶剂造成大量繁琐工序及由此带来的安全风险,五步反应总摩尔收率最高可达到76%以上。
- 还没有人留言评论。精彩留言会获得点赞!