基于CRISPR/Cas13a的IHHNV的检测试纸条及其制备方法与流程
本发明涉及一种检测试纸条及其制备方法,尤其涉及一种基于crispr/cas13a的ihhnv的检测试纸条及其制备方法,其属于水生动物病毒病害检测。
背景技术:
1、试纸检测技术是一种基于目视判别颜色变化的可视化快速检测技术,具有直观、快速检测的特点,试纸条技术突破了制约安全监管能力的技术瓶颈,具有便携、简易、快速的特点,适用于田间与基层检测。试纸条技术目前已在食品检测、医学检测等领域得到广泛应用,如转基因食品检测试纸条、早早孕试纸、沙门氏菌检测试纸条、病毒性脑病与视网膜病试纸等。基于试纸条检测的原理,试纸条主要包括胶体金免疫层析试纸、酸碱试纸(ph试纸)、核酸试纸等。
2、酶联免疫技术(elisa)是一项现代医学、生物学检测常用的技术。尽管在90年代初期,由于以pcr技术为代表的分子生物学技术的发明,人们开始预测,酶联免疫技术将会被更高、更灵敏的方法所替代。但是由于免疫临床标记物质具有无法替代的意义,以及酶联免疫实验是一种基于蛋白水平上的检测,检测结果稳定,不易受分子生物检测假阳性气溶胶等一些极微量物质的干扰,因而并没有被淘汰,加之酶联免疫系统检测方法近些年来在灵敏度和特异性方面也在不断的完善,因而该项技术还是在传染病血清学检测、肿瘤检测方面占据主导地位。
3、分子生物学技术与酶联免疫技术的结合将分子生物学检测的高特异性、高灵敏度与酶联免疫技术的可视化相结合,在一定程度上为疫病检测突破常规实验室检测仪器与环境的束缚奠定了强有力的基础,rpa-crispr检测试纸就是一种将核酸的聚合酶扩增与信号的酶联免疫放大相结合的技术,具有直观、可视、便携的优点,rpa-crispr是一种基于探针对目的蛋白靶序列的检测,该检测方法灵敏度高,探针特异性好,但对水生动物疫病的检测方法,目前还未见有报道。
技术实现思路
1、本发明的目的是:为克服现有技术中存在的不足,提供一种基于crispr/cas13a的ihhnv的检测试纸条及其制备方法,该检测试纸条具有超强的灵敏性及特异性,有望为水生动物病毒病害的动态检测和控制提供新的分子检测技术。
2、本发明解决上述技术问题的技术方案如下:
3、一种基于crispr/cas13a的ihhnv的检测试纸条,所述检测试纸条包括用于ihhnv检测的rpa扩增体系和crispr/cas13a检测体系;
4、所述rpa扩增体系包括针对ihhnv基因的特异性rpa引物;所述特异性rpa引物为ihhnv-rpa-f和ihhnv-rpa-r,二者的核苷酸序列如下:
5、ihhnv-rpa-f:
6、5’-cctctaatacgactcactataggcctcgcctatttgggagttacctttgctg-3’;
7、ihhnv-rpa-r:5’-atggtccgtctactgcgtcttcgtctctt-3’;
8、所述crispr/cas13a检测体系包括针对ihhnv基因的特异性crrna,所述特异性crrna为ihhnv-crrna。
9、一种基于crispr/cas13a的ihhnv的检测试纸条的制备方法,包括以下步骤:
10、步骤一、胶体金标记抗fam小鼠igg抗体的最佳浓度:
11、利用mey氏稳定性试验确定抗fam小鼠igg抗体与胶体金最佳标记量,分别在酶标孔加入胶体金溶液100μl,依次加入抗fam小鼠igg抗体3、4、5、6、7、8、9、10、11、12、13、14μg/ml;混匀静置5min,而后加入10%氯化钠溶液20μl,静置15min观察,随着加入单抗量的增加,胶体金颜色由紫黑色逐渐变为红色并稳定,越接近胶体金本色的溶液中所含的浓度最合适,即最佳标记量为8μg/ml;
12、步骤二、胶体金标记抗fam小鼠igg抗体的最佳ph值:
13、取一条酶标板,在前七个加入100μl的胶体金溶液和上面确定的最合适浓度抗fam小鼠igg抗体,之后从前往后依次加入5μl,7μl,9μl,11μl,13μl,15μl,17μl的0.01mol/l的k2co3溶液,室温静置15min;使用酶标仪进行扫描,获得胶体金可见光od520值,以出现最大od520值时所对应的胶体金ph为最佳标ph值,即每毫升胶体金加入13μl 0.01mol/l k2co3为最佳标记ph;
14、步骤三、蛋白a和链霉亲和素蛋白包被浓度和金标抗体喷量的确定:
15、确保试纸条的检测线t在一定的范围内颜色不消失,同时检测线t和质控线c的比值呈一定的比例变化,确立的最佳反应条件为:检测线t包被蛋白a浓度为0.12mg/ml,以1μl/cm的浓度喷洒;质控线c包被链霉亲和素蛋白浓度为1mg/ml,以1μl/cm的浓度喷洒;样品垫上金标抗体的喷量为3.8μl/cm,此时,阳性结果的t线和c线显色适中,且能呈一定的比例变化;
16、步骤四、试纸条的组装:
17、根据上述摸索的条件,用胶体金制作系统将蛋白a和链霉亲和素蛋白包被在硝酸纤维素膜上,室温干燥,包被好的硝酸纤维素膜和干燥剂放置于铝箔袋,避光干燥4℃保存备用;从上至下依次将样品垫、金垫、硝酸纤维素膜、吸水纸首尾互相衔接,粘贴在pvc底板上,用胶体金制作系统将试纸条裁剪合适的规格,试纸条和干燥剂放置于铝箔袋,避光干燥4℃保存备用。
18、更进一步的,针对ihhnv的保守区设计了crrna,ihhnv的crrna序列构成主要为:t7启动子序列、lwcas13a repeatrna间隔序列和ihhnv的保守区,所述ihhnv-crrna序列为:
19、5’-taatacgactcactataggggauuuagacuaccccaaaaacgaaggggacuaaaactgututttctuucuugtugtcgcttcugctt-3’。
20、更进一步的,在所述crispr/cas13a检测体系中,lwcas13a蛋白的最佳工作浓度为2.2ng/μl。
21、更进一步的,在所述crispr/cas13a检测体系中,crrna的最佳工作浓度为3.125ng/μl。
22、所述检测试纸条在制备检测ihhnv产品中的应用。
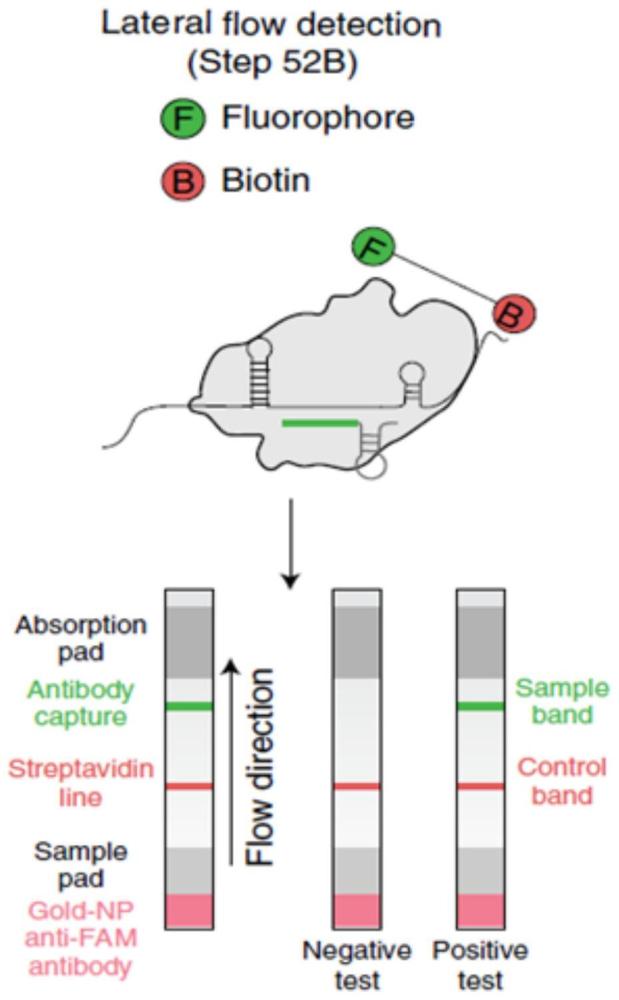
23、本发明的有益效果是:采用crispr技术,设计筛选靶向病原特异性序列的向导rna,并结合rpa技术,构建核酸检测扩增体系,通过设计使rna的等温扩增步骤和cas酶检测的化学反应在同一个反应管中进行,从而降低检测流程的复杂性以及由于样本转移步骤可能带来的污染,最终结果通过试纸条上条带的位置进行判定。该检测试纸条具有超强的灵敏性及特异性,实现针对虾病原的快速灵敏的即时检测鉴定,有望为水生动物病毒病害的动态检测和控制提供新的分子检测技术。
技术特征:
1.一种基于crispr/cas13a的ihhnv的检测试纸条,其特征在于:所述检测试纸条包括用于ihhnv检测的rpa扩增体系和crispr/cas13a检测体系;
2.一种基于crispr/cas13a的ihhnv的检测试纸条的制备方法,其特征在于,包括以下步骤:
3.根据权利要求1所述的基于crispr/cas13a的ihhnv的检测试纸条,其特征在于:针对ihhnv的保守区设计了crrna,ihhnv的crrna序列构成主要为:t7启动子序列、lwcas13arepeatrna间隔序列和ihhnv的保守区,所述ihhnv-crrna序列为:
4.根据权利要求1所述的基于crispr/cas13a的ihhnv的检测试纸条,其特征在于:在所述crispr/cas13a检测体系中,lwcas13a蛋白的最佳工作浓度为2.2ng/μl。
5.根据权利要求1所述的基于crispr/cas13a的ihhnv的检测试纸条,其特征在于:在所述crispr/cas13a检测体系中,crrna的最佳工作浓度为3.125ng/μl。
6.一种权利要求1所述检测试纸条在制备检测ihhnv产品中的应用。
技术总结
本发明涉及一种基于CRISPR/Cas13a的IHHNV的检测试纸条及其制备方法,属于水生动物病毒病害检测技术领域,所述检测试纸条包括用于IHHNV检测的RPA扩增体系和CRISPR/Cas13a检测体系;所述RPA扩增体系包括针对IHHNV基因的特异性RPA引物;所述特异性RPA引物为IHHNV‑RPA‑F和IHHNV‑RPA‑R,所述CRISPR/Cas13a检测体系包括针对IHHNV基因的特异性crRNA,所述特异性crRNA为IHHNV‑crRNA。该检测试纸条具有超强的灵敏性及特异性,有望为水生动物病毒病害的动态检测和控制提供新的分子检测技术。
技术研发人员:梁君妮,尹伟力,刘秀丽,杨柏,张静,王云霞,李金庆,史青,徐娟
受保护的技术使用者:烟台海关技术中心
技术研发日:
技术公布日:2024/4/22
- 还没有人留言评论。精彩留言会获得点赞!