一种精准延迟药物释放的DNA计时器装置
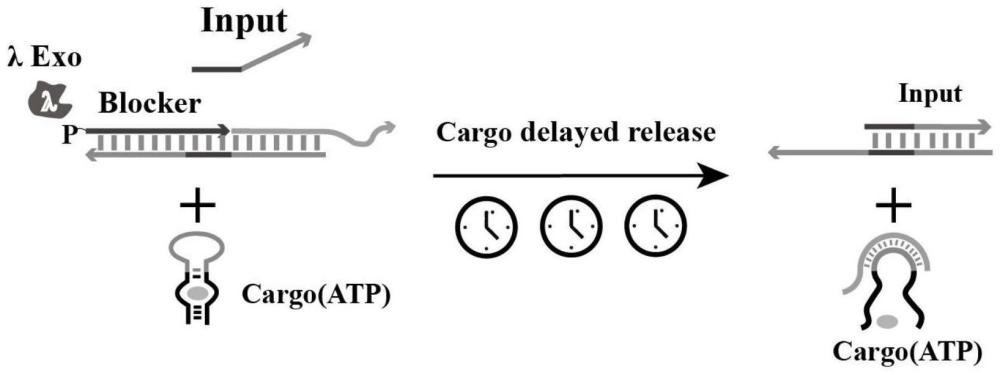
本发明涉及一种动态dna纳米技术,通过dna计时器装置中的blocker浓度与λexo浓度的调控来精准延迟dna链置换反应,从而进一步延迟药物(atp)的释放。
背景技术:
1、随着分子生物学和分析化学的快速发展,近年来构建了众多可实现各种先进功能的人工分子反应网络,并在程序化材料的自组装、逻辑运算、以及信息存储与加密等方面取得了突破性进展。其中,核酸纳米技术以其高精度、高灵敏度、优良的可编程性等特点,成为构建新型分子反应网络的理想工具。其特有的沃森-克里克碱基对相互作用、可编程模块、精细调整的动力学和可预测的结构使精确控制和预测化学反应成为可能。
2、为提高疾病治疗的疗效,临床常采用多药联合治疗,但多药联合用药往往导致多药耐药和性能下降,产生的副作用比单药治疗更严重。根据疾病的治疗阶段,在不同的时间或不同的位置有控制的顺序释放药物,可以简化治疗,减少给药次数,避免多次数、大剂量带来的耐药性和毒副作用。从而缩短康复时间,减少不必要的医疗费用,更利于复杂疾病尤其是慢性疾病的有效治愈。目前临床一般通过外界植入装置来定时释放药物,但仍存在侵入性、排斥反应、植入与导出的操作复杂性等。要实现药物的顺序释放,同时满足无创、生物兼容、操作简便,仍然是个难题。
3、为了应对这些挑战,本发明利用磷酸标记的封闭链(blocker)对底物链toehold区域进行封闭,利用λ核酸外切酶(λexo)从dna双链的5’磷酸端向3’端的水解方向性,对封闭链进行逐步水解。只有在blocker完全水解之后,才可以发生链置换反应,从而达到控制链置换反应时间的目的。通过可以精确延迟的链置换反应构建起一种动态dna计时器装置,实现对反应时间维度的控制。进一步将反应的输出链设计为药物适配体链的互补序列,通过控制输出链的释放,即可实现药物的延迟释放。本发明通过控制λexo的浓度和封闭链浓度两个维度,分别实现了对药物的顺序释放,且释放效率能维持在95%以上。我们证明该方法对药物延迟释放具有较好的控制能力,有望解决临床用药时对释放时间的精准控制的难题,在提高疗效、降低副作用和耐药性等方面,具有巨大潜力。
技术实现思路
1、本发明的目的是开发出一种简单、直接、可精准延迟dna链置换反应和药物(atp)释放的dna计时器装置。
2、具体技术方案如下:
3、1.一种精准延迟药物释放的dna计时器装置,其构建方法包括以下步骤:
4、(1)探针组装:
5、dna计时器装置的封闭连,模板探针,荧光探针,猝灭探针和触发链在1×λexo反应缓冲液(67mm glycine-koh,2.5mm mgcl2,50μg/ml bsa)中95℃5min后,以每秒0.1℃的速率下降至4℃,并保持30min,放在4℃冰箱备用;
6、(2)聚丙烯酰胺凝胶电泳流程
7、向体系中加入dna延迟链置换各个组件和相应触发链,反应在pcr管中进行,孵育后将反应产物加入配制好的聚丙烯酰胺凝胶中进行电泳;15ml 12%聚丙烯酰胺凝胶的配制方法为:向管中加入ddh2o(6ml),30%acrylamide(6ml),5×tbe(3ml),temed(10μl),(10%)ap(110μl),37℃孵育;通过产物条带的变化分析链置换反应发生情况和酶对blocker的消耗情况;
8、(3)dna适配体装载与释放atp货物
9、atp与dna适配体链在1×λexo反应缓冲液中(67mm glycine-koh,2.5mm mgcl2,50μg/ml bsa)用pcr管混合。atp适配体在5′端和3′端分别用bhq1和fam标记,在37℃下与atp孵育1h,确保适配体与atp完全结合并猝灭荧光;适配体互补链相比于atp更容易与适配体结合的序列,体系中存在一定浓度的适配体互补链后,互补链与适配体结合,从而释放出大量atp;
10、(4)pcr循环仪器实时荧光分析
11、加入不同blocker浓度或不同λexo浓度来调控链置换反应或atp延迟释放的时间,反应温度为37℃,反应时间为150-200分钟,反应体系为20μl,在pcr管中进行;延迟系统使用1×λexo缓冲液:67mm glycine-koh,2.5mm mgcl2,50μg/ml bsa。在添加λexo和触发链后,立即用实时pcr循环仪器(rotor gene,qiagen)在37℃下记录荧光,时间间隔为20s。
12、2.所述步骤(2)中聚丙烯酰胺凝胶37℃孵育时间为60min。
13、3.所述步骤(2)中dna计时器装置各个探针的浓度是400nm。
14、4.所述步骤(2)中触发链的浓度是300nm。
15、5.所属步骤(2)中电泳的电压和电流条件分别为130v与90ma。
16、6.所述步骤(3)中atp浓度是0.5mm。
17、7.所述步骤(3)中atp dna适配体浓度是100nm。
18、8.所述步骤(4)中λexo梯度浓度是0.001u/μl,0.002u/μl,0.003u/μl,0.004u/μl,0.005u/μl。
19、9.所述步骤(4)中blocker梯度浓度是200nm,400nm,600nm,800nm,1000nm。
20、10.所述步骤(4)中λexo缓冲液ph是9.4。
21、本发明利用动态dna纳米技术编程链置换系统,开发了一种能够精准延迟dna链置换反应和药物atp释放的dna计时器装置。通过加入blocker将链置换反应的toehold区域进行封闭,只有在blocker完全被水解后,toehold区域才得以暴露出来。因此通过控制blocker完全水解的时间,可以实现对链置换反应开始发生的精准时间调控。本发明之所以可以精准编程时间信息,是因为选择的λexo作用于双链dna,沿5′→3′方向逐步切去5′单核苷酸。最适底物是5′磷酸化的双链dna。由于其切割双链dna的方向性,使得在模板链上的blocker还未完全暴露出toehold区域时,就及时被新的游离blocker替换,保证了toehold区域直至所有游离blocker完全水解后才能真正暴露。临床上对药物的延迟释放仍是通过外界植入装置来定时释放药物,仍然存在植入与导出的操作复杂性,因此控制给药后药物在体内的释放时间是最为有效的解决方案之一。通过应用动态dna纳米技术编程链置换系统的计时器特点,我们成功实现了精确延迟药物atp的高效率释放。
22、page(聚丙烯酰胺凝胶电泳)分析首先用于验证链置换反应发生情况和酶对blocker的消耗情况。图1中前五个泳道分别是动态dna编程计时器的各个组件,后面五个泳道的page结果说明在λexo存在的条件下,blocker可以被完全消耗,链置换反应可以随之发生。如果存在blocker和input触发链,在没有λexo存在的条件下,不会发生任何链置换反应,证明blocker可以很好地封闭住toehold区域,在没有酶存在的条件下阻止链置换反应的发生。
23、接着我们通过监测链置换反应荧光动力学来确定影响反应发生时间的因素。我们的触发链(input)可以通过toehold介导的链置换反应置换掉标记有bhq基团的猝灭链,使bhq与fam分离而发出荧光(图2)。通过pcr循环仪器(rotor gene,qiagen)检测荧光强度即可监测链置换反应的延迟情况。我们分别从blocker浓度与λexo浓度两个维度调节链置换反应发生的时间。从图3-4可以看出,随着blocker浓度的增加,链置换反应发生时间延长。同理,随着λexo浓度的下降,反应时间也逐渐变长(图5-6)。接着我们将输出链换为atp适配体的互补序列,在输出链游离的条件下会与atp适配体结合,从而阻止atp与适配体链的结合,实现药物的释放。在37℃1h孵育后,所有的atp适配体序列都装载了药物atp。接着在图7中,我们将装载药物与dna计时器装置混合在同一体系中,在输入触发链和λexo后就开始了延迟atp释放的反应。通过调控blocker浓度与λexo浓度,我们成功实现了atp的延迟释放,且释放时间与两者具有很好的相关性(图8-11)。
24、进一步,我们通过输入不同浓度的触发链可以释放相应浓度的atp,随着触发链浓度的增高,atp浓度也会进一步升高(图12)。可以看出在图13中,加入blocker链发生延迟后,atp的释放量依旧与触发链浓度正相关。通过统计同浓度触发链释放atp有延迟和无延迟情况的比例,我们发现即使在有延迟的情况下,atp的释放效率依旧很高(图14)。
25、本专利提出了一种简单精准的dna计时器装置,利用动态dna纳米技术的可编程性,只需要简单的元件调控就可实现对药物的精准延迟释放。该方法的简易性、精准性、稳定性、普适性,使其可以进一步扩展到包括药物的多个领域进行实际应用。未来有望进一步用于设计更为智能和复杂的体内和体外药物释放反应网络。
- 还没有人留言评论。精彩留言会获得点赞!