一种抗人白介素12P70抗体及其应用的制作方法
本发明涉及生物检测领域。具体地说,本发明涉及一种抗人白介素12p70抗体及其应用。
背景技术:
1、白介素12p70(il-12p70)是一种多生物学活性的细胞因子,其在抗瘤免疫中的重要作用是通过巨噬细胞、nk细胞调节的自然抵抗力以及通过th1细胞、nk1.1+tcrint细胞、ctl细胞介导的获得性免疫之间建立联系的。白介素12p70调节肿瘤患者的免疫应答是肿瘤治疗的一个新的、有前途的策略。因此开发一种高灵敏度的白介素12p70蛋白检测方法学,具有非常重要的临床意义。
2、il-12p70在正常人体内含量极低(小于100ng/l),目前市场上的检测方法均为elisa法,比如r&d公司的il-12elisa试剂盒检测灵敏度为15ng/l,线性区间为31.2-2,000ng/l,批内cv%大于5.5。对于低于31.2ng/l和高于2,000ng/l的患者难以准确测定。因此,本领域需要建立一种高灵敏宽检测区间的il-12p70的检测方法。
3、此外,目前市场上的部分检测方法为cba(cytometric bead array)法。以bd公司的il-12p70 cbakit为例,其灵敏度为10ng/l,线性区间为20-5000ng/l。其灵敏度和线性范围仍有待提高。更重要的是,人体中除il-12p70外还存在il-12p40、il-23、il-35等与il-12p70具有高度同源性的物质,在检测时容易出现假阳性。
4、为了提高cba检测方法的特异性和灵敏度,目前业内的共识是采取抗白介素12p70的单克隆抗体对来开发相应的cba检测试剂盒。但是,目前市面上针对白介素12p70的cba检测试剂盒,其灵敏度和特异性普遍较低。并且所使用的小鼠单克隆抗体依赖于传统的杂交瘤方法开发和生产,制备工艺相较于重组单抗更为复杂,也存在较大批间差。因此,利用小鼠单抗所开发elisa检测试剂盒存在着灵敏度不高、线性范围窄、批间差较难控制等挑战。
5、现有技术(cn201410837988.7)公开了一种il-12检测试剂盒,其利用alphalisa技术进行检测。虽然较elisa法进行了改进提高了灵敏度、线性范围有所加宽,但是仍存在可以改进的空间。
6、因此,本领域需要建立一种高灵敏、宽检测区间、高特异性的il-12p70的检测方法。
技术实现思路
1、本发明的目的就是提供一种高灵敏、宽检测区间、高特异性的il-12p70的检测方法。
2、本发明提供了一种抗人白介素12p70抗体和抗体组合。
3、本发明提供了包含抗人白介素12p70抗体组合的检测试剂盒及其应用。
4、在本发明的第一方面,提供了一种抗人白介素12p70蛋白的抗体,所述的抗体包括重链和轻链,所述的重链包括重链可变区hcvr,所述的轻链包括轻链可变区lcvr,其中,所述的重链可变区包括以下互补决定区cdr:
5、氨基酸序列如seq id no:2所示的cdr-h1;
6、氨基酸序列如seq id no:4所示的cdr-h2;
7、氨基酸序列如seq id no:6所示的cdr-h3;
8、所述的轻链可变区包括以下互补决定区cdr
9、氨基酸序列如seq id no:8所示的cdr-l1;
10、氨基酸序列如seq id no:10所示的cdr-l2;
11、氨基酸序列如seq id no:12所示的cdr-l3。
12、在另一优选例中,所述重链可变区和轻链可变区分别进一步包括骨架区(fr)。
13、在另一优选例中,所述的轻重链可变区的cdr1、cdr2和cdr3分别由骨架区fr1、fr2、fr3和fr4所隔开。
14、在另一优选例中,所述抗体的hcvr氨基酸序列如seq id no:14所示,或与其具有≥85%、≥90%、≥95%、≥96%、≥97%、≥98%或≥99%的序列同一性。
15、在另一优选例中,所述抗体的lcvr氨基酸序列如seq id no:16所示,或与其具有≥85%、≥90%、≥95%、≥96%、≥97%、≥98%或≥99%的序列同一性。
16、在另一优选例中,所述抗体的hcvr具有如序列seq id no:14所示的氨基酸序列,和/或lcvr具有如seq id no:16所示的氨基酸序列。
17、在另一优选例中,所述的抗体的轻链和/或重链进一步包括恒定区。
18、在另一优选例中,所述的恒定区为人源恒定区。
19、在另一优选例中,所述抗体的重链氨基酸序列如seq id no:18所示,或与其具有≥85%、≥90%、≥95%、≥96%、≥97%、≥98%或≥99%的序列同一性。
20、在另一优选例中,所述抗体的轻链氨基酸序列如seq id no:20或与其具有≥85%、≥90%、≥95%、≥96%、≥97%、≥98%或≥99%的序列同一性。
21、在另一优选例中,所述抗体的重链具有如seq id no:18所示的氨基酸序列,和/或轻链具有如seq id no:20所示的氨基酸序列。
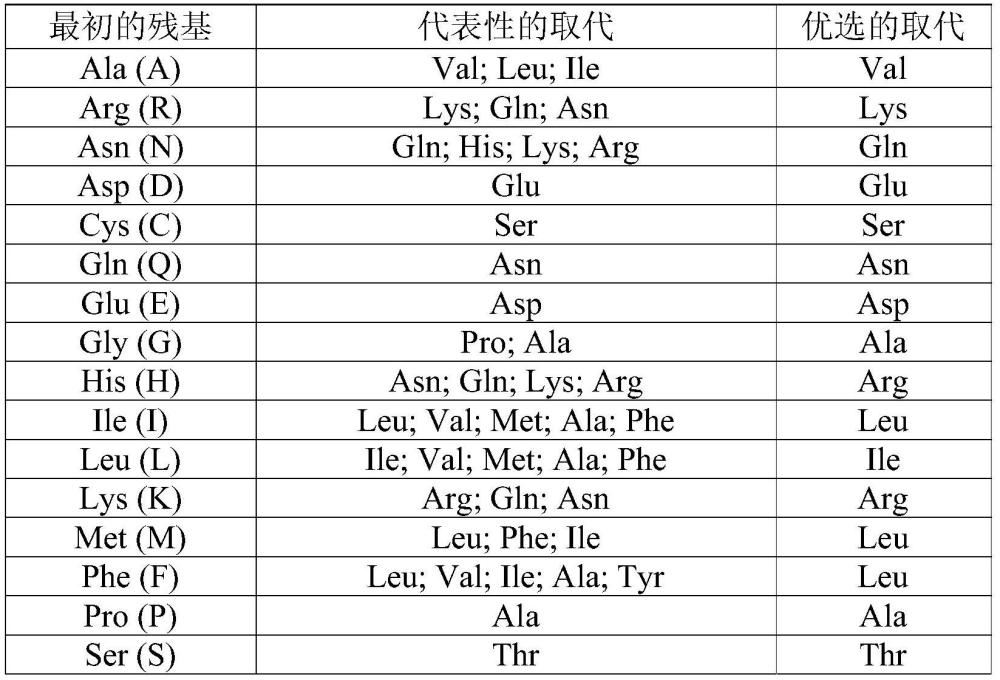
22、在另一优选例中,上述氨基酸序列中任意一种还包括任选地经过添加、缺失、修饰和/或取代至少一个氨基酸的,并能够保留人白介素12p70蛋白结合亲和力的衍生序列。
23、在另一优选例中,所述添加、缺失、修饰和/或取代的氨基酸数量,不超过初始氨基酸序列总氨基酸数量的30%,较佳地为20%,更佳地为10%。
24、在另一优选例中,所述的抗体为动物源抗体、嵌合抗体或人源化抗体。
25、在另一优选例中,所述的抗体为单链抗体、双链抗体、或抗原结合片段。
26、在本发明的第二方面,提供了一种融合蛋白,所述融合蛋白包括:
27、(1)如本发明第一方面所述的抗体;和
28、(2)任选的协助表达和/或纯化的标签序列。
29、在另一优选例中,所述标签包括fc标签、flag标签、6his标签,或其组合。
30、在本发明的第三方面,提供了一种多核苷酸,所述多核苷酸编码如本发明第一方面所述的抗体或如本发明第二方面所述的融合蛋白。
31、在本发明的第四方面,提供了一种载体,所述载体含有如本发明第三方面所述的多核苷酸。
32、在另一优选例中,所述表达载体选自下组:dna、rna、病毒载体、质粒、转座子、其他基因转移系统,或其组合。优选地,所述表达载体包括病毒载体,如慢病毒、腺病毒、aav病毒、逆转录病毒,或其组合。
33、在本发明的第五方面,提供了一种遗传工程化的宿主细胞,所述宿主细胞含有如本发明第四方面所述的载体、或基因组中整合有外源的如本发明第三方面所述的多核苷酸。
34、在另一优选例中,所述宿主细胞包括原核细胞或真核细胞。
35、在另一优选例中,所述宿主细胞选自下组:大肠杆菌、酵母细胞、哺乳动物细胞。
36、在本发明的第六方面,提供了一种抗体偶联物,该抗体偶联物含有:
37、(a)抗体部分,所述抗体部分为如本发明第一方面所述的抗体;和
38、(b)与所述抗体部分偶联的偶联部分,所述偶联部分选自下组:可检测标记物、药物、或其组合。
39、在另一优选例中,所述抗体部分与所述可检测标记物通过化学键或接头进行偶联。
40、在另一优选例中,所述可检测标记物选自下组:荧光或发光标记物、生物素、放射性标记物、mri(磁共振成像)或ct(电子计算机x射线断层扫描技术)造影剂,或能够产生可检测产物的酶、金纳米颗粒/纳米棒、纳米磁粒、或任何形式的纳米颗粒。
41、在另一优选例中,所述的可检测标记物为生物素。
42、在另一优选例中,所述的药物为小分子药物、生物因子、或其组合。
43、在另一优选例中,所述的药物为细胞毒性药物(毒素)。
44、在另一优选例中,所述的细胞毒性药物选自下组:抗微管蛋白药物、dna小沟结合试剂、dna复制抑制剂、烷化试剂、抗生素、叶酸拮抗物、抗代谢药物、化疗增敏剂、拓扑异构酶抑制剂、长春花生物碱、或其组合。
45、在本发明的第七方面,提供了一种抗人白介素12p70蛋白的抗体组合,所述抗体组合包括:
46、抗体s1,所述抗体s1的重链可变区包括以下互补决定区cdr:
47、氨基酸序列如seq id no:1所示的cdr-h1,
48、氨基酸序列如seq id no:3所示的cdr-h2,
49、氨基酸序列如seq id no:5所示的cdr-h3,
50、抗体s1的轻链可变区包括以下互补决定区cdr:
51、氨基酸序列如seq id no:7所示的cdr-l1,
52、氨基酸序列如seq id no:9所示的cdr-l2,
53、氨基酸序列如seq id no:11所示的cdr-l3;和
54、抗体s2,所述抗体s2为如本发明第一方面所述的抗体。
55、在另一优选例中,所述重链可变区和轻链可变区分别进一步包括骨架区(fr)。
56、在另一优选例中,所述的轻重链可变区的cdr1、cdr2和cdr3分别由骨架区fr1、fr2、fr3和fr4所隔开。
57、在另一优选例中,抗体s1的hcvr具有如序列seq id no:13所示的氨基酸序列和/或lcvr具有如seq id no:15所示的氨基酸序列。
58、在另一优选例中,抗体s2的hcrv具有如序列seq id no:14所示的氨基酸序列和/或lcvr具有如seq id no:16所示的氨基酸序列。
59、在另一优选例中,所述的抗体的轻链和/或重链进一步包括恒定区。
60、在另一优选例中,所述的恒定区为人源恒定区。
61、在另一优选例中,抗体s1的重链具有如seq id no:17所示的氨基酸序列,和/或轻链具有如seq id no:19所示的氨基酸序列。
62、在另一优选例中,抗体s2的重链具有如seq id no:18所示的氨基酸序列,和/或轻链具有如seq id no:20所示的氨基酸序列。
63、在另一优选例中,上述氨基酸序列中任意一种还包括任选地经过添加、缺失、修饰和/或取代至少一个氨基酸的,并能够保留人白介素12p70蛋白结合亲和力的衍生序列。
64、在另一优选例中,所述添加、缺失、修饰和/或取代的氨基酸数量,不超过初始氨基酸序列总氨基酸数量的30%,较佳地为20%,更佳地为10%。
65、在另一优选例中,所述的抗体为动物源抗体、嵌合抗体或人源化抗体。
66、在另一优选例中,所述的抗体为单链抗体、双链抗体、或抗原结合片段。
67、在本发明的第八方面,提供了如本发明第一方面所述的抗体、如本发明第三方面所述的多核苷酸、如本发明第四方面所述的载体、如本发明第五方面所述的宿主细胞、如本发明第六方面所述的抗体偶联物、或如本发明第七方面所述的抗体组合的用途,用于制备:
68、i)检测人白介素12p70蛋白的试剂或试剂盒;
69、ii)治疗人白介素12p70相关疾病的制剂或药物。
70、在另一优选例中,所述人白介素12p70相关疾病选自下组:炎症相关疾病、肿瘤、自身免疫疾病、或其组合。
71、在另一优选例中,所述的制剂或药物为液体剂型,较佳地为注射剂。
72、在另一优选例中,所述的药物为细胞治疗药物。
73、在本发明的第九方面,提供了一种人白介素12p70蛋白检测试剂盒,所述试剂盒包含如本发明第一方面所述的抗体、如本发明第六方面所述的抗体偶联物、或如本发明第七方面所述的抗体组合。
74、在另一优选例中,所述的检测试剂盒用于双抗夹心法检测。
75、在另一优选例中,所述的检测试剂盒用于cba检测、elisa检测和/或胶体金检测。
76、在另一优选例中,所述的试剂盒为cba试剂盒。
77、在另一优选例中,所述的检测试剂盒包含如本发明第六方面所述的抗体组合,其中,抗体s1固定于载体并用于捕获人白介素12p70蛋白,抗体s2偶联检测标记物。
78、在另一优选例中,所述的检测试剂盒中包含微球(如荧光微球),所述微球包被有所述抗体s1。
79、在另一优选例中,所述的检测试剂盒中包括带有生物素的抗体s2。
80、在另一优选例中,所述的检测试剂盒进一步包括人白介素12p70蛋白标准品。
81、在另一优选例中,所述的检测试剂盒进一步包括选自下组的组分:荧光蛋白标记的链霉亲和素、冻干白介素12p70标准品、洗液、样品稀释液、基质缓冲液、或其组合。
82、在另一优选例中,所述的荧光蛋白为藻红蛋白。
83、在本发明的第十方面,提供了一种检测样品中白介素12p70的方法,使用如本发明第一方面所述的抗体、如本发明第六方面所述的抗体偶联物、如本发明第七方面所述的抗体组合、或如本发明第九方面所述的检测试剂盒进行检测。
84、在另一优选例中,所述的方法包括以下步骤:
85、1)将抗体s1固定于载体上;
86、2)使用可检测标记物标记抗体s2;
87、3)将所述抗体s1、s2和待测样品共同孵育,从而使抗体s1、s2与样品中的白介素12p70结合;
88、4)洗去未结合于载体的试剂,检测所述可检测标记物,从而检测白介素12p70。
89、在另一优选例中,所述的检测为定量检测。
90、在另一优选例中,所述的载体为微球,较佳地为荧光微球。
91、在另一优选例中,所述的可检测标记物为生物素。
92、在另一优选例中,步骤4)中,包括步骤:
93、加入荧光蛋白标记的亲和素并孵育从而连接抗体s2上的生物素,并对所述荧光蛋白进行检测。
94、在另一优选例中,所述的亲和素为链霉亲和素。
95、在另一优选例中,所述的荧光蛋白为藻红蛋白。
96、在另一优选例中,所述的方法还包括步骤:对白介素12p70标准品进行检测从而获得标准曲线,根据标准曲线计算被测样品中白介素12p70的含量。
97、在另一优选例中,所述的所述白介素12p70为人白介素12p70。
98、在另一优选例中,所述的待测样品选自下组:细胞培养液、全血、血清、血浆、体液、或其组合。
99、在本发明的第十一方面,提供了一种药物组合物,其含有:
100、(i)如本发明第一方面所述的抗体、如本发明第三方面所述的多核苷酸、如本发明第四方面所述的载体、如本发明第五方面所述的宿主细胞、如本发明第六方面所述的抗体偶联物、或如本发明第七方面所述的抗体组合、或其组合;和
101、(ii)药学上可接受的载体。
102、在另一优选例中,所述的药物组合物为注射剂型。
103、在另一优选例中,所述的药物组合物中还含有其他的治疗炎症相关疾病、肿瘤、或自身免疫疾病的药物。
104、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!