钙蛋白粒子的吸附材料以及吸附除去系统及其利用方法与流程
本发明涉及体液中的钙蛋白粒子(calciproteinparticle)的吸附技术。
背景技术:
当高血压症、糖尿病、脂质异常症等生活习惯病、慢性肾脏病、因吸烟或增龄等引起的动脉硬化变严重时,由于血管的慢性炎症等而在血管内形成的斑块将吸收血液中的钙而会引起异位钙化。由于异位钙化而在血管内形成的血管钙化,在如脑血管、冠动脉这样的动脉引起狭窄,与脑梗塞、狭心症、心肌梗塞等的发病直接相关。已知血液中的钙离子例如以属于磷酸钙与血清蛋白fetuin-a的复合体的钙蛋白粒子(calciproteinparticle;cpp)的形式存在,会成为引起这样的血管钙化、慢性炎症等的原因物质。另外,还报道有上述钙蛋白粒子在慢性肾脏病患者中随着肾功能下降而血中量上升,即使透析也无法除去(非专利文献1~3)。
因此,对于动脉硬化变严重的患者以及慢性肾脏病等的高危患者,给药抑制血液凝固的抗血小板药,或者以间接地控制血液中的磷量为目的,进行饮食控制或给药磷吸附药等来实施预防、治疗,但尽管如此,仍然对很多患者无法控制风险。此外,不存在直接地减少血液中的钙蛋白粒子的治疗药,也不存在从体液高效地除去钙蛋白粒子的方法。
现有技术文献
非专利文献
非专利文献1:clincalcium.2014(24)1785-92
非专利文献2:jamsocnephrol.2010(21)1998-2007
非专利文献3:nephroldialtransplant.2012(27)1957-66
技术实现要素:
本发明是着眼于如上的情况而完成的,其目的在于对钙蛋白粒子进行吸附。
本发明如下所述。
[1]一种钙蛋白粒子的吸附材料,其特征在于,在水不溶性载体的表面介由烃基共价键合有选自氨基、羧基、磷酸基、膦酰基、膦基、硫醇基中的至少1种。
[2]根据[1]所述的吸附材料,其中,上述烃基为直链状烃基。
[3]根据[1]或[2]所述的吸附材料,其特征在于,2个以上的膦酰基与上述烃基共价键合。
[4]根据[1]~[3]中任一项所述的吸附材料,其中,上述烃基为直链状丙基、直链状丁基或直链状己基,在其末端的碳原子共价键合有1个羟基和2个膦酰基。
[5]根据[1]或[2]所述的吸附材料,其中,上述烃基为直链状十一烷基,在其末端的碳原子共价键合有1个膦酰基。
[6]根据[1]~[5]中任一项所述的吸附材料,其中,上述载体为多孔。
[7]根据[1]~[6]中任一项所述的吸附材料,其中,用于吸附存在于体液中的钙蛋白粒子。
[8]一种钙蛋白粒子的吸附器,其在具有液体的入口和出口的容器内填充有[1]~[7]中任一项所述的吸附材料。
[9]一种钙蛋白粒子的吸附系统,其具备[8]所述的吸附器和用于对该吸附器供给液体的泵而成,且能够与透析器或血浆分离器连接。
[10]一种钙蛋白粒子的吸附方法,包括使[1]~[7]中任一项所述的吸附材料与含有钙蛋白粒子的液体接触的工序。
[11]一种除去了钙蛋白粒子的液体的制造方法,包括:使[1]~[7]中任一项所述的吸附材料与含有钙蛋白粒子的液体接触的工序。
根据本发明,可以对钙蛋白粒子进行吸附。
附图说明
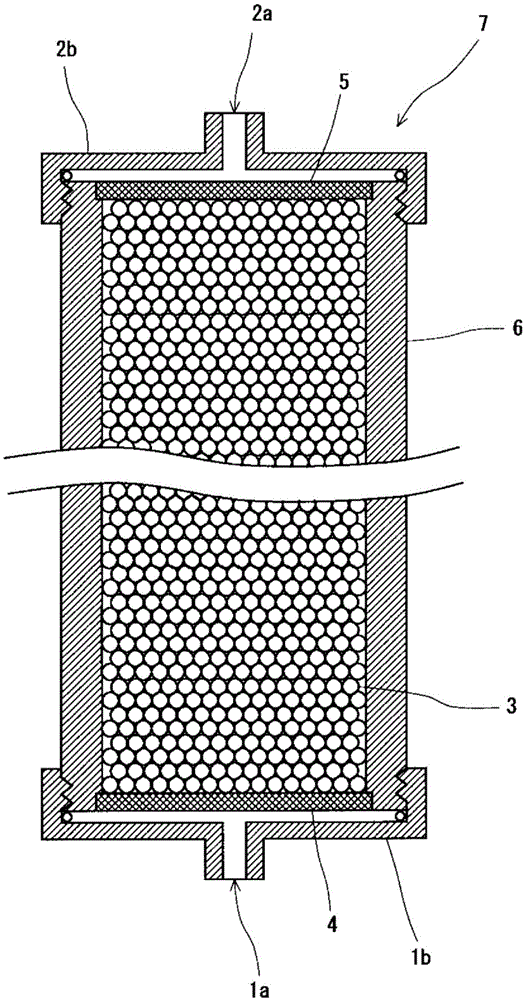
图1是表示本发明的吸附器的一个例子的简要截面图。
具体实施方式
本发明的目的在于吸附钙蛋白粒子。钙蛋白粒子是磷酸钙与蛋白质的复合体,更具体而言,是指磷酸钙(特别是波斯纳集群(posnercluster;成分为ca9(po4)6))和fetuin-a等的复合体,优选为通过将含有磷酸钙的fetuin-a等进行聚合而形成的纳米粒子。上述磷酸钙包含三斜磷钙石(monetite:cahpo4)、透钙磷石(brushite:cahpo4·2h2o)、无定形磷酸钙(ca9po4)6)、羟基磷灰石(ca10(po4)6(oh)2)等,优选为无定形磷酸钙、羟基磷灰石。该钙蛋白粒子可以是磷酸钙晶体暴露到表面的结构(初期cpp),也可以是其后通过相变而形成的、磷酸钙晶体被fetuin-a等包围的结构(次级cpp),优选为初期cpp。对于cpp而言,fetuin-a以外的体液中的蛋白质也作为复合体混入,例如,包含白蛋白、纤维蛋白原、rankl(receptoractivatorofnuclearfactorkappa-bligand)、bmp-2(bonemorphogeneticprotein2)、bmp-7(bonemorphogeneticprotein7)、osteoprotegerin等。作为钙蛋白粒子和复合体混入的蛋白质可以用荧光标记等检测用官能团、用于提高与其它分子的键合能力的反应性基团等来进行修饰,该修饰可以在体内进行也可以在体外进行。此外,也包括由遗传因子等的突变而产生的异常形式。
上述钙蛋白粒子可以利用在水不溶性载体的表面介由烃基共价键合了供电子性基的吸附材料来进行吸附或除去。供电子性基为与钙蛋白粒子进行相互作用的部位,烃基为具有间隔物的机能的部位。由于存在间隔物,可以使上述供电子性基远离载体,可以提高供电子性基与钙蛋白粒子的接触概率,可以提高吸附效率。
上述烃基可以是直链状烃基,可以是支链状烃基,也可以是环状烃基,不论哪种情况,均优选为饱和烃基。更优选为直链状烃基或支链状烃基,进一步优选为直链状烷基或支链状烷基,最优选为直链状烷基。此外,烃基的最长部分的碳原子数例如为1以上,优选为2以上,更优选为3以上,最优选为4以上,例如为20以下,优选为12以下,更优选为8以下。
作为上述供电子性基,可举出氢原子键合于n、s、p等而成的基团以及来自含氧酸的基团等具有酸性质子的基团。作为氢原子键合于杂原子而成的基团,可例示氨基、硫醇基、膦基等。作为具有酸性质子的基团,可以例示羧基(羧酸基)、磷酸基、膦酰基(膦酸基)等。这些氢原子键合于n、s、p等而成的基团和具有酸性质子的基团可以单独使用或组合使用2种以上。优选供电子性基为具有酸性质子的基团,更优选为磷酸基、膦酰基(膦酸基)。
将共价键合有上述供电子性基的烃基称为配体。该配体中,可以在烃基的任意位置共价键合供电子性基,但优选在烃基的末端共价键合供电子性基。此外,共价键合于1个烃基的供电子性基的数量不限于1个,优选为2个以上,特别优选共价键合有2个供电子性基。通过使配体具有2个以上的供电子性基,可以提高吸附力。具有2个以上的供电子性基时的供电子性基间的碳原子的数量例如为1~5个,优选为1~3个,更优选为1个。
配体具有2个以上的供电子性基时,优选至少1个或2个为具有酸性质子的基团。若具有2个以上的酸性质子的基团(尤其是膦酰基)共价键合于烃基,则容易提高吸附力。
构成上述配体的烃基上,也可以键合有除上述供电子性基以外的极性基团、例如羟基。羟基与上述供电子性基进行协同作用而对提高与钙蛋白粒子的相互作用性有效。羟基与供电子性基之间的碳原子的数量例如为1~5个,优选为1~3个,更优选为1个。
优选的配体是在烃基(优选为直链状烷基)的末端的碳原子共价键合有1个或2个供电子性基且共价键合有0或1个羟基的配体。作为最优选的配体,可举出在直链状烷基(特别是直链状丙基、直链状丁基、直链状己基等碳原子数为3~10左右的直链状烷基,更优选为碳原子数为4~6左右的直链状烷基)的末端的碳原子共价键合有1个羟基和2个膦酰基的配体;在直链状烷基(特别是直链状十一烷基等碳原子数8~15左右的直链状烷基)的末端的碳原子共价键合有1个膦酰基的配体等。
上述配体优选在水不溶性载体的单位体积(1ml)当中含有10nmol以上。优选为100nmol以上,进一步优选为1μmol以上,最优选为3μmol以上。此外,上述配体在水不溶性载体的单位体积(1ml)当中,例如为100μmol以下,优选为50μmol以下。
另外,水不溶性载体的体积是指在水中一边施加振动一边使水不溶性载体进行沉淀时,确认到其沉淀停止,即使施加振动,水不溶性载体的体积也不会变化时的体积(沉淀体积)。确定沉淀体积时的水只要是在载体沉淀时产生上清液的程度的量即可。
上述水不溶性载体在常温常压下为固体,可以采用粒状、板状、纤维状以及中空丝状、无纺布状等各种形状,大小也没有特别限定,优选为粒状且具有规定的范围的大小。粒状水不溶性载体的个数基准的平均粒径例如为10μm以上,优选为100μm以上,更优选为200μm以上,例如为5mm以下,优选为1mm以下,更优选为0.8mm以下。应予说明,粒状水不溶性载体的平均粒径可以从通过实体显微镜等得到的载体的放大照片分别测定直径,以个数基准求出。
若根据材质将水不溶性载体分类,则作为代表可举出玻璃珠、硅胶等无机载体;交联聚乙烯醇、交联聚丙烯酸酯、交联聚丙烯酰胺、交联聚苯乙烯等合成高分子载体和由二种以上构成的合成聚合物载体;由结晶性纤维素、交联纤维素、交联琼脂糖、交联糊精等多糖类形成的有机载体;以及,通过组合它们得到的有机-有机、有机-无机等复合载体等。
上述水不溶性载体优选具有亲水性。具体而言,优选将羟基、醚基、氨基等的亲水性基露出在表面。此外,优选对体液中的成分的非特异吸附少,优选血液适合性等安全性优异的载体。作为具有这样的特性的载体,可举出交联聚乙烯醇、由多糖类构成的有机载体等。
此外,上述水不溶性载体可举出具有大量具有适当大小的细孔的多孔结构的载体(多孔载体)、高分子网状结构以三维形成的载体、具有多个孔且其至少一部分为贯通孔的整体式载体等,但不限定于它们,优选为多孔载体。
在多孔载体的情况下,优选具有吸附对象物质(即钙蛋白粒子)能够进入细孔内的程度的排除极限分子量。这里所说的排除极限分子量一般如书籍(例如,波多野博行、花井俊彦著、实验高效液相色谱仪、化学同人等)中所阐述的那样,是指在凝胶渗透色谱法中无法进入细孔内的分子中的具有最小的分子量的分子的分子量,一般使用球状蛋白质等进行测定。多孔载体中,其排除极限分子量例如为1万以上,优选为10万以上,进一步优选为100万以上,没有特别的上限,但若排除极限分子量过大,则不溶性载体的密度下降,对不溶性载体的强度即耐压性能产生影响。从这样的观点出发,优选的是排除极限分子量例如为1亿以下,优选为5000万以下,更优选为1000万以下。
上述吸附材料例如可以通过将具有烃基、供电子性基和键形成性官能团的配体分子或具有烃基、供电子性基和键形成性官能团的配体聚合物键合于水不溶性载体的表面的亲水性基而制造。在将上述配体分子或聚合物与载体键合时,可使用具有与配体分子或聚合物的键形成性官能团反应的第1官能团和与水不溶性载体的亲水性基反应的第2官能团的中间分子。通过将配体分子或聚合物的键形成性官能团与水不溶性载体的亲水性基或中间分子的第1官能团键合,从而制造上述吸附材料。
作为上述中间分子所具有的第1官能团,可例示氨基、酰胺基、羧酸基(包含羰基卤素基、羧酸酐基、羧酸酯基等活性化羧酸基)、磺酸基(包含磺酰卤素基等活性化磺酸基)、羟基、硫醇基、醛基、卤素基、环氧基、硅醇基等各种官能团。此外,作为第2官能团,可例示卤素基、磺酸基(包含磺酰卤素基等活性化磺酸基)、羧酸基(包含羰基卤素基、羧酸酐基等活性化羧酸基)等。作为具有这些第1官能团和第2官能团的中间分子,例如优选为具有环氧基和卤素基的分子(例如,表氯醇等)。通过将卤素基以水不溶性载体的羟基进行亲核取代,从而中间分子与水不溶性载体键合。
配体分子或聚合物所具有的键形成性官能团分成使用中间分子的情况和不使用中间分子的情况进行指定。在不使用中间分子时,作为该键形成性官能团,可以采用与亲水性基具有结合反应性的基团,可以从与上述中间分子的第2官能团同样的范围内选择。此外,在使用中间分子时,可以从与上述中间分子的第1官能团同样的范围内,选择与中间分子的第1官能团成为相容性良好的组合的官能团作为键形成官能团。
作为上述配体分子,优选为具有作为供电子性基的膦酰基、根据需要可结合的羟基、作为键形成性官能团的氨基或硫醇基以及作为烃基的直链烷基的分子,特别优选为巯基-正烷基膦酸、氨基-1-羟基-正烷叉基双膦酸等。作为巯基-正烷基膦酸,可例示3-巯基-正丙基膦酸、11-巯基-正十一烷基膦酸等碳原子数1~20、优选为碳原子数8~15的分子。作为氨基-1-羟基-正烷叉基双膦酸,可例示帕米膦酸、阿仑膦酸、奈立膦酸等碳原子数为1~20、优选为碳原子数3~10、更优选为碳原子数4~6左右的分子。
以上的吸附材料可以处理含有钙蛋白粒子的各种液体,例如,可以处理脑脊液、血液、血浆、血清、腹水、淋巴液、关节内液体、骨髓液和含有由它们得到的馏分成分的各种来自生物的液性成分。此外,只要是有可能含有钙蛋白粒子的液体,则也可以处理水、缓冲液等。
使用吸附材料从液体吸附钙蛋白粒子时,需要在使吸附材料与液体接触后,将吸附材料与液体分离。例如,可以在容器中放入吸附材料和液体,通过静置、振荡等使其充分接触后,采用倾析、过滤等适当的固液分离方法,优选使用在具有液体的入口和出口的容器(中空容器)填充有吸附材料的吸附器,其安全且简便,优选。通过使吸附材料与液体接触,可得到除去了钙蛋白粒子的液体。
作为吸附器,例如,可举出图1所例示的吸附器。图1的吸附器7是将粒状吸附材料3填充于中空圆筒型容器(柱)6而成的。在中空圆筒型容器6的两端安装有过滤器4、5,防止吸附材料3的流出,另一方面,可以使液体流过吸附材料3。此外,在中空圆筒型容器6的过滤器4、5安装面利用螺钉等安装有能够液密地固定于中空圆筒型容器6的盖体1b、2b,通过形成于该盖体1b、2b的液体的流入口1a·流出口2a,可以对中空圆筒型容器6内的吸附材料3供给液体。
也可以在上述吸附器安装用于更有效地吸附除去钙蛋白粒子的器具而构成吸附系统。例如,可以配置用于供给液体的泵等,也可以连接透析器(渗析器)、血浆分离器、血液过滤器等。此外,上述吸附器可以填充1种吸附材料,也可以填充2种以上的不同的吸附材料。而且,也可以使用2个以上的吸附器,填充于2个以上的吸附器的吸附材料可以互相相同,也可以不同。2个以上的吸附器可以串联使用,也可以并联使用。
优选的吸附系统由用于供给液体的泵和吸附器构成。更优选的是在上述吸附器的上游侧或下游侧连接透析器(渗析器)或血浆分离器,可以在透析血液或者进行血浆分离、过滤的同时除去钙蛋白粒子。
本申请基于2016年8月1日提出申请的日本专利申请第2016-151390号主张优先权的权益。2016年8月1日提出申请的日本专利申请第2016-151390号的说明书的全部内容通过参考而援引于本申请中。
实施例
以下,举出实施例更具体地说明本发明,但本发明不受下述实施例的限制,当然也可以在能够适合于前述·后述的主旨的范围适当施加变更而实施,这些均包含于本发明的技术范围。
实施例1
对多孔纤维素珠(排除极限分子量500万,粒径400~500μm)40ml加入碱性水溶液使总容量为80ml后,加入表氯醇30ml,在40℃反应2小时。反应后将珠用水充分清洗而得到环氧化纤维素珠。在所得的环氧化纤维素珠中加入帕米膦酸水溶液,在50℃振荡5小时以上。其后,用水充分清洗而得到帕米膦酸固定纤维素珠(吸附材料a)。在干燥的吸附材料a中加入硫酸和硝酸,以微波分解装置进行加压酸分解,进行通过icp-aes法得到的溶液的p元素的含量测定。根据元素分析的结果,帕米膦酸的固定化量为2μmol/ml。
实施例2
将实施例1的帕米膦酸水溶液替换为阿仑膦酸水溶液,得到阿仑膦酸固定纤维素珠(吸附材料b)。根据元素分析的结果,阿仑膦酸的固定化量为5μmol/ml。
实施例3
将实施例1的帕米膦酸水溶液替换为奈立膦酸水溶液,得到奈立膦酸固定纤维素珠(吸附材料c)。根据元素分析的结果,奈立膦酸的固定化量为6μmol/ml。
实施例4
对实施例1中得到的环氧化纤维素珠加入含有11-巯基十一烷基膦酸的乙醇水溶液,在40℃振荡24小时。其后,用水充分清洗而得到11-巯基十一烷基膦酸固定纤维素珠(吸附材料d)。根据元素分析的结果,11-巯基十一烷基膦酸的固定化量为10μmol/ml。
吸附性评价1
在实施例1~4的吸附材料a、b、c、d的珠30μl中加入含有钙蛋白粒子(cpp)的血清120μl,在室温下振荡1小时。未处理血清和振荡1小时后的上清液中的cpp量如表1所示。
应予说明,在上述实验中,cpp量以如下方式测定。
在含有cpp的测定对象液中放入近红外线荧光探针(osteosense(注册商标))使其与cpp结合后,用凝胶过滤旋转柱进行层析,将包含cpp的高分子量馏分的荧光以近红外线扫描器进行定量。
[农1]
产业上的可利用性
若使用本发明的吸附材料,则可以期待用作被认为与体内的钙蛋白粒子的积蓄相关的各种疾病的治疗或者预防法。此外,通过将可能含有钙蛋白粒子的体液等液体用本发明的吸附材料进行处理,能够净化液体。
符号说明
1a.液体的流入口
1b.盖体
2a.液体的流出口
2b.盖体
3.吸附材料
4、5.过滤器
6.中空圆筒型容器(柱)
7.吸附器
- 还没有人留言评论。精彩留言会获得点赞!