一种基于纳米结构的高性能片上毛细管电泳系统的制作方法
本发明属于生物技术领域,具体涉及一种基于纳米结构的高性能片上毛细管电泳系统。
背景技术:
传统毛细管电泳(capillaryelectrophoresis,ce)是以高压直流电场驱动石英毛细管内样本溶液中待测生物分子分离的技术,对于蛋白质和dna的分离与分析具有重要意义。然而,传统毛细管电泳耗时较长,需要大型仪器和专业操作人员且荧光信号在待测生物分子(如氨基酸、蛋白质和dna等)浓度较低时很弱,使得分析速度和分离效率偏低。
技术实现要素:
针对传统毛细管电泳的灵敏度低,耗时长和操作复杂等缺点,本发明提出一种基于纳米结构的高性能片上毛细管电泳系统。该毛细管电泳系统可以实现生物分子(如氨基酸、蛋白质和dna等)的快速、高灵敏度检测。
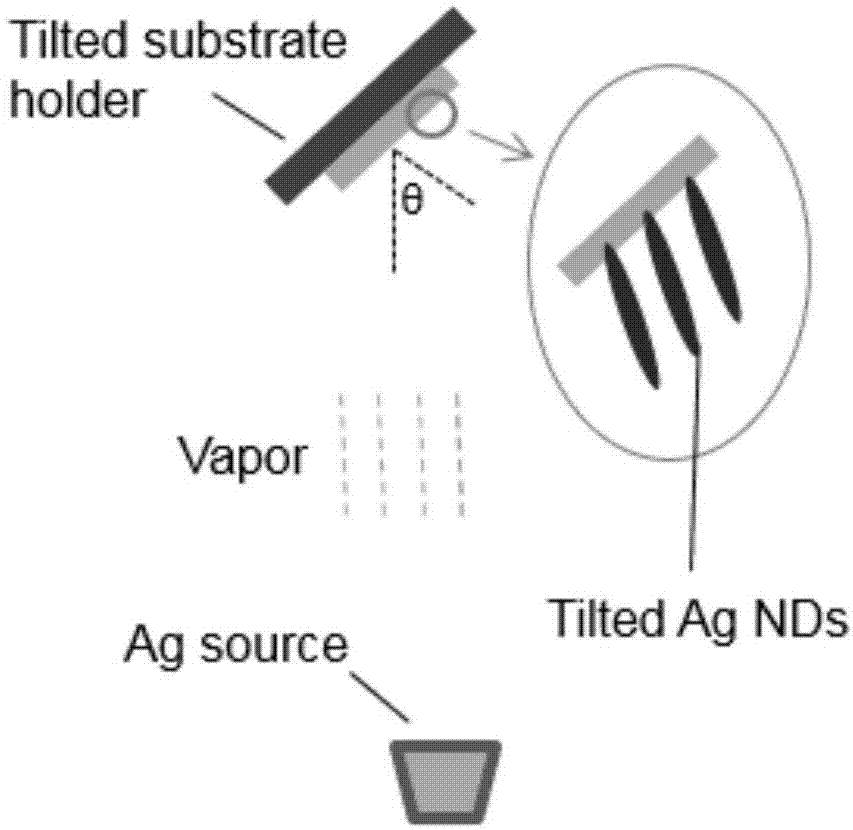
本发明采用一种基于倾斜角沉积(obliqueangledeposition,oad)技术的纳米结构制备工艺。oad是一种物理气相沉积方法,其原理为通过阴影效应和吸附原子的扩散作用在基底上生长可控的三维纳米阵列(如图1)。本发明集成的纳米阵列(金、银和二氧化硅等)平均直径为50nm-200nm,厚度为100nm-3000nm,间距为50nm-500nm(如图2)。
进一步,本发明通过沉积模板(depositionmask)将上述纳米结构可控地集成在玻璃片一定区域(如图3)。该区域为毛细管电泳系统的检测区域,其中的金属纳米阵列可通过荧光增强效应极大提高生物分子的检测灵敏度。
进一步,本发明采用一种具有“十字”沟道的微流控芯片(如图4)。该芯片由一长一短两个通道垂直相交得到,各通道顶端共连接4个进样口。该芯片可以实现ce,其中短通道提供进样,长通道截取部分样品并实现分离与检测,高压直流电场为整个系统提供动力。
进一步,该芯片有两种制备方法。第一种制备方法(如图5):制备具有十字沟道的聚二甲基硅氧烷(pdms),并通过等离子体反应(plasma)与集成有纳米结构的玻璃片载体键合得到完整芯片。第二种制备方法:制备具有十字沟道且集成有纳米结构的玻璃片,并通过plasma与平整pdms键合得到完整芯片。
进一步,通过labview软件编写程序得到ce所需的电压控制与反应延时指令,并传输给可外控的高压电源。由此组成的外部环境系统可给该芯片的四个进样口提供合适的电压与反应延时。
本发明一种基于纳米结构的高性能片上毛细管电泳系统检测速度快、灵敏度高、操作简单,操作者只需先将ce芯片各沟道与进样口用溶液充满,再在其中一个进样口加入待检测样本,该样本中的生物分子就会在电脑程序与外部高压电源的控制下实现电泳分离,并在集成金属纳米棒的检测区域捕获分离信号并分析处理。
有益效果:本发明提出的基于纳米结构的高性能片上毛细管电泳系统实现了生物分子的快速、高灵敏度检测。该毛细管电泳系统将整个检测过程集成在微流控芯片上,因而进样量少、反应速度快且操作简单便捷。同时,通过在检测区域集成金属纳米结构实现荧光增强,大大提高了芯片的检测灵敏度。
附图说明
图1为倾斜角沉积示意图。
图2为银纳米阵列sem图。
图3为玻璃片上部分区域集成纳米结构图。
图4为ce芯片的“十字”沟道结构图。
图5为“十字”沟道pdms与集成银纳米棒的玻璃片组成芯片图。
具体实施方式
下面结合附图和实施例对本发明作详细描述,但本发明的实施不仅限于此。
实施例1
采用倾斜角沉积在玻璃片上蒸镀银纳米结构
在沉积之前,将玻璃片在丙酮,异丙醇和去离子(di)水中超声处理,然后通过氮气干燥。为了增强银纳米棒与玻璃片之间的粘附性,首先以沉积角θ=0°蒸镀厚度为10nm的ti薄膜层。然后以沉积角θ=86°蒸镀具厚度分别为300nm,500nm,1000nm,2000nm和3000nm的银纳米棒。
实施例2
制备器件在pdms上的ce芯片
首先通过正面光刻su8光刻胶,在硅片上制备一定厚度的su8硅片模板。将a/b=1/10的一定量pdms溶液混合搅拌均匀后抽真空除气泡,再将清澈的pdms混合液加在su8硅片模板表面并于80℃下固化1h。轻轻撕下整片pdms并将包含单个十字沟道的pdms用小刀切割分离并打孔。清洗pdms,过程为先用丙酮超声清洗5min,再用异丙醇超声清洗5min,再用diwater超声清洗5min并用n2气吹干。对干净的带十字沟道pdms与集成有金属纳米棒的玻璃片在60wplasma下打60s并立刻bonding在一起,得到器件在pdms上的集成纳米结构ce芯片。
实施例3
制备器件在玻璃片上的生物检测芯片
先通过正面光刻在玻璃片上制备一定厚度光刻胶的带器件玻璃片模板。再将该模板浸没在boe溶液湿法刻蚀,或者对该模板使用干法刻蚀,得到玻璃片上具有一定厚度“十字”沟道。再通过倾斜角沉积对该玻璃片的检测区域蒸镀纳米结构。将带单个十字沟道的玻璃片切割分离并清洗干净。对干净的带器件且集成纳米结构的玻璃片与打了4个进样孔的平整pdms基底在60wplasma下打60s并立刻bonding在一起,得到器件在玻璃片上的集成纳米结构ce芯片。
实施例4
使用该ce芯片分离两种氨基酸
对实施例2中的器件在pdms上ce芯片。首先在diwater中配置浓度为10mm的四硼酸钠(sodiumtetraboratedecahydrate)缓冲液并通过孔径为0.22μm膜过滤器去除杂质。将精氨酸(arg)和甘氨酸(gly)分别溶解在缓冲液中,浓度均为1mm,并都以100:1(v/v)比例与1mm溶在丙酮中的荧光素-5-异硫氰酸酯(fluoresceine-5-isothiocyanate)混合在黑暗中过夜,实现荧光标记两种氨基酸。在分析之前,将两种荧光标记的氨基酸以1:1(v/v)比例混合并稀释至10μm。
为方便统计,对ce芯片从最左端的进样口沿顺时针标记为v1、v2、v3和v4。将20μl的缓冲液依次加入芯片左端3个进样口(v1、v2、v4),等待1min溶液自动进样到最右端进样口(v3)后再将20μl该溶液加入其中,实现整个沟道充满缓冲液。用无尘纸吸取进样口v2中的缓冲液并加入20μl浓度为10μm两种荧光标记的氨基酸混合液。将电脑控制的高压电源四个铂电极输出口固定在四个进样口中,通过labview控制首先以v1:v2:v3:v4=150v:300v:150v:0v反应20s实现进样,再以v1:v2:v3:v4=300v:150v:0v:150v反应2min实现氨基酸分离,通过荧光显微镜捕获荧光分离信号。
技术特征:
技术总结
本发明公开了属于生物技术的一种基于纳米结构的高性能片上毛细管电泳系统。本发明包括三维纳米阵列、微流控芯片,所述三维纳米阵列集成在玻璃片的检测区域,微流控芯片由两个微米尺寸的通道垂直相交得到(十字沟道),通道的四个顶端各连接1个进样口。本发明通过毛细管电泳系统将整个检测过程集成在微流控芯片上,因而进样量少、反应速度快且操作简单便捷。同时,通过在检测区域集成金属纳米结构实现荧光增强,大大提高了芯片的检测灵敏度。
技术研发人员:曹臻;杨文婷;陈亮;赵炅东
受保护的技术使用者:江苏医联生物科技有限公司
技术研发日:2018.09.29
技术公布日:2019.01.08
- 还没有人留言评论。精彩留言会获得点赞!