反相/离子交换混合模式色谱固定相、制备方法与应用与流程
本发明涉及液相色谱固定相及其制备方法与应用。
背景技术:
药物分析技术在药物的研发生产和贮存流通过程中的质量控制起着重要作用。为了提高药物对疾病的治疗效果,不同单个组分药品的联合用药成为广泛应用的策略,但是联合用药引起药物依从性降低,增加患者的风险。近年来发展起来的固定剂量复方药物是含有两个或以上的有效成分的单一剂型,如胶囊或药丸。既能利用不同药物成分的协同作用,提高药物的治疗效果,又能减少患者服用的药片数量,因此,受到了医生和患者的欢迎,产品涵盖抗艾滋病药、抗高血压药、抗感冒药。由于复方药物中含有多种活性成分,与单一组分药物相比,其质量控制的难度大幅增加,迫切需要开发适用的分析方法。
根据《中国药典》2015版及相关文献记载,单一组分药物质量控制中,包括鉴别、含量测定和杂质分析,应用最为广泛的分析技术是反相液相色谱,例如使用十八烷基键合硅胶固定相的反相色谱,但是这类反相色谱柱对于一些极性或离子型化合物的保留较弱,并且由于其表面残留的硅羟基解离与碱性药物发生静电相互作用而造成色谱峰拖尾,影响色谱分离的分辨率,无法实现复方药物中中性及极性离子型化合物的同时分析。为了增加离子型化合物的保留,通常在反相色谱流动相中加入离子型表面活性剂,通过与被分析的反号离子型化合物形成离子对而实现中性与离子型化合物的同时分析。但是离子对色谱技术因为存在两个致命的缺点,使得它在复方药物分析中应用受到极大的限制。其一是在分离过程中涉及离子对试剂在固定相表面的动态吸附平衡,其平衡时间较长,导致在实际药物分离过程中不能使用梯度洗脱,对不同极性或保留能力的组分进行同时分析。其次,由于离子对试剂难以挥发,在离子化过程中引起离子源污染,使得离子对色谱不能与质谱联用,限制了液相色谱-质谱联用技术对不同成分进行结构鉴定的应用。
混合模式色谱是取代离子对色谱,对中性和离子型化合物进行同时分析的优选方法。与传统的单一模式色谱不同,混合模式色谱使用多功能团色谱固定相,其保留机理涉及两种或两种以上不同类型的分子间相互作用,因此具有更强的分离能力。最为常用的混合模式色谱是反相/离子交换色谱,所使用的固定相表面含有疏水和可解离功能基团,因此能够通过范德华尔力和静电力的协同作用,对中性和离子型化合物实现保留和同时分离。由于流动相中不需要添加表面活性剂,因此不存在离子对色谱中所存在的问题,不仅可以使用梯度洗脱分析,还可以与质谱联用,因此,在药物分析中展现了广阔的应用前景。但是,到目前为止,混合模式色谱固定相的品种不多,结构单一,不能适应药物分析领域中日益增长的复杂成分,尤其是复方药物,的分析需求。
技术实现要素:
本发明的目的在于提供一种新的混合模式色谱固定相,并给出其简便可行的制备方法及其在药物分析领域的应用。
一种反相/离子交换混合模式色谱固定相,称之为十八烷基/磺酸基混合色谱固定相,由键合在多孔硅胶表面的十八烷基和磺酸基组成,其化学结构式为:
所述的色谱固定相的制备方法,包括步骤如下:
(1)活化硅胶的制备:将一定量硅胶微粒加入hcl溶液里进行80℃-105℃的回流反应,用水洗至中性,真空干燥;
(2)环氧基硅胶的制备:将上述酸化的硅胶微粒,每克加入1.92mmol-3.6mmol的γ-(2,3-环氧丙氧)丙基三甲氧基硅烷,在140℃-160℃下密封反应,用无水乙醇洗涤,过滤收集产品并真空干燥,得到环氧基功能化多孔硅胶微球;
(3)磺酸基硅胶的制备:将上述环氧基功能化多孔硅胶微球分散到质量数为8-10倍的超纯水中,按照每克环氧基功能化多孔硅胶微球加入1.92mmol-3.6mmol亚硫酸氢钠的量加入亚硫酸氢钠,混匀,利用三乙胺调ph值至7-8,85℃反应,用水洗涤并真空干燥,得到磺酸基键合硅胶微球;
(4)十八烷基/磺酸基硅胶的制备:将上述磺酸基键合硅胶微球分散在质量数为8-10倍的n,n-二甲基甲酰胺(dmf)中,在冰浴条件下,按照每克磺酸基键合硅胶微球加入1.92mmol-3.6mmol十八烷基酰氯的量滴加十八烷基酰氯;滴加结束后,40-65℃搅拌反应,过滤收集产品,后依次用甲苯和乙醇洗涤并真空干燥,得到十八烷基/磺酸基混合模式色谱固定相。
利用所述的色谱固定相可以制得反相/离子交换混合液相色谱柱。
所述的色谱柱的制备采用高压匀浆法,工艺条件为:按照正己醇:四氯化碳的质量配比6:4制备匀浆液装,以正己烷为顶替液,装柱压力为300bar。
所述的反相/离子交换混合液相色谱柱应用于药物分离。
本发明的混合模式固定相以环氧基为连接臂,结合十八烷基长链,相对于传统苯磺酸键合相中的苯基的柔性更大,疏水性更高,与被分离的碱性化合物之间的协同作用更强,因而分离效果更好。此外,因为连接臂中存在醚键和羟基等亲水基团,易于结合流动相中的极性分子,因此可以防止十八烷基链在流动相中水含量较高时十八烷基链倒伏而引起被分析物的保留下降的问题。
本发明采用气相化学沉积法对多孔硅胶进行硅烷化反应,使其结合具有较大化学活性的环氧基团,继而利用环氧基的开环反应和羟基与酰氯的缩合反应,制备得到十八烷基/磺酸基混合模式色谱固定相。与常规液相反应法相比,化学气相沉积法避免使用如甲苯等有毒有害有机溶剂,极大地降低了对人体的危害和对环境的污染。利用环氧基功能化硅胶作为中间相,桥接反相和离子交换基团,简化了合成步骤,并且反相和离子交换基团的比例可调。所发明的制备方法具有原料价廉易得,工艺路线简便可行,易于放大规模的工业化生产。
本发明的固定相可以应用于固定剂量复方药物中多组分的同时分离与测定。而目前药典中往往需要离子对色谱或者多次分离才能进行多组分分析。利用本发明的固定相不仅能够进行多组分同时分离,并且分离的效果优于传统离子对反相色谱,并且可以采用梯度洗脱,直接与质谱联用,在线对复方药物进行定性定量一次性分析,节省大量的分析时间和运行成本。
附图说明
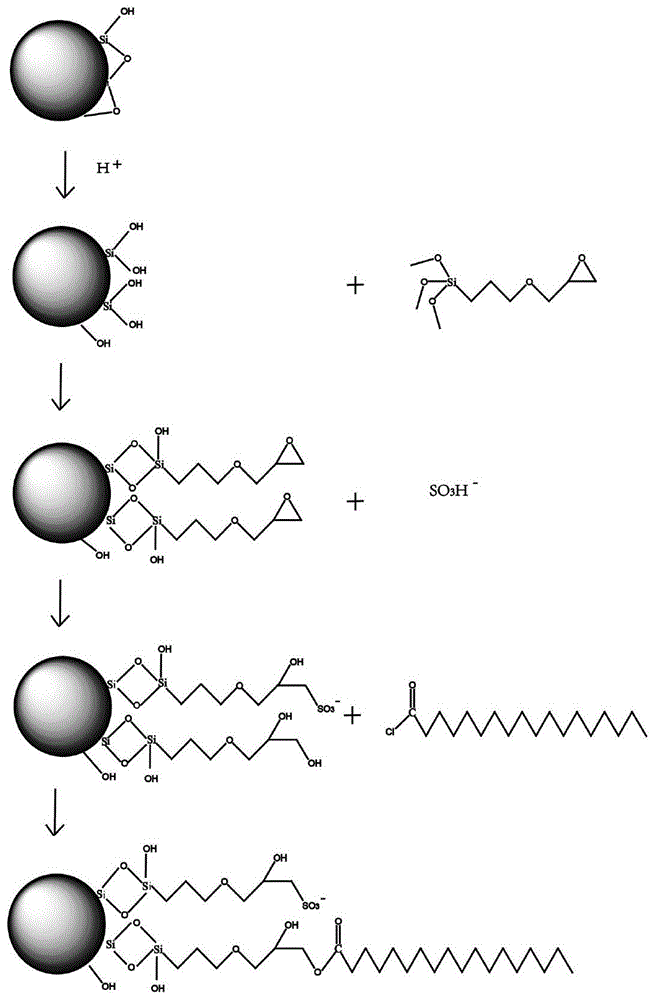
图1混合模式色谱固定相的制备流程。
图2实施例1活化微球的红外表征
图3实施例2环氧基硅胶微球的红外表征
图4实施例3制备二醇基官能团的化学反应式
图5实施例3二醇基硅胶微球的红外表征
图6实施例3二醇基硅胶微球的核磁表征
图7实施例4制备十八烷基功能化微球的化学反应式
图8实施例4十八烷基功能化硅胶微球的红外表征
图9实施例4十八烷基功能化硅胶微球的核磁表征
图10实施例5制备磺酸基官能团的化学反应式
图11实施例5磺酸基功能化硅胶微球的红外表征
图12实施例5磺酸基功能化硅胶微球的核磁表征
图13实施例6制备十八烷基磺酸基功能化微球的化学反应式
图14实施例6十八烷基/磺酸基硅胶微球的红外表征
图15实施例6十八烷基/磺酸基硅胶微球的核磁表征
表1实施例2-6的元素分析表征
图16烷基苯同系物在十八烷基、磺酸基和十八烷基/磺酸基色谱柱上的分离。
图17双氰胺,三聚氰胺和二甲双胍在十八烷基、磺酸基和十八烷基/磺酸基色谱柱上的分离。
图18苯胺同系物在十八烷基、磺酸基和十八烷基/磺酸基色谱柱上的分离。
图19常见碱性药物在十八烷基/磺酸基色谱柱上的分离。
图20复方甲氧那明胶囊在十八烷基/磺酸基色谱柱上的分离。
图21复方双肼屈嗪片在十八烷基/磺酸基色谱柱上的分离。
图22复方利血平氨苯喋啶片在十八烷基/磺酸基色谱柱上的分离,检测波长为268nm。
图23复方利血平氨苯喋啶片在十八烷基/磺酸基色谱柱上的分离,检测波长为310nm。
图24复方利血平片在梯度洗脱条件下,十八烷基/磺酸基色谱柱上的分离的紫外色谱图。
图25复方利血平片中有机组分的离子流图和对应质谱图。
具体实施方式
本发明提供一种结构新颖的反相/离子交换混合模式色谱固定相,在离子型功能基团的周边键合疏水且柔软的烷基烃长链,可以通过协同的反相与离子交换保留机理与被分析化合物发生作用,从而具有高色谱选择性,适用于复方药物中多成分的同时分析与含量测定。本发明给出其简便可行的混合模式色谱固定相的制备技术,采用干法衍生化反应替代传统的湿法,避免使用有毒有害有机溶剂,保护健康和环境。该制备技术反应路线简单可控,原料价廉易得,适合于工业化放大生产。本发明的再一个目的是提供混合模式色谱固定相在药物分析中的独特应用,不仅可以实现梯度洗脱分析并且能与质谱联用,实现复方药物中多组分的快速含量测定和结构鉴定。
本发明制备的混合色谱固定相由键合在多孔硅胶表面的十八烷基和磺酸基组成。首先通过化学气相沉积法将γ-(2,3-环氧丙氧)丙基三甲氧基硅烷(kh-560)键合到多孔硅胶微粒表面,以kh-560为连接臂分别与亚硫酸氢钠和十八烷基酰氯反应,制备出十八烷基/磺酸基混合色谱固定相,并应用于复方药物分离。其制备流程如图1所示。具体操作步骤如下:
活化硅胶的制备:将一定量硅胶微粒加入质量8-10倍的10%-15%的hcl溶液,搅拌,105℃回流反应8h,用水洗至中性,80℃真空干燥。
环氧基硅胶的制备:将上述酸化的硅胶微粒放入具有特氟龙内胆的高压釜中,每克加入1.92mmol-3.6mmol的γ-(2,3-环氧丙氧)丙基三甲氧基硅烷,密封高压釜,在150℃下反应8h。用无水乙醇洗去未反应硅烷化试剂,过滤收集产品,80℃下真空干燥,得环氧基功能化多孔硅胶。
磺酸基硅胶的制备:将上述键合环氧基的硅胶微球分散到质量数为8-10倍的超纯水中,每克加1.92mmol-3.6mmol亚硫酸氢钠,超声混匀,三乙胺调ph值至7-8,85℃反应8h,蒸馏水洗涤,120℃真空干燥,得到磺酸基键合硅胶微球。
十八烷基/磺酸基硅胶的制备:将上述磺酸基功能化硅胶微球分散在质量数为8-10倍的n,n-二甲基甲酰胺(dmf)中,在冰浴条件下,缓慢滴加每克1.92mmol-3.6mmol十八烷基酰氯。滴加结束后,60℃搅拌反应9h,过滤收集产品,后依次用甲苯和乙醇洗涤,80℃真空干燥,得到十八烷基/磺酸基混合模式色谱固定相。
高压液相色谱柱的制备:采用常规高压匀浆法将色谱固定相填充到不锈钢柱管中,得反相/离子交换混合液相色谱柱。具体条件为正己醇:四氯化碳6:4为匀浆液装,正己烷为顶替液,装柱压力为300bar。
高压液相色谱柱的反相色谱行为:以不同链长的苯同系物(甲苯-戊苯)为分子探针,测定它们在十八烷基固定相、磺酸基固定相和十八烷基/磺酸基固定相上的保留值,比较固定相的反相色谱保留强度。
色谱条件:固定相,(a)十八烷基键合相,(b)磺酸基键合相,(c)十八烷基/磺酸基键合相;15x0.46cm;流动相,60%甲醇-40%水;流速,1ml/min;检测波长,254nm。
高压液相色谱柱的离子交换色谱行为:以双氰胺,三聚氰胺和二甲双胍为分子探针,测定它们在十八烷基相、磺酸基相和十八烷基/磺酸基相上的保留值,比较固定相的离子交换保留的强度。
色谱条件:固定相,(a)十八烷基键合相,(b)磺酸基键合相,(c)十八烷基/磺酸基键合相;15x0.46cm;流动相,30%乙腈-70%磷酸二氢胺溶液(1.7%,ph3);流速,1ml/min;检测波长,220nm。
高压液相色谱柱的反相/离子交换混合色谱保留行为:不同链长的烷基苯胺(甲基苯胺-戊基苯胺)具有疏水基团烷基苯和可解离基团胺,因此,选择它们作为分子探针,测定它们在十八烷基相、磺酸基相和十八烷基/磺酸基相上的保留值,比较固定相的混合模式色谱保留强度。
色谱条件:固定相,(a)十八烷基键合相,(b)磺酸基键合相,(c)十八烷基/磺酸基键合相;15x0.46cm;流动相,40%乙腈-60%磷酸二氢钾溶液(30mm,ph2.5);流速,1ml/min;检测波长,254nm。
常见碱性药物的分离:以常见碱性药物硫酸沙丁胺醇,可乐定,普鲁卡因胺,普萘洛尔,阿米替林为模型化合物,测定它们在十八烷基/磺酸基相上的保留值,展示固定相对碱性药物的分离效果。
色谱条件:固定相,十八烷基/磺酸基键合相;15x0.46cm;流动相,30%乙腈-70%磷酸二氢钾溶液(30mm,ph2.5);流速,1ml/min;检测波长,220nm。
复方甲氧那明胶囊的分离:取复方甲氧那明胶囊的内容物,精密称定,研细,配制成约相当于盐酸甲氧那明浓度0.1mg/ml-1mg/ml的样品,过0.22m滤膜,取续滤液作为样品,精密量取10-30l注入液相色谱仪。色谱条件:碳十八/磺酸基混合模式色谱柱;以50%磷酸二氢钾缓冲盐(30mm,ph2.5)-50%乙腈为流动相;流速,1ml/min;检测波长为230nm。
复方硫酸双肼屈嗪片的分离:取复方硫酸双肼屈嗪片,研细,精密称取适量,配制成约相当于双肼屈嗪浓度0.1mg/ml-1mg/ml的样品,过0.22m滤膜,取续滤液作为样品,精密量取10-30l注入液相色谱仪。色谱条件:碳十八磺酸基混合模式色谱柱;以50%磷酸二氢钾缓冲盐(30mm,ph2.5)-50%乙腈为流动相;流速,1ml/min;检测波长为220nm。
复方利血平氨苯喋啶片中利血平的分析:复方利血平氨苯喋啶片,研细,精密称取适量0.1mg/ml-1mg/ml,过0.22m滤膜,取续滤液作为样品,精密量取10-30l注入液相色谱仪。色谱条件:碳十八磺酸基混合模式色谱柱;以50%磷酸二氢钾缓冲盐(30mm,ph2.5)-50%乙腈为流动相;流速,1ml/min;检测波长为268nm。
复方利血平氨苯喋啶片中氢氯噻嗪,硫酸双肼屈嗪和氨苯喋啶,研细,精密称取适量0.1mg/ml-1mg/ml,过0.22m滤膜,取续滤液作为样品,精密量取10-30l注入液相色谱仪。色谱条件:碳十八磺酸基混合模式色谱柱;以50%磷酸二氢钾缓冲盐(30mm,ph2.5)-50%乙腈为流动相;流速,1ml/min;检测波长为310nm。
复方利血平片的分离:复方利血平片,研细,精密称取适量,相当于双肼屈嗪浓度0.1mg/ml-1mg/ml的样品,过0.22m滤膜,取续滤液作为样品,精密量取10-30l注入液相色谱仪。色谱条件:碳十八磺酸基混合模式色谱柱;50mm甲酸铵(ph3)为流动相a,乙腈为流动相b,洗脱梯度为0-3min0%b,3-7min40%b,7-40min40%b,40-45min0%b;流速,1ml/min;检测波长为268nm与质谱联用正离子模式检测。
为了更好地理解本发明的技术,下面以实施例进一步说明本发明,但本发明并不限于以下实施例。
实施例1硅胶微球的活化
取10g硅胶微球加入到250ml三口瓶中,加入100ml10%的hcl溶液,机械搅拌,105℃回流反应8h,用水洗至中性,120℃真空干燥过夜,得活化硅胶微球,酸化后的硅胶微球的红外表征图谱如图2所示,在3400cm-1有较大的硅羟基吸收峰。
实施例2环氧基键合硅胶微球的干法制备
取10g按实施例1所制备的活化硅胶微球放到高压釜中,加入5.31mlγ-(2,3-环氧丙氧)丙基三甲氧基硅烷,150℃反应8h。用无水乙醇洗涤,80℃真空干燥,得环氧基功能化硅胶微球。环氧基功能化的硅胶的红外此法的表征图谱如图3所示,在键和环氧基后在2800cm-1和2890cm-1附近出现c-h的伸缩振动峰,表明环氧基键和到硅胶表面,元素分析表征如表1所示,碳含量为8.05%,计算出的表面键和量为4.50mol/m2。该方法突出优点在于不使用甲苯等有害有机溶剂,有利于保护健康和环境。
实施例3二醇基键合硅胶微球的制备
取10g按实施例2中所得的环氧基功能化微球,分散在100ml的0.5%h2so4,加热反应8h,用水洗至中性,80℃真空干燥,得二醇基键合硅胶微球,其反应方程式如图4所示,二醇基固定相红外表征如图5所示,在3400cm-1有明显o-h峰,并且在2800cm-1和2890cm-1附近出现c-h的伸缩振动峰,核磁表征图谱如图6所示有明显的共振峰,其元素分析表征数据如表1所示,碳含量为5.52%,表面键和密度2.95mol/m2,表明在酸性条件下反应环氧基链有一定的脱落。
实施例4十八烷基功能化微球的制备
取4g按实施例3中所制备的二醇基微球分散在25mln,n-二甲基甲酰胺(dmf)中,在冰浴条件下,缓慢滴加6ml十八烷基酰氯;滴加完成后,加热升温,在60℃反应9h。依次用dmf和乙醇洗涤,80℃干燥,得十八烷基功能化硅胶微球,其反应化学方程式如图7所示,十八烷基功能化微球的红外表征如图8所示,有明显的c-h伸缩振动峰,核磁表征图谱如图9所示有明显的十八烷基链的碳的核磁峰,元素分析结果如表1所示十八烷基的键和密度为1.08mol/m2。
实施例5磺酸基功能化微球制备
取10g按实施例2所制备的环氧基键合硅胶微球分散到100ml超纯水中,依次加入5g亚硫酸氢钠,超声混匀,三乙胺调ph值至7-8,加热升温,在85℃反应8h,蒸馏水洗涤,120℃真空干燥8h,得到磺酸基键合硅胶微球,其反应化学方程式如图10所示,红外表征图谱如图11所示,有明显的c-h伸缩振动峰,在650cm-1处有磺酸基的特征峰,核磁共振图谱如图12所示,在40ppm左右出现明显的峰分裂出两个肩峰,是由于磺酸基,元素分析表征如表1所示。
实施例6十八烷基/磺酸基功能化微球的制备(十八烷基:磺酸基=1:2)
取4g按实施例5所制备的磺酸基微球分散在25mln,n-二甲基甲酰胺(dmf)中,在冰浴条件下,缓慢滴加6ml十八烷基酰氯;滴加完成后,加热升温,在60℃反应9h。依次用dmf和乙醇洗涤,80℃干燥,得到十八烷基/磺酸基硅胶微球。其反应方程式如图13所示,红外表征图谱如图14所示存在c-h的伸缩振动峰和磺酸基特征吸收峰,核磁表征图谱如图15所示,在60ppm左右出现明显的十八烷基链的核磁共振峰,并且在50ppm左右出现峰裂分成两个峰,表明有磺酸基的影响,元素分析表征结果如表1所示,碳载量10.93%,硫载量0.81%计算得到碳十八的键和量为0.67mol/m2,磺酸基键和量为1.13mol/m2。
表1元素分析表征
实施例7环氧基键合硅胶微球的湿法制备
取10g按实施例1所制备的活化多孔硅胶,置于100ml的三口瓶中,安装冷凝管和干燥管。加入无水甲苯100ml、γ-(2,3-环氧丙氧)丙基三甲氧基硅烷5.31ml。氮气保护下机械搅拌并加热至110℃反应9h。冷却后过滤,并依次用甲苯、甲醇洗涤。在60℃下真空干燥12h。得环氧基功能化硅胶。与实施例2的干法相比,此法的缺点是需要消耗大量的有毒溶剂甲苯。
实施例8色谱评价:反相保留行为
以不同链长的苯同系物为分子探针,测定它们在本发明中所制备的中间相(十八烷基固定相、磺酸基固定相)和混合色谱固定相(十八烷基/磺酸基固定相)上的保留值,比较固定相的反相色谱保留强度。
样品制备:分别取甲苯,乙苯,丙苯,丁苯和戊苯50l于10ml容量瓶内,加甲醇-水(60:40)稀释至刻度线,过0.22m的滤膜,配制成烷基苯同系物样品。
色谱条件:固定相,(a)十八烷基键合相,(b)磺酸基键合相,(c)十八烷基/磺酸基键合相;15x0.46cm;流动相,60%甲醇-40%水;流速,1ml/min;检测波长,254nm。溶质:(1)甲苯;(2)乙苯;(3)丙苯;(4)丁苯;(5)戊苯。
如图16所示,固定相的疏水保留强度以磺酸基相<十八烷基/磺酸基相<十八烷基相的序列增加,反映了强疏水的十八烷基对非极性相互作用的决定性贡献。
实施例9色谱评价:离子交换行为
以双氰胺,三聚氰胺和二甲双胍为分子探针,测定它们在十八烷基相、磺酸基相和十八烷基/磺酸基相上的保留值,比较固定相的离子交换保留的强度。
样品配制:分别取双氰胺,三聚氰胺和二甲双胍10mg,置于10ml的容量瓶内,加乙腈-ph3,1.7%磷酸二氢铵(30:70)的混合溶液至刻度线,配制成1mg/ml的样品。
色谱条件:固定相,(a)十八烷基键合相,(b)磺酸基键合相,(c)十八烷基/磺酸基键合相;15x0.46cm;流动相,30%乙腈-70%磷酸二氢铵溶液(1.7%,ph3);流速,1ml/min;检测波长,220nm。溶质:(1)双氰胺;(2)三聚氰胺;(3)二甲双胍。
如图17所示,三聚氰胺和二甲双胍的保留值都以十八烷基相<磺酸基相<十八烷基/磺酸基相>的序列增加,反映了强阳离子交换基团磺酸基对静电相互作用的决定性贡献。
实施例10色谱评价:反相/离子交换混合色谱保留行为
不同链长的烷基苯胺具有疏水基团烷基苯和可解离基团胺,因此,选择它们作为分子探针,测定它们在十八烷基相、磺酸基相和十八烷基/磺酸基相上的保留值,比较固定相的混合模式色谱保留强度。
样品配制:分别取4-甲基苯胺50mg,4-乙基苯胺,4-丙基苯胺,4-丁基苯胺和4-戊基苯胺50l于10ml容量瓶内,加乙腈-水(40:60)稀释至刻度线,过0.22m的滤膜,配制成烷基苯胺同系物样品。
色谱条件:固定相,(a)十八烷基键合相,(b)磺酸基键合相,(c)十八烷基/磺酸基键合相;15x0.46cm;流动相,40%乙腈-60%磷酸二氢钾溶液(30mm,ph2.5);流速,1ml/min;检测波长,254nm。溶质:(1)4-甲基苯胺;(2)4-乙基苯胺;(3)4-丙基苯胺;(4)4-丁基苯胺;(5)4-戊基苯胺。
如图18所示,在相同条件下,烷基苯在单模式固定相上只有微弱保留,而在混合模式固定相上的保留大为增加,且出峰次序与烷基苯上的碳链长度成正比,反映了反相/强阳离子交换混合保留机理对色谱保留值的决定性贡献。
实施例11色谱应用:常见碱性药物分离
色谱评价结果表明,十八烷基/磺酸基混和固定相对苯胺类化合物具有优异的保留和分离能力,展现了在药物分析中的应用潜力。以常见碱性药物硫酸沙丁胺醇,可乐定,普鲁卡因胺,普萘洛尔,阿米替林为模型化合物,测定它们在十八烷基/磺酸基相上的保留值,展示固定相对碱性药物的分离效果。
样品配制:分别取沙丁胺醇,可乐定,普鲁卡因胺,普萘洛尔和阿米替林10mg,置于10ml的容量瓶内,加乙腈-ph3,30mm磷酸二氢钾(30:70)的混合溶液至刻度线,过0.22
m的滤膜,配制成1mg/ml的样品。
色谱条件:固定相,十八/磺酸基键合相;15x0.46cm;流动相,30%乙腈-70%磷酸二氢钾溶液(30mm,ph2.5);流速,1ml/min;检测波长,220nm。溶质:(1)沙丁胺醇;(2)可乐定;(3)普鲁卡因胺;(4)普萘洛尔和(5)阿米替林。
如图19所示,五个药物在混合模式固定相上均有较强的保留,且峰型比较对称,没有发现常规反相色谱柱上经常出现的峰拖尾现象。在等度洗脱条件下,全部化合物在55min内获得了基线分离。
实施例12色谱应用:复方甲氧那明胶囊的色谱分离
复方甲氧那明胶囊含有四个有效成分。通过对复方甲氧那明胶囊的主要组分的分离,展现本发明的混合色谱固定相对复方药物中多组分分离的独特优势。
样品制备:取本品20粒的内容物,精密称定,研细,精密称取适量(约相当于盐酸甲氧那明25mg)置50ml容量瓶中,加乙腈20ml超声5分钟,加水10ml超声5分钟,加乙腈稀释至刻度,摇匀,过0.22m滤膜,取续滤液作为样品,精密量取20l注入液相色谱仪。
色谱条件:十八烷基/磺酸基键合相色谱柱,15x0.46cm;流动相,50%乙腈-50%磷酸二氢钾溶液(30mm,ph2.5);流速,1ml/min;检测波长,254nm。溶质:(1)氨茶碱;(2)甲氧那明;(3)那可丁;(4)氯苯那敏。
如图20所示,在混合模式色谱柱上复方甲氧那明胶囊中的四个组分的柱效以理论塔板数计均大于15000/m,拖尾因子均小于1.4。组分间的分离度均大于1.5。完全能满足复方甲氧那明的鉴别和含量测定的要求。
实施例13色谱应用:复方硫酸双肼屈嗪片的色谱分离
复方硫酸双肼屈嗪片含有三个有效成分。通过对复方硫酸双肼屈嗪的主要组分的分离,进一步展现本发明的混合色谱固定相对复方药物中多组分分离的独特优势。
样品制备:取本品20片药片,研细,精密称取适量(约相当双肼屈嗪25mg)置50ml容量瓶中,加甲醇20ml超声5分钟,加水10ml超声5min,加甲醇稀释至刻度,摇匀,过0.22m滤膜,取续滤液作为样品,精密量取20l注入液相色谱仪。
色谱条件:十八烷基/磺酸基混合模式色谱柱,15x0.46cm;流动相,50%乙腈-50%磷酸二氢钾溶液(30mm,ph2.5);流速,1ml/min;检测波长,220nm。溶质:(1)氢氯噻嗪,(2)可乐定,(3)双肼屈嗪。
如图21所示,在混合模式色谱柱上复方硫酸双肼屈嗪中的3组分的分离度都大于1.5,可乐定和双肼屈嗪的柱效大于20000/m,拖尾因子均在1.05以下。
实施例13色谱应用:复方利血平氨苯喋啶片的色谱分离
复方利血平氨苯喋啶片含有四个有效成分。通过对复方利血平氨苯喋啶的主要组分的分离,进一步展现本发明的混合色谱固定相对复方药物中多组分分离的独特优势。
样品制备:取本品20片药片,研细,精密称取适量(约相当双肼屈嗪25mg)置50ml容量瓶中,加甲醇20ml超声5min,加水10ml超声5min,加甲醇稀释至刻度,摇匀,过0.22m滤膜,取续滤液作为样品,精密量取20l注入液相色谱仪。
色谱条件:十八烷基/磺酸基混合模式色谱柱,15x0.46cm;流动相,50%甲醇-50%磷酸二氢钾溶液(30mm,ph2.5);流速,1ml/min;检测波长,268或310nm。溶质:(1)氢氯噻嗪;(2)双肼屈嗪;(3)氨苯喋啶和(4)利血平。
如图22所示,在混合模式色谱柱上,检测波长为268nm时,复方利血平氨苯喋啶中的四个组分分离度都大于1.5,双肼屈嗪,氨苯喋啶和利血平其柱效都大于15000/m,拖尾因子均在1.3以下。
图23为复方利血平氨苯喋啶片在检测波长为310nm时的分离色谱图。在此条件下,利血平不能检出。复方利血平氨苯喋啶片中的其他三个组分分离度都大于1.5,双肼屈嗪和氨苯喋啶柱效都大于15000/m,拖尾因子均在1.0左右。
实施例14色谱应用:复方利血平片中有效成分的色谱分离与质谱鉴定
复方利血平片为复方制剂,含有利血平、氢氯噻嗪、维生素b6、混旋泛酸钙、三硅酸镁、氯化钾、维生素b1、硫酸双肼屈嗪和盐酸异丙嗪。利用梯度洗脱模式色谱和质谱联用技术对复方利血平片中的主要组分进行分离和鉴定,进一步展现本发明的混合模式固定相在复方药物分离分析中的独特优势。
样品制备:取本品10片,25ml容量瓶中,加甲醇10ml超声5min,加水10ml超声5min,加甲醇稀释至刻度,摇匀,过0.22m滤膜,取续滤液作为样品,精密量取20l注入液相色谱仪。
色谱条件:十八烷基/磺酸基混合模式色谱柱,15x0.46cm;流动相,50mm甲酸铵(ph3)为流动相a,乙腈为流动相b,洗脱梯度为0-3min0%b,3-7min40%b,7-40min40%b,40-45min0%b;流速,1ml/min;检测波长,268nm,
质谱检测:正离子模式,扫描范围100m/z-1000m/z.
图24为复方利血平片的紫外色谱图。在梯度洗脱条件下,可以明显分离出七个色谱峰。
应用质谱联用技术对图24中的色谱峰进行鉴定。图25为相应色谱峰的离子流图及其质谱图。通过谱图分析,可以确定紫外色谱图中峰所对应的组分:(1)氢氯噻嗪,(2)维生素b6,(3)双肼屈嗪,(4)利血平,(6)维生素b1,(7)异丙嗪,囊括了除泛酸之外的所有有机成分。泛酸在检测波长268nm无吸收。色谱峰5为杂质峰,可能来自药物辅料。
- 还没有人留言评论。精彩留言会获得点赞!