一体化样品萃取盒的制作方法
本实用新型涉及分析样品前处理领域,尤其涉及一种一体化样品萃取盒。
背景技术:
样品分析过程中,从前处理到进样的整体流程一般都会用到采样管、离心管、萃取柱或萃取器皿、收集管、进样瓶等耗材,上述过程是样品分析检测中消耗人工成本最大的部分;人工加耗材通常是化学分析的主要成本,而且大量的一次性耗材也是目前分析实验室的主要固废来源,既消耗资源,增加成本,也污染环境。
样品的分析检测涉及多个环节,而且每个环节又涉及多个步骤。譬如血样中的药物分析,第一个环节是采集血样,包括用采血管从用过药的生物体抽取血样,接着离心分离去掉样品中的细胞和血小板并把上层血浆转移到新的样品管中;第二个环节是对血浆进行样品前处理,主要是排除血浆中的蛋白,必要时还需采取液液萃取或固相萃取步骤把血样中存在的营养物、电解质、代谢物等可能干扰分析检测的内源物质排除掉,该过程涉及一至多次离心、移液、蒸干、复溶等操作。整个过程中几乎每一步都要用到移液枪头、试管、离心管等耗材,最后还需要用带密封盖的进样瓶盛装处理好的样品液。因此,对于血样中药物的分析检测,从采血到上机测定需要用到多种和多个耗材,操作上既费时、费事,也容易出错。事实上,绝大部分分析检测工作与血样中药物分析非常类似,大约80%以上的出错的情况以及时间和耗材的消耗都发生在样品处理过程中。
由于生物样品相对于其他类型的样品更为复杂,而且样品量通常较小,只有几十微升到几毫升,样品处理难度相应也比较大,而且样品处理一旦出错不容易补救。目前生物样品尤其是血样中的药物检测分析,通常用蛋白沉淀、液液萃取或固相萃取方法分离提取其中的药物分子,其具体做法和特点列举如下:
1.蛋白沉淀法
具体步骤包括:①定量吸取样品到离心管,②加入有机试剂、强碱、强酸、盐类等使得蛋白发生变性而沉淀析出,振动离心管使得反应充分,③离心几分钟,④取离心管中的上层清液转移到进样瓶,⑤将待测物转移到自动进样器的样品盘中然后开始检测。处理一批100个样品大约需要2~3小时,所需耗材包括离心管、两次移液的移液枪头、进样瓶以及密封瓶盖,费用约为每个样品¥2.3元。蛋白沉淀是目前最常用的快速生物样品处理方法,然而,蛋白沉淀的过程仍然涉及多步移液、振荡、离心、样品转移、容器标记等操作,费时费事又易于出错,而且非特异性沉淀既存在待测物与蛋白共沉淀的可能性又没有消除基质效应的功能,对不少待测物并不适用。
2.液-液萃取
遇到蛋白沉淀不能适用的情形,生物样品前处理通常首选液-液萃取方法,液-液萃取是通过待测物在互不相溶的溶剂中溶解度的差异实现分离,此方法无需特殊器具易于实现且相对便宜,其缺点是必须事先花费大量时间精力开发方法,萃取过程也相对繁琐复杂,仍然涉及多步移液、振荡、离心、样品转移、容器标记等操作,很耗时费力,而且需要用到较大量有机试剂,导致环境的污染和成本增加。液液萃取通常需要用到移液枪头、离心管、进样瓶及密封瓶盖等耗材,每个样品的耗材(包括溶剂)的费用大约需要¥3元以上,而一批100个样品需要的处理时间至少1~2天,如果萃取液体积太大需要浓缩的情况,处理时间和耗材费用将相应提高。
3.固相萃取法
本方法通过选择性吸附、洗脱等方式对样品进行分离、富集、净化,能有效降低基质干扰,提高检测灵敏度。采用固相萃取需要事先做方法开发,而且方法开发对专业水平和经验要求较高。固相萃取操作比较复杂繁琐,耗材费用每个样品需要¥15~20元甚至更高。处理一批100个样品所需时间在4~16小时左右(视固相萃取柱的具体形式而定)。本实用新型的萃取功能可视为一种一体化的固相萃取装置,目前市场上具有代表性的类似产品有以下几个:
固相萃取柱类似产品(thermoscientificsola):在传统固相萃取柱基础上,更改成无需筛板,将聚乙烯筛板材料和基质组分融为均一的吸附柱床,原理和使用上与固相萃取柱无明显差异,但采用了过滤方式,比传统固相萃取柱简单易行,几乎无需方法开发,但费用与其他固相萃取柱一样高昂,而且仅用于样品萃取,也没有收集和取代进样瓶的功能,单个产品本身平摊到每个样品约为¥15元,加上进样瓶和盖子约每个样品需要¥17元左右。
市场上现有固相萃取产品很多,但针对生物样品,特别是血样,的固相萃取柱在实际工作中很少使用,主要是因为普通固相萃取产品需要费时间开发方法,操作过程也较为复杂,而且每个萃取柱上费用都在¥10元以上。目前市面上也出现了针对血浆处理的过滤式萃取柱,如thermosola和博纳艾杰尔mas-c系列产品,这类产品通过多官能化的复合吸附材料,将生物样品中的主要干扰杂质吸附在填料上,而被测物质倾向于留在样品溶液中,经抽滤后收集滤液便得到分析样品。因此,这类产品操作简单而且几乎不需要方法开发。然而,这类产品同样不能直接用作自动进样器的进样盘,单个样品的处理费用约为¥10元,加上其它耗材和进样瓶及瓶盖的费用,总共约为¥13元。
以上各种方案均存在一定不足,尤其没能把样品处理与进样分析整合为一体以提高速度和降低开支。
技术实现要素:
为解决上述技术问题,本实用新型提供一种一体化样品萃取盒,包括收集盒、能部分包含于所述收集盒的萃取单元阵列层、以及既能盖住所述萃取单元阵列又可以扣合并密封所述收集盒的顶盖,其中所述收集盒内设置按阵列排布的多个收集孔;所述萃取单元阵列层包括多个与所述收集盒的收集孔一一对应的萃取单元,每个所述萃取单元上端有接纳样品的容量杯,所述容量杯底部压填有一片上筛片,所述筛片下方设置填充柱,所述填充柱内填装有填充材料,且所述填充柱的底部压填一片下筛片并收缩为具有尖端的流出口;所述顶盖包括与收集盒匹配的盒盖和内置的密封垫,所述盒盖顶面设置有与收集孔阵列排布方式相同的穿透孔。
进一步地,所述萃取单元中上筛片的上表面包含亲水性高分子材料层。
进一步地,所述收集孔的深度为10~50mm,内部体积为0.1~2ml。
进一步地,所述收集孔顶部边沿高出收集盒顶面并形成闭合边界,且所述填充材料为线性分子或网状分子且以舒展方式沿轴向填装在填充柱中。
进一步地,所述萃取单元阵列层顶部平面向四周延伸并垂直向下延伸形成裙壁,所述萃取单元阵列的顶面与所述裙壁形成一个开口朝下的密封盒。
进一步地,所述萃取单元的填充柱部分的外部轮廓与所述收集盒上收集孔的内部轮廓匹配,且所述萃取单元的填充柱外径和高度对应性地小于收集孔的内径和深度。
进一步地,所述穿透孔上开设有孔洞,所述穿透孔的孔洞的直径与收集孔的最大直径大致相同。
进一步地,所述收集盒的四周垂直壁的外表面上分别设有一至多个卡口,在盒盖四周垂直壁的内表面对应位置处分别设置有一个或多个卡扣,所述卡口和卡扣数量相同。
进一步地,所述盒盖四周垂直壁中至少有一侧的垂直壁设有两条切口,而且该内壁的所有卡扣分布于所述两条切口之间。
有益效果:本实用新型实施例提供一种一体化样品萃取盒,将采样、萃取、收集、进样等耗材集成为一个盒子,样品分析从采样、处理到进样、存样集成化,大大简化操作难度。
与类似产品相比,本实用新型的一体化样品萃取盒无需转移收集液或使用进样瓶及瓶盖,当本实用新型的填充柱中顶端筛片采用可以稳定细胞的线状亲水材料附着在其上表面的处理之后,可以直接用于全血处理,目前任何类似产品都没有处理全血样品的功能。因此本实用新型既保留了任何现有固相萃取产品的功能,又提供了萃取液与分析检测所用自动进样器的无障碍对接,节省了收集液的转移及进样瓶和密封盖,从而最大限度简便了萃取操作和耗材费用。
附图说明
附图用来提供对本实用新型的进一步理解,并且构成说明书的一部分,与本实用新型的实施例一起用于解释本实用新型,并不构成对本实用新型的限制。其中:
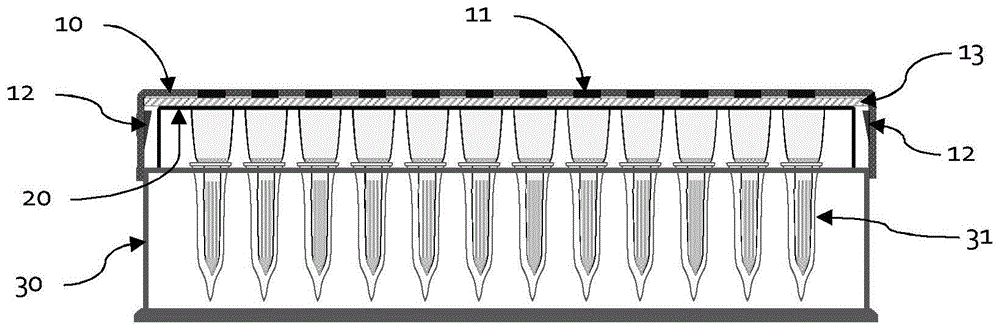
图1为本实用新型提出的一体化样品萃取盒的剖视图;
图2为样品萃取盒拆散后的剖视图;
图3为样品处理完成之后顶盖卡压到收集盒变成进样盒的示意图;
图4为顶盖穿通孔、萃取单元、收集孔阵列排布示意图;
图5为抽空过滤示意图。
图中标记为:
10—顶盖;11—穿透孔;12—卡扣;13—内置密封垫;
20—萃取单元阵列层;21—萃取单元;22—萃取单元填充柱;23—上筛片;
24—下筛片;25—裙壁;
30—收集盒;31—收集孔;32—卡口;
40—阵列。
50—抽空过滤装置或真空腔。
具体实施方式
下面将结合具体实施例及附图,对本实用新型的技术方案进行进一步描述,需要说明的是,所描述的实施例仅仅是用于解释本实用新型,而非用于限制本实用新型。
结合图1和图2,本实用新型实施例提供了一种一体化样品萃取盒,包括收集盒30、萃取单元阵列层20、顶盖10。
具体地,收集盒30的材质选用耐化学试剂、耐有机溶剂、耐强酸强碱以及对有机物没有吸附作用的材料,如聚丙烯、聚乙烯、聚四氟乙烯或者玻璃等。且收集盒30尺寸与标准96孔孔板一致,为长*宽=127x85mm的长方板块,与常用液相色谱仪的进样器相匹配。收集盒30中间是多个收集孔31组成的阵列40(如图4所示),用于收集过滤液,收集孔阵列可以是8行12列、或6行9列、或6行8列等形式,收集孔31的阵列形式可以任意选定以便与自动进样器匹配。每个收集孔31的深度在10~50mm之间,内部体积通常设为0.1~2ml。
本申请的说明书中描述的“多个”“多种”是指多于一个,即2个或者更多。
如果本申请的说明书中对一个结构和组分没有明确的数量限制,则表明该结构、组分的数量不受限制,即,可以为一个或多个。
如图2所示,收集孔31顶部边沿高出收集盒30顶面0.5~3mm,形成一个闭合边界,以使得收集的样品液不至于溢出进入到邻近收集孔而造成交叉污染,凸出的边在压上密封垫后得到更好的密封效果。
萃取单元阵列层20具体也是由耐化学试剂、耐有机溶剂、耐强酸强碱且对有机物没有吸附作用的材料如聚丙烯、聚乙烯、聚四氟乙烯、玻璃等制成。该阵列层20的材质可以与收集盒30的材质相同或者不相同。萃取单元阵列层20的排列形式与收集盒30的收集孔阵列完全一致,即一一对应,并且萃取单元21与收集盒30上的收集孔31形成相互配合的结构,即萃取单元21的填充柱23的外部轮廓与收集孔31的内部轮廓一致,但萃取单元21的尺寸略小。该收集孔31是一个微型试管,底部以尖形为佳,如图2所示。每个萃取单元21顶部是一个接纳样品和溶剂的容杯,容杯向上开口,下方连接填充柱22形成一体,在容杯底部填充柱顶部压填有一片上筛片23用于阻挡填充柱22内的填料在被倒置时不被倒出,上筛片23的上表面可以附着一层能稳定细胞的亲水性高分子聚合材料,当全血样品加到该层表面时能迅速分布,血样中的细胞得到该层亲水聚合物的保护而不被后继加入的有机试剂破坏,从而使得血样采集可以直接用萃取单元的容杯作为采集容器,既节省了采血容器又省掉了离心分离步骤。填料柱22中填装的填料可以是任何现有的固相萃取材料,最佳填料是分子呈线性或网状的天然或人工合成材料以及经化学改性处理后这类材料,填充时尽量保留材料分子的舒展状态,亦即线性分子沿填充柱22轴向而网状分子则以平展卷席状沿填充柱22轴向平行填装,填充柱22底部收缩为尖形流出口以便于过滤后的液体(待测样品)流入收集孔31,收缩出口内部压填有一块下筛片24用于阻挡填料和样品中沉淀物质进入收集孔31。所有萃取单元21的顶部相互分离且相互连接形成一个密闭面(成型时各萃取单元21顶部在同一个平面)。
另外,萃取单元21的填料柱部分22外径和高度与所述收集盒上收集孔31的内径和深度略小一些,使之全部或部分能与所述收集盒上的收集孔31相匹配,包装运输时萃取单元阵列层叠加在收集盒上,每个萃取单元21的填料柱22能刚好插入收集盒上对应的收集孔32中,使得包装既稳定又紧凑。
为了便于萃取单元阵列层20进行密封,萃取单元阵列层20中萃取单元21之间的链接形成的密闭面(黏连,不隔断或镂空而形成密封面即顶部平面)边沿部分向四周延伸3~20mm并垂直向下延伸2-20mm,形成裙壁25,该裙壁25的厚度优选为1-3mm,且裙壁25的下边沿平滑,当萃取单元阵列层20放置在接口尺寸与萃取单元阵列层20轮廓相匹配的抽滤装置上时,萃取单元阵列层20的密闭面和裙壁25与抽滤接口的密封圈能形成一个密封的真空抽滤腔,而不必通过对每个萃取单元21与抽滤腔独立对接并分别进行密封,使得抽滤装置50设计简化(如图5所示),而且由于萃取单元阵列层20与抽真空装置50的对接是通过平滑且窄小的裙壁25底边与密封圈的抵压接触,极大减少密封线的长度,密封效果和稳定性会大幅改善。
具体地,顶盖10是一个长方形盒盖内置一片密封垫13组成,盒盖11可以由塑料、木料、金属或玻璃等材料制成,盒盖的顶面是一个阵列40的穿透孔11,穿透孔11的排列方式与收集盒30上收集孔31的排列相一致,每个穿透孔11的孔洞直径与收集盒上对应的收集孔31的最大直径相同或略小,优选相同。如果孔洞太小,进样器进样针容易扎歪从而误扎到孔洞边沿导致针损坏,同时在盒盖顶部内表面设置密封垫13。
为了便于收集盒30和顶盖10的相对固定,在收集盒30的四周垂直壁的外表面上分别设有一至多个卡口32,同时在盒盖11四周垂直壁的内表面各设置有一个或多个卡扣12与卡口32相对应,如图2所示。卡扣12的数目及位置与收集盒上的卡口32一一对应。此种设置便于带密封垫14的顶盖能压扣到收集盒31上形成紧密贴合,从而使得每个收集孔31得到严密密封。
另一方面密封垫13置于盒盖10顶面的内表面与卡扣12之间并被卡扣12限制而避免从顶盖掉落,当顶盖压盖到所述收集盒上后,每个卡扣12正好扣到卡口32中,使得顶盖10内的密封垫13紧密封住每个收集孔31,顶盖10和收集盒30结合形成一个结合牢固的进样盒,可以直接放置在自动进样器的进样盘中进行样品注射和分析检测。但是,由于每次样品数不一定刚好用完一整盒萃取盒,没有用完的萃取单元可以保存到下一次使用,这就要求压扣好的进样盒能够较方便打开再次收集萃取液后再压扣回去成为密封的进样盒,为了方便顶盖能反复压扣到收集盒上和打开,顶盖盒的四周垂直壁的每一侧或至少一侧可以开两条跨越垂直壁上所有卡扣的垂直切口,所述切口使得盒盖与收集盒压扣之后还能打开,从而萃取盒没有被一次用完时还可以继续使用。
密封垫13的厚度以1-2mm为佳,本实用新型采用1.6mm。如果厚度过薄容易导致压紧程度不严,难以保证密封;过厚则可能使得进样针无法扎穿密封垫,导致进样针损坏。密封垫13一般采用一层弹性软垫如硅胶、橡胶等加上一层致密薄膜如聚丙烯膜、四氟乙烯膜、聚乙烯膜等构成。弹性软垫是为了压紧后保证密封性,而且具备一定的自愈功能,待进样针扎过后能恢复密封性从而防止溶液挥发;致密膜层朝下面向收集溶液主要是为了防止密封垫与收集液发生化学反应、吸附、溶出等相互作用,从而避免发生干扰。如果弹性软垫层所用材质本身具备足够惰性则致密层就可以省去。
本实用新型实施例最佳模式是采用能对样品基质有强吸附作用而对待测物质吸附作用较小的填料装填萃取柱,以过滤方式去掉样品基质的干扰而让待测物被洗脱溶液冲洗出萃取单元,获得与固相萃取相同的对样品起到萃取纯化的效果,由此最大限度提高样品处理的速度和效率。然而,本实用新型也可以采用常用固相萃取填料装填萃取柱,通过常用固相萃取步骤达到样品萃取提纯的目的,只是在最后一步收集时将收集盒对准萃取柱阵列,接收最后的洗脱液用于进样或进一步的浓缩与重溶处理。
对于血样、体液或水样的处理,本实用新型实施例使用的填料是对水分子及强亲水性分子有很强吸附作用的线性或网状物质,填装时尽可能保证填料分子以舒展形式待填入到萃取柱中,待测样品中的水分子沿填料分子形成一层连续吸附的水膜,样品中水溶性强的分子则既分布在水膜中同时又被线性设置的填料吸附,从而不容易被洗脱剂洗脱因此能最大程度的滞留;待分析的有机物分子,如化学药物或农业残留分子等,一般都有一定程度的厌水性(疏水性),因此不容易被填料吸附并更容易分布到洗脱剂中而被洗脱到收集液中。
在用于全血样品的前处理的实施方案中,该萃取单元21中上筛片23的上表面包含一层对细胞有保护作用的亲水性高分子材料,使得该产品可以直接用于全血处理,当全血样品加到上面后,所述保护材料能防止血液中细胞被后继加入的试剂或溶剂破坏,从而避免细胞内的物质进入最终分析样品而产生干扰,所述细胞保护材料可选用强亲水性高分子纤维,譬如棉纤维和其它植物纤维以及化学改性增强了吸水性的此类纤维。
本实用新型实施例提供的萃取盒优选适用于检测生物体内及其他待测样品中的药物。
样品从采集、处理、直至上机分析,整个过程除了使用到移液和抽滤,一切实验耗材都包括在本实用新型上述实施例之内,无需使用其他耗材,因此,本实用新型的萃取盒可以极大限度简化操作过程、减少耗材用量、方便废料回收。本实用新型的顶盖和收集盒既作为萃取单元的包装材料以便于产品的运输与存储,又在样品处理过程中取代了费用较高的收集管、进样瓶和进样瓶的密封盖。由顶盖与收集盒压扣成的进样盒(如图3所示)由于采用整片密封垫,进样针刺穿进样后不会发生变形,自愈恢复密封能力比单个进样瓶盖的密封垫大有改进。实验结果显示,进样针连续刺穿同一个位置8次后仍能保证本实用新型实施例的萃取盒倒置后不会有溶液渗出。
本实用新型实施例提供的萃取盒可以用于抽滤,也可以用于其它方式的压差过滤,如对萃取单元层的上方加压进行过滤。
此外,本实用新型实施例提供的进样盒(萃取盒)可以上下稳定相叠,对于样品存储尤为方便,一个中小型冰箱就可以叠放储存上万个样品。进样盒外形尺寸与国际标准96孔板一致,与所有常用自动进样器相匹配,也与实验室常用自动化液体处理设备无障碍匹配。
根据本实用新型另一实施例,该一体化样品萃取盒的使用方法如下:
1、把收集盒30放进抽滤装置50的底部,落实定位;
2、把萃取单元阵列层20放进真空抽滤装置50的对接窗口,压实;
3、把样品逐一加入到萃取单元阵列层20的萃取单元21中的上筛片23上,加入样品的体积视单个萃取单元容量而定,通常在5μl~5ml;
4、向每个萃取单元21中加入冲洗溶液,溶液组分和加入体积由具体需要分离的物质及萃取单元的特性而定,一般加入体积是50μl~10ml;
5、启动抽滤,让样品和冲洗溶液在萃取单元中经历混合、吸附、分布、洗脱等过程,最后收集从萃取单元洗脱的待测物溶液于收集孔31中;
6、直至所有萃取单元被抽干,溶液全部进入到下方的收集孔31之后,关闭抽滤,并打开泄气阀慢慢消除压差;
7、将萃取单元阵列层20从抽滤装置中取下,放进废料回收;
8、打开真空腔,取出收集盒30,将顶盖10压盖到收集盒30上,使卡扣12都扣进收集盒周边四壁的卡口32中,两者相互扣合,卡合后的进样盒可直接放置在自动进样器中进行上机检测。
9、如果需要重新使用收集盒,可用手指扒开带有切口的顶盖垂直侧壁,顶盖就可以从收集盒脱开,将收集盒放入抽空装置50重复以上1~8步骤则可以将萃取单元剩下未用的单元逐步用完。
以下结合具体实施例对本实用新型的技术方案进行进一步说明。
实施例1
用本实用新型实施例提供的萃取盒做血样中药物分子萃取,可以直接把全血样品加到萃取单元中,然后加入蛋白沉淀剂和洗脱剂,抽滤后收集滤出液即可以用于分析检测。蛋白沉淀剂通常是甲醇、乙腈、高氯酸、或强酸强碱溶液等,洗脱溶液可以是甲醇、乙腈、醋酸溶液、二甲基硫砜、乙酸乙酯、三氯甲烷、四氯化碳等常见有机溶剂。全血样品中的红细胞、白细胞、血小板等可以被填料柱中的顶端筛板及填料挡住,血中的蛋白接触到沉淀剂后变成固体沉淀被填料挡住及填充柱低端的筛板挡住,血样中的内源物质,如磷脂、血糖、血脂、多肽和电解质等能被填料吸附,只有药物分子能被洗脱溶液从填充柱中洗脱出来而进入收集盒,得到的收集液用于lc/ms/ms定量分析。全过程比起常用的蛋白沉淀法处理血样节省时间90%以上,而且最后得到萃取好的样品储备在密封的进样盒中,可以反复用于分析进样,也便于堆放,一个0.5立方米的中小型冰箱就可以放置约1500多盘进样盒,近15,000个样品。如果填料选择合适,经处理后的溶液基本排除了血样中能产生基质效应的干扰物质,那么用本实用新型处理后的血样可以通过直接注射进行质谱定量分析,而本实用新型可以制作成96-孔甚至384-孔阵列形式,因而可以支持最大限度的高通量定量分析体系。
实施例2
用本实用新型实施例提供的萃取盒处理环境水样,只需用1~5ml样品加到萃取单元上,直接抽滤。每个萃取柱可选用聚乙二胺、聚乙二醇、聚乙酰胺、棉纤、改性植物纤维等吸水性极强的填料填装,样品中的水分子及亲水性物质如腐殖酸、糖类等被吸附在填料上,而水样中的固体物质则被填充柱的上筛板及填料挡住,吸附性差的待测分子则被洗脱剂冲洗出萃取单元进入到收集盒,使得收集到的水样既除去了大部分水及水中的干扰物,又富集了待测物,一步就完成了水样处理。
而目前环境水样的处理方法一般采用液液萃取,这样的萃取一般采样500ml以上,加入分液漏斗,再加入与水不混溶的有机溶剂,摇晃20分钟至几个小时,然后静置分层,再把有机相分离出来蒸干,最好将蒸干得到的干渣用少许有机溶剂溶解,得到的溶液再用于上机分析。比较本实用新型实施例的一步到位的样品处理,液液萃取或固相萃取,用本实用新型比液液萃取或固相萃取,节省时间95%以上。同时加样量大幅减少,且检测灵敏度不变。
以水中磺胺类抗生素检测的样品前处理为例,现有国标方法包括:①取水样1.00l置于分液漏斗中;②加内标物于分液漏斗中,混合均匀;③用50%硫酸溶液或10m氢氧化钠溶液调节水样至所需ph5.0;④向装有水样的分液漏斗中加入60ml二氯甲烷;⑤盖好分液漏斗,充分振荡,并周期性地放气以释放过剩的压力;⑥静置10min,让有机相与水相分离;⑦收集溶剂萃取液于锥形烧瓶中;⑧重复步骤①~⑦萃取两次,将3次萃取液合并;⑨旋转蒸发至5~10ml然后氮吹至干渣;⑩用5.00ml甲醇溶解干渣并过滤后即得到待测溶液。全过程大约需要4小时,检测灵敏度对于大部分磺胺类抗生素大约为0.1ppm。采用本实用新型处理相同的水样只需要三步:①取5.00m加入吸水性极强的萃取柱;②抽滤至水样全部吸附到柱中填料上;③加2.00ml甲醇再抽滤,得到约250μl滤出液可直接用于分析检测。全过程约5分钟,得到的检测灵敏度对于大部分磺胺类抗生素约为0.1ppm。
以上所述,仅为本实用新型较佳的具体实施方式,但本实用新型的保护范围并不局限于此,任何熟悉本技术领域的技术人员在本实用新型揭露的技术范围内,根据本实用新型的技术方案及其实用新型构思加以等同替换或改变,都应涵盖在本实用新型的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!