可裂解的多醇基微胶囊的制作方法
1.本发明涉及一种制备基于可裂解(cleavable)多醇(multi
‑
alcohols)的微胶囊的新方法。可裂解的多醇基微胶囊也是本发明的一个目的。包含所述胶囊的加香组合物和消费品,特别是家庭护理或个人护理产品形式的已加香消费品,也是本发明的一部分。
背景技术:
2.香料(日化香精)工业面临的问题之一是有气味化合物由于其挥发性,特别是“前调(头香)”的挥发性,其所提供的嗅觉益处相对较快地丧失。为了调整挥发物的释放速率,需要使用递送系统(例如含有香料的微胶囊)来保护并在触发时释放核心有效载荷。对于这些系统,业界的一项关键要求是要能够在具有挑战性的基料中保持悬浮状态,而不会发生物理分解或降解。这被称为递送系统的稳定性。例如,含有高含量侵蚀性表面活性剂清洁剂的芳香化个人和家用清洁剂对于微胶囊的稳定性非常具有挑战性。
3.聚脲和聚氨酯基的微胶囊浆料在香料工业中被广泛使用,例如它们在施用于不同的基底上后提供持久的、令人愉悦的嗅觉效果。这些微胶囊已在现有技术中广泛公开(参见例如来自申请人的wo2007/004166或ep 2300146)。
4.仍然需要提供新的微胶囊,同时又不损害微胶囊的性能,特别是在诸如消费品基料之类的具有挑战性的介质中的稳定性方面,以及在活性成分递送方面的递送良好性能方面,例如在加香成分的情况下具有嗅觉性能。
5.本发明通过使用基于可逆反应的共价适应性网络提供基于可裂解多醇的新型微胶囊来提出上述问题的解决方案。
技术实现要素:
6.现在令人惊奇地发现,通过使用可裂解多醇作为制备微胶囊的聚合壁的结构单元,可以获得表现为包封疏水性成分的核
‑
壳微胶囊。已经表明,共价适应性网络的存在可以提供性能良好的微胶囊。
7.因此,本发明的方法提供了上述问题的解决方案,因为它允许制备在具有挑战性的料中具有所需稳定性的微胶囊。
8.在第一形态中,本发明涉及一种用于制备核
‑
壳微胶囊浆料的方法,包括以下步骤:
9.a)在疏水性材料优选香料中加入至少一种多官能单体以形成油相;
10.b)制备分散相,其中该分散相与该油相不混溶;
11.c)将该油相加入到该分散相中,以形成两相分散体;
12.d)可选地,向步骤c)中获得的分散体中加入反应物;和
13.e)进行固化步骤,以形成浆料形式的核
‑
壳微胶囊,
14.其中在步骤a)和/或步骤b)中加入稳定剂,和
15.其中在步骤a)中和/或在步骤b)中和/或在步骤c)中和/或在步骤d)中加入至少一
种可裂解多醇,
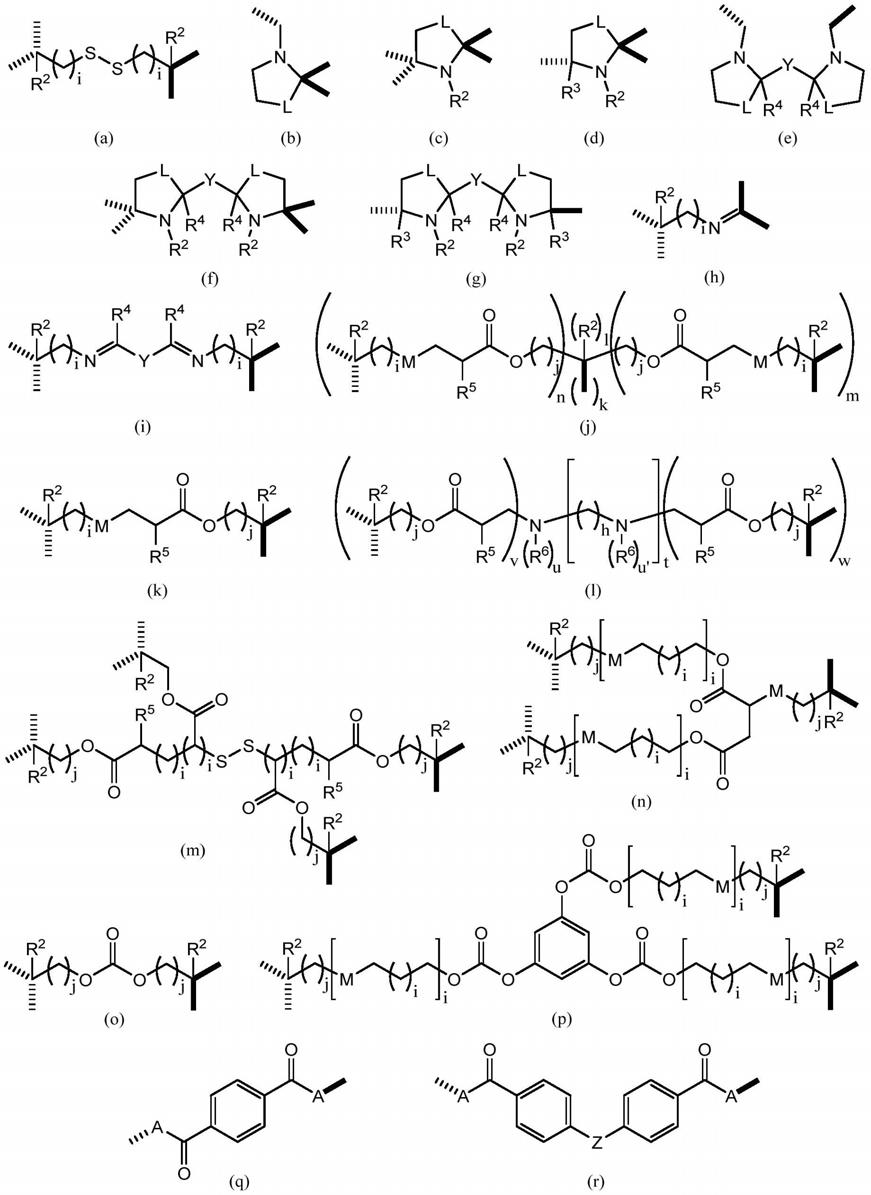
16.其中可裂解多醇具有下式(i):
[0017][0018]
其中每个r1独立地是h或ch2oh并且其中p和q是在1和3之间变化的整数,优选p和q是1或2,并且
[0019]
其中x是c2至c
30
烃基,可能包含一至十个选自o、s和n的杂原子以形成醚、酯、羧酸、醛、酮、醇、硫醇、二硫化物、硫醚、硫酯、氨基甲酸酯、酰胺、肟、亚胺、胺或腈官能团。
[0020]
在第二形态中,本发明涉及一种核
‑
壳微胶囊,其包含:
[0021]
‑
油基核,其包含疏水性材料,优选香料,和
[0022]
‑
壳,其包含多官能单体与如上定义的可裂解多醇之间的反应产物。
[0023]
本发明的第三个目的是包含至少一种微胶囊的核
‑
壳微胶囊浆料,该微胶囊具有:
[0024]
‑
油基核,其包含疏水性材料,优选香料,和
[0025]
‑
壳,其包含多官能单体与如上定义的可裂解多醇之间的反应产物。
[0026]
本发明的第四个目的是可通过如上定义的方法获得的核
‑
壳微胶囊浆料。
[0027]
包含如下成分的加香组合物是本发明的另一个目的:
[0028]
(i)如上定义的微胶囊或微胶囊浆料,其中疏水性材料包含香料,
[0029]
(ii)至少一种从由香料载体和香料基料构成的群组中选出的成分,和
[0030]
(iii)视情况使用的至少一种香料佐剂。
[0031]
本发明的另一个目的是一种消费品,其包含:
[0032]
‑
个人护理活性基料,以及
[0033]
‑
如上定义的微胶囊或微胶囊浆料或如上定义的加香组合物,
[0034]
其中消费品是个人护理组合物的形式。
[0035]
本发明的另一个目的是一种消费品,其包含:
[0036]
‑
家庭护理或织物护理活性基料,以及
[0037]
‑
如上定义的微胶囊或微胶囊浆料或如上定义的加香组合物,
[0038]
其中消费品是家庭护理或织物护理组合物的形式。
[0039]
发明详述
[0040]
除非另有说明,百分比(%)是指组合物的重量百分比。
[0041]
通过“活性成分”,是指单一化合物或多种成分的组合。
[0042]
通过“香料油或调味料油”,是指单一的加香或调味化合物,或几种加香或调味化合物的混合物。
[0043]
通过“消费品”或“最终产品”,是指准备好由消费者分发、出售和使用的制成品。
[0044]
为了清楚起见,本发明中的表述“分散体”是指一种体系,其中颗粒分散在不同组成的连续相中,并且其具体包括悬浮液或乳液。
[0045]
本发明中的“微胶囊”或类似表述是指核
‑
壳微胶囊具有微米范围的粒度分布(例如平均直径(d(v,0.5)),其为约1至3000微米,优选为1至1000微米,更优选为1至500微米,甚至更优选为5至50微米)并包含外部的基于固体聚合物的壳和被外壳包围的内部连续油
相。
[0046]
通过“微胶囊浆料”,是指分散在液体中的微胶囊。根据一个实施方案,浆料是含水浆料,即微胶囊分散在水相中。
[0047]
通过“多官能单体”,是指一种分子,其作为单元,以化学方式反应或结合以形成聚合物或超分子聚合物。本发明的多官能单体具有至少两个能够与另一单体的官能团反应或结合以形成(聚合的)微胶囊壳的官能团。措辞“壳”和“壁”在本发明中被无差别地使用。
[0048]
通过“可裂解多醇”,是指具有下式的多醇(multiol)或多元醇(polyol):
[0049][0050]
其中每个r1独立地是h或ch2oh并且其中p和q是在1和3之间变化的整数,优选p和q是1或2,并且
[0051]
其中x是c2至c
30
烃基,可能包含一至十个选自o、s和n的杂原子以形成醚、酯、羧酸、醛、酮、醇、硫醇、二硫化物、硫醚、硫酯、氨基甲酸酯、酰胺、肟、亚胺、胺或腈官能团。
[0052]
根据本发明,由于氧化还原反应、水解、逆向1,4
‑
加成、光的作用和/或它们的组合,x可以通过一个或多个共价键的断裂而分裂成至少两个单独的部分。
[0053]
根据本发明,无差别地使用措词“聚酰氯(poly acid chloride)”和“聚酰基氯(poly acyl chloride)”。
[0054]
已经发现,通过在形成聚合胶囊壳的过程中使可裂解多醇与至少一种其他多官能单体反应,可以获得在具有挑战性的基料中总体良好性能的核
‑
壳微胶囊。当作为共聚单体存在于壳中时,这些可裂解多醇在具有挑战性的基料中出乎预料地稳定。
附图说明
[0055]
图1表示根据本发明的聚(氨基甲酸酯)核
‑
壳微胶囊的光学显微照片。
具体实施方式
[0056]
制备微胶囊浆料的方法
[0057]
本发明的第一个目的是一种制备核
‑
壳微胶囊浆料的方法,包括以下步骤:
[0058]
a)在疏水性材料优选香料中加入至少一种多官能单体以形成油相;
[0059]
b)制备分散相,其中该分散相与该油相不混溶;
[0060]
c)将该油相加入到该分散相中,以形成两相分散体;
[0061]
d)可选地,向步骤c)中获得的分散体中加入反应物;和
[0062]
e)进行固化步骤,以形成浆料形式的核
‑
壳微胶囊,
[0063]
其中在步骤a)和/或步骤b)中加入稳定剂,和
[0064]
其中在步骤a)中和/或在步骤b)中和/或在步骤c)中和/或在步骤d)中加入至少一种可裂解多醇,
[0065]
其中可裂解多醇具有下式(i):
[0066][0067]
其中每个r1独立地是h或ch2oh并且其中p和q是在1和3之间变化的整数,优选p和q是1或2,并且
[0068]
其中x是c2至c
30
烃基,可能包含一至十个选自o、s和n的杂原子以形成醚、酯、羧酸、醛、酮、醇、硫醇、二硫化物、硫醚、硫酯、氨基甲酸酯、酰胺、肟、亚胺、胺或腈官能团。
[0069]
步骤a):在疏水性材料优选香料中加入至少一种多官能单体以形成油相
[0070]
疏水性材料
[0071]
根据本发明的疏水性材料可以是“惰性”材料,如溶剂或活性成分。
[0072]
当疏水性材料是活性成分时,其优选从由调味料、调味料成分、香料、香料成分、营养制品、化妆品、有害生物(pest)防治剂、杀生物剂活性物质以及它们的混合物构成的群组中选出。
[0073]
根据一个特定的实施方案,疏水性材料包含香料与另一种成分的混合物,所述另一种成分从由营养保健品,化妆品,有害生物防治剂和杀生物剂活性成分构成的群组中选出。
[0074]
根据一个特定的实施方案,疏水性材料包含杀生物剂活性成分与另一种成分的混合物,所述另一种成分从由香料,营养保健品,化妆品,有害生物防治剂构成的群组中选出。
[0075]
根据一个特定的实施方案,疏水性材料包含有害生物防治剂与另一种成分的混合物,所述另一种成分从由香料,营养保健品,化妆品,杀生物剂活性成分构成的群组中选出。
[0076]
根据一个特定的实施方案,疏水性材料包含香料。
[0077]
根据一个特定的实施方案,疏水性材料由香料组成。
[0078]
根据一个特定的实施方案,疏水性材料由杀生物剂活性成分组成。
[0079]
根据一个特定的实施方案,疏水性材料由有害生物防治剂组成。
[0080]
通过“香料”(或也称为“香料油”),在这里是指在约20℃下为液体的成分或组合物。根据以上实施方案中的任何一个,所述香料油可以是单独的加香成分或加香组合物形式的成分的混合物。作为“加香成分”,在此是指一种化合物,其主要目的是用于赋予或调节气味。换言之,要被认为是加香成分的这种成分必须被本领域技术人员认识到能够至少以主动或令人愉快的方式赋予或改变组合物的气味,而不仅仅是具有气味。为了本发明的目的,香料油还包括加香成分与共同改善、增强或改变加香成分的递送的物质的组合,例如香料前体、乳液或分散体,以及赋予除改变或赋予气味之外的其他益处的组合,所述益处例如持久、迸发、恶臭抵消、抗菌效果、微生物稳定性、有害生物防治。
[0081]
在油相中存在的加香成分的性质和类型在这里不保证有更详细的描述,其无论如何都不会穷尽,本领域技术人员能够基于其普通常识并根据预期使用或应用以及所需的感官效果来选择它们。一般而言,这些加香成分属于不同的化学类别,如醇类、醛类、酮类、酯类、醚类、乙酸酯类、腈类、萜类化合物、含氮或含硫杂环化合物和精油,并且所述加香助成分可以是天然来源的或合成来源的。无论如何,许多的这些助成分列于参考文献诸如s.arctander的著作perfume and flavor chemicals,1969,montclair,new jersey,usa或其更新的版本或类似性质的其他著作中,以及香料业领域内丰富的专利文献中。还应当理
解,所述成分也可以是已知以受控方式释放各种类型的加香化合物的化合物,也被称为香料前体(properfume)或芳香剂前体(profragrance)。合适的香料前体的非限制性例子可包括4
‑
(十二烷基硫代)
‑4‑
(2,6,6
‑
三甲基
‑2‑
环己烯
‑1‑
基)
‑2‑
丁酮、4
‑
(十二烷基硫代)
‑4‑
(2,6,6
‑
三甲基
‑1‑
环己烯
‑1‑
基)
‑2‑
丁酮、反式
‑3‑
(十二烷基硫代)
‑1‑
(2,6,6
‑
三甲基
‑3‑
环己烯
‑1‑
基)
‑1‑
丁酮、氧代(苯基)乙酸2
‑
苯基乙酯、氧代(苯基)乙酸3,7
‑
二甲基辛
‑
2,6
‑
二烯
‑1‑
基酯、氧代(苯基)乙酸(z)
‑
己
‑3‑
烯
‑1‑
基酯、十六烷酸3,7
‑
二甲基
‑
2,6
‑
辛二烯
‑1‑
基酯、琥珀酸双(3,7
‑
二甲基辛
‑
2,6
‑
二烯
‑1‑
基)酯、(2
‑
((2
‑
甲基十一碳
‑1‑
烯
‑1‑
基)氧基)乙基)苯、1
‑
甲氧基
‑4‑
(3
‑
甲基
‑4‑
苯乙氧基丁
‑3‑
烯
‑1‑
基)苯、(3
‑
甲基
‑4‑
苯乙氧基丁
‑3‑
烯
‑1‑
基)苯、1
‑
(((z)
‑
己
‑3‑
烯
‑1‑
基)氧基)
‑2‑
甲基十一碳
‑1‑
烯、(2
‑
((2
‑
甲基十一碳
‑1‑
烯
‑1‑
基)氧基)乙氧基)苯、2
‑
甲基
‑1‑
(辛
‑3‑
基氧基)十一碳
‑1‑
烯、1
‑
甲氧基
‑4‑
(1
‑
苯乙氧基丙
‑1‑
烯
‑2‑
基)苯、1
‑
甲基
‑4‑
(1
‑
苯乙氧基丙
‑1‑
烯
‑2‑
基)苯、2
‑
(1
‑
苯乙氧基丙
‑1‑
烯
‑2‑
基)萘、(2
‑
苯乙氧基乙烯基)苯、2
‑
(1
‑
((3,7
‑
二甲基辛
‑6‑
烯
‑1‑
基)氧基)丙
‑1‑
烯
‑2‑
基)萘或它们的混合物。
[0082]
可以将加香成分溶解在香料工业中当前使用的溶剂中。溶剂优选不是醇。此类溶剂的例子为邻苯二甲酸二乙酯、肉豆蔻酸异丙酯、(松香树脂,可从伊士曼(eastman)获得)、苯甲酸苄酯、柠檬酸乙酯、柠檬烯或其他萜烯或异链烷烃。优选地,该溶剂是非常疏水的和高度空间受阻的,例如或苯甲酸苄酯。优选地,香料包含少于30%的溶剂。更优选地,香料包含少于20%,甚至更优选地少于10%的溶剂,所有这些百分比均相对于香料的总重量以重量计。最优选地,香料基本上不含溶剂。
[0083]
优选的加香成分是具有高空间位阻的成分,特别是来自以下组中之一的那些成分:
[0084]
‑
组1:包含被至少一个直链或支链c1‑
c4烷基或烯基取代基取代的环己烷、环己烯、环己酮或环己烯酮环的加香成分;
[0085]
‑
组2:包含被至少一个直链或支链c4‑
c8烷基或烯基取代基取代的环戊烷、环戊烯、环戊酮或环戊烯酮环的加香成分;
[0086]
‑
组3:包含苯环的加香成分,或者包含被至少一个直链或支链c5‑
c8烷基或烯基取代基取代的、或被至少一个苯基取代基取代并且可选地被一个或多个直链或支链c1‑
c3烷基或烯基取代基取代的环己烷、环己烯、环己酮或环己烯酮环的加香成分;
[0087]
‑
组4:包含至少两个稠合或连接的c5和/或c6环的加香成分;
[0088]
‑
组5:包含樟脑样环结构的加香成分;
[0089]
‑
组6:包含至少一个c7至c
20
环结构的加香成分;
[0090]
‑
组7:logp值高于3.5并含有至少一个叔丁基或至少一个三氯甲基取代基的加香成分;
[0091]
来自这些组中每一组成分的例子有:
[0092]
‑
组1:2,4
‑
二甲基
‑3‑
环己烯
‑1‑
甲醛(来源:firmenich sa,瑞士日内瓦)、异环柠檬醛、薄荷酮、异薄荷酮、2,2
‑
二甲基
‑6‑
亚甲基
‑1‑
环己烷甲酸甲酯(来源:firmenich sa,瑞士日内瓦)、橙花酮、萜品醇、二氢萜品醇、乙酸萜烯酯、乙酸二氢萜烯酯、二戊烯(dipentene)、桉油醇、己酸酯(hexylate)、玫瑰醚、(s)
‑
1,8
‑
对薄荷二烯
‑7‑
醇(来源:
firmenich sa,瑞士日内瓦)、l
‑
对薄荷烯
‑4‑
醇、乙酸(1rs,3rs,4sr)
‑3‑
对薄荷酯、(1r,2s,4r)
‑
4,6,6
‑
三甲基
‑
双环[3,1,1]庚
‑2‑
醇、四氢
‑4‑
甲基
‑2‑
苯基
‑
2h
‑
吡喃(来源:firmenich sa,瑞士日内瓦)、乙酸环己酯、乙酸三甲基环己酯(cyclanol)、1,4
‑
环己烷二乙基二甲酸酯(来源:firmenich sa,瑞士日内瓦)、(3ars,6sr,7asr)
‑
全氢
‑
3,6
‑
二甲基
‑
苯并[b]呋喃
‑2‑
酮(来源:firmenich sa,瑞士日内瓦)、(6r)
‑
全氢
‑
3,6
‑
二甲基
‑
苯并[b]呋喃
‑2‑
酮(来源:firmenich sa,瑞士日内瓦)、2,4,6
‑
三甲基
‑4‑
苯基
‑
1,3
‑
二恶烷、2,4,6
‑
三甲基
‑3‑
环己烯
‑1‑
甲醛;
[0093]
‑
组2:(e)
‑3‑
甲基
‑5‑
(2,2,3
‑
三甲基
‑3‑
环戊烯
‑1‑
基)
‑4‑
戊烯
‑2‑
醇(来源:givaudan sa,瑞士韦尔涅)、(1'r,e)
‑2‑
乙基
‑4‑
(2',2',3'
‑
三甲基
‑
3'
‑
环戊烯
‑
1'
‑
基)
‑2‑
丁烯
‑1‑
醇(来源:firmenich sa,瑞士日内瓦)、(1'r,e)
‑
3,3
‑
二甲基
‑5‑
(2',2',3'
‑
三甲基
‑
3'
‑
环戊烯
‑
1'基)
‑4‑
戊烯
‑2‑
醇(来源:firmenich sa,瑞士日内瓦)、2
‑
庚基环戊酮(fleuramone)、甲基
‑
顺
‑3‑
氧
‑2‑
戊基
‑1‑
环戊烷乙酸酯(来源:firmenich sa,瑞士日内瓦)、2,2,5
‑
三甲基
‑5‑
戊基
‑1‑
环戊酮(来源:firmenich sa,瑞士日内瓦)、3,3
‑
二甲基
‑5‑
(2,2,3
‑
三甲基
‑3‑
环戊烯
‑1‑
基)
‑4‑
戊烯
‑2‑
醇(来源:firmenich sa,瑞士日内瓦)、3
‑
甲基
‑5‑
(2,2,3
‑
三甲基
‑3‑
环戊烯
‑1‑
基)
‑2‑
戊醇(来源:givaudan sa,瑞士韦尔涅);
[0094]
‑
组3:大马酮、1
‑
(5,5
‑
二甲基
‑1‑
环己烯
‑1‑
基)
‑4‑
戊烯
‑1‑
酮(来源:firmenich sa,瑞士日内瓦)、nectalactone((1'r)
‑2‑
[2
‑
(4'
‑
甲基
‑
3'
‑
环己烯
‑
1'
‑
基)丙基]环戊酮)、α
‑
紫罗兰酮、β
‑
紫罗兰酮、大马烯酮、1
‑
(5,5
‑
二甲基
‑1‑
环己烯
‑1‑
基)
‑4‑
戊烯
‑1‑
酮和1
‑
(3,3
‑
二甲基
‑1‑
环己烯
‑1‑
基)
‑4‑
戊烯
‑1‑
酮的混合物(来源:firmenich sa,瑞士日内瓦)、1
‑
(2,6,6
‑
三甲基
‑1‑
环己烯
‑1‑
基)
‑2‑
丁烯
‑1‑
酮(来源:firmenich sa,瑞士日内瓦)、丙酸(1s,1'r)
‑
[1
‑
(3',3'
‑
二甲基
‑
1'
‑
环己基)乙氧基羰基]甲酯(来源:firmenich sa,瑞士日内瓦)、乙酸2
‑
叔丁基
‑1‑
环己酯(来源:international flavors and fragrances,美国)、1
‑
(2,2,3,6
‑
四甲基
‑
环己基)
‑3‑
己醇(来源:firmenich sa,瑞士日内瓦)、反式
‑1‑
(2,2,6
‑
三甲基
‑1‑
环己基)
‑3‑
己醇(来源:firmenich sa,瑞士日内瓦)、(e)
‑3‑
甲基
‑4‑
(2,6,6
‑
三甲基
‑2‑
环己烯
‑1‑
基)
‑3‑
丁烯
‑2‑
酮、异丁酸萜烯酯、乙酸4
‑
(1,1
‑
二甲基乙基)
‑1‑
环己酯(来源:firmenich sa,瑞士日内瓦)、8
‑
甲氧基
‑1‑
对薄荷烯、丙酸(1s,1'r)
‑2‑
[1
‑
(3',3'
‑
二甲基
‑
1'
‑
环己基)乙氧基]
‑2‑
甲基丙酯(来源:firmenich sa,瑞士日内瓦)、对叔丁基环己酮、薄荷烯硫醇、1
‑
甲基
‑4‑
(4
‑
甲基
‑3‑
戊烯基)
‑3‑
环己烯
‑1‑
甲醛、环己基丙酸烯丙酯、水杨酸环己酯、碳酸2
‑
甲氧基
‑4‑
甲基苯基酯甲酯、碳酸乙酯2
‑
甲氧基
‑4‑
甲基苯基酯、碳酸4
‑
乙基
‑2‑
甲氧基苯基酯甲酯;
[0095]
‑
组4:甲基柏木酮(来源:international flavors and fragrances,美国)、2
‑
甲基丙酸(1rs,2sr,6rs,7rs,8sr)
‑
三环[5.2.1.0~2,6~]癸
‑3‑
烯
‑8‑
基酯与2
‑
甲基丙酸(1rs,2sr,6rs,7rs,8sr)
‑
三环[5.2.1.0~2,6~]癸
‑4‑
烯
‑8‑
基酯的混合物、岩兰醇(vetyverol)、岩兰酮(vetyverone)、1
‑
(八氢
‑
2,3,8,8
‑
四甲基
‑2‑
萘基)
‑1‑
乙酮(来源:international flavors and fragrances,美国)、(5rs,9rs,10sr)
‑
2,6,9,10
‑
四甲基
‑1‑
氧杂螺[4.5]癸
‑
3,6
‑
二烯和(5rs,9sr,10rs)异构体、6
‑
乙基
‑
2,10,10
‑
三甲基
‑1‑
氧杂螺[4.5]癸
‑
3,6
‑
二烯、1,2,3,5,6,7
‑
六氢
‑
1,1,2,3,3
‑
五甲基
‑4‑
茚酮(来源:international flavors and fragrances,美国)、3
‑
(3,3
‑
二甲基
‑5‑
茚满基)丙醛和3
‑
(1,1
‑
二甲基
‑5‑
茚满基)丙醛的混合物(来源:firmenich sa,瑞士日内瓦)、3',4
‑
二甲基
‑
三环[6.2.1.0(2,
7)]十一碳
‑4‑
烯
‑9‑
螺
‑
2'
‑
环氧乙烷(来源:firmenich sa,瑞士日内瓦)、9/10
‑
乙基二烯
‑3‑
氧杂三环[6.2.1.0(2,7)]十一烷、(乙酸全氢
‑
5,5,8a
‑
三甲基
‑2‑
萘基酯(来源:firmenich sa,瑞士日内瓦)、1
‑
萘醇(octalynol)、(十二氢
‑
3a,6,6,9a
‑
四甲基萘并[2,1
‑
b]呋喃(来源:firmenich sa,瑞士日内瓦)、乙酸三环[5.2.1.0(2,6)]癸
‑3‑
烯
‑8‑
基酯和乙酸三环[5.2.1.0(2,6)]癸
‑4‑
烯
‑8‑
基酯以及丙酸三环[5.2.1.0(2,6)]癸
‑3‑
烯
‑8‑
基酯和丙酸三环[5.2.1.0(2,6)]癸
‑4‑
烯
‑8‑
基酯、(+)
‑
(1s,2s,3s)
‑
2,6,6
‑
三甲基
‑
双环[3.1.1]庚烷
‑3‑
螺
‑
2'
‑
环己烯
‑
4'
‑
酮;
[0096]
‑
组5:樟脑、冰片、乙酸异冰片酯、8
‑
异丙基
‑6‑
甲基
‑
双环[2.2.2]辛
‑5‑
烯
‑2‑
甲醛、蒎烯、莰烯、8
‑
甲氧基雪松烷、(8
‑
甲氧基
‑
2,6,6,8
‑
四甲基
‑
三环[5.3.1.0(1,5)]十一烷(来源:firmenich sa,瑞士日内瓦)、雪松烯、雪松烯醇、雪松醇、9
‑
亚乙基
‑3‑
氧杂三环[6.2.1.0(2,7)]十一碳
‑4‑
酮和10
‑
亚乙基
‑3‑
氧杂三环[6.2.1.0(2,7)]十一碳
‑4‑
酮的混合物(来源:firmenich sa,瑞士日内瓦)、3
‑
甲氧基
‑
7,7
‑
二甲基
‑
10
‑
亚甲基
‑
双环[4.3.1]癸烷(来源:firmenich sa,瑞士日内瓦);
[0097]
‑
组6:(三甲基
‑
13
‑
氧杂双环
‑
[10.1.0]
‑
三癸
‑
4,8
‑
二烯(来源:firmenich sa,瑞士日内瓦)、黄葵内酯lg((e)
‑9‑
环十六烯
‑
16
‑
内酯,来源:firmenich sa,瑞士日内瓦)、环十五烯内酯(来源:firmenich sa,瑞士日内瓦)、麝香烯酮(3
‑
甲基(4/5)
‑
环十五烯酮,来源:firmenich sa,瑞士日内瓦)、3
‑
甲基环十五酮(来源:firmenich sa,瑞士日内瓦)、十五内酯(来源:firmenich sa,瑞士日内瓦)、环十五酮(来源:firmenich sa,瑞士日内瓦)、(1
‑
乙氧基乙氧基)环十二烷(来源:firmenich sa,瑞士日内瓦)、1,4
‑
二氧杂环十七烷
‑
5,17
‑
二酮、4,8
‑
环十二碳二烯
‑1‑
酮;
[0098]
‑
组7:(+
‑
)
‑2‑
甲基
‑3‑
[4
‑
(2
‑
甲基
‑2‑
丙基)苯基]丙醛(来源:givaudan sa,瑞士韦尔涅)、乙酸2,2,2
‑
三氯
‑1‑
苯基乙酯。
[0099]
优选地,香料包含至少30%,优选至少50%,更优选至少60%从如上定义的组1至组7中选出的成分。更优选地,所述香料包含至少30%,优选至少50%从如上定义的组3至组7中选出的成分。最优选地,所述香料包含至少30%,优选至少50%从如上定义的组3、组4、组6或组7中选出的成分。
[0100]
根据另一个优选的实施方案,香料包含至少30%,优选至少50%,更优选至少60%的logp高于3,优选高于3.5,甚至更优选高于3.75的成分。
[0101]
优选地,在本发明中使用的香料含有小于其自身重量10%的伯醇,小于其自身重量15%的仲醇和小于其自身重量20%的叔醇。有利地,在本发明中使用的香料不含任何伯醇,而含有少于15%的仲醇和叔醇。
[0102]
根据一个实施方案,油相(或油基核)包括:
[0103]
‑
25~100wt%的香料油,其包含至少15wt%的具有log t<
‑
4的高冲击香料原料,和
[0104]
‑
0~75wt%的密度平衡材料,其密度大于1.07g/cm3。
[0105]
在wo2018115250中描述了具有log t<
‑
4的高冲击香料原料和具有大于1.07g/cm3的密度的密度平衡材料的性质,其内容通过引用包括在内。
[0106]
术语“杀生物剂(biocide)”是指能够杀死活生物体(例如微生物)或减少或防止其生长和/或积累的化学物质。杀生物剂通常用于医药、农业、林业以及防止例如水、农产品
(包括种子)和输油管道结垢的工业中。杀生物剂可以是农药,包括杀真菌剂、除草剂、杀虫剂、杀藻剂、杀软体动物剂、杀螨剂和灭鼠剂;和/或抗微生物剂,例如杀菌剂、抗生素、抗细菌剂、抗病毒剂、抗真菌剂、抗原生动物和/或抗寄生虫药。
[0107]
如本文所用,“有害生物(pest)防治剂”是指用于排斥或吸引有害生物,以减少、抑制或促进其生长、发育或活性的物质。有害生物是指对植物或动物具有侵入性或麻烦的任何生物体,无论是动物、植物还是真菌,有害生物包括昆虫,尤其是节肢动物、螨虫、蜘蛛、真菌、杂草、细菌和其他微生物。
[0108]
根据一个特定的实施方案,疏水性材料不含任何活性成分(例如香料)。根据该特定的实施方案,其包含疏水性溶剂,优选由其组成,优选选自肉豆蔻酸异丙酯,甘油三酸酯(例如,mct油,植物油),d
‑
柠檬烯,硅油,矿物油以及它们的混合物,以及可选地选自以下的亲水性溶剂:1,4
‑
丁二醇,苄醇,柠檬酸三乙酯,甘油三乙酸酯,乙酸苄酯,乙酸乙酯,丙二醇(1,2
‑
丙二醇),1,3
‑
丙二醇,一缩二丙二醇,甘油,乙二醇醚以及它们的混合物。
[0109]
根据本发明的任一实施方案,相对于在步骤c)之后获得的分散体的总重量,疏水性材料占约10%至60%w/w,或甚至15%至45%w/w,按重量计。
[0110]
根据一个特定的实施方案,油相基本上由多官能单体、可裂解多醇和香料油或调味料油组成。
[0111]
多官能单体
[0112]
根据一个实施方案,多官能单体是从由如下构成的群组中选出的:至少一种多异氰酸酯、聚马来酸酐、聚酰氯、聚环氧化物、聚丙烯酸酯、聚甲基丙烯酸酯、聚烷氧基硅烷以及它们的混合物。
[0113]
基于油相的总量以重量计,本发明方法中使用的多官能单体以0.1至15%,优选0.5至10%,更优选0.8至6%,甚至更优选1至3%的量存在。
[0114]
根据一个特定的实施方案,在步骤a)中加入的单体是至少一种具有至少两个异氰酸酯官能团的多异氰酸酯。
[0115]
根据本发明使用的合适的多异氰酸酯包括芳族多异氰酸酯、脂族多异氰酸酯以及它们的混合物。所述多异氰酸酯包含至少2个,优选至少3个,但是可以包含最多6个,或甚至仅4个异氰酸酯官能团。根据一个特定的实施方案,使用三异氰酸酯(3个异氰酸酯官能团)。
[0116]
根据一个实施方案,所述多异氰酸酯是芳族多异氰酸酯。
[0117]
术语“芳族多异氰酸酯”在本文中意指涵盖任何包含芳族部分的多异氰酸酯。优选的,其包含苯基、甲苯酰基、二甲苯基、萘基或二苯基部分。更优选甲苯酰基或二甲苯基部分。优选的芳族多异氰酸酯是二异氰酸酯的缩二脲、聚异氰脲酸酯和三羟甲基丙烷加合物,更优选包含上述特定芳族部分之一。更优选地,芳族多异氰酸酯是甲苯二异氰酸酯的聚异氰脲酸酯(可从bayer以商品名rc购得)、甲苯二异氰酸酯的三羟甲基丙烷加合物(可从bayer以商品名l75购得)、苯二甲基二异氰酸酯的三羟甲基丙烷加合物(可从mitsui chemicals以商品名d
‑
110n购得)。在一个最优选的实施方案中,芳族多异氰酸酯是苯二甲基二异氰酸酯的三羟甲基丙烷加合物。
[0118]
根据另一个实施方案,所述多异氰酸酯是脂族多异氰酸酯。术语“脂族多异氰酸
酯”定义为不包含任何芳族部分的多异氰酸酯。优选的脂族多异氰酸酯是六亚甲基二异氰酸酯的三聚体、异佛尔酮二异氰酸酯的三聚体、六亚甲基二异氰酸酯的三羟甲基丙烷加合物(可从mitsui chemicals获得)或六亚甲基二异氰酸酯的缩二脲(可商购自bayer,商品名为n 100),其中甚至更优选六亚甲基二异氰酸酯的缩二脲。
[0119]
根据另一个实施方案,该至少一种多异氰酸酯为至少一种脂族多异氰酸酯与至少一种芳族多异氰酸酯的混合物的形式,两者均包含至少两个或三个异氰酸酯官能团,例如六亚甲基二异氰酸酯的缩二脲与苯二甲基二异氰酸酯的三羟甲基丙烷加合物的混合物、六亚甲基二异氰酸酯的缩二脲与甲苯二异氰酸酯的多异氰脲酸酯的混合物、以及六亚甲基二异氰酸酯的缩二脲与甲苯二异氰酸酯的三羟甲基丙烷加合物的混合物。最优选地,它是六亚甲基二异氰酸酯的缩二脲与苯二甲基二异氰酸酯的三羟甲基丙烷加合物的混合物。优选地,当作为混合物使用时,脂族多异氰酸酯与芳族多异氰酸酯之间的摩尔比在80:20至10:90的范围内。
[0120]
根据一个实施方案,本发明方法中使用的至少一种多异氰酸酯以基于油相总量的0.1至15重量%,优选0.5至10重量%,更优选0.8至6重量%,甚至更优选1至3重量%的量存在。
[0121]
根据另一个实施方案,本发明中使用的多官能聚合物是聚酰氯。
[0122]
根据一个实施方案,聚酰氯是从由如下构成的群组中选出的:苯
‑
1,3,5
‑
三甲酰氯、苯
‑
1,2,4
‑
三酰三氯、苯
‑
1,2,4,5
‑
四酰四氯、环己烷
‑
1,3,5
‑
三酰三氯、间苯二酰二氯、氧化二乙酰二氯(diglycolyl dichloride)、琥珀酰二氯、对苯二甲酰氯以及它们的混合物。
[0123]
根据一个特定的实施方案,聚酰氯是1,3,5
‑
苯三甲酰氯。
[0124]
根据一个特定的实施方案,聚酰氯具有下式(ii)
[0125][0126]
其中s是在1至8之间,优选在1和6之间,更优选在1和4之间变化的整数,并且
[0127]
其中q是(s+1)价c3至c6烷基,或包含至少一个选自(i)至(vi)的基团的(s+1)价c2至c
45
烃基,
[0128][0129]
其中r是氢原子或甲基或乙基,优选氢原子。
[0130]
根据一个实施方案,如果烃基q包含若干个选自(i)至(vi)的基团,则它们各自被q的至少一个碳原子隔开。
[0131]
应当理解,通过
“…
烃基
…”
是指所述基团由氢和碳原子组成,并且可以是脂族烃的形式,即直链或支链饱和烃(例如烷基)、直链或支链不饱和烃(例如链烯基或炔基)、饱和环烃(例如环烷基)或不饱和环烃(例如环烯基或环炔基),或可以是芳烃的形式,即芳基,或
者也可以是所述类型基团的混合物的形式,例如,除非具体限制为仅为所提及的一种类型,否则特定基团可包含直链烷基、支链烯基(例如具有一个或多个碳
‑
碳双键)、(多)环烷基和芳基部分。类似地,在本发明的所有实施方案中,当提及基团以多于一种类型的拓扑(例如直链、环状或支链)和/或饱和或不饱和(例如烷基、芳族或烯基)形式时,它还意指可包含如上所述具有任何一种所述拓扑或饱和或不饱和的部分的基团。类似地,在本发明的所有实施方案中,当提及基团以饱和或不饱和的一种形式(例如烷基)时,意指所述基团可以是任何类型的拓扑(例如直链、环状或支链)或具有几种带有各种拓扑结构的部分。
[0132]
应当理解,术语
“…
烃基,可能包含
…”
是指所述烃基可选地包含杂原子以形成醚、硫醚、胺、腈或羧酸基团。这些基团可以取代烃基的氢原子并因此侧接至所述烃,或取代烃基的碳原子(如果化学上可能的话)并因此插入到烃链或环中。
[0133]
根据一个实施方案,当存在基团(vi)时,它仅与基团(i)至(v)中的任一个组合存在。
[0134]
根据一个特定的实施方案,酰氯从由如下构成的群组中选出:丙烷
‑
1,2,3
‑
三酰三氯、环己烷
‑
1,2,4,5
‑
四酰四氯、2,2'
‑
二硫二基二琥珀酰二氯、2
‑
(2
‑
氯
‑2‑
氧代
‑
乙基)硫基丁二酰二氯、(4
‑
氯
‑4‑
氧代丁酰基)
‑
l
‑
谷氨酰二氯、(s)
‑4‑
((1,5
‑
二氯
‑
1,5
‑
二氧戊
‑2‑
基)氨基)
‑4‑
氧代丁酸、4
‑
氯
‑4‑
氧代丁酸2,2
‑
双[(4
‑
氯
‑4‑
氧代丁酰基)氧基甲基]丁基酯、4
‑
氯
‑4‑
氧代丁酸[2
‑
[2,2
‑
双[(4
‑
氯
‑4‑
氧代丁酰基)氧基甲基]丁氧基甲基]
‑2‑
[(4
‑
氯
‑4‑
氧代丁酰基)氧基甲基]丁基]酯、2
‑
氯羰基苯甲酸2,2
‑
双[(2
‑
氯羰基苯甲酰基)氧基甲基]丁基酯、2
‑
氯羰基苯甲酸[2
‑
[2,2
‑
双[(2
‑
氯羰基苯甲酰基)氧基甲基]丁氧基甲基]
‑2‑
[(2
‑
氯羰基苯甲酰基)氧基甲基]丁基]酯、2,4,5
‑
三氯羰基苯甲酸4
‑
(2,4,5
‑
三氯羰基苯甲酰基)氧基丁基酯,以及它们的混合物。
[0135]
步骤b):制备分散相,其中分散相与油相不混溶
[0136]
步骤b)中可以使用的溶剂的性质没有限制,只要它可以溶解稳定剂即可。
[0137]
根据一个特定的实施方案,分散相包含水,优选由水组成。
[0138]
根据另一个特定的实施方案,水的含量基于分散相的总重量以重量计低于或等于10%,优选低于或等于5%,更优选低于或等于3%。
[0139]
根据一个特定的实施方案,分散相不含水。
[0140]
根据一个实施方案,分散相包含从由甘油、1,4
‑
丁二醇、乙二醇以及它们的混合物构成的群组中选出的溶剂。
[0141]
步骤c):将油相加入到分散相中,以形成两相分散体
[0142]
根据本发明,在分散相和/或油相中加入稳定剂以稳定乳液。
[0143]
所述稳定剂可以是离子或非离子乳化剂或胶体稳定剂。
[0144]
稳定剂可以是分子乳化剂(标准乳液)或固体颗粒乳化剂(皮克林乳液)。
[0145]“稳定剂”和“乳化剂”在本发明中无差别地使用。
[0146]
根据一个实施方案,稳定剂是从由如下构成的群组中选出的:阿拉伯胶、改性淀粉、聚乙烯醇(pvoh)、聚乙烯吡咯烷酮(pvp)、羧甲基纤维素(cmc)、阴离子多糖、丙烯酰胺共聚物、无机颗粒、蛋白质如大豆蛋白、大米蛋白、乳清蛋白、卵清蛋白(white egg albumin)、酪蛋白酸钠、明胶、牛血清白蛋白、水解大豆蛋白、水解丝胶、假胶原、丝蛋白、丝胶蛋白粉以及它们的混合物。
[0147]
当稳定剂加入到油相中时,其优选从由如下构成的群组中选出:蛋白质如大豆蛋白、大米蛋白、乳清蛋白、卵清蛋白、酪蛋白酸钠、明胶、牛血清白蛋白、水解大豆蛋白、水解丝胶、假胶原、丝蛋白、丝胶蛋白粉以及它们的混合物。
[0148]
当加入到油相中时,稳定剂可以预先分散在惰性溶剂,例如苯甲酸苄酯中,或者可以混合到活性成分中,优选包含香料油。
[0149]
当稳定剂加入到水相中时,其优选从由如下构成的群组中选出:阿拉伯胶、改性淀粉、聚乙烯醇(pvoh)、聚乙烯吡咯烷酮(pvp)、羧甲基纤维素(cmc)、阴离子多糖、丙烯酰胺共聚物、无机颗粒、蛋白质如大豆蛋白、大米蛋白、乳清蛋白、卵清蛋白、酪蛋白酸钠、明胶、牛血清白蛋白、水解大豆蛋白、水解丝胶、假胶原、丝蛋白、丝胶蛋白粉以及它们的混合物。
[0150]
根据本发明的上述实施方案中的任一个,分散体包含约0.01%至3.0%的稳定剂,百分比以相对于在步骤c)之后获得的水包油乳液的总重量以w/w为基础表示。在本发明的另一形态中,分散体包含约0.05%至1.0%的胶体稳定剂。在本发明的另一形态中,分散体包含约0.1%至0.8%的稳定剂。
[0151]
步骤d):可选地,向步骤c)中获得的分散体中加入反应物
[0152]
在可用于本发明的反应物中,可以列举亲核体化合物。
[0153]
根据本发明,亲核体化合物被定义为一种化学物质,其向亲电子试剂提供电子对以形成与反应相关的化学键。
[0154]
亲核体化合物可从如下构成的群组中选出:氮亲核体、硫亲核体、氧亲核体、碳亲核体、磷亲核体以及它们的混合物。
[0155]
氮亲核体化合物可以具有从由如下构成的群组中选出的至少一个官能团:氨,叠氮化物,胺,亚硝酸盐,羟胺,肼,卡巴氮(carbazide),苯肼,氨基脲(semicarbazide),和酰胺,以及它们的混合物。
[0156]
硫亲核体化合物可以具有从由如下构成的群组中选出的至少一个官能团:硫化氢及其盐,硫醇(rsh),硫醇根阴离子(rs
‑
),硫醇羧酸根阴离子(rc(o)
‑
s
‑
),以及二硫代碳酸根(ro
‑
c(s)
‑
s
‑
)和二硫代氨基甲酸根(r2n
‑
c(s)
‑
s
‑
)的阴离子,以及它们的混合物。
[0157]
氧亲核体化合物可以具有从由如下构成的群组中选出的至少一个官能团:水,氢氧根阴离子,醇,醇盐阴离子,羧酸根阴离子,碳酸根,磺酸根,硫酸根,磷酸钠,硅酸钠,硼砂,四硼酸钠,以及它们的混合物。
[0158]
碳亲核体化合物可以具有从由烯醇、烯醇碳亲核体、丙二酸根和乙酰乙酸根构成的群组中选出的至少一个官能团。
[0159]
磷亲核体化合物可以具有从由膦、亚磷酸根阴离子以及它们的混合物构成的群组中选出的至少一个官能团。
[0160]
根据一个特定的实施方案,反应物是从由如下构成的群组中选出的:苯二甲胺、1,2
‑
二氨基环己烷、1,4
‑
二氨基环己烷、l
‑
赖氨酸、l
‑
赖氨酸乙酯、o,o'
‑
双(2
‑
氨基丙基)聚丙二醇
‑
嵌段
‑
聚乙二醇
‑
嵌段
‑
聚丙二醇、乙二胺、1,3
‑
二氨基
‑2‑
羟基丙烷、二亚乙基三胺、精胺、亚精胺、胱胺、胱氨酸、胱氨酸二烷基酯、氨基胍碳酸氢盐、n,n'
‑
二乙基乙二胺、聚酰胺胺(pamam)、壳聚糖、3
‑
氨基丙基三乙氧基硅烷、l
‑
精氨酸、1,3
‑
二氨基丙烷、n
‑
乙基硫酸胍、1,6
‑
二氨基己烷、胍盐、n,n,n',n'
‑
四(3
‑
氨基丙基)
‑
1,4
‑
丁二胺、胍唑、2
‑
氨基
‑
1,3
‑
丙二醇、乙醇胺三(2
‑
氨基乙基)胺、三(3
‑
氨基丙基)胺、三[2
‑
(甲基氨基)乙基]胺、1
‑
(2
‑
氨基乙
基)哌嗪、三亚乙基四胺、三乙醇胺、邻苯二甲酸二钾盐、琥珀酸二钠盐、二硫苏糖醇以及它们的混合物。
[0161]
根据本发明,在步骤a)中和/或在步骤b)中和/或在步骤c)中和/或在步骤d)中加入至少一种式(i)的可裂解多醇。当在步骤a)中加入时,除了多官能单体之外,多醇可以作为单独的组分或以至少一种可裂解多醇与多官能单体之间的反应产物的形式加入到油相中。
[0162]
根据一个实施方案,步骤a)为在疏水性材料中加入所述可裂解多醇与至少一种多官能单体之间的反应产物。
[0163]
根据另一个实施方案,步骤a)为在疏水性材料中加入至少一种可裂解多醇和至少一种多官能单体。
[0164]
可裂解多醇
[0165]
根据本发明,可裂解多醇具有下式(i)
[0166][0167]
其中每个r1独立地是h或ch2oh并且其中p和q是在1和3之间变化的整数,优选p和q是1或2,并且
[0168]
其中x是c2至c
30
烃基,可能包含一至十个选自o、s和n的杂原子以形成醚、酯、羧酸、醛、酮、醇、硫醇、二硫化物、硫醚、硫酯、氨基甲酸酯、酰胺、肟、亚胺、胺或腈官能团。
[0169]
根据本发明,由于氧化还原反应、水解、逆向1,4
‑
加成、光的作用和/或它们的组合,x可以通过一个或多个共价键的断裂而分裂成至少两个单独的部分。
[0170]
根据一个实施方案,x是选自二硫化物、恶唑烷、亚胺、1,4
‑
加成产物、碳酸酯和芳基酮衍生物的化合物。
[0171]
优选地,x是从由以下构成的群组中选出的:
[0172][0173]
其中l是o或s原子或nh基团,优选o原子,m是s原子或nr6基团,优选s原子,y是ch2、ch2‑
ch2或苯基,z是o(ch2)
x
o或(ch2)
x
基团,其中x是在1和4之间变化的整数,a是cooch2(cr2r2)
i
、chr2och2(cr2r2)
i
或(cr2r2)(chr2)
x
基团,
[0174]
每个r2独立地是h、ch3、ch2ch3、ch2oh或ch2ch2oh基团并且每个r3独立地是ch3或ch2ch3基团,
[0175]
r4为h或ch3,或者如果y不是苯基,则两个r4合在一起可以代表ch2或ch2‑
ch2基团,
[0176]
r5是h或ch3,
[0177]
r6是h、c1‑
c6烷基或ch2‑
ch2‑
(ch2)
j
‑
oh基团,如果t=1,两个r6合在一起可能形成ch2‑
ch2‑
(ch2)
i
基团,
[0178]
h是在1和6之间变化的整数,每个i彼此独立地为0或1,每个j彼此独立地为一个在0和2之间变化的整数,并且
[0179]
k和l是在0和2之间变化的整数,m和n是1或2,条件是k+l+m+n=4,
[0180]
t、u和u'为0或1,v和w为1或2,条件是u+v+w=3(如果t=0)或u+u'+v+w=4(如果t=1),和
[0181]
其中阴影线和粗线与氢原子连接或表示所述x与式(i)的多醇的(chr1oh)
p
(阴影线)或(chr1oh)
q
(粗线)基团之间的键,条件是x的至少一条阴影线和至少一条粗线连接到chr1oh基团。
[0182]
根据一个实施方案,可裂解多醇是从由二硫化物、恶唑烷、亚胺/席夫碱、1,4
‑
加成产物、碳酸根、芳基酮衍生物以及它们的混合物构成的群组中选出的化合物。
[0183]
多醇的非限制性例子是从由以下构成的群组中选出的化合物:
[0184]
‑
选自以下的二硫化物:2,2'
‑
二硫烷二基双(乙
‑1‑
醇)、2,2'
‑
二硫烷二基双(丙烷
‑
1,3
‑
二醇)、3
‑
(2,3
‑
二羟丙基二硫烷基)丙烷
‑
1,2
‑
二醇、2,2'
‑
(二硫烷二基双(亚甲基))双(2
‑
甲基丙烷
‑
1,3
‑
二醇)或2,2'
‑
(二硫烷二基双(亚甲基))双(2
‑
乙基丙烷
‑
1,3
‑
二醇)、3,3'
‑
二硫烷二基二丙酸双(3
‑
羟基
‑2‑
(羟甲基)
‑2‑
甲基丙基)酯、2,2'
‑
二硫烷二基二琥珀酸四(2
‑
羟乙基)酯,和/或
[0185]
‑
选自以下的恶唑烷:(3
‑
(2
‑
羟乙基)恶唑烷
‑
2,2
‑
二基)二甲醇、恶唑烷
‑
2,2,4
‑
三基三甲醇、2,2'
‑
(乙烷
‑
1,2
‑
二基双(2
‑
甲基恶唑烷
‑
2,3
‑
二基))双(乙
‑1‑
醇)、(乙烷
‑
1,2
‑
二基双(2
‑
甲基恶唑烷
‑
2,4,4
‑
三基))四甲醇、2,2'
‑
(1,4
‑
亚苯基双(恶唑烷
‑
2,3
‑
二基))双(乙
‑1‑
醇)、2,2'
‑
(呋喃
‑
2,5
‑
二基双(恶唑烷
‑
2,3
‑
二基))双(乙
‑1‑
醇)、2,2'
‑
(环己烷
‑
1,4
‑
二基双(恶唑烷
‑
2,3
‑
二基))双(乙
‑1‑
醇)、2,2'
‑
(1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
4,12
‑
二基)双(乙
‑1‑
醇)、(1,4
‑
亚苯基双(恶唑烷
‑
2,4,4
‑
三基))四甲醇、(1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
3,3,11,11
‑
四甲醇、(1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
3,11
‑
二基)二甲醇、(3,11
‑
二乙基
‑
1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
3,11
‑
二基)二甲醇、(1,4
‑
亚苯基双(4
‑
乙基恶唑烷
‑
2,4
‑
二基))二甲醇、(3,11
‑
二乙基
‑
1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
3,11
‑
二基)二甲醇、2,2'
‑
(3,11
‑
双(羟甲基)
‑
1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
4,12
‑
二基)双(乙
‑1‑
醇),和/或
[0186]
‑
选自以下的亚胺和席夫碱:2,2'
‑
((1,4
‑
亚苯基双(甲基亚基(methanylylidene)))双(氨基亚基(azanylylidene)))双(丙烷
‑
1,3
‑
二醇)、2,2'
‑
((呋喃
‑
2,5
‑
二基双(甲基亚基))双(氨基亚基))双(丙烷
‑
1,3
‑
二醇),和/或
[0187]
‑
选自以下的1,4
‑
加成产物:3
‑
((2
‑
羟乙基)硫代)丙酸2
‑
羟乙酯、3
‑
((3
‑
羟基
‑2‑
(羟甲基)
‑2‑
甲基丙基)硫代)
‑2‑
甲基丙酸3
‑
羟基
‑2‑
(羟甲基)
‑2‑
甲基丙酯、(s)
‑3‑
((2,3
‑
二羟丙基)硫代)丙酸3
‑
羟基
‑2‑
(羟甲基)
‑2‑
甲基丙酯、双(3
‑
((2
‑
羟乙基)硫代)丙酸)2
‑
乙基
‑2‑
(((3
‑
((2
‑
羟乙基)硫代)丙酰基)氧基)甲基)丙烷
‑
1,3
‑
二基酯、3
‑
((1,3
‑
二羟基丙
‑2‑
基)氨基)丙酸4
‑
羟基丁酯、3,3'
‑
(丁基氨叉基(azanediyl))二丙酸双(2
‑
羟乙基)酯、3,
3'
‑
((4
‑
羟丁基)氨叉基)二丙酸双(2
‑
羟乙基)酯、3,3'
‑
(哌嗪
‑
1,4
‑
二基)二丙酸双(2
‑
羟乙基)酯、3,3',3”,3”'
‑
(丙烷
‑
1,3
‑
二基双(氨爪基(azanetriyl)))四丙酸四(2
‑
羟乙基)酯,2
‑
((2
‑
羟乙基)硫代)琥珀酸双(3
‑
((2
‑
羟乙基)硫代)丙基)酯,和/或
[0188]
‑
选自以下的碳酸酯:碳酸双(2,3
‑
二羟丙基)酯、碳酸双(3
‑
羟基
‑2‑
(羟甲基)
‑2‑
甲基丙基)酯、三(3
‑
((2
‑
羟乙基)硫代)丙基)三碳酸苯
‑
1,3,5
‑
三基酯,和/或
[0189]
‑
选自以下的芳基酮衍生物:双(2
‑
羟乙基)2,2'
‑
(亚甲基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸酯)、双(2,2
‑
双(羟甲基)丁基)2,2'
‑
(亚甲基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸酯)、双(2
‑
羟乙基)2,2'
‑
(乙烷
‑
1,2
‑
二基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸酯)、双(3
‑
羟基
‑2‑
(羟甲基)
‑2‑
甲基丙基)2,2'
‑
(1,4
‑
亚苯基)双(2
‑
氧代乙酸酯)、1,1'
‑
(1,4
‑
亚苯基)双(5
‑
羟基戊
‑1‑
酮),以及它们的混合物。
[0190]
根据一个特定的实施方案,可裂解多醇不是三羟甲基丙烷。
[0191]
根据一个实施方案,单体以0.01%至50%,优选0.02%至20%,更优选0.1%至10%并且甚至更优选0.5%至5%的浓度存在于疏水性材料中。
[0192]
将本发明的可裂解多醇化合物加入到浆料中以获得0.01至10,更优选0.1至5,更优选0.2至1并且甚至更优选0.25至0.75的所述可裂解多醇化合物的oh基团与所述单体的官能团之间的摩尔比。
[0193]
用于制备给定聚合物的根据式(i)多醇的结构的选择将取决于聚合反应的条件。这意味着,并非任何多醇都一定是最适合各种聚合反应的单体。例如,如果聚合反应在强水解条件下,即在非常高或非常低的ph值下进行,那么容易水解的多醇可能不如在反应条件下不易裂解的其他多醇有利。在这种情况下,在光或氧化还原反应的影响下裂解的多醇可能是优选的。类似地,如果使用光引发的聚合反应,水解方式可裂解多醇可能比光敏结构更可取。
[0194]
步骤e):进行固化步骤以形成浆料形式的核
‑
壳微胶囊
[0195]
固化步骤e)允许以浆料形式的微胶囊结束。
[0196]
根据优选的实施方案,为了增强动力学,所述步骤在60至80℃的温度下,可能在压力下进行1至4小时。更优选地,在50至90℃下进行30分钟至4小时。然而,固化步骤可以在室温下进行。
[0197]
可选步骤:可选的外涂层
[0198]
根据本发明的一个特定的实施方案,在步骤e)结束时或在步骤e)期间,还可以向本发明的浆料中添加从由非离子多糖、阳离子聚合物以及它们的混合物构成的群组中选出的聚合物,以形成微囊的外涂层。
[0199]
非离子多糖聚合物是本领域技术人员众所周知的,并且描述于例如wo2012/007438第29页第1至25行和wo2013/026657第2页第12至19行和第4页第3至12行。优选的非离子多糖从由刺槐豆胶、木葡聚糖、瓜尔胶、羟丙基瓜尔胶、羟丙基纤维素以及羟丙基甲基纤维素构成的群组中选出。
[0200]
阳离子聚合物是本领域技术人员公知的。优选的阳离子聚合物的阳离子电荷密度为至少0.5meq/g,更优选至少约1.5meq/g,但也优选小于约7meq/g,更优选小于约6.2meq/g。阳离子聚合物的阳离子电荷密度可以通过凯氏定氮法(kjeldahl method)测定,如美国药典在用于氮测定的化学测试中所述。优选的阳离子聚合物选自那些含有伯、仲、叔和/或
季胺基团的单元,所述单元可以形成主聚合物链的一部分或可以由与其直接连接的侧取代基承载。阳离子聚合物的重均分子量(mw)优选为10,000至3.5m道尔顿,更优选为50,000至1.5m道尔顿。根据一个特定的实施方案,将使用基于丙烯酰胺、甲基丙烯酰胺、n
‑
乙烯基吡咯烷酮、季铵化的n,n
‑
二甲基氨基甲基丙烯酸酯、二烯丙基二甲基氯化铵、季铵化的乙烯基咪唑(3
‑
甲基
‑1‑
乙烯基
‑
1h
‑
咪唑
‑3‑
鎓氯化物)、乙烯基吡咯烷酮、丙烯酰胺丙基三甲基氯化铵、决明子羟丙基三甲基氯化铵、瓜尔胶羟丙基三甲基氯化铵或聚半乳甘露聚糖2
‑
羟丙基三甲基氯化铵醚、淀粉羟丙基三甲基氯化铵和纤维素羟丙基三甲基氯化铵的阳离子聚合物。优选地,共聚物应从由聚季铵盐
‑
5、聚季铵盐
‑
6、聚季铵盐
‑
7、聚季铵盐10、聚季铵盐
‑
11、聚季铵盐
‑
16、聚季铵盐
‑
22、聚季铵盐
‑
28、聚季铵盐
‑
43、聚季铵盐
‑
44、聚季铵盐
‑
46、决明子羟丙基三甲基氯化铵、瓜尔胶羟丙基三甲基氯化铵或聚半乳甘露聚糖2
‑
羟丙基三甲基氯化铵醚、淀粉羟丙基三甲基氯化铵和纤维素羟丙基三甲基氯化铵构成的群组中选出。作为市售产品的具体例子,可以列举sc60(丙烯酰胺丙基三甲基氯化铵和丙烯酰胺的阳离子共聚物,来源:basf)或例如pq 11n、fc 550或style(聚季铵盐
‑
11~68或乙烯基吡咯烷酮季铵化的共聚物,来源:basf),或(c13s或c17,来源:rhodia)。
[0201]
根据本发明的上述实施方案中的任何一个,添加了一定量的上述聚合物,其含量为约0%至5%w/w,或者甚至为约0.1%至2%w/w,百分数相对于在步骤d)之后获得的浆料的总重量以w/w基础来表示。本领域技术人员清楚地理解,仅所述添加的聚合物的一部分将被掺入到微胶囊壳中/沉积在微胶囊壳上。
[0202]
制备微胶囊粉末的方法
[0203]
本发明的另一个目的是制备微胶囊浆料的方法,其包括如上定义的步骤和另外的步骤,该另外的步骤包括将步骤e)或f)中获得的浆料进行干燥,例如喷雾干燥,以原样提供微胶囊,即粉末形式。应当理解,本领域技术人员已知的进行这种干燥的任何标准方法也是适用的。特别地,可以优选在聚合物载体材料例如聚乙酸乙烯酯,聚乙烯醇,糊精,天然或改性淀粉,植物胶,果胶,黄原胶,藻酸盐,角叉菜胶或纤维素衍生物的存在下将浆料喷雾干燥,以提供粉末形式的微胶囊。
[0204]
然而,也可以列举其他干燥方法,例如挤出、包覆、喷雾造粒、流化床,或甚至使用满足如wo2017/134179中公开的特定标准的材料(载体、干燥剂)在室温下干燥。
[0205]
根据一个特定的实施方案,载体材料包含游离的香料油,其可以与来自微胶囊核的香料相同或不同。
[0206]
根据一个特定的实施方案,载体材料包含游离的香料油,其可以与来自微胶囊核的香料相同或不同。
[0207]
本发明的另一个目的是一种固体颗粒,包含:
[0208]
‑
载体材料,优选为从由聚乙酸乙烯酯、聚乙烯醇、糊精、天然或改性淀粉、植物胶、果胶、黄原胶、藻酸盐、角叉菜胶、纤维素衍生物以及它们的混合物构成的群组中选出的聚合载体材料,和
[0209]
‑
包埋在所述载体材料中的如上定义的微胶囊,和
[0210]
‑
视情况使用的包埋在所述载体材料中的游离香料。
[0211]
在本发明中可以无差别地使用如上定义的固体颗粒和微胶囊粉末。
[0212]
多重微胶囊系统
[0213]
根据一个实施方案,本发明的微胶囊(第一种类型的微胶囊)可以与第二种类型的微胶囊组合使用。
[0214]
本发明的另一个目的是一种微胶囊递送系统,其包含:
[0215]
‑
本发明的微胶囊作为第一种类型的微胶囊,和
[0216]
‑
第二种类型的微胶囊,其中第一种类型的微胶囊和第二种类型的微胶囊在它们的疏水性材料和/或它们的壁材料和/或它们的涂层材料方面不同。
[0217]
微胶囊浆料
[0218]
本发明的另一个目的是可通过上述方法获得的微胶囊浆料。
[0219]
壳的组成能够提供在产品基料中显示出所需稳定性的微胶囊(例如,有效地抵消消费品的表面活性剂对香料的提取)。
[0220]
因此,本发明的另一个目的是核
‑
壳微胶囊,或具有至少一种核
‑
壳微胶囊的核
‑
壳微胶囊浆料,所述核
‑
壳微胶囊包含:
[0221]
‑
油基核,其包含疏水性材料,优选香料,和
[0222]
‑
壳,其包含多官能单体与可裂解多醇之间的反应产物,
[0223]
其中可裂解多醇具有下式(i)
[0224][0225]
其中每个r1独立地是h或ch2oh并且其中p和q是在1和3之间变化的整数,优选p和q是1或2,并且
[0226]
其中x是c2至c
30
烃基,可能包含一至十个选自o、s和n的杂原子以形成醚、酯、羧酸、醛、酮、醇、硫醇、二硫化物、硫醚、硫酯、氨基甲酸酯、酰胺、肟、亚胺、胺或腈官能团。
[0227]
先前描述的实施方案和定义(例如,疏水性材料、多官能单体、可裂解多醇)也适用于微胶囊。
[0228]
共聚物
[0229]
包含多官能单体与如上定义的至少一种可裂解多醇之间的反应产物的共聚物也是本发明的一个目的。
[0230]
先前描述的实施方案也适用于先前公开的微胶囊和共聚物。
[0231]
加香组合物和消费品
[0232]
本发明的微胶囊可以与活性成分组合使用。因此,本发明的一个目的是一种组合物,其包含:
[0233]
(i)如上定义的微胶囊;
[0234]
(ii)活性成分,优选选自化妆品成分、皮肤护理成分、香料成分、调味料成分、恶臭抵消成分、杀菌剂成分、杀真菌剂成分、药物或农业化学成分、消毒成分、驱虫剂或诱虫剂,以及它们的混合物。
[0235]
本发明的胶囊在挑战性介质中的稳定性方面表现出良好的性能。
[0236]
本发明的另一个目的是一种加香组合物,其包含:
[0237]
(i)如上定义的微胶囊或微胶囊浆料,其中该油包含香料;
[0238]
(ii)至少一种从由香料载体、香料助成分以及它们的混合物构成的群组中选出的成分;
[0239]
(iii)视情况使用的至少一种香料佐剂。
[0240]
作为液体香料载体,可以列举作为非限制性例子的乳化体系,即溶剂和表面活性剂体系,或通常用于香料中的溶剂。香料中通常使用的溶剂的性质和类型的详细描述是无法穷尽的。然而,可以列举作为非限制性例子的溶剂,例如一缩二丙二醇、邻苯二甲酸二乙酯、肉豆蔻酸异丙酯、苯甲酸苄酯、2
‑
(2
‑
乙氧基乙氧基)
‑1‑
乙醇或柠檬酸乙酯,它们是最常使用的。对于包含香料载体和香料助成分的组合物,除了先前明确的之外,其他合适的香料载体也可以是乙醇、水/乙醇混合物、柠檬烯或其他萜烯、异链烷烃,例如以商标(来源:exxon chemical)公知的那些,或二醇醚和二醇醚酯,例如以商标(来源:dow chemical company)公知的那些。通过“香料助成分”,在此是指这样一种化合物,其用于加香制剂或组合物中以赋予快感效果,并且不是如上定义的微胶囊。换句话说,要被认为是加香的助成分,其必须被本领域技术人员公认为能够以主动或愉快的方式赋予或改变组合物的气味,而不仅仅是具有气味。
[0241]
存在于加香组合物中的加香助成分的性质和类型在此不保证更详细的描述,其无论如何都是无法穷尽的,技术人员能够根据其常识并根据预期用途或应用以及所需的感官效果来选择它们。一般而言,这些加香助成分属于不同的化学分类,如醇类、内酯、醛类、酮类、酯类、醚类、乙酸酯类、腈类、萜类化合物、含氮或含硫杂环化合物和精油,并且所述加香助成分可以是天然来源的或合成来源的。无论如何,许多这些助成分都列于参考文献诸如s.arctander的著作perfume and flavor chemicals,1969,montclair,new jersey,usa或其更新的版本或类似性质的其他著作中,以及香料领域内丰富的专利文献中。还可理解的是,所述助成分还可以是已知的以受控方式释放各种类型加香化合物的化合物。
[0242]
通过“香料佐剂”,这里是指能够赋予额外的附加益处(如颜色、特定耐光性、化学稳定性等)的成分。通常用于加香基料中的佐剂的性质和类型的详细描述是无法穷尽的,但是必须提及所述成分是本领域技术人员众所周知的。
[0243]
优选地,根据本发明的加香组合物包含0.01至30重量%的如上定义的微胶囊。
[0244]
本发明的微胶囊可以有利地用于许多应用领域并用于消费品。微胶囊可以以适用于液体消费品的液体形式使用,也可以以适用于粉末消费品的粉末形式使用。
[0245]
根据一个特定的实施方案,如上定义的消费品是液体,并且包含:
[0246]
a)相对于消费品总重量为2至65重量%的至少一种表面活性剂;
[0247]
b)水或与水混溶的亲水性有机溶剂;和
[0248]
c)如上定义的微胶囊浆料或微胶囊,
[0249]
d)视情况使用的非包封的香料。
[0250]
根据一个特定的实施方案,如上定义的消费品为粉末形式,并且包含:
[0251]
a)相对于消费品总重量为2至65%重量的至少一种表面活性剂;
[0252]
b)如上定义的微胶囊粉末。
[0253]
c)视情况使用的香料粉末,其不同于如上定义的微胶囊。
[0254]
在包括香料油基核的微胶囊的情况下,本发明的产品尤其可用于已加香消费品,例如属于精细芳香剂或“功能性”香料的产品。功能性香料尤其包括个人护理产品,包括头发护理、身体清洁、皮肤护理、卫生护理以及家庭护理产品,包括衣物护理和空气护理。因此,本发明的另一个目的在于一种已加香消费品,其包含作为加香成分的如上定义的微胶囊或如上定义的加香组合物。所述消费品的香料成分可以是如上定义的香料微胶囊和游离或非包封的香料,以及除了这里公开的那些之外的其他类型的香料微胶囊的组合。
[0255]
特别地,如下的液体消费品是本发明的另一个目的,其包含:
[0256]
a)相对于消费品总重量为2至65重量%的至少一种表面活性剂;
[0257]
b)水或与水混溶的亲水性有机溶剂;和
[0258]
c)如上定义的加香组合物。
[0259]
同样,如下的粉末状消费品也是本发明的一部分,其包含:
[0260]
(a)相对于消费品总重量为2至65重量%的至少一种表面活性剂;和
[0261]
(b)如上定义的加香组合物。
[0262]
因此,本发明的微胶囊可以原样添加或作为本发明的加香组合物的一部分添加到已加香消费品中。
[0263]
为了清楚起见,必须提及的是,“已加香消费品”是指一种消费品,其预期将不同益处中的加香效果递送给施用了其的表面(例如皮肤、头发、纺织品、纸张或家庭表面)或空气中(空气清新剂、体香剂/除臭剂等)。换言之,根据本发明的已加香消费品是一种经加工的产品,其包含功能性配方(也称为“基料”)以及有益剂,其中有效量的根据本发明的微胶囊。
[0264]
已加香消费品的其他成分的性质和类型不保证在这里更详细的描述,其无论如何都是无法穷尽的,技术人员能够根据他的一般知识并根据所述产品的性质和期望效果来选择它们。在与这种产品有关的大量文献中可以找到其中可以掺入本发明微胶囊的消费品的基料配方。这些配方并不保证在这里的详细描述,其无论如何都是无法穷尽的。配制这样的消费品领域的技术人员完全能够根据他的一般知识和可用文献来选择合适的组分。
[0265]
合适的已加香消费品的非限制性例子可以是香水,例如精细香水,古龙水,须后水,涂抹式香水(body splash);织物护理产品,例如液体或固体洗涤剂,片剂和囊剂,织物柔软剂,干衣片(dryer sheet),织物清新剂,熨烫水,或漂白剂;个人护理产品,例如头发护理产品(例如洗发剂(香波)、头发调理剂(护发素)、着色制剂(染色剂)或头发喷雾剂(发胶)),化妆品制剂(例如雪花膏、身体乳液、或体香剂(除臭剂)或止汗剂),或皮肤护理产品(例如香皂、浴用摩丝、沐浴液(body wash)、浴油或沐浴露、浴盐、或卫生用品);空气护理产品,例如空气清新剂或“即用型”粉状空气清新剂;或家庭护理产品,例如通用清洁剂,液体或粉状或片状洗碗产品,马桶清洁剂或用于清洁各种表面的产品,例如用于处理/翻新纺织品或硬表面(地板、瓷砖、石制地板等)的喷剂和擦拭巾;卫生用品,例如卫生巾、尿布、卫生纸。
[0266]
本发明的另一个目的是一种消费品,其包含:
[0267]
‑
个人护理活性基料,以及
[0268]
‑
如上定义的微胶囊或微胶囊浆料或如上定义的加香组合物,
[0269]
其中消费品是个人护理组合物的形式。
[0270]
在与这种产品有关的大量文献中可以找到其中可以掺入本发明微胶囊的个人护
理活性基料。这些配方并不保证在这里的详细描述,其无论如何都是无法穷尽的。配制这样的消费品领域的技术人员完全能够根据他的一般知识和可用文献来选择合适的组分。
[0271]
个人护理组合物优选从由如下构成的群组中选出:头发护理产品(例如洗发剂,头发调理剂,着色制剂或头发喷雾剂),化妆品制剂(例如雪花膏、身体乳液、或体香剂或止汗剂),或皮肤护理产品(例如香皂、浴用摩丝、沐浴液、浴油或沐浴露、浴盐、或卫生用品)。
[0272]
本发明的另一个目的是一种消费品,其包含:
[0273]
‑
家庭护理或织物护理活性基料,以及
[0274]
‑
如上定义的微胶囊或微胶囊浆料或如上定义的加香组合物,
[0275]
其中消费品是家庭护理或织物护理组合物的形式。
[0276]
在与这种产品有关的大量文献中可以找到其中可以掺入本发明微胶囊的家庭护理或织物护理基料。这些配方并不保证在这里的详细描述,其无论如何都是无法穷尽的。配制这样的消费品领域的技术人员完全能够根据他的一般知识和可用文献来选择合适的组分。
[0277]
优选地,消费品包含0.1至15重量%,更优选0.2至5重量%的本发明微胶囊,这些百分比以相对于消费品的总重量的重量计。当然,可以根据每种产品所需的有益效果来调节上述浓度。
[0278]
织物柔软剂
[0279]
本发明的一个目的是织物柔软剂组合物形式的消费品,其包含:
[0280]
‑
织物柔软剂活性基料;优选从由如下构成的群组中选出:二烷基季铵盐,二烷基酯季铵盐(酯季铵盐(esterquat)),hamburg酯季铵盐(heq),teaq(三乙醇胺季铵盐),有机硅以及它们的混合物,基于组合物的总重量,优选含量为85至99.95重量%,
[0281]
‑
如上定义的微胶囊或微胶囊浆料,基于组合物的总重量,优选含量为0.05至15重量%,更优选0.1至5重量%。
[0282]
液体洗涤剂
[0283]
本发明的一个目的是液体洗涤剂组合物形式的消费品,其包含:
[0284]
‑
液体洗涤剂活性基料;优选从由如下构成的群组中选出:阴离子表面活性剂,例如烷基苯磺酸盐(abs),仲烷基磺酸盐(sas),伯醇硫酸盐(pas),月桂基醚硫酸盐(les),甲基酯磺酸盐(mes),和非离子表面活性剂,例如烷基胺,烷醇酰胺,脂肪醇聚(乙二醇)醚,脂肪醇乙氧基化物(fae),环氧乙烷(eo)和环氧丙烷(po)共聚物,氧化胺,烷基聚葡糖苷,烷基聚葡糖酰胺,基于组合物的总重量,优选含量为85至99.95重量%,
[0285]
‑
如上定义的微胶囊或微胶囊浆料,基于组合物的总重量,优选含量为0.05至15重量%,更优选0.1至5重量%。
[0286]
固体洗涤剂
[0287]
本发明的一个目的是固体洗涤剂组合物形式的消费品,其包含:
[0288]
‑
固体洗涤剂活性基料;优选从由如下构成的群组中选出:阴离子表面活性剂,例如烷基苯磺酸盐(abs),仲烷基磺酸盐(sas),伯醇硫酸盐(pas),月桂基醚硫酸盐(les),甲基酯磺酸盐(mes),和非离子表面活性剂,例如烷基胺,烷醇酰胺,脂肪醇聚(乙二醇)醚,脂肪醇乙氧基化物(fae),环氧乙烷(eo)和环氧丙烷(po)共聚物,氧化胺,烷基聚葡糖苷,烷基聚葡糖酰胺,基于组合物的总重量,优选含量为85至99.95重量%,
[0289]
‑
如上定义的微胶囊或微胶囊浆料,基于组合物的总重量,优选含量为0.05至15重量%,更优选0.1至5重量%。
[0290]
洗发剂/沐浴露
[0291]
本发明的一个目的是洗发剂或沐浴露组合物形式的消费品,其包含:
[0292]
‑
洗发剂或沐浴露活性基料;优选从由如下构成的群组中选出:烷基醚硫酸钠,烷基醚硫酸铵,烷基两性乙酸盐,椰油酰胺基丙基甜菜碱,椰油酰胺mea,烷基葡糖苷和基于氨基酸的表面活性剂,以及它们的混合物,基于组合物的总重量,优选含量为85至99.95重量%,
[0293]
‑
如上定义的微胶囊或微胶囊浆料,基于组合物的总重量,优选含量为0.05至15重量%,更优选0.1至5重量%。
[0294]
洗去型调理剂
[0295]
本发明的一个目的是洗去型调理剂组合物形式的消费品,其包含:
[0296]
‑
洗去型调理剂活性基料;优选从由如下构成的群组中选出:十六烷基三甲基氯化铵,硬脂基三甲基氯化铵,苯扎氯铵,山嵛基三甲基氯化铵以及它们的混合物,基于组合物的总重量,优选含量为85至99.95重量%,
[0297]
‑
如上定义的微胶囊或微胶囊浆料,基于组合物的总重量,优选含量为0.05至15重量%,更优选0.1至5重量%。
[0298]
染发剂
[0299]
本发明的一个目的是氧化性染发组合物形式的消费品,其包含:
[0300]
‑
包含氧化剂的氧化相和包含碱性试剂、染料前体和偶联化合物的碱相;其中所述染料前体和所述偶联化合物在氧化剂的存在下形成氧化性染发剂,基于组合物的总重量,优选含量为85至99.95重量%,
[0301]
‑
如上定义的微胶囊或微胶囊浆料,基于组合物的总重量,优选含量为0.05至15重量%,更优选0.1至5重量%。
[0302]
通过“氧化性染发组合物”,是指一种组合物,其包含两组无色染料分子:染料前体和偶联剂。通过氧化过程相互反应时,它们形成各种有色分子(染料),然后由于其大小而被捕获到头发中。换句话说,染料前体和偶联化合物在氧化剂的存在下形成氧化性染发剂。
[0303]
在本发明中无差别地使用“染料前体”和“氧化性染料前体”。
[0304]
染料前体可以是衍生自苯的芳族化合物,其在对位或邻位上取代有至少两个电子供体基团,例如nh2和oh,以赋予易氧化的特性。
[0305]
根据一个实施方案,染料前体从由如下构成的群组中选出:对苯二胺,2,5
‑
二氨基甲苯,n,n
‑
双(2
‑
羟甲基)对苯二胺,4
‑
氨基苯酚,1,4
‑
二氨基苯,以及它们的混合物。
[0306]
初级染料前体与偶联剂结合使用。偶联剂优选是衍生自苯并在间位上取代有诸如nh2和oh之类基团的芳族化合物,并且不会单独产生颜色,而是会改变由染料前体形成的颜色、浓淡或强度。
[0307]
根据一个实施方案,偶联剂从由如下构成的群组中选出:间苯二酚,2
‑
甲基间苯二酚,4
‑
氯间苯二酚,2,5
‑
二氨基甲苯,1,3
‑
二氨基苯,2,4
‑
二氨基苯氧基乙醇hcl,2
‑
氨基
‑
羟乙基氨基苯甲醚硫酸盐,4
‑
氨基
‑2‑
羟基甲苯,以及它们的混合物。
[0308]
基于组合物的总重量,氧化性染料前体的用量优选为0.001重量%至5重量%,优
选为0.1重量%至4重量%。
[0309]
氧化性染料前体和偶联剂在染发制剂中的用途已在现有技术中广泛公开,并且是本领域技术人员公知的。可以列举例如ep0946133a1,其内容通过引用并入于此。
[0310]
碱相包含碱性试剂,优选从由如下构成的群组中选出:氢氧化氨,碳酸氨,乙醇胺,氢氧化钾,硼酸钠,碳酸钠,三乙醇胺,以及它们的混合物。
[0311]
基于组合物的总重量,碱性试剂的优选用量为1重量%至10重量%,优选为3重量%至9重量%。
[0312]
根据本发明,偶联剂和染料前体在碱性介质中在氧化剂存在下形成氧化性染发剂。
[0313]
氧化剂将提供必要的氧气以形成颜色分子并改变头发的颜色。
[0314]
氧化剂应安全有效地用于本文的组合物中。
[0315]
优选地,当以液体形式和/或打算使用的形式使用时,适用于本文的氧化剂将可溶于根据本发明的组合物中。
[0316]
优选地,适用于本文的氧化剂将是水溶性的。用于本文的合适的氧化剂选自无机过氧氧化剂、预制的有机过氧酸氧化剂和有机过氧化物氧化剂或它们的混合物。
[0317]
基于组合物的总重量,氧化剂的用量优选为5至30重量%,优选为5至25重量%。
[0318]
可以将化妆品组合物中常用的组分加入到本发明所定义的染发组合物中。可以列举例如表面活性剂,阳离子聚合物,油性物质,有机硅衍生物,游离香料,防腐剂,紫外线吸收剂,抗氧化剂,杀菌剂,推进剂,增稠剂。
[0319]
根据一个特定的实施方案,染发组合物包含一种或多种季铵化合物,优选从由如下构成的群组中选出:十六烷基三甲基氯化铵,硬脂基三甲基氯化铵,苯扎氯铵,山嵛基三甲基氯化铵以及它们的混合物,以赋予头发调理剂有益效果。
[0320]
加香组合物
[0321]
根据一个特定的实施方案,消费品为加香组合物的形式,基于加香组合物的总重量,其包含:
[0322]
‑
0.1至30重量%,优选0.1至20重量%的先前定义的微胶囊或微胶囊浆料,
[0323]
‑
0至40重量%,优选3至40重量%的香料,以及
[0324]
‑
20至90重量%,优选40至90重量%的乙醇。
[0325]
现在将通过实施例进一步描述本发明。应当理解,所要求保护的本发明无意以任何方式被这些实施例所限制。
[0326]
实施例
[0327]
在下文中,通过以下实施例更详细地描述本发明,其中缩写具有本领域中的通常含义,温度以摄氏度(℃)表示。nmr光谱数据是在bruker amx 500光谱仪上在氘化二甲亚砜(dmso)
‑
d6中记录的,在500mhz下进行1h,在125.8mhz下进行
13
c,如果没有另外说明,化学位移δ相对于si(ch3)4作为标准以ppm表示,耦合常数j以hz表示(br.=宽峰)。反应在标准玻璃器皿中在n2下进行。除非另有说明,否则使用可商购的试剂和溶剂而无需进一步纯化。
[0328]
尽管对某些化合物指明了特定的构象或构型,但这并不意味着将这些化合物的使用限制为所描述的异构体。根据本发明,预期所有可能的构象或构型异构体都具有相似的效果。
[0329]
2,2'
‑
二硫烷二基双(乙
‑1‑
醇)(多醇1)是可商购的,根据式(i)的多醇的其他非限制性例子如实施例1中所述制备。
[0330]
实施例1
[0331]
根据式(i)的可裂解多醇的制备
[0332]
(a)2,2'
‑
二硫烷二基双(丙烷
‑
1,3
‑
二醇)(多醇2)的合成
[0333]
将amberlyst 15h(3.0g)加入到1,3
‑
二(叔丁基二甲基甲硅烷氧基)
‑
丙烷
‑2‑
硫醇(38.1g,0.11mol,如j.e.casida等人的bioorganic&medicinal chemistry,2010,18,1942
‑
1947中所述制备)和甲醇(300ml)的双相混合物中。在室温下搅拌过夜后,将悬浮液过滤,用甲醇(50ml)冲洗并将滤液浓缩以得到25.0g的双相混合物。加入丙酮(50ml)并加热至约50℃得到溶液,将其冷却至室温并置于冷冻箱中结晶。滤出固体,用冰冷的丙酮洗涤,真空(0.43mbar)干燥,得到3.4g白色晶体。浓缩母液,悬浮在丙酮(50ml)中并置于冰浴上2小时。过滤,用冰冷的丙酮(25ml)冲洗并真空干燥,得到另外4.0g白色晶体作为目标化合物(30%)。
[0334]1h
‑
nmr(cd3od):4.83(br.s,4h),3.78(dd,j=5.9,2.3,8h),2.93(五重峰,j=6.1,2h).
[0335]
13
c
‑
nmr(cd3od):62.39,57.89.
[0336]
(b)(
±
)
‑3‑
(2,3
‑
二羟丙基二硫烷基)丙烷
‑
1,2
‑
二醇(多醇3)的合成
[0337]
将硫酸亚铁水合物(feso4×
7h2o,85mg,0.3mmol)加入到3
‑
巯基丙烷
‑
1,2
‑
二醇(35ml,390.0mmol)在水(35ml)中的搅拌溶液中。然后用20分钟滴加过氧化氢(35%,29.15g,300.0mmol)。反应是放热的,温度用冰浴保持在大约40℃,期间加入h2o2。除去冰浴后,将反应搅拌5小时,然后倒入到含有乙酸乙酯(100ml)的分液漏斗中。萃取后,分离各相,水层用乙酸乙酯(100ml)再萃取,有机层用水(50ml)洗涤。浓缩水相,然后加入甲苯(250ml)并进一步浓缩混合物。在真空(0.14mbar)下干燥得到44.0g(定量)粗产物。
[0338]1h
‑
nmr:4.53(br.s,4h),3.69
–
3.62(m,2h),3.46
–
3.29(m,4h),2.95
–
2.87(m,2h),2.75
–
2.66(m,2h).
[0339]
13
c
‑
nmr:70.13,70.10,64.43,64.42,43.10,43.05.
[0340]
(c)2,2'
‑
(二硫烷二基双(亚甲基))双(2
‑
甲基丙烷
‑
1,3
‑
二醇)(多醇4)的合成
[0341]
在室温下将硫酸亚铁水合物(feso4×
7h2o,28mg,0.04mmol)加入到(2,2,5
‑
三甲基
‑
1,3
‑
二氧杂环己烷
‑5‑
基)甲硫醇(8.81g,50.0mmol)在水(50ml)中的搅拌乳液中。然后滴加过氧化氢(35%,3.7g,38.5mmol)(放热反应)。将混合物搅拌过夜,然后倒入到含有乙酸乙酯(100ml)的分液漏斗中。萃取后,分离各相,水层用乙酸乙酯(100ml)再萃取,有机层用水(50ml)和饱和nacl水溶液(50ml)洗涤,干燥(na2so4)并浓缩得到2.06g(30%)的目标化合物。
[0342]1h
‑
nmr(cd3od):4.85(s,4h),3.45(s,8h),2.92(s,4h),0.93(s,6h).
[0343]
13
c
‑
nmr(cd3od):67.10,46.84,42.75,18.86.
[0344]
(d)(3
‑
(2
‑
羟乙基)恶唑烷
‑
2,2
‑
二基)二甲醇(多醇5)的合成
[0345]
将1,3
‑
二羟基丙
‑2‑
酮(4.06g,50.0mmol)悬浮在四氢呋喃(thf,150ml)中。然后加入2,2'
‑
氨叉基(azanediyl)双(乙
‑1‑
醇)(6.31g,60.0mmol)和无水na2so4(10.0g)。在室温下搅拌约90小时后,将反应混合物过滤并浓缩。产物连续用环己烷(25ml)——其在50℃下
搅拌15分钟后倾析出来——和甲苯(50ml)——其在50℃下搅拌15分钟后倾析出来——进行处理。浓缩剩余产物并真空干燥,得到8.64g粗产物。
[0346]1h
‑
nmr(600mhz):4.48(br.s,1h),4.33(br.s,2h),3.80(t,j=6.2,2h),3.45(q,j=5.7,2h),3.34(s,4h),2.99(t,j=6.2,2h),2.79(t,j=6.2,2h).
[0347]
13
c
‑
nmr(151.0mhz):96.02,64.44,62.31,60.28,50.96,50.79.
[0348]
(e)(
±
)
‑
恶唑烷
‑
2,2,4
‑
三基三甲醇(多醇6)的合成
[0349]
将2
‑
氨基丙烷
‑
1,3
‑
二醇(2.78g,30.0mmol)悬浮在thf(75ml)中。然后加入na2so4(2.00g,14.1mmol,预先在150℃的烘箱中干燥)和1,3
‑
二羟基丙
‑2‑
酮(2.70g,30.0mmol)。在室温下搅拌大约5天后,将反应混合物浓缩并真空干燥,得到2.93g(52%)的目标化合物,含有约13重量%的thf。
[0350]1h
‑
nmr:4.71(t,j=5.6,1h),4.61(t,j=6.1,1h),4.44(t,j=6.3,1h),3.74(t,j=6.9,1h),3.49
–
3.18(m,8h),2.82
–
2.68(br.m,1h).
[0351]
13
c
‑
nmr:97.86,67.48,62.82,62.59,61.13,58.84.
[0352]
(f)(
±
)
‑
2,2'
‑
(乙烷
‑
1,2
‑
二基双(2
‑
甲基恶唑烷
‑
2,3
‑
二基))双(乙
‑1‑
醇)(多醇7)的合成
[0353]
将2,2'
‑
氨叉基双(乙
‑1‑
醇)(4.2g,39.9mmol)加入到2,5
‑
己二酮(1.17g,10.3mmol)在甲苯(50ml)中的溶液中。将反应混合物在dean
‑
stark装置中加热回流过夜。在冷水浴上冷却至室温后,获得双相混合物。倾析甲苯层并离心。浓缩和重复的球对球蒸馏(在室温和50℃下为0.011mbar)以除去剩余的甲苯,得到1.70g目标化合物,其为非对映异构体的混合物,以及一些单反应产物和剩余的2,2'
‑
氨叉基双(乙
‑1‑
醇)。
[0354]1h
‑
nmr:4.50
–
4.38(m,2h),3.80
–
3.73(m,2h),3.64(q,j=7.5,2h),3.50
–
3.40(m,4h),3.11
–
3.04(m,2h),2.69(q,j=7.9,2h),2.59
–
2.51(m,2h),2.39
–
2.31(m,2h),1.67
–
1.54(m,2h),1.47
–
1.35(m,2h),0.99(s,6h).
[0355]
13
c
‑
nmr:95.15,95.12,63.35,60.54,60.52,50.88,69.64,49.63,30.98,30.67,19.97,19.82.
[0356]
(g)(
±
)
‑
2,2'
‑
(1,4
‑
亚苯基双(恶唑烷
‑
2,3
‑
二基))双(乙
‑1‑
醇)(多醇8)的合成
[0357]
将对苯二甲醛(4.11g,30.0mmol)溶解在甲苯(75ml)中。然后加入2,2'
‑
氨叉基双(乙
‑1‑
醇)(7.01g,66.0mmol)和4
‑
甲基苯磺酸一水合物(0.29g,1.5mmol)。将混合物加热回流过夜,共沸除去水(dean
‑
stark)。冷却至室温后,获得双相体系。倾析出甲苯层,油状物用甲苯(25ml)洗涤。将油状物溶解在热的2
‑
丙醇(10ml)中,冷却至室温并保存在冷藏箱中。几天后,形成结晶,用冷的2
‑
丙醇洗涤,溶解在甲醇中,浓缩并真空干燥,得到白色固体。用2
‑
丙醇(15ml)重结晶,冷却至室温并保存在冷藏箱中,得到2.55g白色晶体。将反应后倾析出的甲苯浓缩得到油状物。将油状物溶解在热的2
‑
丙醇(5ml)中,冷却至室温并保存在冷藏箱中,得到另外1.07g白色晶体,其为非对映异构体的混合物。总共获得3.62g(39%)的目标化合物。
[0358]1h
‑
nmr:7.40(s,4h),4.85(2s,2h),4.51
–
4.44(m,2h),3.93
–
3.85(m,4h),3.51
–
3.39(m,4h),3.31
–
3.23(m,2h),2.71
–
2.63(m,2h),2.58
–
2.48(m,2h),2.41
–
2.32(m,2h).
[0359]
13
c
‑
nmr:140.29,127.25,127.22,96.20,64.65,64.62,60.02,53.97,53.94,51.80.
[0360]
(h)(
±
)
‑
2,2'
‑
(呋喃
‑
2,5
‑
二基双(恶唑烷
‑
2,3
‑
二基))双(乙
‑1‑
醇)(多醇9)的合成
[0361]
将5
‑
(羟甲基)呋喃
‑2‑
甲醛(5.04g,40.0mmol)溶解在dmso(80ml)中。加入nabr(1.24g,40.0mmol)并将混合物在150℃下加热18小时。冷却至室温后,将反应混合物吸收在乙酸乙酯(100ml)中并用水(100ml,3x)和饱和nacl溶液(100ml)洗涤。水相用乙酸乙酯(100ml)再萃取。干燥(na2so4)有机相并浓缩。柱层析法(sio2,庚烷/乙酸乙酯7:3)得到2.17g(44%)的呋喃
‑
2,5
‑
二甲醛(参见例如:c.laugel等人的chemcatchem,2014,6,1195
‑
1198)。
[0362]1h
‑
nmr:9.82(s,2h),7.68(s,2h).
[0363]
13
c
‑
nmr:180.68,153.65,122.04.
[0364]
将呋喃
‑
2,5
‑
二甲醛(0.75g,6.0mmol)溶解在甲苯(50ml)中。然后加入2,2'
‑
氨叉基双(乙
‑1‑
醇)(1.51g,14.4mmol)和一些甲苯。在室温下搅拌5分钟后,将混合物加热回流15小时,共沸除去水(dean
‑
stark),得到棕色固体和黄色溶液的混合物。倾析出液体,浓缩并真空干燥,得到1.38g目标化合物(77%),为非对映异构体的混合物,仍含有甲苯和一些剩余的2,2'
‑
氨叉基双(乙
‑1‑
醇)。
[0365]1h
‑
nmr:6.35(s,2h),5.06(2s,2h),4.54
–
4.48(m,2h),3.88
–
3.78(m,4h),3.51
–
3.41(m,4h),3.26
–
3.19(m,2h),2.80
–
2.73(m,2h),2.66
–
2.59(m,2h),2.52
‑
2.43(m,2h).
[0366]
13
c
‑
nmr:153.14,153.13,108.47,108.40,90.07,90.05,64.23,60.06,54.82,54.78,51.52.
[0367]
(i)(
±
)
‑
2,2'
‑
(环己烷
‑
1,4
‑
二基双(恶唑烷
‑
2,3
‑
二基))双(乙
‑1‑
醇)(多醇10)的合成
[0368]
将环己烷
‑
1,4
‑
二基二甲醇(熔融,13.24g,90.0mmol)溶解在乙酸乙酯(300ml)中。添加聚合物固定化的(2,2,6,6
‑
四甲基哌啶
‑1‑
基)氧基(tempo)(pipo af 944 974265,1.0g,4.9mmol)、kbr(0.1g,0.8mmol)和khco3(2.25g,22.5mmol)。然后用2小时滴加naocl水溶液(10%,165ml),同时将反应温度保持在28~30℃。将两相混合物搅拌2小时,然后分离各相。水层用乙酸乙酯(150ml)萃取,合并的有机相用饱和nacl水溶液(150ml)、饱和nahco3水溶液(2x)洗涤,再用饱和nacl水溶液(150ml)洗涤,干燥(na2so4)并浓缩,得到4.12g(33%)的环己烷
‑
1,4
‑
二甲醛,其为顺式/反式异构体(主要/次要约3:1)的混合物,并指定光谱数据如下。
[0369]1h
‑
nmr(cdcl3,主要):9.63(s,2h),2.42
–
2.32(m,2h),2.16
–
2.07(m,2h),1.87
–
1.69(4h),1.43
–
1.30(m,2h).
[0370]1h
‑
nmr(cdcl3,次要):9.65(s,2h),2.29
–
2.19(m,2h),1.87
–
1.69(m,8h).
[0371]
13
c
‑
nmr(cdcl3,主要):204.12,47.80,23.12.
[0372]
13
c
‑
nmr(cdcl3,次要):203.65,49.47,24.75.
[0373]
将环己烷
‑
1,4
‑
二甲醛(1.00g,7.2mmol)溶解在甲苯(25ml)中。然后加入2,2
’‑
氨叉基双(乙
‑1‑
醇)(1.82g,17.3mmol)。将混合物加热回流20小时,共沸除去水(dean
‑
stark)。冷却至室温后,获得双相混合物。倾析出甲苯,浓缩并真空干燥,得到油状物。将油状物吸收在乙醇中并保存在冷冻箱中。乙醇的浓缩最终得到晶体。吸取上清液并用冷乙醇洗涤残余物,得到0.88g(12%)的目标化合物,其为非对映异构体的混合物形式。
[0374]1h
‑
nmr:4.44(br.m,2h),3.84
–
3.79(m,2h),3.70
–
3.57(m,4h),3.51
–
3.41(m,4h),3.07和3.05(t,j=6.1,2h),2.66
–
2.54(m,4h),2.43
–
2.34(m,2h),1.85
–
1.74(m,2h),1.73
–
1.62(m,2h),1.30
–
1.16(m,2h),1.04
–
0.85(m,4h).
[0375]
13
c
‑
nmr:100.01,99.99,63.53,63.50,60.43,56.33,56.31,52.19,41.05,28.36,28.09,26.35,26.02.
[0376]
(j)(
±
)
‑
2,2'
‑
(1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
4,12
‑
二基)双(乙
‑1‑
醇)(多醇11)的合成
[0377]
将环己烷
‑
1,4
‑
二酮(2.86g,25.0mmol)溶解在甲苯(50ml)中。在室温下搅拌10分钟后,加入2,2
’‑
氨叉基双(乙
‑1‑
醇)(7.96g,75.0mmol)。将混合物在室温下搅拌5分钟,在回流下加热3小时,共沸除去水(dean
‑
stark)并在室温下搅拌过夜。观察到晶体的形成。倾析出甲苯,将残余物溶解在热乙醇(50ml)中。冷却至室温后,将产品放入到冷藏箱中,然后放入到冷冻箱中结晶。过滤并用冰冷的乙醇洗涤残余物,得到4.20g晶体。母液经浓缩后放入冷藏箱中重结晶。过滤后回收到另外1.56g晶体。总共获得5.76g(80%)的目标化合物。
[0378]1h
‑
nmr:4.40(t,j=5.6,2h),3.74(t,j=6.6,4h),3.45(q,j=6.2,4h),2.92(t,j=6.6,4h),2.49(t,j=6.6,4h),1.68
–
1.57(m,4h),1.42
–
1.32(m,4h).
[0379]
13
c
‑
nmr:93.69,62.77,60.58,50.99,49.81,28.27.
[0380]
(k)(
±
)
‑
(1,4
‑
亚苯基双(恶唑烷
‑
2,4,4
‑
三基))四甲醇(多醇12)的合成
[0381]
将2
‑
氨基
‑2‑
(羟甲基)丙烷
‑
1,3
‑
二醇(4.86g,40.0mmol)悬浮在乙醇(90ml)中。然后加入对苯二甲醛(2.74g,20.0mmol)并将混合物加热回流16小时。真空浓缩并干燥得到白色结晶固体。溶于热乙醇(30ml),冷却至室温并保存在冷藏箱中,得到白色结晶,将其过滤,用冷乙醇洗涤并真空干燥,得到4.19g(62%)的目标化合物,其为非对映异构体以及少量的(((1e,1'e)
‑
1,4
‑
亚苯基双(甲基亚基))双(氨基亚基))双(2
‑
(羟甲基)丙烷
‑
1,3
‑
二醇)(约10%)的混合物。
[0382]1h
‑
nmr:7.42(s,4h),5.35(d,j=9.5,2h),4.84(t,j=5.6,2h),4.71(t,j=5.5,2h),3.74
–
3.57(m,4h),3.50
–
3.37(m,8h),2.79
–
2.67(m,2h).
[0383]
13
c
‑
nmr:140.21,126.02,91.25,91.23,68.85,67.19,63.04,62.24.
[0384]
(l)(
±
)
‑
(1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
3,3,11,11
‑
四基)四甲醇(多醇13)的合成
[0385]
将环己烷
‑
1,4
‑
二酮(3.96g,34.6mmol)溶解在甲苯(90ml)中。然后加入2
‑
氨基
‑2‑
(羟甲基)丙烷
‑
1,3
‑
二醇(7.27g,59.9mmol)和4
‑
甲基苯磺酸一水合物(0.1g,0.5mmol)。将混合物加热回流16小时,共沸除去水(dean
‑
stark),得到白色悬浮液。将悬浮液在室温下搅拌1小时并过滤。固体用甲苯(20ml)洗涤并在干燥器中真空干燥,得到9.46g(99%)的目标化合物。
[0386]1h
‑
nmr:4.60(t,j=5.6,4h),3.57(s,4h),3.36
–
3.26(m,8h),2.41(br.s,2h),1.63
–
1.52(m,8h).
[0387]
13
c
‑
nmr:94.19,67.93,66.17,63.46,34.52.
[0388]
(m)(
±
)
‑
(1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
3,11
‑
二基)二甲醇(多醇14)的合成
[0389]
将环己烷
‑
1,4
‑
二酮(2.28g,19.9mmol)溶解在甲苯(50ml)中。然后加入2
‑
氨基丙
烷
‑
1,3
‑
二醇(5.58g,60.0mmol)。将混合物加热回流过夜,共沸除去水(dean
‑
stark)。观察到沉淀物的形成。冷却至室温后,倾析出溶剂,残余物用甲苯洗涤并溶解在热乙醇(30ml)中。冷却至室温并保存在冷藏箱中后,形成晶体。过滤并用冰冷的乙醇洗涤,得到3.87g(75%)的目标化合物。
[0390]1h
‑
nmr:4.68(t,j=5.5,2h),3.70(t,j=7.1,2h),3.50
–
3.25(m,8h),2.41(br.s,2h),1.69
–
1.45(m,8h).
[0391]
13
c
‑
nmr:94.93,66.36,61.34,58.59,33.97,32.58.
[0392]
(n)(
±
)
‑
(3,11
‑
二甲基
‑
1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
3,11
‑
二基)二甲醇(多醇15)的合成
[0393]
将环己烷
‑
1,4
‑
二酮(4.00g,35.0mmol)溶解在甲苯(90ml)中。然后加入2
‑
氨基
‑2‑
甲基丙烷
‑
1,3
‑
二醇(6.31g,60.0mmol)和4
‑
甲基苯磺酸一水合物(0.1g,0.5mmol)。将混合物加热回流16小时,共沸除去水(dean
‑
stark),得到棕色固体和浅黄色溶液的混合物。倾析出液体,冷却至室温以形成白色沉淀。悬浮液在室温下搅拌1小时并过滤。将固体用甲苯(20ml)和戊烷(20ml)洗涤并在干燥器中真空干燥,得到5.74g(67%)的目标化合物,其为非对映异构体的混合物,比例约为2:1。
[0394]1h
‑
nmr(400mhz):4.76
–
4.68(m,2h),3.69
–
3.63(m,2h),3.37
–
3.28(m,2h),3.28
–
3.09(m,4h),2.33(br.s,2h),1.71
–
1.45(m,8h),1.07(2s,6h).
[0395]
13
c
‑
nmr(100.6mhz,主要异构体):94.33,71.47,66.48,62.03,34.87,34.80,34.43,34.37,23.58,23.55or 23.53.
[0396]
13
c
‑
nmr(100.6mhz,次要异构体):94.67,71.43,66.48,62.22,35.07,35.00,34.65,34.57,23.58,23.55or 23.53.
[0397]
(o)(
±
)
‑
(1,4
‑
亚苯基双(4
‑
乙基恶唑烷
‑
2,4
‑
二基))二甲醇(多醇16)的合成
[0398]
在50℃下将对苯二甲醛(2.74g,20.0mmol)溶解在乙醇(90ml)中。然后加入2
‑
氨基
‑2‑
乙基丙烷
‑
1,3
‑
二醇(4.91g,40.0mmol)。将混合物在室温下搅拌数天。在真空下浓缩并干燥,得到粘稠的淡黄色油状物,该油状物缓慢结晶,由目标化合物和2,2'
‑
(((1e,1'e)
‑
1,4
‑
亚苯基双(甲基亚基))双(氨基亚基))
‑
双(2
‑
乙基丙烷
‑
1,3
‑
二醇)组成,比例约为4:1,为非对映异构体的混合物。
[0399]
(p)(
±
)
‑
(3,11
‑
二乙基
‑
1,9
‑
二氧杂
‑
4,12
‑
二氮杂二螺[4.2.48.25]十四烷
‑
3,11
‑
二基)二甲醇(多醇17)的合成
[0400]
将环己烷
‑
1,4
‑
二酮(3.96g,34.6mmol)溶解在甲苯(90ml)中。然后加入2
‑
氨基
‑2‑
乙基丙烷
‑
1,3
‑
二醇(7.34g,59.7mmol)和4
‑
甲基苯磺酸一水合物(0.1g,0.5mmol)。将混合物加热回流16小时,共沸除去水(dean
‑
stark),得到棕色固体和棕色溶液的混合物。倾析出液体,冷却至室温以形成米色沉淀。将悬浮液在室温下搅拌1小时并过滤。固体用甲苯(20ml)洗涤并在干燥器中真空干燥,得到2.58g白色晶体。将母液浓缩,重新溶解在乙醇(10ml)中并继续结晶,得到另外1.01g的晶体。总共获得3.59g(38%)的目标化合物。
[0401]1h
‑
nmr:4.65(t,j=5.5,2h),3.62(d,j=8.3,2h),3.38(d,j=8.3,2h),3.27
–
3.17(m,4h),2.19(s,2h),1.63
–
1.52(m,8h),1.51
–
1.36(m,4h),0.81(t,j=7.5,6h).
[0402]
13
c
‑
nmr:94.12,70.46,64.83,63.98,34.68,34.33,28.16,8.38.
[0403]
(q)2,2'
‑
(((1e,1'e)
‑
1,4
‑
亚苯基双(甲基亚基))双(氨基亚基))双(丙烷
‑
1,3
‑
二
醇)(多醇18)的合成
[0404]
将2
‑
氨基丙烷
‑
1,3
‑
二醇(3.72g,40.0mmol)溶解在乙醇(90ml)中。然后加入对苯二甲醛(2.74g,20.0mmol)和乙醇(60ml)。将混合物回流加热19小时,得到白色悬浮液。冷却至室温,过滤,用乙醇(15ml)洗涤,真空干燥,得到4.95g(88%)的目标化合物。
[0405]1h
‑
nmr:8.33(s,2h),7.81(s,4h),4.58(t,j=5.6,4h),3.64(五重峰,j=5.3,4h),3.47
–
3.40(m,4h),3.37
–
3.29(m,2h).
[0406]
13
c
‑
nmr:160.47,137.78,128.03,74.81,62.16.
[0407]
(r)2,2'
‑
(((1e,1'e)
‑
呋喃
‑
2,5
‑
二基双(甲基亚基))双(氨基亚基))双(丙烷
‑
1,3
‑
二醇)(多醇19)的合成
[0408]
将2
‑
氨基丙烷
‑
1,3
‑
二醇(3.72g,40.0mmol)溶解在乙醇(150ml)中。然后加入呋喃
‑
2,5
‑
二甲醛(2.48g,20.0mmol,如实施例1h中所述制备)。将混合物回流加热16小时,得到橙色溶液。冷却至室温后,产物结晶。用冰浴冷却,过滤并用冷乙醇(20ml)洗涤得到3.97g,浓缩滤液得到另外1.42g产物。总共获得5.39g(99%)的目标化合物。
[0409]1h
‑
nmr:8.13(s,2h),7.01(s,2h),4.60(t,j=5.8,4h),3.65
–
3.57(m,4h),3.45
–
3.37(m,4h),3.30
–
3.22(m,2h).
[0410]
13
c
‑
nmr:152.26,149.79,115.87,75.03,62.05.
[0411]
(s)3
‑
((2
‑
羟乙基)硫代)丙酸2
‑
羟乙酯(多醇20)的合成
[0412]
在氮气下的干燥装置中,将2
‑
巯基乙醇(9.3ml,132.0mmol)和1,8
‑
二氮杂双环[5.4.0]十一碳
‑7‑
烯(dbu,0.1ml,120.0mmol)加入到干燥的thf(150ml)中。用冰浴冷却至0~5℃后,用20分钟将丙烯酸2
‑
羟乙酯(13.93g,120.0mmol)滴加到搅拌溶液中。用thf(15ml)冲洗后,将反应混合物在冰浴上搅拌3小时,然后在室温下搅拌过夜。然后将反应混合物浓缩,倒入hcl水溶液(1%)中并用乙酸乙酯(100ml,2x)萃取。有机层用水(50ml,2x)和饱和nacl水溶液(50ml)洗涤。干燥(na2so4)合并的有机层并浓缩,得到6.11g粗产物。然后用乙酸乙酯萃取水层,用nacl饱和并用乙酸乙酯(100ml)再萃取。干燥(na2so4)并浓缩得到7.59g粗产物。第二部分产物的柱层析(sio2,乙酸乙酯/乙醇19:1)得到3.13g目标化合物。
[0413]1h
‑
nmr(cdcl3):4.28
–
4.24(m,2h),3.86
–
3.81(m,2h),3.76(t,j=6.0,2h),2.89(br.s,2h),2.85(t,j=7.1,2h),2.75(t,j=6.0,2h),2.69(t,j=6.9,2h).
[0414]
13
c
‑
nmr(cdcl3):172.27,66.31,60.87,60.78,35.23,34.83,26.92.
[0415]
(t)2
‑
乙基
‑2‑
(((3
‑
((2
‑
羟乙基)硫代)丙酰基)氧基)甲基)丙烷
‑
1,3
‑
二基双(3
‑
((2
‑
羟乙基)硫代)丙酸酯(多醇21)的合成
[0416]
在氮气下的干燥装置中,将2
‑
巯基乙醇(16.0ml,228.0mmol)和dbu(0.1ml,120.0mmol)加入到干燥的thf(150ml)中。用冰浴冷却至0~5℃后,用20分钟将二丙烯酸2
‑
((丙烯酰氧基)甲基)
‑2‑
乙基丙烷
‑
1,3
‑
二基酯(三羟甲基丙烷三丙烯酸酯,22.00g,74.2mmol)滴加到搅拌溶液中。用thf(15ml)冲洗后,将反应混合物在冰浴上搅拌3小时,然后在室温下搅拌过夜。然后将反应混合物浓缩,倒入hcl水溶液(1%)中并用乙酸乙酯(100ml,2x)萃取。有机层用水(50ml,2x)和饱和nacl水溶液(50ml)洗涤。干燥(na2so4)合并的有机层并浓缩,得到39.43g(定量)的目标化合物。
[0417]1h
‑
nmr(cdcl3):4.09(s,6h),3.76(t,j=5.9,6h),2.82(t,j=7.1,6h),2.74(t,j=5.9,6h),2.65(t,j=6.9,6h),1.51(q,j=7.6,2h),0.91(t,j=7.6,3h).
[0418]
13
c
‑
nmr(cdcl3):171.71,63.96,60.82,40.85,35.40,34.76,26.84,23.01,7.38.
[0419]
(u)3
‑
((1,3
‑
二羟基丙
‑2‑
基)氨基)丙酸4
‑
羟基丁酯(多醇22)的合成
[0420]
将2
‑
氨基丙烷
‑
1,3
‑
二醇(1.86g,20.0mmol)加入到丙烯酸4
‑
羟基丁酯(2.97g,20.0mmol)在乙腈(250ml)中的溶液中。将反应混合物在室温下搅拌数天。将反应混合物浓缩(0.4mbar,45℃)得到4.75g(定量)的目标化合物以及一些剩余的起始材料。
[0421]1h
‑
nmr:4.42(br.s,1h),4.35(br.s,2h),4.01(t,j=6.7,2h),3.40(t,j=6.3,2h),3.38
–
3.25(m,4h),2.79(t,j=6.7,2h),2.52
–
2.45(m,1h),2.40(t,j=6.8,2h),1.68
–
1.55(m,2h),1.50
–
1.40(m,2h).
[0422]
13
c
‑
nmr:172.12,63.63,61.06,60.79,60.17,42.74,34.99,28.76,24.88.
[0423]
(v)3,3'
‑
(丁基氨叉基)二丙酸双(2
‑
羟乙基)酯(多醇23)的合成
[0424]
用1小时将丁
‑1‑
胺(2.52g,34.5mmol)在乙腈(10g)中的溶液在0℃下滴加到丙烯酸2
‑
羟乙酯(8.00g,69.0mmol)在乙腈(28g)中的溶液中。在室温下搅拌过夜后,蒸发溶剂。柱层析法(sio2,乙酸乙酯)得到5.60g的目标化合物,以及一些部分水解的产物和乙烷
‑
1,2
‑
二醇。
[0425]1h
‑
nmr(cd3od):4.82(br.s,2h),4.16
–
4.11(m,4h),3.75
–
3.70(m,4h),2.79(t,j=7.1,4h),2.50(t,j=7.1,4h),2.49
–
2.40(m,2h),1.48
–
1.39(m,2h),1.35
–
1.26(m,2h),0.92(t,j=7.4,3h).
[0426]
13
c
‑
nmr(cd3od):174.30,66.95,61.01,54.58,50.22,33.10,30.15,21.59,14.38.
[0427]
(w)3,3'
‑
((4
‑
羟丁基)氨叉基)二丙酸双(2
‑
羟乙基)酯(多醇24)的合成
[0428]
在0℃下,用45分钟将4
‑
氨基
‑1‑
丁醇(3.06g,34.3mmol)在乙腈(10g)中的溶液滴加到丙烯酸2
‑
羟乙酯(8.02g,69.1mmol)在乙腈(27g)中的溶液中。在室温下搅拌过夜后,蒸发溶剂。柱层析法(sio2,乙酸乙酯/乙醇4:1)得到9.25g的目标化合物,以及一些部分水解的产物和乙烷
‑
1,2
‑
二醇。
[0429]1h
‑
nmr(cd3od):4.82(br.s,3h),4.17
–
4.11(m,4h),3.75
–
3.70(m,4h),3.57
–
3.51(m,2h),2.80(t,j=7.1,4h),2.52(t,j=6.9,4h),2.50
–
2.44(m,2h),1.57
–
1.49(m,4h).
[0430]
13
c
‑
nmr(cd3od):174.29,67.00,62.88,61.02,54.72,50.17,33.04,31.61,24.65.
[0431]
(x)3,3'
‑
(哌嗪
‑
1,4
‑
二基)二丙酸双(2
‑
羟乙基)酯(多醇25)的合成
[0432]
将丙烯酸2
‑
羟乙酯(8.30g,71.5mmol)、哌嗪(3.08g,35.8mmol)在乙腈(35.9g)中的溶液在室温下搅拌4小时。形成沉淀,过滤,用新鲜乙腈洗涤并真空干燥,得到9.15g的目标化合物,以及一些部分水解的产物和乙烷
‑
1,2
‑
二醇。
[0433]1h
‑
nmr(cd3od):4.83(br.s,2h),4.18
–
4.13(m,4h),3.74
–
3.69(m,4h),2.70(t,j=7.2,4h),2.60
–
2.45(br.m,8h),2.56(t,j=7.2,4h).
[0434]
13
c
‑
nmr(cd3od):173.89,67.00,61.01,54.50,53.56,32.70.
[0435]
(y)3,3',3”,3”'
‑
(丙烷
‑
1,3
‑
二基双(氨爪基))四丙酸四(2
‑
羟乙基)酯(多醇26)的合成
[0436]
在0℃下,用45分钟将1,3
‑
二氨基丙烷(1.44g,19.4mmol)在乙腈(9g)中的溶液滴加到丙烯酸2
‑
羟乙酯(9.02g,77.7mmol)在乙腈(30g)中的溶液中。在室温下搅拌过夜后,蒸发溶剂。柱层析法(sio2,乙酸乙酯/乙醇4:1)得到11.40g的目标化合物,以及一些部分水解的产物和乙烷
‑
1,2
‑
二醇。
[0437]1h
‑
nmr(cd3od):4.82(br.s,4h),4.17
–
4.12(m,8h),3.75
–
3.70(m,8h),2.78(t,j=7.0,8h),2.51(t,j=6.9,8h),2.50
–
2.42(m,4h),1.66
–
1.55(m,2h).
[0438]
13
c
‑
nmr(cd3od):174.35,66.98,61.03,52.75,50.25,33.16,25.33.
[0439]
(z)3,3'
‑
二硫烷二基二丙酸双(3
‑
羟基
‑2‑
(羟甲基)
‑2‑
甲基丙基)酯(多醇27)的合成
[0440]
将3
‑
(2
‑
羧乙基二硫烷基)丙酸(10.73g,50.0mmol)、1,1,1
‑
三(羟甲基)乙烷(18.39g,150.0mmol)和甲苯
‑4‑
磺酸一水合物(0.30g,1.7mmol)在甲苯(125ml)中的溶液在dean
‑
stark装置中回流加热24小时。冷却至室温后,得到非均相混合物。倾析出甲苯层并将剩余的固体吸收在乙酸乙酯(100ml)中并在0℃下搅拌30分钟。滤出固体并用冷乙酸乙酯(25ml)洗涤,浓缩滤液,得到18.75g粗化合物。柱层析法(sio2,乙酸乙酯/乙醇95:5)并在高真空(0.06mbar,温和加热)下干燥,得到11.41g(55%)的目标化合物。
[0441]1h
‑
nmr:4.48
–
4.42(m,4h),3.90(s,4h),3.26(t,j=4.8,4h),2.92(t,j=6.9,4h),2.75
–
2.68(m,4h),1.99(s,2h),1.18(t,j=7.1,2h),0.79(s,6h).
[0442]
13
c
‑
nmr:171.06,66.29,63.35,40.49,33.42,32.66,16.37.
[0443]
(aa)2,2'
‑
二硫烷二基二琥珀酸(
±
)
‑
四(2
‑
羟乙基)(多醇28)的合成
[0444]
将硫酸亚铁水合物(feso4×
7h2o,80mg,0.3mmol)加入到2
‑
巯基琥珀酸(29.6g,197.1mmol)在水(250ml)中的搅拌溶液中。然后用5~10分钟滴加过氧化氢(35%,14.59g,150.1mmol),同时用冰浴将温度保持在35℃以下。在室温下搅拌过夜后,用乙酸乙酯(250ml,3x)萃取反应混合物。水层用乙酸乙酯(250ml)再萃取,合并的有机层用饱和的nacl水溶液(100ml,2x)洗涤,干燥(na2so4)并浓缩(45℃,5mbar)至得到23.40g固体。将固体(22.38g)在干燥器(0.06mbar)中研磨并干燥,得到22.10g(79%)的2,2'
‑
二硫烷二基二琥珀酸,其为非对映异构体的混合物。
[0445]1h
‑
nmr:12.69(br.s,4h),3.81
–
3.73(m,2h),2.85and 2.82(dd,j=9.6,3.5,2h),2.71(dd,j=17.0,4.8,2h).
[0446]
13
c
‑
nmr:171.45,171.38,171.27,47.94,47.35,35.83,35.59.
[0447]
将2,2'
‑
二硫烷二基二琥珀酸(1.00g,3.4mmol)和甲苯
‑4‑
磺酸一水合物(0.05g,0.3mmol)在乙烷
‑
1,2
‑
二醇(25ml)中的混合物在120℃下加热在dean
‑
stark仪器中过夜。球对球蒸馏(0.067mbar,130℃)以除去过量的乙烷
‑
1,2
‑
二醇,得到1.78g粗产物,将其溶解在乙酸乙酯(20ml)中,并用饱和nahco3水溶液(5ml)洗涤。水相用乙酸乙酯(25ml)再萃取,合并的有机层干燥(na2so4),浓缩并在0.087mbar真空下干燥,得到1.04g的目标化合物,其为非对映异构体的混合物。
[0448]1h
‑
nmr:4.85
–
4.76(m,4h),4.14
–
3.91(3m,10h),3.62
–
3.52(2m,8h),3.05
–
2.95(m,2h),2.90
–
2.82(m,2h).
[0449]
13
c
‑
nmr:169.96,169.88,169.84,66.83,66.80,66.21,66.20,58.70,58.63,47.19,46.96,35.38,35.29.
[0450]
(ab)2,2'
‑
(亚甲基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸)双(2
‑
羟乙基)酯(多醇29)的合成
[0451]
在氮气下,在2~3℃下用40分钟将2
‑
氯
‑2‑
氧代乙酸乙酯(41.80g,306.2mmol)在ch2cl2(75ml)中的溶液滴加到alcl3(40.80g,306.0mmol)在ch2cl2(250ml)中的悬浮液中。在
2~3℃下搅拌30分钟后,用45分钟滴加二苯基甲烷(16.80g,99.9mmol)在ch2cl2(75ml)中的溶液。将混合物在2~3℃下继续搅拌3小时,然后温热至室温过夜。将反应混合物倒在冰(200g)上,倾析,有机层用水(200ml,3x)洗涤。水相用ch2cl2(50ml)再萃取,合并的有机层干燥(na2so4)并浓缩,得到35.52g粗化合物。27.77g的柱层析(sio2,正庚烷/乙酸乙酯4:1)产生10.05g(35%)的2,2'
‑
(亚甲基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸)二乙酯。
[0452]1h
‑
nmr(cdcl3):7.98
–
7.94(m,4h),7.34
–
7.30(m,4h),4.44(q,j=7.2,4h),4.14(s,2h),1.41(t,j=7.2,6h).
[0453]
13
c
‑
nmr(cdcl3):185.83,163.75,147.25,131.02,130.56,129.52,62.36,42.09,14.11.
[0454]
将碳酸钾(0.50g)加入到2,2'
‑
(亚甲基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸)二乙酯(10.19g,27.7mmol)和乙烷
‑
1,2
‑
二醇(75.00g)的混合物中。将反应混合物在80℃下搅拌1小时,然后冷却至室温并搅拌过夜。用乙酸乙酯(150ml)和水(250ml)稀释后,倾析有机层并用乙酸乙酯(100ml,2x)萃取水相。合并的有机层用饱和nacl水溶液(100ml,3x)洗涤,干燥(na2so4)并浓缩。球对球蒸馏(70℃,0.057mbar)以去除剩余的挥发性化合物,得到8.00g(72%)的目标化合物。
[0455]1h
‑
nmr(cdcl3):7.98
–
7.92(m,4h),7.30
–
7.25(m,4h),4.51
–
4.44(m,4h),4.08(s,2h),3.95
–
3.89(m,4h),3.05(br.s,2h).
[0456]
13
c
‑
nmr(cdcl3):185.55,163.43,147.46,130.78,130.72,129.54,67.50,60.40,42.05.
[0457]
(ac)2,2'
‑
(亚甲基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸)双(2,2
‑
双(羟甲基)丁基)酯(多醇30)的合成
[0458]
将碳酸钾(0.05g)加入到2,2'
‑
(亚甲基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸)二乙酯(1.00g,2.7mmol,如实施例1ab中所述制备)和2
‑
乙基
‑2‑
(羟甲基)丙烷
‑
1,3
‑
二醇(5.00g)的混合物中。将反应混合物在80℃下搅拌20小时,冷却至室温后,用甲基叔丁基醚(mtbe)和水稀释。倾析水相并用mtbe(50ml)再萃取。有机层用水(25ml,3x)和饱和nacl水溶液(25ml)洗涤。干燥(na2so4)合并的有机层并浓缩,得到1.11g(74%)的目标化合物。
[0459]1h
‑
nmr:7.96
–
7.91(m,4h),7.56
–
7.50(m,4h),4.57(t,j=5.1,4h),4.25(s,4h),4.23(s,2h),3.33
–
3.26(m,8h),1.31(q,j=7.5,4h),0.83(t,j=7.5,6h).
[0460]
13
c
‑
nmr:186.84,164.37,148.80,130.65,130.59,130.28,66.74,61.05,43.24,41.39,22.05,7.77.
[0461]
(ad)2,2'
‑
(乙烷
‑
1,2
‑
二基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸)双(2
‑
羟乙基)酯(多醇31)的合成
[0462]
在氮气下,在2~3℃下用50分钟将2
‑
氯
‑2‑
氧代乙酸乙酯(41.80g,306.2mmol)在ch2cl2(75ml)中的溶液滴加到alcl3(40.80g,306.0mmol)在ch2cl2(250ml)中的悬浮液中。在2~3℃下搅拌30分钟后,用45分钟滴加1,2
‑
二苯基乙烷(18.60g,100.0mmol)在ch2cl2(75ml)中的溶液。将混合物在2~3℃下继续搅拌1小时,并在室温下搅拌4小时。将反应混合物缓慢倒在冰(200g)上,用ch2cl2(100ml)稀释,倾析有机层,用水(150ml,3x)洗涤。水相用ch2cl2(50ml)再萃取,合并的有机层干燥(na2so4)并浓缩,得到39.22g浅黄绿色固体状粗化合物。用丙酮在
‑
20℃下(2x)和室温下用正庚烷/乙醚(2:1)重复重结晶,得到总共22.69g
(59%)的2,2'
‑
(乙烷
‑
1,2
‑
二基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸)二乙酯。
[0463]1h
‑
nmr(cdcl3):7.95
–
7.90(m,4h),7.31
–
7.25(m,4h),4.45(q,j=7.1,4h),3.04(s,4h),1.42(t,j=7.2,6h).
[0464]
13
c
‑
nmr(cdcl3):185.98,163.90,148.70,130.72,130.35,129.08,62.33,37.27,14.12.
[0465]
将碳酸钾(0.25g)加入到2,2'
‑
(乙烷
‑
1,2
‑
二基双(4,1
‑
亚苯基))双(2
‑
氧代乙酸)二乙酯(23.01g,60.2mmol)在乙烷
‑
1,2
‑
二醇(144g)中的悬浮液中。将反应混合物在80℃下搅拌20小时。然后加入更多的碳酸钾(0.75g),并将反应在80℃下继续搅拌8小时。冷却至室温过夜后,得到固体产物。加热反应混合物,然后用乙酸乙酯(150ml)和水(250ml)稀释。倾析有机层,水层用乙酸乙酯(100ml,2x)萃取。合并的有机层用饱和nacl水溶液洗涤,干燥(na2so4)并浓缩,得到22.33g粗产物。在冰箱中用丙酮(50ml)重结晶得到3.25g(13%)的目标化合物。
[0466]1h
‑
nmr(cdcl3):7.97
–
7.91(m,4h),7.29
–
7.23(m,4h),4.53
–
4.46(m,4h),3.98
–
3.92(m,4h),3.02(s,4h),2.58(br.s,2h).
[0467]
13
c
‑
nmr(cdcl3):185.62,163.66,148.85,130.57,130.49,129.14,67.45,60.54,37.25.
[0468]
(ae)三(3
‑
((2
‑
羟乙基)硫代)丙基)三碳酸苯
‑
1,3,5
‑
三基酯(多醇32)的合成
[0469]
将苯
‑
1,3,5
‑
三醇(7g,55.6mmol)和三乙胺(24ml,172mmol)溶解在250ml圆底烧瓶中的thf(100ml)中。用冰冷却反应混合物的温度并加入烯丙基碳氯化物(18ml,169mmol)。形成白色沉淀并将反应混合物在0℃下搅拌3小时。过滤白色固体,减压浓缩反应混合物。获得无色油状物并溶解在乙酸乙酯(100ml)中。有机溶液用k2co3(5%,
×
3 100ml)溶液洗涤。有机层用无水na2so4干燥,过滤并浓缩,得到三碳酸三烯丙基苯
‑
1,3,5
‑
三基酯。
[0470]1h
‑
nmr(cdcl3):7.05(s,3h),5.98(qt,3h),5.43(dq,3h),5.34(dq,3h),4.73(dt,6h).
[0471]
13
c
‑
nmr(cdcl3):152.52,151.46,130.81,119.89,112.02,69.49.
[0472]
将该油状物(6.0g,15.8mmol)和2,2
‑
二甲氧基
‑
1,2
‑
二苯基乙酮(0.1g,0.39mmol)溶解在250ml圆底烧瓶中的thf(30ml)中,得到无色溶液。然后加入2
‑
巯基乙醇(3.96g,50.7mmol)并将反应混合物在uv
‑
a光下以2mw/cm2照射5小时。在减压下浓缩反应混合物,在乙酸乙酯(40ml)中稀释,用k2co3(5%在水中,25ml x2)的溶液洗涤。有机层用无水na2so4干燥,过滤并浓缩以提供三(3
‑
((2
‑
羟乙基)硫代)丙基)三碳酸苯
‑
1,3,5
‑
三基酯。
[0473]1h
‑
nmr(cdcl3):7.05(s,3h),4.37(t,6h),3.75(q,6h),2.74(t,6h),2.66(t,6h),2.48(t,3h),2.03(五重峰,6h).
[0474]
13
c
‑
nmr(cdcl3):152.63,151.42,112.04,67.55,60.54,35.15,28.54,27.88.
[0475]
(af)2
‑
((2
‑
羟乙基)硫代)琥珀酸双(3
‑
((2
‑
羟乙基)硫代)丙基)酯(多醇33)的合成
[0476]
在100ml圆底烧瓶中,将马来酸二烯丙酯(3ml,16.39mmol)和三乙胺(0.25ml,1.794mmol)溶解在thf(50ml)中,得到无色溶液。加入2
‑
巯基乙醇(1.4ml,19.98mmol)并将反应混合物在0℃下搅拌。加入2,3,4,6,7,8,9,10
‑
八氢嘧啶并[1,2
‑
a]氮杂环庚三烯(0.1ml,16.39mmol)并将反应混合物在室温下搅拌5小时,最后在减压下浓缩得到2
‑
((2
‑
羟
乙基)硫代)琥珀酸二烯丙酯。
[0477]1h
‑
nmr(cdcl3):5.92(m,2h),5.35(m,2h),5.26(m,2h),4.64(m,4h),3.80(m,3h),2.90(m,6h)
[0478]
13
c
‑
nmr(cdcl3):171.51,170.43,131.61,118.89,118.71,66.16,65.77,60.99,41.16,36.36,35.14.
[0479]
在100ml圆底烧瓶中,将2
‑
((2
‑
羟乙基)硫代)琥珀酸二烯丙酯(3.5g,12.7mmol)和2
‑
巯基乙醇(1.9ml,27.1mmol)溶解在thf(50ml)中,得到无色溶液。加入2,2
‑
二甲氧基
‑
1,2
‑
二苯基乙酮(0.1g,0.39mmol)并将反应混合物在uv
‑
a光下以2mw/cm2照射3小时。减压浓缩反应混合物并加入乙酸乙酯(50ml)。有机溶液用k2co3(5%在水中,25ml)的溶液和水(25ml)洗涤。有机层用无水na2so4干燥,过滤并浓缩以提供2
‑
((2
‑
羟乙基)硫代)琥珀酸双(3
‑
((2
‑
羟乙基)硫代)丙基)酯。
[0480]1h
‑
nmr(cdcl3):4.28(t,2h),4.22(t,2h),3.80(m,2h),3.74(m,4h),2.99(m,2h),2.93(m,2h),2.83(m,2h),2.73(m,6h),2.65(t,2h),2.61(t,2h),1.97(m,2h),1.94(m,2h).
[0481]
13
c
‑
nmr(cdcl3):171.86,170.77,64.00,63.63,61.64,60.67,60.60,41.35,36.46,35.10,35.07,34.88,28.68,28.64,28.09,28.05.
[0482]
(ag)碳酸双(3
‑
羟基
‑2‑
(羟甲基)
‑2‑
甲基丙基)酯(多醇34)的合成
[0483]
将1,1,1
‑
三(羟甲基)乙烷(24.5g,200.0mmol)悬浮在thf(250ml)中。然后加入2,2
‑
二甲氧基丙烷(32ml,0.84g ml
‑1,258.1mmol)和对甲苯磺酸(50mg)。搅拌1小时后,加入k2co3(1.0g)并将混合物搅拌1小时,然后过滤并减压浓缩(45℃,4mbar)。加入primol
tm
(5.06g)作为压载物后,分馏(0.2mbar,70℃)得到总共31.0g(97%)的(2,2,5
‑
三甲基
‑
1,3
‑
二氧杂环己烷
‑5‑
基)甲醇,其为无色油状物。
[0484]1h
‑
nmr(cdcl3):3.69(s,2h),3.64(dd,j=35.2,12.0,4h),2.22(br.s,1h),1.44(s,3h),1.40(s,3h),0.83(s,3h).
[0485]
13
c
‑
nmr(cdcl3):97.98,66.34,65.91,34.75,27.30,20.14,17.58.
[0486]
将(2,2,5
‑
三甲基
‑
1,3
‑
二氧杂环己烷
‑5‑
基)甲醇(3.88g,24.2mmol)、碳酸二乙酯(1.20g,10.0mmol)和甲醇钠(11mg)的混合物加热至90℃持续5小时,然后在125℃下过夜。冷却至室温后,产物结晶。在庚烷(10ml,加热时)中重结晶,过滤,用庚烷洗涤并真空干燥,得到1.02g(29%)的碳酸双((2,2,5
‑
三甲基
‑
1,3
‑
二氧杂环己烷
‑5‑
基)甲基)酯,其为白色晶体。
[0487]1h
‑
nmr(cdcl3):4.23(s,4h),3.65(dd,j=30.3,11.9,8h),1.44(s,6h),1.40(s,6h),0.87(s,6h).
[0488]
13
c
‑
nmr(cdcl3):155.45,98.09,70.36,66.09,33.68,27.29,20.02,17.60.
[0489]
将碳酸双((2,2,5
‑
三甲基
‑
1,3
‑
二氧杂环己烷
‑5‑
基)甲基)酯(1.00g,2.9mmol)和khso4(33mg)在甲醇(9ml)和水(1ml)中的混合物在室温下搅拌3小时。然后加入nahco3(250mg)并蒸发溶剂。将反应混合物吸收在乙酸乙酯(20ml)中并用饱和nacl水溶液(10ml)洗涤。干燥(na2so4)有机层,过滤并浓缩。产物在丙酮中重结晶。放入冷冻箱后,过滤晶体并用最少量的冰冷丙酮洗涤,得到0.06g(8%)的目标化合物。
[0490]1h
‑
nmr(cd3cocd3):4.11(s,4h),3.76(t,j=5.4,4h),3.49(t,j=5.3,8h),0.89(s,6h).
[0491]
13
c
‑
nmr(cd3cocd3):156.51,70.50,65.72,41.73,16.78.
[0492]
实施例2
[0493]
含有式(i)的可裂解多醇的聚氨酯核
‑
壳微胶囊的制备及其在揉搓时在棉上释放香味的性能
[0494]
(a)香料1的制备
[0495]
制备香料1,其为2,2
‑
二甲基
‑6‑
亚甲基环己烷甲酸甲酯(来源:firmenich sa)、乙酸2
‑
叔丁基
‑1‑
环己酯(来源:international flavors and fragrances)、4
‑
叔丁基
‑1‑
环己基乙酸酯、3
‑
(4
‑
异丙基苯基)
‑2‑
甲基丙醛和(2z)
‑2‑
苯基
‑2‑
己烯腈(来源:firmenich sa)的等量混合物。
[0496]
(b)多醇与异氰酸酯在油水界面的共聚
[0497]
为了验证可裂解多醇与异氰酸酯在香料存在下共聚形成聚氨酯,在水相顶部的油相之间的界面处以二维方法形成膜。
[0498]
将多醇(1当量的
‑
oh基团)与精确量的柠檬酸钠(约0.4当量)一起溶解在聚乙烯醇(pvoh)在水(5g)中的1重量%溶液中。将市售的多异氰酸酯d
‑
110n(来源:mitsui chemicals,0.33g,0.86mmol;0.7当量的
‑
nco基团)单独溶解在香料1(4.7g)中,并轻轻移取到30ml小瓶中。将小瓶不搅动放置在水浴中,在25℃下保持30分钟,用1小时分四步加热至70℃(40;50;60;70℃),在70℃下保持2小时,最后冷却至室温。
[0499]
用镊子小心地从聚合瓶中取出在中间相处形成的膜。将水相小心地转移到圆底烧瓶中并在干冰上冷冻。通过冷冻干燥(christ alpha 1
‑
4,fischer science)除去所有水,所得粉末在d2o中通过nmr光谱表征。多醇的
13
c光谱中所有三重峰的平均信号与柠檬酸盐之比(47~49ppm的三重峰)用于计算留在水相中(即未与异氰酸酯反应)的单体分数。
[0500]
可裂解多醇的以下部分与异氰酸酯反应并因此结合到聚合物膜中:
[0501] 已反应多醇的分数[%]多醇2314多醇246多醇2515多醇2637
[0502]
因此,通过与多异氰酸酯的界面反应,不同的多醇成功地结合到二维膜中。
[0503]
(c)微胶囊1~3的制备
[0504]
将如实施例1中所述制备的柠檬酸钠(约0.91g)和一种根据式(i)的多醇(1当量的
‑
oh基团)溶解在pvoh在水(35g)中的1重量%溶液中。将d
‑
110n——苯二甲基二异氰酸酯的三羟甲基丙烷加合物,来源:日本mitsui chemicals,inc.,多异氰酸酯在乙酸乙酯中的75%溶液(3.12g,8.2mmol;0.7当量的
‑
nco基团)溶解在香料1(21g)中。用(ika 25;3分钟最高速度)将油相乳化在含有多醇的1重量%的pvoh溶液(35g)中。将乳液转移到装有机械搅拌器(rw20,ika labortechnik)和水浴的反应器中。在25℃下1小时后,用1小时分四步将混合物加热至70℃(40;50;60;70℃)。加入水(10g)并将混合物在70℃下保持2小时,然后冷却至室温以得到微胶囊1~3的分散体。胶囊的显微图像拍摄于取出水浴后约1小时(见图1)。
[0505]
制备了以下核
‑
壳微胶囊:
[0506]
ꢀꢀ
多醇的量[g]乳液的ph微胶囊1多醇231.755.53微胶囊2多醇241.244.89微胶囊3多醇261.585.15
[0507]
如图1所示,形成了核
‑
壳微胶囊。
[0508]
(d)在揉搓和不揉搓的棉上的芳香剂释放性能
[0509]
为了证明微胶囊的释放特性,测定了在揉搓和不揉搓的情况下沉积在棉巾上的微胶囊的2,2
‑
二甲基
‑6‑
亚甲基环己烷甲酸甲酯的顶空浓度。2,2
‑
二甲基
‑6‑
亚甲基环己烷甲酸甲酯的释放被认为是香料1中其他香料分子的代表。
[0510]
将约0.15g微胶囊1~3的分散体稀释在约15g软化水中。对于每个样品,预先洗涤三或四张棉片,切成12x12cm2,并用直径为10cm的圆圈标记。将稀释的微胶囊分散体(1ml)移液到一张棉片上填充所标记的圆形区域。将布片晾干1小时,然后将它们储存在铝箔中。第二天,将每张棉片放在覆盖有铝箔的1l烧杯中平衡5分钟。然后通过大气压化学电离质谱法用2分钟测量2,2
‑
二甲基
‑6‑
亚甲基环己烷甲酸甲酯的量(参见例如:o.viry等人的food res.int.,2018,109,p.52
‑
58)。然后将棉片手动揉搓10次,使其在烧杯中再平衡5分钟,并用2分钟再次测量。将1分钟内记录的不同芳香剂质子化摩尔质量离子的平均强度(139、172、183和191g/mol)减去背景,再除以稀释分散体中微胶囊的浓度,得到相对顶空强度。
[0511]
以下量的2,2
‑
二甲基
‑6‑
亚甲基环己烷甲酸甲酯从微胶囊中释放出来:
[0512] 揉搓前归一化顶空强度[a.u.]揉搓后归一化顶空强度[a.u.]微胶囊1185(
±
34)1316(
±
149)微胶囊2225(
±
62)1276(
±
166)微胶囊3188(
±
42)1305(
±
134)
[0513]
因此,含有根据式(i)的可裂解多醇的微胶囊1~3适用于在棉上包封和递送芳香剂。
[0514]
实施例3
[0515]
含有式(i)的可裂解多醇的聚酰胺微胶囊的制备
[0516]
表1:香料2的组成:
[0517]
原料%2
‑
甲基
‑
戊酸乙酯3.20桉叶油醇7.802,4
‑
二甲基
‑3‑
环己烯
‑1‑
甲醛
1)
0.75癸醛0.75香茅腈4.30乙酸异冰片酯3.00乙酸2
‑
叔丁基
‑1‑
环己酯
2)
9.80乙酸香茅酯1.302
‑
甲基十一醛3.00
二苯醚0.80十二醛1.30乙酸二环戊二烯酯9.85β
‑
紫罗兰酮3.30γ
‑
十一内酯18.75水杨酸己酯15.90水杨酸苄酯16.20总计100
[0518]
1)来源:瑞士日内瓦firmenich sa
[0519]
2)来源和商标:美国iff
[0520]
用多醇1(双(2
‑
羟乙基)二硫化物)制备微胶囊4
[0521]
在圆底烧瓶中,将均苯三甲酰氯(tmcl,0.18g)溶解在苯甲酸苄酯(0.5g)中。将双(2
‑
羟乙基)二硫化物(0.16g)溶解在苯甲酸苄酯(5g)中,并将该溶液加入到第一溶液中并在60℃下搅拌10分钟(溶液a)。将酪蛋白酸钠(1g)分散在香料2(25g)中。制备tmcl(1.56g)在苯甲酸苄酯(2g)中的第二溶液并将其加入到香料分散体中。最后将溶液a加入到该分散体中以提供油相。后者用ultra turrax t25(s 25n
‑
10g)以24,000rpm分散在l
‑
赖氨酸(2.55g)在水(95g)中的溶液中持续5分钟。用5分钟滴加乙二胺(eda,0.22g)在水(5g)中的溶液。将反应混合物在定轨振荡器(ika ks 3000)中在30℃下以250rpm搅拌4小时,得到白色分散体。
[0522]
微胶囊5是使用0.16g多醇1根据微胶囊4的方案制备的。
[0523]
用多醇2(2,2'
‑
二硫烷二基双(丙烷
‑
1,3
‑
二醇))制备微胶囊6
[0524]
微胶囊6:在圆底烧瓶中,在60℃下将牛血清白蛋白(bsa,0.95g)分散在苯甲酸苄酯(5.00g)中。将tmcl(0.88g)在苯甲酸苄酯(2.50g)中的溶液加入到bsa分散体中。在另一个圆底烧瓶中,将多醇2(0.38g)在丙酮(5.00g)中的溶液加入到tmcl(0.88g)在苯甲酸苄酯(2.50g)中的溶液中,并将反应混合物搅拌几分钟。在室温下将溶液和分散体加入到香料2(25.14g)中以提供油相。后者用ultra turrax t25(s 25n
‑
10g)以24,000rpm分散在l
‑
赖氨酸(2.50g)在水(94.05g)中的溶液中持续1分钟。用5分钟滴加eda(0.48g)在水(5.00g)中的溶液。将反应混合物在定轨振荡器(ika ks 3000)中在30℃下以250rpm搅拌4小时,得到白色分散体。
[0525]
微胶囊7是根据微胶囊6的方案制备的,其中eda溶液被胱胺二盐酸盐(1.8g)在碳酸胍水溶液(30重量%,5.00g)中的溶液代替。
[0526]
用多醇3(3
‑
(2,3
‑
二羟基丙基二硫烷基)丙烷
‑
1,2
‑
二醇)制备微胶囊8~11
[0527]
微胶囊8:在圆底烧瓶中,将tmcl(0.89g)溶解在苯甲酸苄酯(2.59g)中。将多醇3(0.55g)溶解在苯甲酸苄酯(2.51g)中,并将该溶液加入到第一溶液中,并在60℃下搅拌1小时(溶液a)。将酪蛋白酸钠(1.94g)分散在香料2(24.92g)中。制备tmcl(1.76g)在苯甲酸苄酯(2.49g)中的第二溶液并将其加入到香料分散体中,然后将溶液a加入到该分散体中以提供油相。后者用ultra turrax t25(s 25n
‑
10g)以24,000rpm分散在l
‑
赖氨酸(2.57g)在水(94.39g)中的溶液中持续5分钟。用5分钟滴加eda(0.24g)在水(5.30g)中的溶液。将反应混合物在定轨振荡器(ika ks 3000)中在30℃下以250rpm搅拌4小时,得到白色分散体。
[0528]
微胶囊9:在圆底烧瓶中,将tmcl(2.63g)溶解在苯甲酸苄酯(2.53g)中。将多醇3(0.22g)溶解在丙酮(2.64g)中,并将该溶液加入到第一溶液中,并在60℃下搅拌1小时(溶液a)。将酪蛋白酸钠(1.03g)分散在苯甲酸苄酯(5.03g,溶液b)中。将溶液a和b加入到香料2(25.6g)中以提供油相。后者用ultra turrax t25(s 25n
‑
10g)以24,000rpm分散在l
‑
赖氨酸(2.56g)在水(94.27g)中的溶液中持续5分钟。用5分钟滴加eda(0.73g)在水(5.15g)中的溶液。将反应混合物在定轨振荡器(ika ks 3000)中在30℃下以250rpm搅拌4小时,得到白色分散体。
[0529]
微胶囊10是使用0.31g多醇3根据微胶囊8的方案制备的。
[0530]
微胶囊11:在圆底烧瓶中,将tmcl(2.68g)溶解在苯甲酸苄酯(2.62g)中。将多醇3(0.34g)溶解在丙酮(2.66g)中,并将该溶液加入到第一溶液中,并在60℃下搅拌1小时(溶液a)。将酪蛋白酸钠(0.98g)在60℃下分散在苯甲酸苄酯(5.09g,溶液b)中持续30分钟。将溶液a和b加入到香料2(24.6g)中以提供油相。后者用ultra turrax t25(s25n
‑
10g)以24,000rpm分散在l
‑
赖氨酸(2.49g)和eda(0.75g)在水(95.65g)中的溶液中持续5分钟。将反应混合物在定轨振荡器(ika ks3000)中在30℃下以250rpm搅拌4小时,得到白色分散体。
[0531]
用多醇8(2,2'
‑
(1,4
‑
亚苯基双(恶唑烷
‑
2,3
‑
二基))双(乙
‑1‑
醇))制备微胶囊12~14
[0532]
微胶囊12:在圆底烧瓶中,在60℃下将tmcl(0.88g)在苯甲酸苄酯(2.50g)中的溶液加入到牛血清白蛋白(bsa,0.95g)在苯甲酸苄酯(5.00g)中的分散体中持续10分钟。在另一个圆底烧瓶中,将多醇8(1.54g)在丙酮(5.00g)中的溶液加入到tmcl(0.88g)在苯甲酸苄酯(2.50g)中的溶液中,并将反应混合物搅拌几分钟。在室温下将溶液和分散体加入到香料2(25.14g)中以提供油相。后者用ultra turrax t25(s 25n
‑
10g)以24,000rpm分散在l
‑
赖氨酸(2.50g)在水(94.05g)中的溶液中持续1分钟。用5分钟滴加eda(0.48g)在水(5.00g)中的溶液。将反应混合物在定轨振荡器(ika ks 3000)中在30℃下以250rpm搅拌4小时,得到白色分散体。
[0533]
微胶囊13是根据微胶囊12的方案制备的,其中eda溶液被胱胺二盐酸盐(1.8g)在碳酸胍水溶液(30重量%,5.00g)中的溶液代替。
[0534]
微胶囊14是根据微胶囊12的方案制备的,其中eda溶液被二亚乙基三胺(0.83g)在水(5.00g)中的溶液代替。
[0535]
用水中的多醇1(双(2
‑
羟乙基)二硫化物)和油中的多醇3(3
‑
(2,3
‑
二羟丙基二硫烷基)丙烷
‑
1,2
‑
二醇)制备微胶囊15
[0536]
在圆底烧瓶中,将tmcl(2.65g)溶解在苯甲酸苄酯(5.00g)中。将多醇3(1.14g)溶解在丙酮(2.60g)中。将该溶液加入到第一溶液中并在60℃下搅拌1小时。将该溶液加入到香料2(25g)中以提供油相。后者用ultra turrax t25(s 25n
‑
10g)以24,000rpm分散在阿拉伯胶(senegal,1重量%,95.22g)的水溶液中持续5分钟。用5分钟滴加多醇1(0.78g)在水(5.00g)中的溶液。通过加入碳酸氢钠水溶液(5重量%,70.77g)将乳液的ph值控制在4.0。将反应混合物在90℃下搅拌4小时,得到白色分散体。
[0537]
用多醇4(2,2'
‑
(二硫烷二基双(亚甲基))双(2
‑
甲基丙烷
‑
1,3
‑
二醇)制备微胶囊16~18
[0538]
在烧杯中,将酪蛋白酸钠(2g)分散在香料2(25g)中。将分散体在60℃下搅拌1小
时。在圆底烧瓶中,将tmcl(1.74g)溶解在苯甲酸苄酯(5.14g)中。在40℃下将多醇4(0.68g)溶解在丙酮(2.49g)中。将该溶液加入到第一溶液中并在室温下搅拌1小时。将该溶液加入到香料2分散体(25g)中以提供油相。后者用ultra turrax t25(s 25n
‑
10g)以24,000rpm分散在l
‑
赖氨酸(2.56g)在水(95g)中的溶液中持续5分钟。用5分钟滴加乙二胺(0.12g)在水(5.00g)中的溶液。将反应混合物在30℃下搅拌4小时,得到白色分散体。
[0539]
微胶囊17是使用0.44g多醇4和0.17g乙二胺根据微胶囊16的方案制备的。
[0540]
微胶囊18是使用0.28g多醇4和0.20g乙二胺根据微胶囊16的方案制备的。
[0541]
实施例4
[0542]
由式(i)的可裂解多醇进行的可裂解多异氰酸酯的制备及其核
‑
壳微胶囊的制备
[0543]
可裂解多异氰酸酯1~5的制备
[0544]
三(3
‑
(异氰酸根合甲基)苄基氨基甲酸)(((((苯
‑
1,3,5
‑
三基三(氧基))三(羰基))三(氧基))三(丙烷
‑
3,1
‑
二基))三(硫烷二基))三(乙烷
‑
2,1
‑
二基)酯(多异氰酸酯1)的制备
[0545]
在氮气下将1,3
‑
双(异氰酸根合甲基)苯(1.55ml,9.90mmol)和2
‑
乙基己酸锡(ii)(0.09g,0.011mmol)引入到50ml圆底三颈烧瓶中,得到无色溶液。用5分钟滴加乙酸乙酯(4.4ml)中的三(3
‑
((2
‑
羟乙基)硫代)丙基)三碳酸苯
‑
1,3,5
‑
三基酯(多醇32,2.04g,3.33mmol)。将反应混合物在50℃下搅拌3小时,然后将介质在搅拌下缓慢冷却至室温然后使用。
[0546]1h
‑
nmr(cdcl3):7.39
–
7.33,7.28
–
7.27,7.22,7.16,7.00,4.53,4.47,4.33,4.25,2.75,2.68,2.04,2.01.
[0547]
13
c
‑
nmr(cdcl3):156.36,152.64,154.39,137.62,129.41,129.19,127.03,126.29,125.84,125.75,125.05,112.05,67.57,64.10,46.30,44.83,30.98,28.40.
[0548]
双(3
‑
((2
‑
(((3
‑
(异氰酸根合甲基)苄基)氨基甲酰基)氧基)
‑
乙基)硫代)丙酸)2
‑
乙基
‑2‑
(1
‑
(3
‑
(异氰酸根合甲基)苯基)
‑
3,10
‑
二氧代
‑
4,11
‑
二氧杂
‑7‑
硫杂
‑2‑
氮杂十二碳
‑
12
‑
基)丙烷
‑
1,3
‑
二基酯(多异氰酸酯2)的制备
[0549]
将1,3
‑
双(异氰酸根合甲基)苯(1.4ml,8.9mmol)和2
‑
乙基己酸锡(ii)的乙酸乙酯溶液(0.09g,0.34mmol)引入到50ml圆底三颈烧瓶中,得到无色溶液。滴加双(3
‑
((2
‑
羟乙基)硫代)丙酸)2
‑
乙基
‑2‑
(((3
‑
((2
‑
羟乙基)硫代)丙酰基)氧基)
‑
甲基)丙烷
‑
1,3
‑
二基酯(多醇21,1.54g,2.89mmol)在乙酸乙酯(3.1ml)中的溶液。将反应混合物在50℃下搅拌3小时,然后在搅拌下缓慢冷却至室温。
[0550]1h
‑
nmr(cdcl3):8.74,7.75,7.71,7.42,7.41,7.36,7.34,7.32,7.24,7.21,7.12,6.64,4.62,4.58,4.25,4.21,4.19,4.15,4.08,4.00,3.32,2.73,2.62,2.50,1.42,0.82.
[0551]
13
c
‑
nmr(cdcl3):170.20,158.10,156.13,141.45,140.79,140.24,139.65,137.75,137.22,137.17,128.98,128.54,128.11,126.28,126.11,125.67,125.40,125.35,125.25,125.04,122.76,63.33,63.00,59.16,45.74,45.69,45.57,43.66,43.54,42.89,42.76,40.40,34.22,29.98,26.34,22.31,13.98,7.14.
[0552]
双(3
‑
(((2
‑
((((5
‑
异氰酸根合
‑
1,3,3
‑
三甲基环己基)
‑
甲基)氨基甲酰基)氧基)乙基)硫代)丙酸)2
‑
乙基
‑2‑
(1
‑
(5
‑
异氰酸根合
‑
1,3,3
‑
三甲基环己基)
‑
3,10
‑
二氧代
‑
4,11
‑
二氧杂
‑7‑
硫杂
‑2‑
氮杂十二碳
‑
12
‑
基)丙烷
‑
1,3
‑
二基酯(多异氰酸酯3)的制备
[0553]
将5
‑
异氰酸根合
‑1‑
(异氰酸根合甲基)
‑
1,3,3
‑
三甲基环己烷(3.1ml,14.63mmol)和2
‑
乙基己酸锡(ii)(0.09g,0.011mmol)引入到50ml圆底三颈烧瓶中得到无色溶液。将反应混合物在50℃下搅拌5分钟。用5分钟滴加乙酸乙酯(6.3ml)中的双(3
‑
((2
‑
羟乙基)硫代)丙酸)2
‑
乙基
‑2‑
(((3
‑
((2
‑
羟乙基)硫代)丙酰基)氧基)
‑
甲基)丙烷
‑
1,3
‑
二基酯(多醇21,2.53g,4.77mmol)。将反应混合物在50℃下搅拌3小时,反应产物无需进一步纯化即可使用。
[0554]1h
‑
nmr(cdcl3):5.18,4.90,4.21,4.07,3.81,3.65,3.06,3.03,2.94,2.83,2.77,2.65,1.91,1.84,1.81,1.74,1.51,1.25,0.80.
[0555]
13
c
‑
nmr(cdcl3):156.72,155.50,122.84,121.88,63.89,63.73,57.02,56.84,54.61,50.83,48.72,48.60,48.20,48.07,46.61,46.55,46.31,46.09,44.69,43.85,43.65,43.39,40.80,36.57,36.53,35.10,34.97,34.86,34.79,34.69,31.92,31.88,31.45,27.67,27.62,27.57,27.55,27.30,23.41,23.36,23.28,22.97,7.40.
[0556]
三(((5
‑
异氰酸根合
‑
1,3,3
‑
三甲基环己基)
‑
甲基)氨基甲酸)(((((苯
‑
1,3,5
‑
三基三(氧基))三(羰基))三(氧基))三(丙烷
‑
3,1
‑
二基))三(硫烷二基))三(乙烷
‑
2,1
‑
二基)酯(多异氰酸酯4)的制备
[0557]
在氮气下将5
‑
异氰酸根合
‑1‑
(异氰酸根合甲基)
‑
1,3,3
‑
三甲基环己烷(2.15ml,10.15mmol)和2
‑
乙基己酸锡(ii)(0.09g,0.011mmol)加入到50ml圆底三颈烧瓶中得到无色溶液。用5分钟滴加乙酸乙酯(3ml)中的(3
‑
((2
‑
羟乙基)硫代)丙基)三碳酸苯
‑
1,3,5
‑
三基酯(多醇32,2.02g,3.30mmol)。将反应混合物在50℃下搅拌3小时,然后在搅拌下缓慢冷却至室温。
[0558]1h
‑
nmr(cdcl3):7.04,6.99,4.96,4.67,4.37,4.21,3.80,3.66,3.50,3.47,3.38,3.35,3.33,3.25,3.23,3.21,3.06,3.01,2.93,2.90,2.76,2.70,1.85,1.83,1.78,1.72,1.25
‑
0.80.
[0559]
13
c
‑
nmr(cdcl3):156.71,155.41,152.66,151.44,121.92,112.07,67.55,63.73,57.02,56.83,54.61,50.80,48.68,48.59,48.39,48.20,48.05,47.87,46.59,46.54,46.29,46.07,44.69,43.85,43.63,43.38,41.49,36.65,36.52,35.04,34.93,34.86,34.83,34.69,34.57,31.89,31.86,31.05,28.50,28.41,28.35,27.64,27.59,27.54,26.85,23.38,23.34,23.23.
[0560]2‑
((2
‑
(((3
‑
(异氰酸根合甲基)苄基)氨基甲酰基)氧基)乙基)硫代)琥珀酸双(3
‑
((2
‑
(((3
‑
(异氰酸根合甲基)苄基)氨基甲酰基)氧基)乙基)硫代)丙基)酯(多异氰酸酯5)的制备
[0561]
将1,3
‑
双(异氰酸根合甲基)苯(1.4ml,8.94mmol)和2
‑
乙基己酸锡(ii)(0.09g,2.90mmol)加入到25ml圆底三颈烧瓶中得到无色溶液。滴加2
‑
((2
‑
羟乙基)硫代)琥珀酸双(3
‑
((2
‑
羟乙基)硫代)丙基)酯(多醇33,1.25g,2.90mmol)在乙酸乙酯(0.28ml)中的溶液。将反应混合物在50℃下搅拌3小时,然后在搅拌下冷却至室温。
[0562]1h
‑
nmr(cdcl3):7.41,7.38,7.37,7.32,7.28,7.27,7.22,7.16,4.52,4.48,4.29,4.21,3.69,2.93,2.85,2.71,2.60,2.04,1.90,1.71.
[0563]
用包含式(i)的可裂解多醇的可裂解多异氰酸酯制备本发明的微胶囊19和20
[0564]
由多异氰酸酯4制备微胶囊19
[0565]
将多异氰酸酯4(4.64g)与香料油(香料1,20.01g)在150ml烧杯中混合,得到黄色
溶液。将该混合物搅拌5分钟。将pvoh 18
‑
88(来源:瑞士aldrich)在水(1中%,46.31g)中的溶液加入到混合物中。用ultra turrax(s25n 10g)通过以17,500rpm搅拌反应混合物3分钟来制备乳液。液滴尺寸由光学显微镜控制(ph=4.79)。将反应混合物注入到250ml反应器中并在室温下以350rpm搅拌1小时。然后,用1小时将温度升至70℃,最后在70℃下以350rpm搅拌2小时(ph=5.68)。用氢氧化钠溶液将ph值调节至8.8。
[0566]
由多异氰酸酯3制备微胶囊20
[0567]
微胶囊20是根据微胶囊19所述的方案由多异氰酸酯3(5.32g)在香料油中制备的。
[0568]
实施例5
[0569]
织物柔软剂应用中的香料泄漏量
[0570]
在织物柔软剂配方(参见表2中的组成)中评估胶囊的储存稳定性。将胶囊分散体在织物柔软剂(29.73g)中稀释以获得0.20重量%的香料2的最终浓度。柔软剂在37℃下储存长达1个月。然后通过在搅拌下用异辛烷(10ml)进行溶剂萃取来测量从胶囊中泄漏出的香料的量。
[0571]
表2:织物柔软剂的组成:
[0572]
产品来源重量%stepantex vl 90astepan8.88氯化钙溶液10% 0.36proxel gxlavecia0.04水 90.72总计 100
[0573]
稳定性评估方案
[0574]
将包含微胶囊(2g)的织物柔软剂基料引入到20ml小瓶中。使用socorex 10ml瓶口分配器用水(2ml)稀释样品以降低粘度。使用设置为40rpm的turbulat shaker将样品振摇5分钟。将含有1,4
‑
二溴苯作为内标的异辛烷加入到小瓶(10ml)中,浓度精确到大约90ng/μl。将样品以40rpm振摇45分钟以提取游离香料,然后以3.0g离心10分钟以分离两相。回收溶剂相并在mgso4上干燥用于gc分析。
[0575]
表3:在37℃下储存3天后,织物柔软剂中微胶囊的香料泄漏量:
[0576]
微胶囊泄漏量(%)523.0619.8910.01010.01110.0
[0577]
因此,根据本发明的微胶囊在织物柔软剂中显示出良好的稳定性。
[0578]
实施例6
[0579]
液体洗涤剂组合物
[0580]
将本发明的微胶囊1~20分散在表4中所述的液体洗涤剂基料中,以获得0.22%的已包封香料油的浓度。
[0581]
表4:液体洗涤剂的组成:
[0582][0583]
1)hostapur sas 60;来源:clariant
[0584]
2)edenor k 12
‑
18;来源:cognis
[0585]
3)genapol la 070;来源:clariant
[0586]
4)aculyn 88;来源:dow chemical
[0587]
实施例7
[0588]
洗去型调理剂
[0589]
将本发明的微胶囊1~20分散在表5中所述的洗去型调理剂基料中,以获得0.5%的已包封香料油的浓度。
[0590]
表5:洗去型调理剂组合物:
[0591][0592]
1)genamin kdm p,clariant
[0593]
2)tylose h10 y g4,shin etsu
[0594]
3)lanette o,basf
[0595]
4)arlacel 165
‑
fp
‑
mbal
‑
pa
‑
(rb),croda
[0596]
5)incroquat behenyl tms
‑
50
‑
mbal
‑
pa
‑
(mh)ha4112,croda
[0597]
6)sp brij s20 mbal
‑
pa(rb),croda
[0598]
7)xiameter dc mem
‑
0949乳液,dow corning
[0599]
8)alfa aesar
[0600]
实施例8
[0601]
洗发剂组合物
[0602]
称取本发明的微胶囊1~20,并混合到洗发剂组合物中,以添加相当于0.2%的香料。
[0603]
表6:洗发剂组合物:
[0604][0605]
1)ucare polymer jr
‑
400,noveon
[0606]
2)schweizerhall
[0607]
3)glydant,lonza
[0608]
4)texapon nso is,cognis
[0609]
5)tego betain f 50,evonik
[0610]
6)amphotensid gb 2009,zschimmer&schwarz
[0611]
7)monomuls 90l
‑
12,gruenau
[0612]
8)尼泊金单钠,nipa
[0613]
实施例9
[0614]
止汗剂走珠乳液组合物
[0615]
称取本发明的微胶囊1~20,并混合到止汗剂走珠乳液组合物中,以添加相当于0.2%的香料。
[0616]
表7:止汗剂走珠乳液组合物:
[0617]
成分量(重量%)硬脂醇聚醚
‑21)
(a部分)3.25硬脂醇聚醚
‑
21
2)
(a部分)0.75ppg
‑
15硬脂醚
3)
(a部分)4去离子水(b部分)51氯化羟铝50%水溶液
4)
(c部分)40芳香剂(d部分)1
[0618]
1)brij 72;来源:ici
[0619]
2)brij 721;来源:ici
[0620]
3)arlamol e;来源:uniqema
‑
croda
[0621]
4)locron l;来源:clarian
[0622]
将a部分和b部分分别加热到75℃;在搅拌下将a部分加入到b部分中,并将混合物均化10分钟。然后,在搅拌下将混合物冷却。当混合物达到45℃时,缓慢加入c部分,当混合物达到35℃时,缓慢加入d部分,同时搅拌。然后将混合物冷却至室温。
[0623]
实施例10
[0624]
沐浴露组合物
[0625]
称取本发明的微胶囊1~20,并混合到以下组合物中,以添加相当于0.2%的香料。
[0626]
表8:沐浴露组合物:
[0627]
成分量(重量%)功能去离子水49.350溶剂edta四钠
1)
0.050螯合剂丙烯酸酯共聚物
2)
6.000增稠剂c12
‑
c15链烷醇聚醚硫酸钠
3)
35.000表面活性剂氢氧化钠20%水溶液1.000ph调节剂椰油酰胺丙基甜菜碱
4)
8.000表面活性剂甲基氯异噻唑啉酮和甲基异噻唑啉酮
5)
0.100防腐剂柠檬酸(40%)0.500ph调节剂
[0628]
1)edeta b powder;商标和来源:basf
[0629]
2)carbopol aqua sf
‑
1polymer;商标和来源:noveon
[0630]
3)zetesol ao 328u;商标和来源:zschimmer&schwarz
[0631]
4)tego
‑
betain f 50;商标和来源:goldschmidt
[0632]
5)kathon cg;商标和来源:rohm&hass。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1