一种碳化铁/锰交联海藻酸钠复合材料的制备方法及应用
1.本发明涉及环境治理领域,特别是涉及一种碳化铁/锰交联海藻酸钠复合材料的制备方法及应用。
背景技术:
2.伴随着工业化的推进,水环境与土壤环境中重金属污染日益严重,严重威胁人类健康和生态发展。研发快速和高效重金属吸附剂,吸附重金属离子,实现重金属离子的高效和快速吸附,将水体中重金属离子降低至国家相关水质标准限定值(比如as为0.05mg/l),对水环境和土壤环境的可持续发展是至关重要的。
3.现有的用于吸附的复合材料不易实现与重金属离子的有效结合制备工艺繁琐,吸附性能比较低,价格比较昂贵等缺陷,使得其对重金属吸附领域的应用受到限制。
技术实现要素:
4.本发明的主要目的在于提出一种碳化铁/锰交联海藻酸钠复合材料的制备方法及应用。
5.本发明的技术问题通过以下的技术方案予以解决:
6.一种碳化铁/锰交联海藻酸钠复合材料的制备方法,包括如下步骤:
7.s1、在2wt%的海藻酸钠水溶液中,滴加铁(ii)盐溶液和/或锰(ii)盐溶液,通过交联反应生成铁/锰交联海藻酸钠,洗涤收集微球形颗粒,并干燥;
8.s2、将步骤s1中的干燥的海藻酸钠在保护气体下在300
‑
900℃下烧结碳化1
‑
4h后,冷却、洗涤、干燥、研磨、过筛得到所述碳化铁/锰交联海藻酸钠复合材料。
9.优选地,所述铁(ii)盐溶液为硫酸亚铁溶液。
10.优选地,所述锰(ii)盐溶液为硫酸锰溶液、氯化锰溶液中的至少一种,优选地,所述锰(ii)盐溶液为硫酸锰溶液。
11.优选地,所述步骤s2中在600℃下烧结碳化2h。
12.优选地,所述步骤s2中的所述过筛是指过60目筛。
13.优选地,当所述步骤s1中滴加的是铁(ii)盐溶液或锰(ii)盐溶液时,所述海藻酸钠水溶液与所述铁(ii)盐溶液或锰(ii)盐溶液的体积比为1:1,且在所述铁(ii)盐溶液中铁(ii)离子的摩尔浓度为0.67mol/l,在所述锰(ii)盐溶液中锰(ii)离子的摩尔浓度为0.67mol/l;当所述步骤s1中滴加的是铁(ii)盐溶液和锰(ii)盐溶液两者的混合溶液时,所述海藻酸钠水溶液与所述混合溶液的体积比为1:2,且在所述混合溶液中铁(ii)离子的摩尔浓度为0.33mol/l,所述锰(ii)离子的摩尔浓度为0.33mol/l。
14.优选地,所述保护气体为氦气、氖气、氩气和氮气中的至少一种;所述步骤s1的滴加指采用转速为3ml/min的蠕动泵进行滴加。
15.一种由所述制备方法制得的碳化铁/锰交联海藻酸钠复合材料。
16.一种所述的碳化铁/锰交联海藻酸钠复合材料在处理重金属离子和/或磷素中的
应用。
17.优选地,所述重金属离子为as(iii)离子、as(v)离子和cr(vi)离子中的至少一种。
18.本发明的有益效果包括:本发明通过交联和热解反应的制备方法可以提高复合材料的比表面积和增加其孔隙度,实现其与重金属离子和/或磷素的有效接触,进而可以快速高效地吸附重金属离子与磷素,并可以同步实现对重金属离子的氧化或还原,降低金属离子的毒性,因此本发明实施例中通过简单工艺流程制备的高效碳化铁/锰交联海藻酸钠复合材料可以同时实现重金属毒性降低与去除、磷素持留和光催化还原吸附重金属。
附图说明
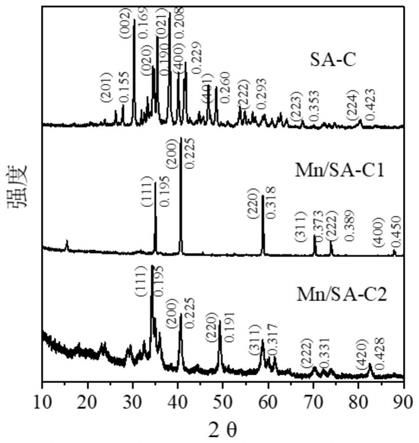
19.图1为本发明实施例1与2制备的复合材料的xrd图。
20.图2为本发明实施例1与2制备的复合材料的ft
‑
ir图。
21.图3为本发明实施例1与2制备的复合材料的sem图。
22.图4为本发明实施例1制备的复合材料吸附as(iii),as(v),和cr(vi)动力学曲线。
23.图5为本发明实施例1制备的复合材料持留磷素动力学曲线。
24.图6为本发明实施例1制备的复合材料持吸附
‑
解析曲线分析(barrett
‑
emmett
‑
teller)。
具体实施方式
25.下面对照附图并结合优选的实施方式对本发明作进一步说明。需要说明的是,在不冲突的情况下,本技术中的实施例及实施例中的特征可以相互组合。
26.本发明实施例提供一种碳化铁/锰交联海藻酸钠复合材料的制备方法,包括如下步骤:
27.s1、在2wt%的海藻酸钠水溶液中,滴加铁(ii)盐溶液和/或锰(ii)盐溶液,通过交联反应生成铁/锰交联海藻酸钠,洗涤收集微球形颗粒,并干燥;
28.s2、将步骤s1中的干燥的海藻酸钠在保护气体下在300
‑
900℃下烧结碳化1
‑
4h后,冷却、洗涤、干燥、研磨、过筛得到所述碳化铁/锰交联海藻酸钠复合材料。
29.在上述技术方案中,通过步骤s1制得的铁/锰交联海藻酸钠呈微球形颗粒形式,由于其表面光滑而不利于与重金属离子等进行有效结合,通过步骤s2对铁/锰交联海藻酸钠进行烧结碳化处理,可以提高复合材料的比表面积和增加其孔隙度,实现其与重金属离子和/或磷素的有效接触,进而可以快速高效地吸附重金属离子与磷素,并可以同步实现对重金属离子的氧化或还原(例如实现六价铬(cr(vi))的还原与三价砷(as(iii))的氧化),降低金属离子的毒性,因此本发明实施例中的碳化铁/锰交联海藻酸钠复合材料可以同时实现重金属毒性降低与去除。
30.在优选的实施例中,所述铁(ii)盐溶液为硫酸亚铁溶液。
31.在优选的实施例中,所述锰(ii)盐溶液为硫酸锰溶液、氯化锰溶液中的至少一种,优选地,所述锰(ii)盐溶液为硫酸锰溶液。
32.在优选的实施例中,所述步骤s2中在600℃下烧结碳化2h。
33.在优选的实施例中,所述步骤s2中的所述过筛是指过60目筛。
34.在优选的实施例中,当所述步骤s1中滴加的是铁(ii)盐溶液或锰(ii)盐溶液时,
所述海藻酸钠水溶液与所述铁(ii)盐溶液或锰(ii)盐溶液的体积比为1:1,且在所述铁(ii)盐溶液中铁(ii)离子的摩尔浓度为0.67mol/l,在所述锰(ii)盐溶液中锰(ii)离子的摩尔浓度为0.67mol/l;当所述步骤s1中滴加的是铁(ii)盐溶液和锰(ii)盐溶液两者的混合溶液时,所述海藻酸钠水溶液与所述混合溶液的体积比为1:2,且在所述混合溶液中铁(ii)离子的摩尔浓度为0.33mol/l,所述锰(ii)离子的摩尔浓度为0.33mol/l。
35.在优选的实施例中,所述步骤s1的滴加指采用转速为3ml/min的蠕动泵进行滴加。
36.在优选的实施例中,所述保护气体为氦气、氖气、氩气和氮气中的至少一种。
37.本发明实施例还提供一种由所述制备方法制得的碳化铁/锰交联海藻酸钠复合材料。
38.本发明实施例还提供一种所述的碳化铁/锰交联海藻酸钠复合材料在处理重金属离子和/或磷素中的应用。
39.在优选的实施例中,所述重金属离子为as(iii)离子、as(v)离子和cr(vi)离子中的至少一种。
40.以下通过具体的示例,对本发明做进一步说明。
41.实施例1
42.3g海藻酸钠在60℃条件下溶于150ml蒸馏水中(可以在溶解过程中滴加一滴醋酸溶液,以协助海藻酸钠溶解)。同时配置100mmol 150ml mnso4溶液充分搅拌2h,并将配置好的2wt%的海藻酸钠溶液通过蠕动泵(转速为3ml/min)滴加于mnso4溶液中,迅速形成微球形颗粒。将制备好的微球形颗粒用去离子水洗涤三次,在80℃烘箱中烘干,收集微球形颗粒。
43.将所得的微球形颗粒放置于瓷坩埚中,在通入氮气的真空马弗炉中600℃反应2h,冷却至室温,用玛瑙研钵研磨微球形复合碳化颗粒,并用球磨仪以220rpm的转速球磨15min之后回收粉末过60目筛,得到碳化锰交联海藻酸钠复合材料,将样品命名为mn/sa
‑
c2保存。
44.实施例2
45.3g海藻酸钠在60℃条件下溶于150ml蒸馏水中(可以在溶解过程中滴加一滴醋酸溶液,来协助海藻酸钠溶解)。同时配置100mmol 150ml mncl2溶液充分搅拌2h,并将配置好的2wt%的海藻酸钠溶液通过蠕动泵(转速为3ml/min)滴加于mncl2溶液中,并迅速形成微球形颗粒。将制备好的微球形颗粒用去离子水洗涤三次,在80℃烘箱中烘干,收集微球形颗粒。
46.将所得的微球形颗粒放置于瓷坩埚中,在通入氮气的真空马弗炉中600℃反应2h,冷却至室温,用玛瑙研钵研磨微球形复合碳化颗粒,并用球磨仪以220rpm的转速球磨15min之后回收粉末过60目筛,得到碳化锰交联海藻酸钠复合材料,将样品命名为mn/sa
‑
c1保存。
47.实施例3
48.3g海藻酸钠在60℃条件下溶于150ml蒸馏水中(可以在溶解过程中滴加一滴醋酸溶液,来协助海藻酸钠溶解)。同时配置100mmol 150ml feso4溶液充分搅拌2h,并将配置好的2wt%的海藻酸钠溶液通过蠕动泵(转速为3ml/min)滴加于此溶液中,并迅速形成微球形颗粒。将制备好的微球形颗粒用去离子水洗涤三次,在80℃烘箱中烘干,收集微球形颗粒。
49.将所得微球形颗粒放置于瓷坩埚中,在通入氮气的真空马弗炉中600℃反应2h,冷却至室温,用玛瑙研钵研磨微球形复合碳化颗粒,并用球磨仪以220rpm的转速球磨15min之
后回收粉末过60目筛,得到碳化锰交联海藻酸钠复合材料,将样品命名为fe/sa
‑
c保存。
50.实施例4
51.3g海藻酸钠在60℃条件下溶于150ml蒸馏水中(可以在溶解过程中滴加一滴醋酸溶液,来协助海藻酸钠溶解)。同时配置100mmol mnso4与100mmol feso
4 300ml混合溶液充分搅拌2h,并将配置好的2wt%的海藻酸钠溶液通过蠕动泵(转速为3ml/min)滴加于此溶液中,并迅速形成微球形颗粒。将制备好的微球形颗粒用去离子水洗涤三次,在80℃烘箱中烘干,收集微球形颗粒。
52.将所得的微球形颗粒放置于瓷坩埚中,在通入氮气的真空马弗炉中600℃反应2h,冷却至室温,用玛瑙研钵研磨微球形复合碳化颗粒,并用球磨仪以220rpm的转速球磨15min之后回收粉末过60目筛,得到碳化锰铁交联海藻酸钠复合材料,将样品命名为mn@fe/sa
‑
c保存。
53.对实施例1和2制备的复合材料进行xrd表征,如图1所示。从xrd图谱中能够发现,在未与mn或fe交联前,海藻酸钠经过碳化后生成的主要物质为碳酸钠,而经过交联后得到的mn/sa
‑
c1复合材料碳化后主要包括碳骨架(本技术实施例中写为sa
‑
c,下同)以及附着在碳骨架上的mno,经过交联后得到的mn/sa
‑
c2保复合材料碳化后主要包括碳骨架以及附着在碳骨架上的mno与mns2。通过结晶度来看,mn/sa
‑
c1复合材料与mn/sa
‑
c2相比具有较好的结晶度,然而mn/sa
‑
c2复合材料在碳化过程中产生mno与mns2,能够与重金属形成硫化物沉淀,具有更好的还原六价铬,氧化三价砷和络合磷素的效果。
54.对实施例1和2制备的复合材料进行ft
‑
ir表征,如图2所示。从ft
‑
ir图谱中可以发现从400
‑
1000cm
‑1处吸收峰波长是mn
‑
o和
‑
coona伸缩振动,由此充分证明通过碳化作用生成了mno。在1134cm
‑1处的吸收波长为mn
‑
oh的伸缩振动,由此可以推断实施例2的通过碳化mnso4交联海藻酸钠产生了mno与mns2。
55.对实施例1和2制备的复合材料进行sem粉末表征,如图3所示,能够发现通过碳化mncl2交联海藻酸钠形成了良好的网状晶格,碳化mnso4交联海藻酸钠形成细小纳米颗粒,为复合材料提供较大比表面积,为重金属吸附提供附着位点。
56.图4是实施例1制备的复合材料吸附重金属as(iii)、as(v)、和cr(vi)的动力学曲线图。反应条件为:30ml 含15mg复合材料和10mg/l重金属离子的溶液。表明:实施例1的mn/sa
‑
c2复合材料能够高效快速吸附as,通过吸附动力学曲线发现as浓度能够在20min能达到地表水质量标准,然而对cr(vi)的吸附时间明显延长,这可能是mns2含量较低所致。
57.图5是实施例1的复合材料对磷素持留的动力学曲线图。反应条件为:30ml含15mg复合材料和20mg/l磷素的溶液。表明:mn/sa
‑
c2复合材料对磷素有较高的吸附容量,能够达到磷素持留的目的。
58.图6通过复合材料的bet分析,发现通过碳化锰元素交联海藻酸钠能够明显增加复合材料的比表面积和孔隙度,mn/sa
‑
c2复合材料的比表面积为77.02m2/g,而单纯sa
‑
c比表面积为3.67m2/g,由此推断交联碳化形成多孔微球性,明显增强复合材料的比表面积,进而充分暴露复合材料中的金属氧化物,为金属氧化物提供碳骨架载体,实现重金属和磷素的高效吸附。
59.以上内容是结合具体的优选实施方式对本发明所作的进一步详细说明,不能认定本发明的具体实施只局限于这些说明。对于本发明所属技术领域的技术人员来说,在不脱
离本发明构思的前提下,还可以做出若干等同替代或明显变型,而且性能或用途相同,都应当视为属于本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1