一种高通量培养脑类器官的微流控芯片
1.本发明涉及脑类器官培养领域,尤其涉及一种高通量培养脑类器官的微流控芯片。
背景技术:
2.人类大脑研究一直是神经科学研究重难点,2013年以来,脑类器官模型的出现马上风靡神经科学领域,其快捷、经济地高还原度模拟体外人脑发育的过程,近期多用于临床人脑疾病模型的建立研究和药物检测研究。然而,由于没有血管的生长,及缺少发育相关细胞因子极化信号浓度梯度引导的作用,目前脑类器官模型生长成熟受限,且缺少组织的完整性和区域间拓扑学的连续性,使得该模型的优越性受到限制,在之上研究的科学问题的普适性也受到挑战。
3.为了研究麻醉药氯胺酮对大脑发育的影响,本发明主要利用微流控芯片技术,克服传统大脑类器官发育的模型的局限性,构建全脑类器官模型。
4.值得注意的是,微流控芯片技术具有在微米级别的通道内对流体进行控制,易于用层流的方式为类器官提供稳定的浓度梯度,可以为脑类器官的培养提供一个相对稳定的微环境,从而研究不同的浓度梯度在脑类器官的分化。由于现有人脑类器官模型的缺陷最核心的关键是,大脑类器官只能产生分散的大脑元件,独立的脑区随机分布于相对杂乱的类器官组织中,同一个脑类器官组织具有不可重复性,因此微流控芯片的相对稳定性将为类器官的培养提供更好的环境,减少不同批次类器官之间的异质性,从而为临床提供更有意义的信息。
5.综上所述,现有的脑类器官模型,大多数基于静态培养,随着培养时间的延长,脑类器官中心区域由于缺乏营养物质和氧气而导致中心区域坏死,而坏死区域的增多,使得无法更好的模拟脑部的发育过程。同时,现有技术生物反应器成本高,对培养基的用量需求高,而且样本组建差异大。
6.因此,本领域的技术人员致力于开发一种八个平行通道构成的用于高通量培养脑类器官的微流控芯片,特别是涉及用胚胎干细胞构建脑类器官,并在芯片内实现从培养、诱导到分化的长期培养。通过随着培养时间的推移来不断提高流速以保证类器官有足够的营养和氧气,使得脑类器官中间坏死区域比传统方法小,从而更加接近实际的大脑发育。
技术实现要素:
7.有鉴于现有技术的上述缺陷,本发明所要解决的技术问题是如何实现脑类器官的长期培养,减少坏死区域。
8.为实现上述目的,本发明提供了一种高通量培养脑类器官的微流控芯片,包括一个入口、八个平行通道和八个出口;所述入口分别与八个所述平行通道连接;八个所述平行通道与八个所述出口一一对应连接;每个所述平行通道的中间包括若干柱子。
9.进一步地,所述出口用于连接注射器。
10.进一步地,在通入样本时,八个所述出口均连接所述注射器。
11.进一步地,某个所述平行通道在引入样本时,去掉所述平行通道对应的所述出口连接的所述注射器,利用压强差来操控样本在所述平行通道内的流动
12.进一步地,所述柱子用于挡住样本,使样本在特定区域培养。
13.进一步地,培养的脑类器官能够在早期被放入到所述微流控芯片。
14.进一步地,所述微流控芯片提供持续的剪切力,促进脑类器官在没有基质胶的情况下进行分化。
15.进一步地,所述微流控芯片通过不断提高培养基的流速来提高脑类器官中心区域获得营养成分和氧气的机会。
16.进一步地,所述微流控芯片能够根据特定时间收集的脑类器官做蛋白组学和代谢组学的分析。
17.进一步地,八个所述平行通道能够同时培养八个脑类器官。
18.与现有技术相比,本发明至少具有如下有益技术效果:
19.1、本发明可以高通量、高重复性、长期培养脑类器官,并为脑部发育的研究提供更接近实际的脑类器官;
20.2、本发明培养的脑类器官坏死区域小,跟传统的方法比较可以更好的模拟脑部发育;
21.3、本发明可以实现实时成像;
22.4、本发明成本相对低、操作简便,对操作人员要求低。
23.以下将结合附图对本发明的构思、具体结构及产生的技术效果作进一步说明,以充分地了解本发明的目的、特征和效果。
附图说明
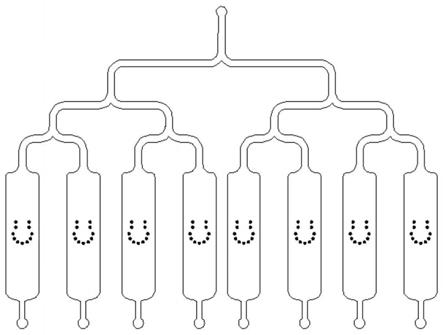
24.图1是本发明的一个较佳实施例的芯片设计图;
25.图2是本发明的一个较佳实施例的脑类器官在芯片内培养八天的示意图;
26.图3是本发明的一个较佳实施例的脑类器官在芯片外培养八天的示意图。
具体实施方式
27.以下参考说明书附图介绍本发明的多个优选实施例,使其技术内容更加清楚和便于理解。本发明可以通过许多不同形式的实施例来得以体现,本发明的保护范围并非仅限于文中提到的实施例。
28.在附图中,结构相同的部件以相同数字标号表示,各处结构或功能相似的组件以相似数字标号表示。附图所示的每一组件的尺寸和厚度是任意示出的,本发明并没有限定每个组件的尺寸和厚度。为了使图示更清晰,附图中有些地方适当夸大了部件的厚度。
29.如图1所示,是本发明的一个较佳实施例的芯片设计图,包括一个入口、八个平行通道和八个出口;每个平行通道的中间包括若干柱子。
30.在通入样本时出口连接注射器,给特定通道引入样本时,通过去掉该通道出口处的注射器来利用压强差来操控样本在通道内的流动。每一个平行通道中间有若干个柱子用于挡住样本,使样本在特定区域培养,以避免样本在培养过程中被冲走。八个平行通道可以
同时培养八个脑类器官。
31.本实施例培养的脑类器官可以在早期便被放入到芯片里,可以从早期开始提供持续的剪切力,促进脑类器官在没有基质胶的情况下也能分化的更好,促进营养成分能进入到类器官的中心区域,大大降低坏死区域。
32.同时,脑类器官在芯片上培养,可以通过不断提高培养基的流速来提高脑类器官中心区域获得足够营养成分和氧气的机会,从而得到更加接近实际脑组织的脑类器官,同时坏死区域小,可以从图2与图3中对比看出,图2是脑类器官在芯片内培养八天的示意图,图3是脑类器官在芯片外培养八天的示意图。
33.本实施例实现从培养、诱导到分化的长期培养,根据不同天数收集脑类器官做蛋白组学和代谢组学的分析,对于脑部发育的过程更加准确的信息。
34.本发明应用微流控技术构建shh(sonic hedgehog)、smad/bmp、成纤维细胞生长因子8(fibroblast growth factor8,fgf8)、wnt、胰岛素(insulin)、重组碱性成纤维细胞生长因子(basic fibroblast growth factor,bfgf)的多维浓度梯度层流系统,诱导培养出不同脑区域的单个脑类器官,并且通过单细胞测序确认其表达图谱差异性,分析其与正常大脑的相似度;得到确定结果后,通氯胺酮模拟麻醉过程,通过免疫荧光、聚合酶链式反应(polymerase chain reaction,pcr)、原位杂交、蛋白质印迹法(western blot,wb)等手段,观察氯胺酮对脑发育的影响。本发明设计的微流控技术已有相对成熟的设计、加工的能力,已设计用于培养类器官的芯片,实现类器官在芯片内的培养。在此技术基础上打造基于微流控的脑类器官的培养以及麻醉药物对脑类器官发育影响的机制研究,未来将可以构建基于全脑类器官的药物精确控制的筛选平台,建立更多全脑的如小头畸等人类特有的发育相关疾病模型,以及如阿尔茨海默病(alzheimer disease,ad)、帕金森症(parkinson disease,pd)等疾病的全脑类器官模型进行研究。
35.以上详细描述了本发明的较佳具体实施例。应当理解,本领域的普通技术无需创造性劳动就可以根据本发明的构思作出诸多修改和变化。因此,凡本技术领域中技术人员依本发明的构思在现有技术的基础上通过逻辑分析、推理或者有限的实验可以得到的技术方案,皆应在由权利要求书所确定的保护范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1