一种Z型C
一种z型c
60
/bi/biobr复合光催化剂及其制备方法和应用
技术领域
1.本发明属于光催化和材料化学技术领域,具体涉及一种z型c
60
/bi/biobr复合光催化剂及其制备方法和应用。
背景技术:
2.由于太阳能具有充足、清洁且可持续利用的优点,因此在当今世界化石燃料日趋减少的情况下,太阳能是最有价值的替代能源。自fujishima和honda在1972年发现tio2在紫外光照射下可以分解水产生h2,frank在1977年利用tio2在水相中降解有害的氰化物之后,光催化技术在能源开发与环境保护领域中的应用研究得到了广泛的关注。其中,由于半导体光催化技术可在大范围内利用太阳能,净化环境污染物,且具有反应在常温常压下进行,所需设备简单,以及排放低等优点,故在有机废水的处理中极具应用潜力。
3.近年来,一种带隙能约为2.8ev、最大吸收波长可达425nm的可见光催化剂-溴氧化铋(biobr),在降解水中有机污染物方面显示出较好的活性,而引起了研究人员的广泛关注。目前,biobr的主要制备方法是利用溶剂热法,将硝酸铋溶解在甲醇,乙醇,乙二醇或丙三醇中,于160℃反应12~24h即可制得。该方法所制备的biobr纯度较高,但存在的主要问题就是其光生电子-空穴的分离效率较低。众所周知,构建带有内电场的异质结光催化剂可以促进光生电子向光催化剂表面移动,从而加快电子和空穴的分离和迁移,因此载流子的快速转移和有效分离是制备高效光催化剂的关键。其中z型异质结的构建被认为是改善光催化剂动力学和热力学的一种很有应用前景的策略。
4.目前,z型biobr半导体复合光催化剂的构筑主要是通过掺杂金属或金属氧化物来完成。但是,该方法需要通过引入其他物质来完成对biobr的改性,不仅增加制备难度,提高生产成本,而且还降低了biobr的纯度。
技术实现要素:
5.为解决背景技术部分指出的技术问题,本发明提供了一种z型c
60
/bi/biobr复合光催化材料及其制备方法,采用乙二醇作为溶剂与反应物,原位引入c
60
和金属bi,一步合成具有高光生载流子分离效率的z型c
60
/bi/biobr复合光催化材料。
6.本发明解决其技术问题所采用的技术方案是:具有高光生载流子分离效率的z型c
60
/bi/biobr复合光催化剂的一步合成法。包括以下步骤:
7.(1)用乙二醇分别将bi(no3)3·
5h2o和kbr溶解,机械搅拌30min后,将上述两种溶液混合,再次避光机械搅拌10h,得混合溶液。其中,乙二醇的总用量为60~100ml,bi(no3)3·
5h2o与kbr的质量比为4~8:1。
8.(2)将步骤(1)所得混合溶液转入至高压反应釜中,在190℃的温度下溶剂热反应1~7h,冷却至室温,常压过滤,用无水乙醇和蒸馏水分别洗涤固体粉末3遍,80℃干燥,研磨,即得c
60
/bi/biobr产品。
9.本发明制备的复合光催化剂用于光催化降解甲基橙和苯甲醛。
10.本发明的有益效果是:
11.(1)在较高的溶剂热温度(190℃)下,较短的反应时间(1~7h)内,乙二醇作为溶剂,促使biobr生成的同时,也可以作为还原剂,将biobr微球表面的bio
+
原位还原成金属bi粒;与此同时,部分乙二醇在bi(no3)3·
5h2o的催化作用下,发生聚合,生成富勒烯-c
60
,其均匀分散在bi/biobr的外层。
12.(2)首次采用一步溶剂热的方法,成功合成了一种高效z型c
60
/bi/biobr异质结光催化剂。c
60
源于乙二醇本身的聚合,均匀地分散在biobr的外层。作为电子传输桥,金属bi粒不仅起到连接c
60
和biobr异质结界面的作用,还导致biobr表面产生了大量的氧空位。
13.(3)该c
60
/bi/biobr复合光催化剂的整体结构呈向日葵状。由于电子反阻挡层的存在,biobr产生的光生电子很容易流过bi桥注入c
60
,从而实现光生电子和空穴的有效分离。c
60
的lumo能级和biobr的价带边能级富集了大量的光生电子和空穴,这不仅提高了整个体系的载流子分离效率,而且有效地保持了其强大的还原和氧化能力。
14.(4)利用c
60
/bi/biobr光降解甲基橙和苯甲醛的过程中,溶液中产生了大量的超氧自由基(
·o2-)。作为反应主要的活性物种,该超氧自由基是通过光生电子还原吸附的氧气所产生的,此外biobr表面存在的氧空位也进一步促进了超氧自由基的生成。与纯biobr及bi/biobr光催化剂相比,z-型c
60
/bi/biobr光催化剂表现出显著的光催化活性,并在短时间内实现了甲基橙和苯甲醛的高效降解。
附图说明:
15.图1(a)是制备的bcb-1901,c
60
/bi/biobr,bcb-1905及bcb-1907的x射线衍射图,(b)是制备的biobr,c
60
/bi/biobr以及bi/biobr的x射线衍射图。
16.图2(a)是biobr,c
60
/bi/biobr,bi/biobr,bcb-1901以及bcb-1905的扫描电镜图,图2(b)是c
60
/bi/biobr的元素面分布分析。
17.图3(a)是bcb-1901,c
60
/bi/biobr,bcb-1905及bcb-1907的拉曼谱图,图3(b)是biobr,c
60
/bi/biobr以及bi/biobr的拉曼谱图。
18.图4(a)、(c)是bcb-1901,c
60
/bi/biobr,bcb-1905及bcb-1907的紫外-可见漫反射光谱图及其对应的固体粉末图,图4(b)、(d)是biobr,c
60
/bi/biobr以及bi/biobr的紫外-可见漫反射光谱图及其对应的固体粉末图。
19.图5是biobr,c
60
/bi/biobr以及bi/biobr的光电流谱图。
20.图6(a)和(b)分别是c
60
/bi/biobr在光照和暗态的氧空位和
·o2-自由基的电子自旋共振谱图。
21.图7(a)是bcb-1901,c
60
/bi/biobr,bcb-1905及bcb-1907的在相同条件下对100ml甲基橙溶液(10mg/l)的可见光降解性能比较图,图7(b)是biobr,bi/biobr以及c
60
/bi/biobr在相同条件下对100ml甲基橙溶液(10mg/l)的可见光降解性能比较图。
22.图8是c
60
/bi/biobr对100ml甲基橙溶液(10mg/l)的四次循环可见光降解性能比较图。
具体实施方式
23.本发明用下列实施例来进一步说明本发明的技术特征,但本发明的保护范围并非
限于下列实施例。
24.实施例1
25.将1.6g bi(no3)3·
5h2o用60ml乙二醇溶解,0.4g kbr用20ml乙二醇溶解,分别机械搅拌30min后,将上述二者溶液混合,再次避光机械搅拌10h,得混合溶液。将该混合溶液转入至高压反应釜中,于190℃的温度下溶剂热反应1h,冷却至室温,抽滤,用无水乙醇和蒸馏水分别洗涤固体粉末3遍,80℃干燥1h,研磨,即得bcb-1901样品。
26.实施例2
27.将1.6g bi(no3)3·
5h2o用60ml乙二醇溶解,0.4g kbr用20ml乙二醇溶解,分别机械搅拌30min后,将上述二者溶液混合,再次避光机械搅拌10h,得混合溶液。将该混合溶液转入至高压反应釜中,于190℃的温度下溶剂热反应3h,冷却至室温,抽滤,用无水乙醇和蒸馏水分别洗涤固体粉末3遍,80℃干燥1h,研磨,即得c
60
/bi/biobr复合光催化剂。
28.实施例3
29.将1.6g bi(no3)3·
5h2o用60ml乙二醇溶解,0.4g kbr用20ml乙二醇溶解,分别机械搅拌30min后,将上述二者溶液混合,再次避光机械搅拌10h,得混合溶液。将该混合溶液转入至高压反应釜中,于190℃的温度下溶剂热反应5h,冷却至室温,抽滤,用无水乙醇和蒸馏水分别洗涤固体粉末3遍,80℃干燥1h,研磨,即得bcb-1905样品。
30.实施例4
31.将1.6g bi(no3)3·
5h2o用60ml乙二醇溶解,0.4g kbr用20ml乙二醇溶解,分别机械搅拌30min后,将上述二者溶液混合,再次避光机械搅拌10h,得混合溶液。将该混合溶液转入至高压反应釜中,于190℃的温度下溶剂热反应7h,冷却至室温,抽滤,用无水乙醇和蒸馏水分别洗涤固体粉末3遍,80℃干燥1h,研磨,即得bcb-1907样品。
32.比较例1
33.将1.6g bi(no3)3·
5h2o用60ml乙二醇溶解,0.4g kbr用20ml乙二醇溶解,分别机械搅拌30min后,将上述二者溶液混合,再次避光机械搅拌10h,得混合溶液。将该混合溶液转入至高压反应釜中,于160℃的温度下溶剂热反应3h,冷却至室温,抽滤,用无水乙醇和蒸馏水分别洗涤固体粉末3遍,80℃干燥1h,研磨,即得biobr光催化剂。
34.比较例2
35.将1.6g bi(no3)3·
5h2o用60ml乙二醇溶解,0.4g kbr用20ml乙二醇溶解,分别机械搅拌30min后,将上述二者溶液混合,再次避光机械搅拌10h,得混合溶液。将该混合溶液转入至高压反应釜中,于210℃的温度下溶剂热反应3h,冷却至室温,抽滤,用无水乙醇和蒸馏水分别洗涤固体粉末3遍,80℃干燥1h,研磨,即得bi/biobr复合光催化剂。
36.以am 1.5g 100mw/cm2的太阳光谱作为标准光源,分别将0.05g上述样品与50ml 10mg/l的甲基橙或苯甲醛溶液混合,在150r/min的磁搅拌转速下进行上述污染物的光催化降解试验。在无光照的条件下,上述悬浮液反应30min后,达到吸附-脱附平衡。将3.0ml的混合溶液取出,于9000r/min的转速离心10min,取1.5ml上层清液,用紫外可见光分光光度计,分别于463及249nm的最大吸收波长处,测定其吸光值。根据标准工作曲线,计算取出液中的甲基橙或苯甲醛浓度。同理,在光照条件下,每隔30min,取样一次,测定其吸光值,计算污染物浓度。
37.其中,甲基橙或苯甲醛的光降解脱除率r(%)可根据式(1)进行计算:
[0038][0039]
式中:c0,ce分别指甲基橙或苯甲醛的初始及平衡质量浓度(mg/l);m指吸附剂的投料量(g);v指甲基橙或苯甲醛溶液的体积(ml)。
[0040]
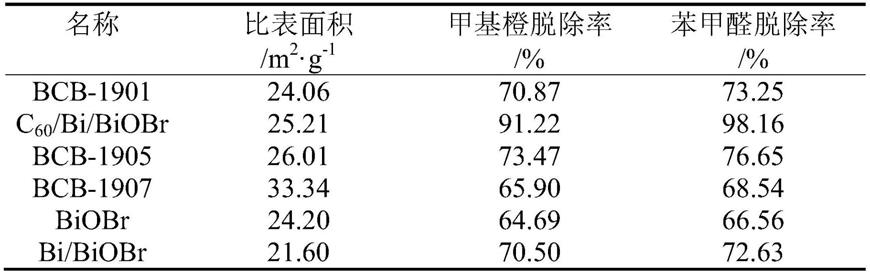
表1列出了bcb-1901,c
60
/bi/biobr,bcb-1905,bcb-1907,biobr及bi/biobr的比表面积,及其对甲基橙、苯甲醛的脱除率比较结果。由表1可以看出,c
60
/bi/biobr复合光催化剂具有较高的比表面积,对甲基橙及苯甲醛具有较高的光降解脱除效果。
[0041]
表1 bcb-1901,c
60
/bi/biobr,bcb-1905,bcb-1907,biobr及bi/biobr的比表面积及其对甲基橙,苯甲醛的脱除率比较
[0042][0043]
如图1(a)、(b)所示,190℃溶剂热反应3h后,c
60
/bi/biobr复合材料的xrd衍射峰分别与c
60
,bi及biobr的标准pdf卡片相对应,说明通过一步溶剂热法,c
60
/bi/biobr复合光催化剂已被成功合成,且具有较高的纯度。
[0044]
如图2(a)所示,190℃溶剂热反应3h后,c
60
及金属bi的引入并未破坏biobr原有的微球状结构。如图2(b)所示,c
60
/bi/biobr复合光催化剂的元素面分布分析谱图证实了c、o、br和bi元素的存在,且上述元素在该材料中的分布均匀。
[0045]
如图3(a)、(b)所示,除了biobr的拉曼特征峰外,c
60
/bi/biobr复合材料还在1040~1450cm-1
的拉曼位移范围内,出现了明显的c
60
特征峰,说明c
60
与biobr间存在较为强烈的相互作用。
[0046]
如图4(a)、(b)、(c)以及(d)所示,相比较bcb-1901,bcb-1905,bcb-1907,biobr,bi/biobr样品,c
60
/bi/biobr复合光催化剂具有适宜的吸收带边(450nm)及带隙能(2.38ev)。
[0047]
如图5所示,在同样的测试条件下,相比较biobr,bi/biobr样品,c
60
/bi/biobr复合光催化剂具有较强的光电流信号,说明其具有较高的光生载流子分离效率。
[0048]
如图6(a)所示,光照后氧空位的电子自旋共振谱图信号值较强,表明c
60
/bi/biobr复合光催化剂的表面存在大量的氧空位。图6(b)显示,光照后dmpo/
·o2-的电子自旋共振谱图信号值较强,说明c
60
/bi/biobr与dmpo悬浮液中产生了大量的
·o2-自由基。
[0049]
如图7(a)、(b)所示,c
60
/bi/biobr复合材料具有较优的光催化活性。经过计算,甲基橙在bcb-1901,bcb-1905,bcb-1907,biobr,bi/biobr以及c
60
/bi/biobr上的光降解率分别为70.87%,73.47%,65.90%,64.69%,70.50%和91.22%。
[0050]
如图8所示,随着循环次数的增加,c
60
/bi/biobr的光催化活性略有下降。光降解810分钟后,甲基橙的降解率从91.22%仅下降至87.91%,表明其具有良好的稳定性。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1