一种双金属氧化物纳米材料及其制备方法与应用
1.本发明属于纳米材料和高级氧化技术交叉领域,具体涉及一种蛋黄/壳结构的双金属氧化物纳米材料及其制备方法与应用。
背景技术:
2.基于过氧单硫酸盐(pms)的高级氧化技术可应用于多种难降解废水的处理和环境修复。该技术可通过催化剂与pms氧化剂反应原位产生硫酸根自由基(so4·-)、羟基(
·
oh)、单线态氧(1o2)等活性物种实现水中有毒难降解污染物的高效氧化分解。然而,水中各种无机离子和腐殖质等溶解性有机物容易与游离态自由基发生反应导致其无效消耗,从而显著降低了传统工艺对目标污染物的去除效率,导致处理成本的提高。与之相比,基于吸附态自由基的高级氧化工艺由于可吸附污染物在催化剂表面发生反应,因此具有更高的氧化剂利用效率,在实际水处理应用中更具有明显优势。
3.催化剂的选择与设计对pms高级氧化技术尤为关键。过渡金属氧化物具有成本低、环境友好、性质灵活可调等优点,被广泛用做类芬顿催化剂,但主要集中于游离态自由基的催化反应体系。目前已报导的可实现吸附态自由基氧化途径的催化剂包括铁氧化物、硫化钴等。有少数研究发现双金属氧化物比单金属氧化物催化剂表现出优异的催化活性。例如,nio-zno异质结复合催化剂被用于活化pms,同时通过游离态自由基和吸附态自由基等途径降解污染物,其催化活性显著优于单独的nio和zno。然而,nio-zno异质结催化剂的制备过程复杂,通常需要先合成空心球结构的zno,再通过二次水热反应生成nio-zno复合材料,或者将花状zno颗粒再分散至硝酸镍溶液中生成nio修饰的zno微花结构复合材料。另外,现有的nio-zno异质结催化剂普遍存在活性较低,金属离子溶出等问题(反应过程中ni
2+
和zn
2+
溶出量分别高达0.3mg/l和13mg/l),从而大大降低了其循环使用的稳定性。
4.为了解决现有技术存在的上述问题,本发明由此而来。
技术实现要素:
5.针对现有的nio-zno两步合成方法操作复杂、能耗高以及所合成的催化剂活性较差等缺点,本发明提供了一种蛋黄/壳结构的双金属氧化物纳米材料的制备新方法并优化了其结构与性能,该纳米材料可作为催化剂被用于多种有机废水的处理和受污染水环境的修复。本发明通过一步水热法获得蛋黄/壳结构的nio-zno复合材料,这类具有蛋黄/壳结构的纳米反应器的介孔壳层有利于反应物分子的快速扩散,而内部空腔可通过限域效应提高反应物和自由基的浓度,有望为4-氯酚等有机污染物的氧化提供动力,与已有的nio-zno氧化物相比,本发明中的蛋黄/壳结构的nio-zno异质结催化剂活性更高而且稳定性更好。
6.本发明的技术方案为:
7.本发明涉及了一种双金属氧化物纳米材料的制备方法,包括以下步骤:
8.s1、将镍盐溶于n,n-二甲基甲酰胺和乙二醇的混合液中,然后加入锌盐,室温下搅拌,然后加入对苯二甲酸,继续搅拌至充分混合均匀;
9.s2、将步骤s1所得溶液转移至聚四氟乙烯反应釜内胆中,套上不锈钢釜套后置于烘箱中,进行水热反应,反应结束后冷却至室温,然后离心、洗涤,真空干燥后得到前驱体;
10.s3、将前驱体进行热处理,得到nio-zno纳米材料。
11.优选地,所述镍盐与所述锌盐的质量比为1:1至1:0.7。
12.优选地,所述镍盐为ni(no3)2·
6h2o,所述锌盐为zn(no3)2·
6h2o。
13.优选地,s1步骤中,n,n-二甲基甲酰胺(dmf)和乙二醇的体积比为7:5至9:5;对苯二甲酸的质量占镍盐质量的55~65%。
14.优选地,s2步骤中,水热反应的温度为140~160℃,时间为5.5~6.5h。
15.优选地,s2步骤中,冷却到室温后,将所得产物进行离心,使用n,n-二甲基甲酰胺(dmf)和无水乙醇各洗涤三次。
16.优选地,s2步骤中,真空干燥的温度为60~80℃,时间为8~12h。
17.优选地,s3步骤中,热处理的条件为:将前驱体在450~550℃下保持20~30min,控制升温速率2℃/min。
18.本发明还涉及了一种双金属氧化物纳米材料,采用上述制备方法制得,具有蛋黄/壳结构,且核与壳之间存在200~300nm间隙。
19.本发明还涉及了上述双金属氧化物纳米材料在活化pms降解有机废水中的有机污染物的应用。进一步优选地,有机废水中的有机污染物可以为4-氯酚(4-cp)、双酚a(bpa)、磺胺(sa)和罗丹明b(rhb)中的至少一种,有机废水中有机污染物的浓度为5~20mg/l,每升有机废水中双金属氧化物纳米材料的添加量为0.05~0.2g/l,pms的添加量为0.04~0.1g/l。
20.本发明的有益效果是:
21.(1)本发明采取一步水热法直接合成蛋黄/壳结构的nio-zno双金属氧化物纳米材料,大大简化了合成工艺,将金属盐共溶于n,n-二甲基甲酰胺和乙二醇混合液中,离心煅烧后形成蛋黄/壳结构的nio-zno氧化物,无需任何模板。
22.(2)本发明所制备的nio-zno双金属氧化物纳米材料具有独特的蛋黄/壳结构,蛋黄/壳结构显著增强了其催化降解效率。多孔壳层可以保护包裹的催化剂免受溶液中恶劣环境的干扰,有限的空腔环境产生瞬间高浓度的so4·-、
·
oh,为促进4-cp等有机污染物催化氧化提供了驱动力,这也暗示多功能的nio-zno蛋黄/壳纳米反应器可能会带来很大的可扩展性,以增强多种环境下污染物的催化降解。
23.(3)本发明所得nio-zno双金属氧化物纳米材料实现nio-zno催化剂活性的提高,同时反应体系中ni
2+
和zn
2+
溶出浓度为0.02mg/l和0.8mg/l,离子溶出量大大减少。
附图说明
24.下面结合附图及实施例对本发明作进一步描述:
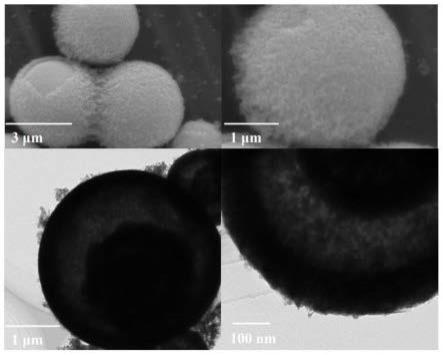
25.图1:实施例1的蛋黄/壳nio-zno纳米材料的sem图、tem图;
26.图2:实施例1的蛋黄/壳nio-zno纳米材料的xrd图;
27.图3:实施例1的蛋黄/壳nio-zno纳米材料活化pms降解4-cp的性能;
28.图4:实施例1的蛋黄/壳nio-zno纳米材料在循环使用4次后对4-cp降解性能的变化;
29.图5:实施例1的蛋黄/壳nio-zno纳米材料活化pms降解多种污染物的性能;
30.图6:实施例1的蛋黄/壳nio-zno纳米材料在不同水环境中活化pms降解4-cp的性能;
31.图7:实施例1的蛋黄/壳nio-zno纳米材料活化pms体系中离子溶出的浓度。
具体实施方式
32.为使本发明的目的、技术方案和优点更加清楚明了,下面结合具体实施方式并参照附图,对本发明进一步详细说明。应该理解,这些描述只是示例性的,而并非要限制本发明的范围。此外,在以下说明中,省略了对公知结构和技术的描述,以避免不必要地混淆本发明的概念。
33.实施例1nio-zno双金属氧化物纳米材料的制备
34.1、将0.25g的ni(no3)2·
6h2o溶解在40ml n,n-二甲基甲酰胺和25ml乙二醇混合液中,完全溶解后加入0.25g的zn(no3)2·
6h2o,室温搅拌半小时后加入0.15g对苯二甲酸,继续搅拌1小时至充分混合均匀。
35.2、将步骤(1)所得亮绿色溶液转移至容积100ml的聚四氟乙烯反应釜内胆中,套上不锈钢釜套后置于烘箱中程序升温至150℃,进行6小时的水热反应,随后自然冷却降温取出;将所得绿色沉淀物进行离心,使用dmf和无水乙醇各洗涤三次,并60℃真空干燥12h,得到亮绿色前驱体。
36.3、将步骤2中所得前驱体在500℃下保持20分钟,控制升温速率2℃/min的条件下进行热处理,得到黑色的nio-zno纳米材料。
37.对比例1nio材料的制备
38.与实施例1的制备条件一致,不同点在于步骤(1)中不加入zn(no3)2·
6h2o,仅加入ni(no3)2·
6h2o。
39.对比例2zno材料的制备
40.与实施例1的制备条件一致,不同点在于步骤(1)中不加入ni(no3)2·
6h2o,仅加入zn(no3)2·
6h2o。
41.对实施例1所合成的nio-zno双金属氧化物纳米材料进行表征分析:
42.材料形貌和结构表征:将材料研磨均匀后进行扫描电子显微镜(sem)和x-射线衍射(xrd)表征。如图1所示,sem图像显示nio-zno具有直径为2~3μm的蛋黄壳微球形貌,破裂的nio-zno微球中能清楚的观察到坚硬的蛋黄微球和薄壳;tem图显示壳与核之间存在200~300nm间隙,表明空腔结构的形成;如图2所示,nio-zno双金属氧化物纳米材料的xrd衍射光谱证明了nio、zno两相的存在。
43.实施例2去除水中4-cp的应用
44.将2mg的nio-zno纳米颗粒溶解于20ml 10mg/l的4-cp溶液中,室温下超声5min后继续搅拌10min使得nio-zno达到吸附平衡,加入40μl 25g/l pms储备液引发反应,对应的nio-zno/pms体系中4-cp的降解速率曲线如图3所示。图3中的pms体系代表pms单独存在时对4-cp的去除效率,nio-zno体系代表nio-zno单独存在时对4-cp的去除效率,nio/pms体系和zno/pms体系分别代表nio和zno与pms共存时对4-cp的去除效果,nio+zno/pms体系代表nio、zno和pms三者共存时对4-cp的去除效果。如图3所示,空白的pms或者nio-zno单独投加
时,仅有4%的4-cp被降解,说明pms的固有氧化能力和nio-zno的吸附能力均可忽略不计。然而当nio-zno与pms同时使用时,10分钟内,nio-zno/pms体系中的4-cp被完全去除,去除速率明显比空白nio/pms和zno/pms体系高,揭示了ni、zn元素间的协同作用及对活化pms的驱动力。同时,检测反应后nio-zno/pms体系中ni
2+
和zn
2+
溶出浓度分别为0.02mg/l和0.8mg/l,解决了现有技术中的ni
2+
和zn
2+
离子溶出问题(图7)。
45.催化反应途径分析:选取乙醇和叔丁醇作为自由基捕获剂加入nio-zno/pms反应体系中,发现其并不能抑制4-cp的降解,排除本体溶液中自由基的存在。选取苯酚作为表面结合自由基的淬灭剂,降解性能几乎被100%抑制。在进行so4·-、
·
oh的探针实验中,检测到苯甲酸和亚甲基蓝探针污染物的降解,可以充分证明表面结合自由基的存在。同时在进行电子顺磁共振波谱(epr)测试时,通过添加氟化钠,促进表面结合自由基的释放,溶液中捕获到自由基的信号,再次验证该体系降解4-cp的机理为表面结合自由基。
46.实施例3蛋黄/壳nio-zno双金属氧化物纳米材料的循环稳定性
47.将实施例1中的nio-zno双金属氧化物纳米材料用于污染物降解的催化剂材料重复使用,具体的去除水中4-cp的处理方法与实施例2一致,每次实验反应后通过离心收集催化剂,并用去离子水清洗后重复上述步骤,共进行四次循环测试,每个循环反应时间为20分钟。如图4所示,在前四次循环中,蛋黄/壳nio-zno纳米材料降解4-cp效率仍然高达95%。将第四次循环后收集的材料干燥后,通过煅烧以去除表面污染物中间体的残留,重复上述实验证实催化剂催化性能恢复。因此,该催化剂在活化pms降解有机污染物方面显示出优异的循环稳定性。
48.实施例4蛋黄/壳nio-zno/pms体系用于实际水样和多种污染物处理
49.将实施例1得到的蛋黄/壳nio-zno/pms双金属氧化物纳米材料投加到以不同污染物为处理对象的溶液中,其中催化剂、pms和4-cp等污染物的浓度均和实施例2中保持一致。图5为nio-zno/pms体系中不同污染物的降解速率曲线。经测试,本发明构建的nio-zno/pms体系均能在20分钟内实现不同有机污染物(如4-cp、bpa、sa、rhb)的完全去除。
50.分别选取去离子水、自来水和湖水进行实际水环境的模拟,具体地,分别取湖水样品(总有机碳浓度为33mg/l)及自来水(总有机碳浓度为20mg/l)样品、去离子水,其中催化剂、pms和4-cp的浓度均和实施例2中保持一致。图6为以不同水样作为反应介质时4-cp的降解速率曲线,其中deionind water代表去离子水样品,tap water代表自来水样品,lake water代表湖水样品,从图6中可以看出,nio-zno/pms体系在不同的水质条件下均能在25min内实现4-cp的完全降解,证明了该体系具有良好的环境适用性和水处理应用前景。
51.本发明所制备的蛋黄/壳nio-zno双金属纳米材料具有优异的催化性能,主要归因于ni、zn元素的协同作用以及蛋黄与壳的双协同作用。(1)nio-zno双金属氧化物对pms的活化效果远远优于空白nio、zno,ni与zn的强相互作用保证了nio-zno双金属氧化物的催化活性和催化稳定性(图3)。(2)蛋黄/壳结构的设计显示了nio-zno纳米反应器在环境修复的潜力。蛋黄/壳结构的nio-zno异质结催化剂实现在10分钟内100%降解10mg/l双酚a(图5)。多孔壳层允许小分子反应物自由进入,保护包裹的催化剂免受溶液中氯离子、硝酸根离子恶劣组分的干扰,即使外壳层的活性位点被占据,内部空腔的催化位点仍有活性。更有利的是,蛋黄与壳间的空腔提供反应的微环境使得瞬间高浓度的so4·-、
·
oh与4-cp受限于有限空间内,限域效应为促进4-cp催化氧化提供了驱动力。
52.应当理解的是,本发明的上述具体实施方式仅仅用于示例性说明或解释本发明的原理,而不构成对本发明的限制。因此,在不偏离本发明的精神和范围的情况下所做的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。此外,本发明所附权利要求旨在涵盖落入所附权利要求范围和边界、或者这种范围和边界的等同形式内的全部变化和修改例。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1