血清样本中葡萄糖能量代谢相关的重要代谢物的分析方法与流程
本发明涉及分析化学领域和生物化学领域,是一种基于气相色谱-三重四级杆质谱联用多反应监测模式进行血清样本中葡萄糖能量代谢相关的重要代谢物分析的方法。
背景技术:
葡萄糖是糖在血液中的运输形式,在机体糖代谢中占据主要地位,是维持生命活动的重要物质。葡萄糖通过糖酵解转变为丙酮酸并产生能量,丙酮酸在有氧条件下经过三羧酸循环和氧化磷酸化彻底氧化形成CO2和H2O,产生大量自由能;而在无氧条件下则转化为乳酸。葡萄糖经糖酵解到彻底氧化不仅为机体提供大量自由能,而且为一些物质合成提供前体物质,其代谢异常与癌症、心血管疾病、代谢综合征、糖尿病等多种疾病密切相关。因此建立简单、稳健、高灵敏的葡萄糖能量代谢相关的重要代谢物的分析方法将为与其代谢相关的生理和病理研究提供帮助。
葡萄糖能量代谢相关的重要代谢物在血中浓度差异非常大,根据HMDB数据库(http://www.hmdb.ca/)中给出的浓度含量范围,相关代谢物的浓度最大相差4个数量级,对其分析造成了很大困难。近年来出现多种技术用于葡萄糖能量代谢相关的重要代谢物的分析。Luo等报道了基于液质联用的靶向分析方法,但存在灵敏度及覆盖度等问题;Ye等报道了基于气质联用的拟靶向方法,存在覆盖度的问题。在定量分析方面,通常对葡萄糖和三羧酸循环中间产物进行分别分析。葡萄糖的测定主要有酶法、电化学法、光化学法等;三羧酸循环中间产物的定量分析多用气质联用的方法,如Calderón-Santiago等采用氯仿甲醇水双相提取,选择离子扫描模式检测,但存在提取复杂、溶剂毒性大等问题。气相色谱-三重四级杆质谱联用技术,作为靶向分析强有力的工具,通过气相色谱分离结合两级质谱的选择离子扫描,最大限度地排除基质干扰,具有灵敏度高、线性范围宽等优点;且尚未见基于气相色谱-三重四级杆质谱联用多反应监测模式分析葡萄糖能量代谢相关的重要代谢物的相关报道。
技术实现要素:
本发明针对现有方法的不足,建立了气相色谱-三重四级杆质谱联用多反应监测模式进行葡萄糖能量代谢相关的重要代谢物的分析方法,可一次进样分析得到血清中葡萄糖能量代谢相关的重要代谢物的含量,用于相关疾病代谢的研究,为了解机体的生理过程及疾病的发生发展机制等提供依据。该方法具有前处理简单、灵敏度高、重复性好、线性范围宽等优点。
本发明采用的技术路线如下:
(1)将-80℃保存的血清样本解冻,涡旋10s,准确移取50μL,加入含内标的甲醇溶液200μL,涡旋1min。甲醇溶液中内标浓度分别为:乳酸-3,3,3-d3(100μg/mL),琥珀酸-2,2,3,3-d4(0.2μg/mL),富马酸-2,3-d2(0.1μg/mL),柠檬酸-2,2,4,4-d4(5μg/mL),葡萄糖-13C6,1,2,3,4,5,6,6-d7(150μg/mL)。4℃下14000rpm离心15min,取200μL上清溶液冷冻干燥。
(2)于冻干血清样本中加入50μL甲氧胺溶液(20mg.ml,吡啶),涡旋30s,超声1min,37℃水浴中反应1.5h;待反应结束,加入40μLN-甲基-N-(三甲基硅烷基)三氟乙酰胺,涡旋10s,37℃水浴中反应1h;反应完成后,4℃下14000rpm离心10min,取上清溶液用于分析。
(3)气相色谱-三重四级杆质谱联用仪器用于样本分析。
气相色谱条件:HP-5MS色谱柱(30m×0.25mm×0.25μm,Agilent Technologies,USA)。柱温采用程序升温,70℃保持1min,5℃/min升至190℃,15℃/min升至310℃,后平衡5min。进样口温度300℃,进样体积1μL,分流比1:5。氦气(99.9995%,China)作为载气,流速1.2mL/min,恒流模式;
质谱条件:EI源,-70eV,传输线和离子源温度分别是280℃和230℃。溶剂延迟时间5.5min。碰撞气为氮气,流速1.5mL/min;淬灭气为氦气,流速为2.25mL/min。采用多反应监测模式检测,对于低含量代谢物,选择丰度高的母离子,对其进行子离子扫描并优化碰撞能,选择S/N最大且特异性好的离子对作为定量离子对,并辅以定性离子对;对于高含量代谢物(乳酸、葡萄糖),选择丰度低的母离子,子离子扫描并优化碰撞能,选择低丰度的离子对作为定量离子对,并辅以定性离子对。附表1为优化后得到的代谢物定量离子对、定性离子对,及其相应的碰撞能信息。
(4)质谱数据用Masshunter Quantitative Analysis Software导出,采用内标法对代谢物进行定量分析。
本方法采用甲醇一步提取,相对于氯仿甲醇水双相提取,该方法操作简单、重复性好、且溶剂毒性小;并采用气相色谱-三重四级杆质谱多反应监测模式进行检测,抗干扰能力强、灵敏度高,对于低含量代谢物检测限在0.17-2.13ng/mL;通过离子对选择及碰撞能优化,可以实现高低含量代谢物同时检测分析。
附图说明
图1为正常人血清样本中葡萄糖能量代谢相关的重要代谢物和内标的总离子流图。
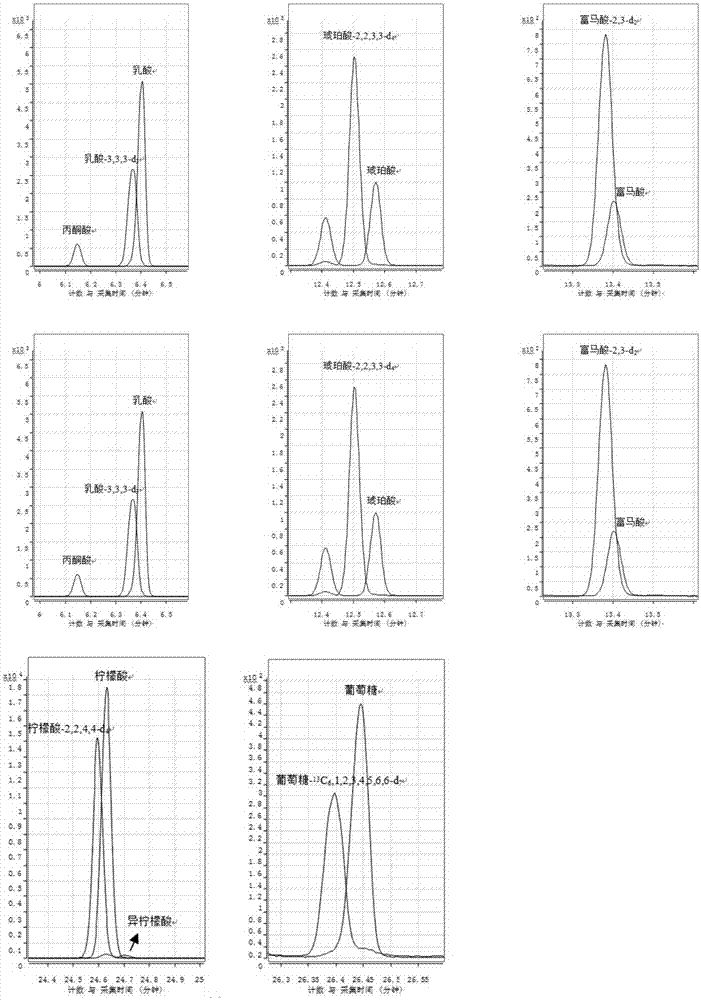
图2为正常人血清样本中葡萄糖能量代谢相关的重要代谢物和内标的定量离子对提取流图。
具体实施方式
下面结合附图对本发明的实施例作详细说明:实施例在以本发明技术方案为前提下进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
实施例一
基于气相色谱-三重四级杆质谱联用检测血清样本中葡萄糖能量代谢相关的重要代谢物方法的评价
参考HMDB数据库(http://www.hmdb.ca/),如不同年龄人群血糖含量范围在1100-16440μM,即198.2-2961.8μg/mL。根据数据库中代谢物的参考浓度范围配制混标溶液,浓度分别为丙酮酸(800.0μg/mL),乳酸(4000μg/mL),琥珀酸(800.0μg/mL),富马酸(800.0μg/mL),苹果酸(800.0μg/mL),2-羟基戊二酸(800.0μg/mL),2-酮戊二酸(800.0μg/mL),乌头酸(800.0μg/mL),柠檬酸(800.0μg/mL),异柠檬酸(800.0μg/mL),葡萄糖(4000μg/mL),用纯水将混标溶液分别稀释1.33倍、1.6倍、2.67倍、4倍、8倍、40倍、80倍、400倍、800倍、4000倍、8000倍、20000倍、40000倍、100000倍、200000倍、500000倍、1000000倍、2500000倍得到不同浓度的混标溶液。取不同浓度的混标溶液各50μL,分别加入200μL含内标的甲醇溶液,涡旋1min;甲醇溶液中内标浓度分别为:乳酸-3,3,3-d3(100μg/mL),琥珀酸-2,2,3,3-d4(0.2μg/mL),富马酸-2,3-d2(0.1μg/mL),柠檬酸 -2,2,4,4-d4(5μg/mL),葡萄糖-13C6,1,2,3,4,5,6,6-d7(150μg/mL)。4℃下14000rpm离心15min,取200μL上清溶液冷冻干燥。
于冻干样本中加入50μL甲氧胺溶液(20mg/ml吡啶),涡旋30s,超声1min,37℃水浴中反应1.5h;待反应结束,加入40μL N-甲基-N-(三甲基硅烷基)三氟乙酰胺,涡旋10s,37℃水浴中反应1h;反应完成后,4℃下14000rpm离心10min,取上清溶液用于气相色谱-三重四级杆质谱联用仪器分析。
气相色谱条件:HP-5MS色谱柱(30m×0.25mm×0.25μm,Agilent Technologies,USA);柱温采用程序升温,70℃保持1min,5℃/min升至190℃,15℃/min升至310℃,后平衡5min;进样口温度300℃,进样体积1μL,分流比1:5;氦气(99.9995%,China)作为载气,流速1.2mL/min,恒流模式。质谱条件:EI源,-70eV,传输线和离子源温度分别是280℃和230℃。溶剂延迟时间5.5min;碰撞气为氮气,流速1.5mL/min;淬灭气为氦气,流速为2.25mL/min。
对于含量低于或等于100μg/mL的代谢物,挑选响应较高的候选母离子在不同碰撞能条件下(CE=0-35V)进行子离子扫描,选择信噪比最高的离子对作为定量离子对;而对于含量高于100μg/mL的代谢物,挑选响应较低的候选母离子在不同碰撞能条件下(CE=0-35V)进行子离子扫描,选择线性范围宽的离子对作为定量离子对,最终得到11种代谢物及其5种内标的定量离子对、定性离子对,及其相应的碰撞能信息见附表1。根据附表1确定的质谱条件采用不同浓度的混标溶液进行方法的线性分析,得到代谢物的线性范围及线性相关系数R2见附表1,均满足分析要求。
考察了方法的回收率,将-80℃保存的血清样本解冻,涡旋10s,分别准确移取50μL血清样本进行空白和加标回收率分析。空白对照样本采用血清加入甲醇10μL,加标回收率样本则在血清样本中分别加入低、中、高浓度混标溶液10μL,上述溶液再加入含内标的甲醇溶液190μL,涡旋1min,考察低、中、高浓度加标回收率。空白和加标回收率均重复6次。中浓度混标溶液浓度分别为:丙酮酸(17.5μg/mL),乳酸(1100μg/mL),琥珀酸(4.0μg/mL),富马酸(1.25μg/mL),苹果酸(3.0μg/mL),2-羟基戊二酸(1.75μg/mL),2-酮戊二酸(15.0μg/mL),乌头酸(1.75μg/mL),柠檬酸 (80.0μg/mL),异柠檬酸(2.5μg/mL),葡萄糖(2000μg/mL);低、高浓度混标溶液的浓度分别是中浓度混标溶液浓度的0.8倍、1.2倍。甲醇溶液中内标浓度分别为:乳酸-3,3,3-d3(100μg/mL),琥珀酸-2,2,3,3-d4(0.2μg/mL),富马酸-2,3-d2(0.1μg/mL),柠檬酸-2,2,4,4-d4(5μg/mL),葡萄糖-13C6,1,2,3,4,5,6,6-d7(150μg/mL)。4℃下14000rpm离心15min,取200μL上清溶液冷冻干燥。衍生后经过分析及计算,在低、中、高浓度的加标回收率均在78.1-112.5%,满足分析要求;且空白、低、中、高加标样品各平行6份的RSD均在10%以内,重复性好。
将中浓度混标溶液分别稀释50倍、100倍、500倍、1000倍、10000倍、50000倍,各取50μL加入200μL甲醇,涡旋混匀后取200μL溶液冻干,然后衍生分析;在低浓度条件下以S/N=3得到低含量代谢物的检测限在0.17-2.13ng/mL范围内(除了乳酸、葡萄糖)见附表1,除了乌头酸与文献报道的基于气质联用的选择离子监测方法的灵敏度相当,其余低含量代谢物的灵敏度提高了3.7-58.3倍。
实施例二
正常人血清样本葡萄糖能量代谢相关的重要代谢物检测
将-80℃保存的正常人血清样本解冻,涡旋10s,准确移取50μL,加入含内标的甲醇溶液200μL,涡旋1min。甲醇溶液中内标浓度分别为:乳酸-3,3,3-d3(100μg/mL),琥珀酸-2,2,3,3-d4(0.2μg/mL),富马酸-2,3-d2(0.1μg/mL),柠檬酸-2,2,4,4-d4(5μg/mL),葡萄糖-13C6,1,2,3,4,5,6,6-d7(150μg/mL)。4℃下14000rpm离心15min,取200μL上清溶液冷冻干燥。于冻干样本中加入50μL甲氧胺溶液(20mg.ml,吡啶),涡旋30s,超声1min,37℃水浴中反应1.5h;待反应结束,加入40μL N-甲基-N-(三甲基硅烷基)三氟乙酰胺,涡旋10s,37℃水浴中反应1h;反应完成后,4℃下14000rpm离心10min,取上清进行气相色谱-三重四级杆质谱联用仪器分析。
气相色谱条件:HP-5MS色谱柱(30m×0.25mm×0.25μm,Agilent Technologies,USA)。柱温采用程序升温,70℃保持1min,5℃/min升至190℃,15℃/min升至310℃,后平衡5min。进样口温度300℃,进样体积1μL,分流比1:5。氦气(99.9995%,China)作为载气,流速1.2mL/min, 恒流模式。质谱条件:EI源,-70eV,传输线和离子源温度分别是280℃和230℃。溶剂延迟时间5.5min。碰撞气为氮气,流速1.5mL/min;淬灭气为氦气,流速为2.25mL/min。采用多反应监测模式检测。
采用上述分析方法,得到正常人血清样本中葡萄糖能量代谢相关的重要代谢物和内标的总离子流图见图1及提取离子流图见图2。采用内标法定量,正常人血清样本中葡萄糖能量代谢相关的重要代谢物的含量分别如下:丙酮酸约0.92μg/mL,乳酸约149.67μg/mL,琥珀酸约0.20μg/mL,富马酸约0.08μg/mL,苹果酸约0.36μg/mL,2-羟基戊二酸约0.08μg/mL,2-酮戊二酸约0.07μg/mL,乌头酸约0.15μg/mL,柠檬酸约12.99μg/mL,异柠檬酸约0.37μg/mL,葡萄糖约737.91μg/mL。
发明效果:
本发明采用甲醇单相提取,结合三重四级杆多反应监测模式进行葡萄糖能量代谢相关的重要代谢物的高灵敏检测分析。与现有的文献报道的方法相比,具有以下几点优势:
1.本发明采用三重四级杆多反应监测模式进行血样样本中葡萄糖能量代谢相关的重要代谢物的高灵敏检测分析,之前未见该检测模式的文献报道;
2.通过离子对的选择及碰撞能的优化,实现了高低含量代谢物的一次进样同时分析;
3.采用多反应监测模式检测,极大地降低了干扰,实现了低含量的葡萄糖能量代谢相关的重要代谢物的高灵敏检测,除了乌头酸与文献报道的灵敏度相当,其余代谢物相对于文献报道灵敏度提高了3.7-58.3倍。
附表1
1:采用富马酸-2,3-d2校正;2:采用乳酸-3,3,3-d3校正;3:采用琥珀酸-2,2,3,3-d4校正;4:采用柠檬酸-2,2,4,4-d4校正;5:采用葡萄糖-13C6,1,2,3,4,5,6,6-d7校正。
- 还没有人留言评论。精彩留言会获得点赞!