生物剂量计及具有其的中子捕获治疗系统的制作方法
本发明一方面涉及辐射剂量测定领域,尤其涉及一种生物剂量计及其使用方法;本发明另一方面涉及一种辐射线照射领域,尤其涉及一种具有生物剂量计的中子捕获治疗系统。
背景技术:
随着科技的发展,核技术已被广泛应用在医学、工业、农业等各个领域,核技术在造福人类的同时也存在一定的核泄漏风险,危害公众健康同时也会对周围环境造成污染。因此有必要确定环境中放射线的剂量以进一步评估辐射剂量对人类或环境的影响,并针对环境中的辐射线剂量采取一定的控制措施。
中子捕获治疗作为一种有效的治疗癌症的手段在近年来的应用逐渐增加,其中以硼中子捕获治疗最为常见。供应硼中子捕获治疗的中子可以由核反应堆或加速器供应,载带有含10b的化合物在病灶处聚积,中子和含10b化合物发生如下反应:
该反应产生的能量摧毁病灶以实现治疗目的。在利用bnct技术进行疾病治疗过程中,中子剂量过低不能使病灶的含硼化合物充分和中子反应,并且病人需要接受辐射的时间较长;中子剂量过高往往伴随着伽马射线或其他辐射源的污染,对患者或医护人员的人身安全造成威胁,因此有必要有在进行中子照射之前对患者所接受的辐射剂量进行预先评估,以在患者受到最低辐射伤害的前提下完成对患者的治疗。
目前已知的生物剂量计主要利用辐射线对rna转录或者蛋白质表达的影响来测量生物分子所接受的剂量,但是这些技术通常需要进行细胞培养、蛋白质分离、计算等一系列复杂的步骤,操作流程繁杂,容易有误差。
技术实现要素:
为了提供一种步骤简化,操作简单并且能够准确测量辐射线剂量的生物剂量计,本发明一方面提供了一种生物剂量计,所述生物剂量计根据蛋白质在辐射场中的降解程度来测量所述蛋白质在辐射场中所接受的剂量。
蛋白质的降解程度可以根据本领域技术人员熟知地使用粘度法、凝胶过滤层析法、凝胶渗透色谱法、凝胶电泳法、光散射法、电喷雾离子化质谱技术(esi-ms)或基质辅助激光解吸电离质谱技术(maldi-ms)或其他能够测定蛋白质分子量的方法来测量经辐射线照射前后的蛋白质的分子量。
优选的是,所述生物剂量计中,用sds-凝胶电泳法测定蛋白质在经辐射线照射前后的分子量并计算蛋白质在辐射线照射后的降解程度。
本发明实施例用经辐射线照射后的蛋白质的分子量和辐射线照射前的蛋白质分子量的比值来量化蛋白质的降解程度。
优选地是,所述生物剂量计中,所述辐射场包括伽马辐射场、质子辐射场、重离子辐射场或者中子与伽马的混合辐射场。
所述生物剂量计通过如下步骤进行辐射剂量的测量。
1)绘制标准曲线的步骤:绘制辐射剂量和蛋白降解程度的标准曲线,再将待测辐射场中蛋白质的降解程度代入所述标准曲线对应的函数以获得蛋白质在待测辐射场中所受的辐射剂量,需要说明的是,通过标准曲线计算得到的辐射剂量是蛋白质在绘制标准曲线所使用的辐射场中的剂量,当待测的辐射场不同于绘制标准曲线所使用的辐射场时,需要将通过标准曲线计算出的剂量值换算成实际使用的待测的辐射场的剂量,具体操作需要通过实验计算出两种不同类型辐射场辐射剂量转换的系数,再根据所述系数将计算出的辐射剂量转换成实际使用的辐射场的剂量。
例如可以利用多组蛋白质在伽马辐射场中接受不同剂量的伽马射线辐照,测量并计算不同剂量伽马射线照射后的蛋白质在辐照前后的分子量和接受到的辐射剂量,其中在绘制标准曲线时,蛋白质在伽马辐射场接受到的辐射剂量用辐染胶片(例如radiochromicfilm或丙胺酸)进行测量,绘制并拟合标准曲线。
2)测量待测辐射场剂量的步骤:配置和上述步骤具有相同浓度的蛋白质溶液,并将其在未知强度的(待测)伽马辐射场、质子辐射场、重离子辐射场或者中子与伽马的混合辐射场中接受辐照,辐照后,测量蛋白质在辐照前后的分子量,计算其降解程度,将代表蛋白质降解程度的数值带入上述的标准曲线,计算得到蛋白质在待测辐射场中接受到的辐射剂量,该剂量是用伽马射线表示的,当待测辐射场是伽马辐射场,所述辐射剂量即可认为蛋白质在伽马辐射场所接受的实际剂量;当待测辐射场是质子辐射场,则需要通过实验计算伽马射线和质子辐射线之间强度换算的系数,进一步计算出在质子辐射场中,蛋白质在辐照时间内所接受到的实际剂量;同样的原理,利用蛋白质在伽马辐射场绘制得的标准曲线亦可用于测量其他种类辐射场的辐射剂量。
进一步优选的是,所述生物剂量计中,当需要测量的辐射场的剂量小于1000gy时,所述蛋白质选用对辐射线敏感的蛋白。
对辐射线敏感的蛋白是在接受1000gy的辐射剂量时,浓度低于1g/l的蛋白质在辐射后的分子量和辐射前蛋白质分子量的比值小于0.8的蛋白质,所述对辐射线敏感的蛋白质包括但不限于牛血清白蛋白(bsa)、卵清蛋白(ovalbumin)、过氧化氢酶(catalase)和转铁蛋白(transferrin)。
需要说明的是本发明实施例提供的生物剂量计能够测量的辐射剂量不限制于小于1000gy,当需要测量的辐射剂量高于1000gy时,可以根据具体待测的辐射场的辐射强度选择对辐射线具有不同敏感度的蛋白,如需要测量辐射剂量为1000gy~8000gy的辐射场时,可以选用酪蛋白在辐射场中的降解程度来测量其具体所受的辐射剂量,其中酪蛋白相对于牛血清白蛋白具有在辐射场更高的稳定性。
优选的是,当需要测量的辐射线剂量高于1000gy时,选用酪蛋白作为生物剂量计测量辐射场中的辐射剂量。
优选的是,所述生物剂量计中,所述蛋白质浓度为0.2g/l~0.6g/l的牛血清白蛋白溶液。
本发明实施例发现低浓度的蛋白质在辐射场中具有较好的灵敏度,其蛋白质的降解程度和辐射场强度具有较好的线性关系。
更进一步优选的是,所述生物剂量计中,所述0.2g/l~0.6g/l的牛血清白蛋白溶液用于测量的辐射剂量为100gy~500gy。
本发明实施例提供的由低浓度(如浓度小于1g/l)蛋白质构成的生物剂量计在测量低剂量的辐射场时具有较高的灵敏度和准确率。当需要测量辐射强度较高的辐射场时,亦可以选用浓度高于1g/l的蛋白溶液绘制标准曲线;或者在使用低浓度的蛋白质作为生物剂量计时,所述低浓度蛋白在高强度的辐射场中接受短时间的辐照,本领域技术人员熟知地,在强度一定的辐射场中,辐照时间越长蛋白质接受的辐射剂量越多,相反,辐照时间越短蛋白质接受的辐射剂量越少。因此可以通过改变蛋白质在辐射场中的照射时间来减少蛋白质接受到的辐射剂量,可以利用较低浓度的蛋白质绘制的标准曲线以提高剂量测量灵敏度。
本发明另一方面提供了所述生物剂量计的使用方法,所述生物剂量计通过如下步骤进行辐射剂量的测量:
绘制标准曲线的步骤:配置多组蛋白质溶液,将所述蛋白质溶液分别置于辐射场中并受到不同剂量辐射线的辐射,终止辐射、测定每组蛋白质溶液接受的辐射剂量并分析辐照后的蛋白质降解程度,绘制并拟合辐射剂量和蛋白质降解程度的标准曲线;
测量待测辐射场剂量的步骤:配置和上述步骤中相同浓度的蛋白质溶液,将蛋白质溶液置于待测辐射环境中接受辐射,终止辐射并测定辐射后蛋白质的降解程度,将能够反映蛋白质降解程度的数值带入上述标准曲线计算蛋白质在经辐射线照射的时间内所受到辐射剂量。
优选的是,所述使用方法中,当通过测量待测辐射场剂量的步骤计算得到的辐射剂量不在绘制标准曲线时所使用的辐射剂量的范围内时,可通过在测量待测辐射场剂量的步骤里调整蛋白质溶液接受辐射线照射时间以使所述蛋白质溶液接受到的辐射剂量在绘制标准曲线使所使用的辐射剂量的范围内,从而进一步提高测量待测辐射场剂量的精准度。
进一步优选的是,所述使用方法中,所述蛋白质溶液为浓度为0.2g/l~0.6g/l的牛血清白蛋白溶液。
本发明第三方面为了测量中子捕获治疗过程中的中子强度,提供了一种中子捕获治疗系统,所述中子捕获治疗系统包括中子源、射束整形体、准直器和如上所述的任一种生物剂量计,其中所述中子源用于产生中子射束,所述射束整形体位于所述中子源后部并将所述中子源产生的具有较宽能谱的中子射束中的快中子调整为超热中子,所述准直器位于射束整形体后部用于汇聚所述超热中子并使超热中子射束照射至特定的空间位置以实现精准治疗,所述生物剂量计用于在准直器后部测量生物剂量计所处位置的辐射剂量。其中,超热中子能区在0.5ev到40kev之间,快中子能区大于40kev。
优选的是,所述中子捕获治疗系统中,所述生物剂量计位于超热中子射束照射至的特定空间位置,并可以在患者进行中子捕获治疗之前测量待接受的辐射剂量,也可以在中子捕获治疗过程中对照射室内的辐射剂量进行监控。
进一步优选的是,所述中子捕获治疗系统中,所述中子源为加速器中子源或反应堆中子源。
更进一步优选的是,所述中子捕获治疗系统中,所述射束整形体包括反射体和缓速体,其中所述反射体包围所述缓速体,用于将向射束整形体外扩散的中子反射回所述缓速体中,所述缓速体用于将快中子缓速为超热中子。
本发明实施例提供的生物剂量计是利用蛋白质在辐射场中的降解程度来测量未知强度辐射场的辐射剂量,以进一步评估或调控辐射场强度;本发明实施例提供的生物剂量计灵敏度高,操作简单,除了能够检测环境中低剂量的辐射泄漏,也能应用于中子捕获治疗系统中对中子剂量的进行预估和调节。
附图说明
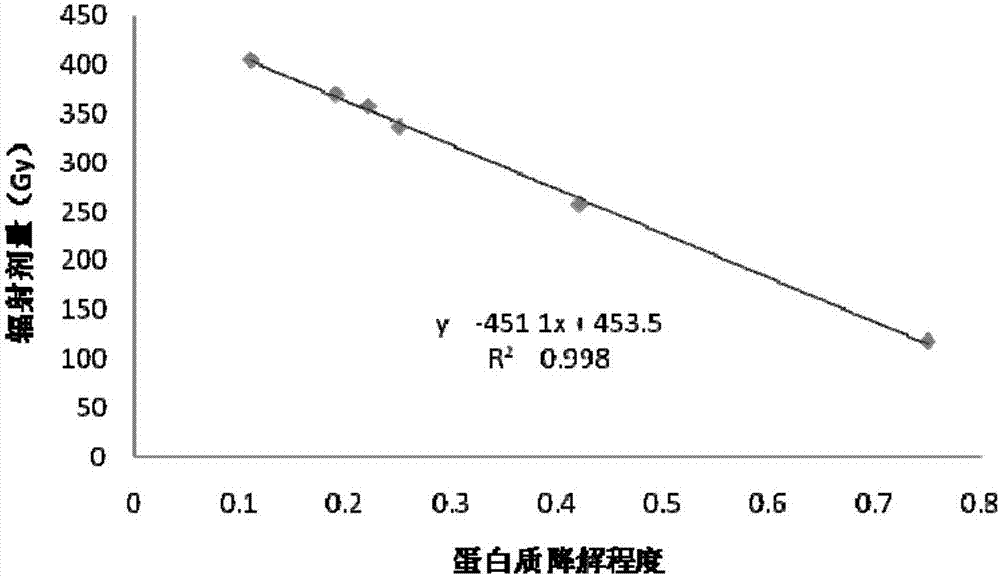
图1是浓度为0.3g/l的牛血清白蛋白溶液在伽马辐射场中的标准曲线;
图2是浓度为0.2g/l的牛血清白蛋白溶液在伽马辐射场中的标准曲线;
图3是浓度为0.5g/l的牛血清白蛋白溶液在伽马辐射场中的标准曲线;
图4是浓度为0.6g/l的牛血清白蛋白溶液在伽马辐射场中的标准曲线;
图5是含有生物剂量计的中子捕获治疗系统。
具体实施方式
下面结合附图对本发明做进一步的详细说明,以令本领域技术人员参照说明书文字能够据以实施。应理解,上述简述和下文的详述为示例性且仅用于解释,而不对本发明主题作任何限制。
应当理解,本文所使用的诸如“具有”、“包含”以及“包括”术语并不排除一个或多个其它成分或其组合的存在或添加。
为了清楚的说明本发明的技术方案,对本发明中出现的名词做如下定义:
蛋白质的降解程度为蛋白质在接受辐照前后分子量的比值;
将蛋白质在待测辐射场中的降解程度的数值带入标准曲线计算出的值叫做辐射剂量;
当待测辐射场不同于绘制标准曲线所使用的辐射场时,所述辐射剂量叫做相对剂量;
当待测辐射场和绘制标准曲线所使用的辐射场属于同一种辐射场时,所述辐射剂量叫做实际剂量。
本发明提供的生物剂量计利用蛋白质在辐射场中的降解程度可以测量多种辐射场(包括混合辐射场)的辐射剂量,生物剂量计的使用方法包括两个步骤:
绘制标准曲线的步骤:配置多组蛋白质溶液,将所述蛋白质溶液分别置于辐射场中并受到不同剂量辐射线的辐照,终止辐射、测定每组蛋白质溶液接受的辐射剂量并分析辐照后的蛋白质降解程度,绘制并拟合辐射剂量和蛋白质降解程度的标准曲线;
测量待测辐射场剂量的步骤:配置和上述步骤中相同浓度的蛋白质溶液,将蛋白质溶液置于待测辐射环境中接受辐射,终止辐射并测定辐射后蛋白质的降解程度,将能够反映蛋白质降解程度的数值代入上述标准曲线计算蛋白质在经辐射线照射的时间内所受到的辐射剂量。
下面通过实施例并结合附图具体说明生物剂量计的使用以及生物剂量计标准曲线的绘制:
<实施例1>生物剂量计标准曲线的绘制
本发明提供的生物剂量计绘制的标准曲线可以根据蛋白质在任何种类的辐射场中的降解程度来绘制,本实施例以牛血清白蛋白在伽马辐射场中的降解程度来绘制标准曲线以举例说明标准曲线的绘制方法。
不同浓度的蛋白质在辐射场中的降解程度不同,蛋白质浓度是影响其在辐射场中降解程度的一个因素,下面以不同浓度的蛋白质在伽马辐射场中的降解程度绘制的标准曲线来进一步说明。
浓度为0.3g/l的牛血清白蛋白溶液在伽马辐射场中标准曲线的绘制:
将0.03g的bsa溶于100g蒸馏水中配置浓度为0.3g/l的bsa溶液,将所述bsa溶液混合均匀并分成若干等份,取其中6份bsa溶液置于伽马辐射场中接受不同剂量伽马辐射线的辐照并用gafchromicfilm测量每份bsa溶液在辐射场中所受到的剂量为118gy、258gy、337gy、358gy、370gy和405gy。
分别将未经辐射线照射的蛋白质和在辐射场中接受不同剂量照射的蛋白质经sds-凝胶电泳并结合imagej计算其分子量,辐照后的蛋白质的分子量和辐照前蛋白质的分子量的比值用来描述蛋白质在该辐射剂量的作用下的降解程度。结果如表1所示:
表1、0.3g/l的牛血清白蛋白在不同剂量伽马辐射线作用下的降解程度
通过以上实验数据,拟合出蛋白质降解程度和蛋白质所接受的辐射剂量之间的函数曲线如附图1所示,从图1所示的0.3g/l的牛血清白蛋白拟合的标准曲线可以看出在辐射剂量为118gy~405gy的范围内,蛋白质的降解程度和其对应的辐射剂量之间呈现较好的线性关系。
同样的方法和步骤分别计算浓度为0.2g/l、0.5g/l、0.6g/l的牛血清白蛋白溶液在伽马辐射场中的降解程度分别如表2、表3、表4所示:
表2、0.2g/l的牛血清白蛋白在不同剂量伽马辐射线作用下的降解程度
表3、0.5g/l的牛血清白蛋白在不同剂量伽马辐射线作用下的降解程度
表4、0.6g/l的牛血清白蛋白在不同剂量伽马辐射线作用下的降解程度
表5、0.1g/l的牛血清白蛋白在不同剂量伽马辐射线作用下的降解程度
表6、1g/l的牛血清白蛋白在不同剂量伽马辐射线作用下的降解程度
根据表2~表4的实验数据分别绘制如图2~图4所示的不同浓度蛋白质在辐射场降解程度的标准曲线,从图中可知不同浓度的蛋白质在辐射场中降解程度和其接受的辐射剂量成较好的线性关系。
表5和表6是浓度分别为0.1g/l和1g/l的牛血清白蛋白在不同剂量伽马辐射线作用下的降解程度,从这两个表格的数据可以发现蛋白质在辐射场中的降解程度和其接受的辐射剂量具有线性关系,说明浓度低于0.2g/l的蛋白质溶液或浓度高于0.6g/l的蛋白质溶液也都可以作为生物剂量计使用。
标准曲线可以用来检测相同浓度的蛋白质在未知强度、未知种类辐射场的辐射剂量,代入标准曲线计算得到的辐射剂量是用伽马射线的剂量来表示的,当未知种类的辐射场为伽马辐射场时,所计算得到的辐射剂量和待测辐射场中蛋白质实际受到的辐射剂量相同;当未知种类的辐射场不是伽马辐射场时,所计算得到的辐射剂量是蛋白质在未知辐射场中的相对剂量,需要通过实验计算出伽马辐射场和待测辐射场之间的转换系数进一步计算。
<实施例2>生物剂量计测量中子和伽马混合辐射场实际辐射剂量的方法
用生物剂量计测量辐射场强度时可以事先以待测辐射场的种类做蛋白质降解程度和辐射剂量之间的标准曲线,也可以使用非待测辐射场做的标准曲线并利用待测辐射场和标准曲线所使用之辐射场的转换系数来测量待测辐射场的实际辐射剂量。
辐射场之间的转换系数需要通过实验进一步确认,本实施例以伽马辐射场和中子辐射场之间转换系数的计算方法为例说明不同辐射场之间转换系数的计算方法。
如<实施例1>的实验步骤配置某一特定浓度的蛋白质溶液,并使所述蛋白质溶液置于伽马辐射场中接受不同剂量(dγ1、dγ2……dγn)伽马射线的辐照,分别计算蛋白质在dγ1、dγ2……dγn辐射剂量下的降解程度x1、x2……xn。
配置上述特定浓度的蛋白质溶液,将其置于中子辐射场中进行辐照,当位于中子辐射场中的蛋白质降解程度分别和位于伽马辐射场中的蛋白质降解程度一致时(也即蛋白质在中子辐射场的降解程度分别为x1、x2……xn时)读取蛋白质所接受的中子剂量dn1、dn2、……dnn。
设定蛋白质在某一特定降解程度时伽马剂量和中子剂量的比值为该降解程度蛋白质对应的中子和伽马之间的转换系数:
ki=dγi/dni,(其中i取值于1~n)
绘制蛋白质降解程度和在该降解程度对应的转换系数之间的曲线,拟合所述曲线的函数:
ki=f(xi)
在用伽马辐射场做的标准曲线计算出蛋白质在中子辐射场的相对辐射剂量时,先根据蛋白质的降解程度带入函数ki=f(xi)计算出该降解程度下的转换系数,再根据转换系数和通过标准曲线计算得到的相对辐射剂量计算蛋白质在中子辐射场中实际所受的中子辐射剂量,蛋白质在中子辐射场中实际所受的中子辐射剂量为所述相对辐射剂量和所述转换系数的比值。
本实施例中蛋白质在辐射场中所受的剂量用radiochromicfilm进行测量计算,也可以根据本领域技术人员熟知地用其他能够测量蛋白质在辐射场所接受辐射剂量的其他方法进行测量。
当待测辐射场为中子和伽马混合辐射场并且所述标准曲线是利用蛋白质在伽马辐射场中的降解程度来绘制时,通过生物剂量计计算出某一蛋白质降解程度xi对应的辐射剂量为蛋白质在伽马辐射场中的相对辐射剂量di,其中di=mj+nj,其中,mj是伽马剂量,nj为中子相对于伽马的等效剂量,其中所述伽马剂量mj可以通过蒙地卡罗计算出来,蛋白质实际所受的中子剂量为中子相对于伽马等效剂量和所述在该蛋白质降解浓度下转换系数(ki)的比值。
<实施例3>包含有生物剂量计的中子捕获治疗系统
本发明实施例提供的生物剂量计用于检测辐射线剂量,不仅可以用来检测环境中辐射污染,也可以用于中子捕获治疗系统中对中子射束的强度或剂量进行预估以指导治疗过程。
中子捕获治疗作为一种有效的治疗癌症的手段近年来的应用逐渐增加,其中以硼中子捕获治疗最为常见,供应硼中子捕获治疗的中子可以由核反应堆或加速器供应。本发明的实施例以加速器硼中子捕获治疗为例,加速器硼中子捕获治疗的基本组件通常包括用于对带电粒子(如质子、氘核等)进行加速的加速器、靶材与热移除系统和射束整形体,其中加速带电粒子与金属靶材作用产生中子,依据所需的中子产率与能量、可提供的加速带电粒子能量与电流大小、金属靶材的物化性等特性来挑选合适的核反应,常被讨论的核反应有7li(p,n)7be及9be(p,n)9b,这两种反应皆为吸热反应。两种核反应的能量阀值分别为1.881mev和2.055mev,由于硼中子捕获治疗的理想中子源为kev能量等级的超热中子,理论上若使用能量仅稍高于阀值的质子轰击金属锂靶材,可产生相对低能的中子,不须太多的缓速处理便可用于临床,然而锂金属(li)和铍金属(be)两种靶材与阀值能量的质子作用截面不高,为产生足够大的中子通量,通常选用较高能量的质子来引发核反应。
理想的靶材应具备高中子产率、产生的中子能量分布接近超热中子能区(将在下文详细描述)、无太多强穿辐射产生、安全便宜易于操作且耐高温等特性,但实际上并无法找到符合所有要求的核反应,本发明的实施例中采用锂金属制成的靶材。但是本领域技术人员熟知的,靶材的材料也可以由其他除了上述谈论到的金属材料之外的金属材料制成。
针对热移除系统的要求则根据选择的核反应而异,如7li(p,n)7be因金属靶材(锂金属)的熔点及热导系数差,对热移除系统的要求便较9be(p,n)9b高。本发明的实施例中采用7li(p,n)7be的核反应。
无论硼中子捕获治疗的中子源来自核反应堆或加速器带电粒子与靶材的核反应,产生的皆为混合辐射场,即射束包含了低能至高能的中子、光子;对于深部肿瘤的硼中子捕获治疗,除了超热中子外,其余的辐射线含量越多,造成正常组织非选择性剂量沉积的比例越大,因此这些会造成不必要剂量的辐射应尽量降低。除了空气射束品质因素,为更了解中子在人体中造成的剂量分布,本发明的实施例中使用人体头部组织假体进行剂量计算,并以假体射束品质因素来作为中子射束的设计参考,将在下文详细描述。
国际原子能机构(iaea)针对临床硼中子捕获治疗用的中子源,给定了五项空气射束品质因素建议,此五项建议可用于比较不同中子源的优劣,并供以作为挑选中子产生途径、设计射束整形体时的参考依据。这五项建议分别如下:
超热中子射束通量epithermalneutronflux>1x109n/cm2s
快中子污染fastneutroncontamination<2x10-13gy-cm2/n
光子污染photoncontamination<2x10-13gy-cm2/n
热中子与超热中子通量比值thermaltoepithermalneutronfluxratio<0.05
中子电流与通量比值epithermalneutroncurrenttofluxratio>0.7
注:超热中子能区在0.5ev到40kev之间,热中子能区小于0.5ev,快中子能区大于40kev。
1、超热中子射束通量:
中子射束通量和肿瘤中含硼药物浓度共同决定了临床治疗时间。若肿瘤含硼药物浓度够高,对于中子射束通量的要求便可降低;反之,若肿瘤中含硼药物浓度低,则需高通量超热中子来给予肿瘤足够的剂量。iaea对于超热中子射束通量的要求为每秒每平方厘米的超热中子个数大于109,此通量下的中子射束对于目前的含硼药物而言可大致控制治疗时间在一小时内,短治疗时间除了对病人定位和舒适度有优势外,也可较有效利用含硼药物在肿瘤内有限的滞留时间。
2、快中子污染:
由于快中子会造成不必要的正常组织剂量,因此视之为污染,此剂量大小和中子能量呈正相关,因此在中子射束设计上应尽量减少快中子的含量。快中子污染定义为单位超热中子通量伴随的快中子剂量,iaea对快中子污染的建议为小于2x10-13gy-cm2/n。
3、光子污染(γ射线污染):
γ射线属于强穿辐射,会非选择性地造成射束路径上所有组织的剂量沉积,因此降低γ射线含量也是中子束设计的必要要求,γ射线污染定义为单位超热中子通量伴随的γ射线剂量,iaea对γ射线污染的建议为小于2x10-13gy-cm2/n。
4、热中子与超热中子通量比值:
由于热中子衰减速度快、穿透能力差,进入人体后大部分能量沉积在皮肤组织,除黑色素细胞瘤等表皮肿瘤需用热中子作为硼中子捕获治疗的中子源外,针对脑瘤等深层肿瘤应降低热中子含量。iaea对热中子与超热中子通量比值建议为小于0.05。
5、中子电流与通量比值:
中子电流与通量比值代表了射束的方向性,比值越大表示中子射束前向性佳,高前向性的中子束可减少因中子发散造成的周围正常组织剂量,另外也提高了可治疗深度及摆位姿势弹性。iaea对中子电流与通量比值建议为大于0.7。
利用假体得到组织内的剂量分布,根据正常组织及肿瘤的剂量-深度曲线,推得假体射束品质因素。如下三个参数可用于进行不同中子射束治疗效益的比较。
1、有效治疗深度:
肿瘤剂量等于正常组织最大剂量的深度,在此深度之后的位置,肿瘤细胞得到的剂量小于正常组织最大剂量,即失去了硼中子捕获的优势。此参数代表中子射束的穿透能力,有效治疗深度越大表示可治疗的肿瘤深度越深,单位为cm。
2、有效治疗深度剂量率:
即有效治疗深度的肿瘤剂量率,亦等于正常组织的最大剂量率。因正常组织接收总剂量为影响可给予肿瘤总剂量大小的因素,因此参数影响治疗时间的长短,有效治疗深度剂量率越大表示给予肿瘤一定剂量所需的照射时间越短,单位为cgy/ma-min。
3、有效治疗剂量比:
从大脑表面到有效治疗深度,肿瘤和正常组织接收的平均剂量比值,称之为有效治疗剂量比;平均剂量的计算,可由剂量-深度曲线积分得到。有效治疗剂量比值越大,代表该中子射束的治疗效益越好。
为了使射束整形体在设计上有比较依据,除了五项iaea建议的空气中射束品质因素和上述的三个参数,本发明实施例中也利用如下的用于评估中子射束剂量表现优劣的参数:
1、照射时间≤30min(加速器使用的质子电流为10ma)
2、30.0rbe-gy可治疗深度≥7cm
3、肿瘤最大剂量≥60.0rbe-gy
4、正常脑组织最大剂量≤12.5rbe-gy
5、皮肤最大剂量≤11.0rbe-gy
注:rbe(relativebiologicaleffectiveness)为相对生物效应,由于光子、中子会造成的生物效应不同,所以如上的剂量项均分别乘上不同组织的相对生物效应以求得等效剂量。
下面结合附图进一步说明包含有生物剂量计的中子捕获治疗系统:图5所示的中子捕获治疗系统中的中子源为加速器中子源,其中加速器10产生的带电粒子形成带电粒子束p,带电粒子束撞击中子产生装置20里的靶t,形成包含热中子、快中子和超热中子的混合辐射场,所述混合辐射场在射束整形体30内依次经过反射体31将向四周扩散的中子反射回所述混合辐射场、缓速体32缓速以及热中子吸收体33吸收能量较低的热中子后,形成以超热中子为主的中子束流n,中子束流经准直器40汇聚以准确照射患者待照射部位,另外为了防止射束整形体30内的辐射线扩散出去,在射束整形体30的后部紧邻射束出口处设置一个辐射屏蔽体34。
在治疗过程中防止辐射线对人体其他正常组织造成伤害往往需要在照射中子束之前对患者在照射室内进行定位,如图5所示,在进行中子照射之前,先将患者待照射部位根据通过准直器的中子射束的方向进行预定位至中子射束方向上x轴和y轴交叉点以实现精准照射。
为了评估中子射束在照射室内患者待治疗部位的中子辐射剂量,需要在照射室内的所述预定位位置处设置一个生物剂量计a,所述生物剂量计用于测量中子射束方向上x轴和y轴交叉点处的辐射剂量,生物剂量计所处的辐射场是中子和伽马混合辐射场,通过生物剂量计根据蛋白质在所述交叉点处的降解程度带入标准曲线计算出的剂量是蛋白在制作标准曲线所使用的辐射场的相对辐射剂量,需要根据<实施例2>的方法分别计算混合辐射场中的中子剂量和伽马剂量。
生物剂量计a除了位于图5所示的位置外,还可以位于照射室其他位置处用于测量生物剂量计所处位置处的辐射场的剂量,由于生物剂量计使用起来简单轻巧,因此可以位于照射室内任意位置处以评价该位置的辐射剂量,进一步判断和控制照射室内的辐射污染,由此可见生物剂量计在中子捕获系统中具有重要意义。
本发明揭示的生物剂量计及中子捕获治疗系统并不局限于以上实施例所述的内容以及附图所表示的结构。在本发明的基础上所做的显而易见地改变、替代或者修改,都在本发明要求保护的范围之内。
- 还没有人留言评论。精彩留言会获得点赞!