一种乙肝疫苗接种效果快速评价试剂盒的制作方法
本实用新型涉及生物检测技术领域,具体涉及一种乙肝疫苗接种效果快速评价试剂盒。
背景技术:
乙型肝炎病毒是一种直径为42nm,属嗜肝DNA病毒科,是一种双链、有包膜的病毒。HBsAg是病毒包膜上的一种脂蛋白,可在血液中循环,呈球状和管状颗粒,直径为22nm。HBsAg含有中和表位,即α抗原决定簇。
人类是乙型肝炎病毒的唯一宿主,乙型肝炎病毒感染人体后,可产生一个广泛的疾病谱,包括无症状感染、急性乙型肝炎和慢性乙型肝炎。人感染乙型肝炎病毒后所形成的慢性感染,可进一步发展成为慢性肝炎,最终会导致肝硬化和肝癌。急性乙肝见于约1%的围产期HBV感染、10%的幼年期(1~ 5岁)HBV感染和30%的其他年龄段(>5岁)HBV感染。爆发型感染见于0.1%~ 0.6%的急性肝炎病例,其病死率约为70%。慢性HBV感染的发生与感染年龄呈负相关,占围产期HBV感染者的80%~90%,占幼儿期(<6岁)HBV感染者的30%,占无其他疾病的成年感染者的<5%。
急性乙型肝炎的临床表现与其他病毒性肝炎难于区别,其确诊需依据血清学试验的结果。从暴露于传染源到黄疸发生的平均潜伏期为90天(范围: 60~150天);从暴漏于传染源到血清丙氨酸氨基转移酶(ALT)异常的平均潜伏期为60天(范围:40~90天)。急性乙型感染前驱期的表现是多样的,其特征表现为不适、厌食、恶心、呕吐、低热、肌痛和易疲劳等症状。在前驱期。5%~10%的患者可出现关节痛或关节炎、皮疹和血管性水肿。伴有黄疸的肝炎病例,黄疸症状通常出现在发病后的1~2周内;茶色尿、陶土色大便发生在黄疸症状出现前的1~5天内。在黄疸期,由于肝脏的轻度肿大,其前驱症状通常表现为消瘦和右上腹部疼痛。10%~30%的急性乙型肝炎病例可以在没有黄疸和其他临床表现的情况下出现肌痛或关节痛,1/3的疾病可出现斑丘疹。急性乙型肝炎的临床症状通常在1~3个月内消失。
慢性HBV感染者有15%~25%可能会因罹患HBV相关的肝硬化和HCC而过早死亡。临床上不可能将乙型肝炎同由其他病毒因子引起的肝炎鉴别开来。因此,必须通过实验室检测来证实诊断。从血清学的角度上来看,急性HBV 感染的特征是存在HBsAg和IgM型抗核心抗原抗体(IgM型抗HBc)。在感染初期,病毒大量复制,病人血清中亦可呈乙肝e抗原(HBeAg)阳性。抗 HBsAg抗体(抗HBs)可于数周后出现,通常IgG型抗HBs用作免疫力的标志物,随之HbsAg被清除。慢性感染的特征是HbsAg(同时可伴有或不伴有 HBeAg)持续存在(>6个月)。HBsAg的持续存在是发生慢性肝病并在生命晚期进展为肝细胞癌的主要危险性标志。HBeAg的存在则提示HBV携带者为血液和体液具有高度的传染性。
目前乙型肝炎还没有明确有效的治疗方法,预防乙肝感染最有效的方法是接种乙肝表面抗原疫苗,乙肝疫苗接种所形成的保护性效力与抗HBs的诱导相关,但也涉及记忆T细胞的诱导。基础免疫最后一针注射后1~3个月,如测得抗体滴度≥10mIU/ml,则可视为集体已对HBV感染具备了抵御能力。完成3针基础免疫后,在95%的婴儿、儿童和年轻成人中可诱导出达到保护性的抗体水平。在40岁以后的成人中,抗体应答率逐渐下降。对于3针基础免疫无应答者(即抗HBs滴度未达到≥10mIU/ml),复种3针后几乎都能诱导出抗体应答。WHO关于“乙型肝炎疫苗”的立场文件中建议对一些高危人群开展接种后免疫力检测。检测应在接种完最后一针乙肝疫苗1~2个月后进行,使用能确定抗HBs保护性滴度(≥10mIU/ml)的方法。欧洲乙肝免疫共识小组建议,免疫功能低下者应每年接受一次检测,评估抗HBs滴度。全程基础免疫结束后,如受种者体内抗HBs滴度<10mIU/ml,应予复种。复种计3针次,在接种完第3针1~2个月后检测抗HBS抗体。
免疫规划工作一直以来都是我国政府工作的重点之一,儿童的预防免疫关乎其一生的健康,疫苗接种、疾病预防远比疫病的治疗更为重要。由于个体免疫水平的差异、疫苗质量、接种程序的规范与否以及随时间推移抗体水平的逐渐下降等原因,疫苗接种后,大部分人群获得了免疫保护,但仍有部分人群由于以上原因导致抗体水平低下,无法抵御相关传染病的侵袭。开展抗体检测,对抗体水平不足的人群进行有针对性的补种,对有效形成免疫屏障、预防传染病的发生、保护相关人群的健康有着十分重要的意义。我国经过多年的努力,计划免疫已取得相当的成就,但疫苗接种后相关对应的抗体水平检测、疫苗接种后免疫效果的评价等工作相对滞后,目前国家已加强了这方面的工作安排部署。
为适应市场、各级临床医院及各级疾病控制中心开展抗体检测的需求,经过努力,我们研制出了适合于全血、血清、血浆样品的乙型肝炎病毒表面抗体诊断试剂盒(胶体金法),试剂盒稳定,其最低检测限为10mIU/ml,有效期达到一年半,每次检测仅需5微升全血、血清/血浆。
本试剂盒适用于乙肝病毒表面抗体的筛查,筛查结果可应用于接种乙型肝炎病毒疫苗后人群产生乙型肝炎病毒抗体阳性率的检测、乙型肝炎相关流行病学调查、个体乙型肝炎病毒易感性的判定。
评价疫苗免疫效果最可靠的方法就是检测接种者体内血清中的特异抗体的含量。当前市场上检测乙肝病毒表面抗体的商品化试剂盒多采用酶联免疫法和化学发光法,这些方法虽然灵敏度高、结果准确、化学发光试剂还可以对抗体进行定量,但在实际操作上存在诸多不便,如步骤复杂、耗时较长,还需使用特定的仪器设备;试剂盒需4℃保存;对样品要求静脉采血等,不易在基层普及运用。
免疫胶体金快速诊断技术是建立在酶联免疫吸附试验、乳胶凝集试验、单克隆抗体技术和免疫胶体金标记技术基础上,以胶体金为标记物,利用特异的抗原抗体反应放大反应信号,通过直接观察就可以判定结果的新技术。该技术具有简单、快速、准确和无污染等优点,在临床医学检测、动物医学检测、激素检测、食品安全检测、药物残留和毒品快速检测等诸多诊断领域迅速发展。目前,胶体金标记快速检测抗体的方法大体分为两种:一种是将抗原标金,待测抗体的抗体划膜;另一种是将抗原划膜,待测抗体的抗体标金。现有研究表明:因为抗体蛋白性质较为稳定,所以对抗体蛋白的胶体金标记较为稳定,上述第一种方法所述的抗原的胶体金标记则存在颇多问题,因为抗原多为病毒类,性质多样,有的大小甚至比胶体金颗粒还大,且稳定性较差,因此很难直接将抗原标记在胶体金颗粒上;即使勉强能将抗原标记上,也需要抗原达到极高的纯度,而对抗原病毒的纯化是一项难度较大、成本较高的工程;也有人寻找抗原的重组抗原来代替这些天然抗原,但是很多抗原很难寻到能替代的重组抗原,而且即使有,成本也是极高的,因此上述第一种方法的局限性比较高。上述的第二种方法是将抗原进行划膜,这种方法使用待测抗体的抗体进行金标记,可以避免抗原金标记的问题,但将抗原划到膜上发生反应,需要抗原具有较高的浓度和纯度,这也增加了产品生产的成本和难度;另外将抗原划到膜上,由于抗原稳定性较差,很难长时间保存,检测试纸的有效期极短。这些都是限制抗体快速检测类试剂盒快速发展的原因。
技术实现要素:
本实用新型所要解决的技术问题是提供一种乙肝疫苗接种效果快速评价试剂盒,解决采用胶体金标记时抗原的颗粒大,纯度要求高以及采用抗原划膜时,由于抗原稳定性差,很难长时间保存,检测试纸的有效期极短的问题。
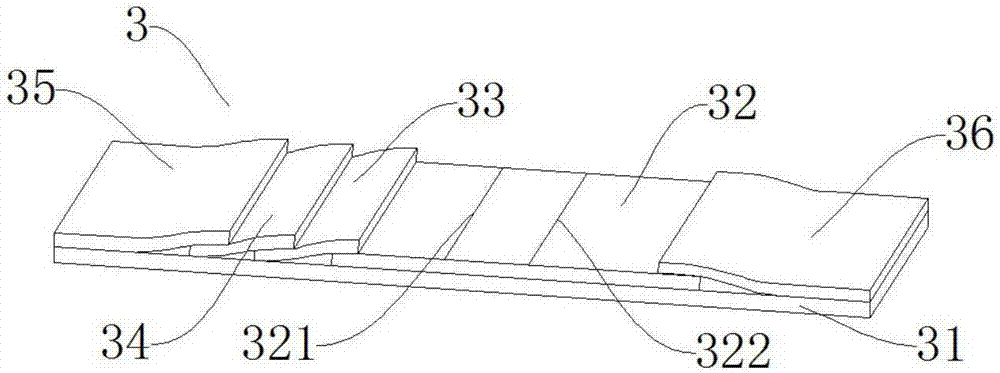
本实用新型解决上述技术问题的技术方案如下:一种乙肝疫苗接种效果快速评价试剂盒,包括包装盒、样品稀释液盛装容器和检测试纸;所述包装盒包括盒体和盖体,所述盒体内设有第一隔板,所述第一隔板将所述盒体分为第一容纳腔和第二容纳腔,所述检测试纸设于所述第一容纳腔内,所述样品稀释液盛装容器设于所述第二容纳腔内;所述盖体包括第一盖体和第二盖体,所述第一盖体设于所述第一容纳腔的上方,所述第二盖体设于所述第二容纳腔的上方;所述第一容纳腔内设有若干个第二隔板,若干个所述第二隔板分别与所述盒体的外壁围成第三容纳腔,所述第三容纳腔内填充有干燥剂;所述第二隔板上设有多个直径小于干燥剂粒径的透气孔;所述第一容纳腔内设有多个第一圆筒,所述第一盖体上设有多个与所述第一圆筒相匹配的第一凸起;所述检测试纸包括包被膜、标记物结合垫和抗原垫;所述抗原垫上包被有乙肝病毒表面抗原,所述标记物结合垫上包被有胶体金标记的鼠抗乙肝病毒表面抗原单克隆抗体,所述包被膜上固定有检测T线和质控C线,所述检测T线上包被有鼠抗人IgG抗体,所述质控C线上包被羊抗鼠IgG抗体;所述检测试纸的最低检测线为10mIU/ml。
本实用新型的有益效果是:所采用的检测试纸,通过引进乙肝病毒表面抗原垫,同时在抗原垫中加入抗原保护液,解决了乙肝病毒表面抗原由于稳定性差而不容易被金标记的问题;另一方面,采用的乙肝病毒表面抗原为粗抗原,在检测试纸反应层析过程中,已经通过双抗体夹心法对粗抗原进行了筛选和纯化,保证了试剂反应的特异性,因此不需对粗抗原进一步纯化就能达到反应效果,制备成本低,利用推广应用。另采用的乙肝疫苗接种效果快速评价试剂盒将样品稀释液盛装容器和检测试纸均设于包装盒内,用户在使用时,无需另外准备样品稀释液,使用更加方便,且样品稀释液盛装容器和检测试纸分别置于试剂盒的两个容纳腔中,且均对应的设置一个盖体,使试剂盒的结构更加紧凑,另用户在使用时只需打开第二盖体即可取出样品稀释液,不会对检测试纸造成干扰;另在包装盒内放有干燥剂,可吸收试剂盒内的湿气、氧气,有效延长试剂瓶储存诊断试剂的保存期限;另将试剂盒的灵敏度设置为10mIU/ml,可实现对乙肝疫苗接种效果的快速评估。
进一步:所述第二隔板的数量为两个,两个所述的第二隔板分别设于所述第一容纳腔的前端和后端。
上述进一步方案的有益效果是:通过设置两个第二隔板,进一步的设置有两个第三容纳腔,且每个第三容纳腔内均放有干燥剂,加强对湿气、氧气的吸收。
进一步:所述第一容纳腔内还设有用于固定所述检测试纸的定位装置。
上述进一步方案的有益效果是:通过定位装置可将检测试纸锁紧在第一容纳腔中,防止其左右晃动。
进一步:所述定位装置包括定位组件和活动组件,所述定位组件和所述活动组件分别设于所述第一容纳腔的左端和右端;所述定位组件包括底板和 U型定位块,所述底板固定于所述盒体上;所述U型定位块固定于所述底板的上方,且所述U型定位块的开口端朝向所述活动组件;所述活动组件包括固定板、活动板和铜片,所述固定板固定于所述盒体上;所述铜片的一端嵌设于所述固定板中,所述铜片的另一端抵设于所述活动板上,所述活动板可在所述盒体内移动。
上述进一步方案的有益效果是:定位组件主要用于对检测试纸的放置位置进行定位,活动组件可根据检测试纸的具体大小进行调整,是检测试纸能够卡紧在包装盒中,避免其左右晃动。
进一步:所述活动板的底部设有若干个凸起,所述盒体的底部设有若干个与所述凸起相匹配的滑槽。
上述进一步方案的有益效果是:活动板的底部设置凸起,且在盒体上设置与所述凸起相匹配的滑槽,可对活动板在盒体内的移动进行导向,防止活动板的偏移。
进一步:所述第一盖体上的加样口的底部向下延伸形成第三圆筒。
上述进一步方案的有益效果是:第三圆筒起到导流的作用,可防止添加样品或添加样品稀释液时,液体到处散溅,且能够保证添加的样品稀释液与样品的位置一致,起到良好的稀释作用。
进一步:所述第二容纳腔内设有第二圆筒,所述第二圆筒用于放置所述样品稀释液盛装容器。
上述进一步方案的有益效果是:将样品稀释液盛装容器卡设于第二圆筒内,使样品稀释液盛装容器的放置更加平稳。
进一步:所述标记物结合垫为玻璃纤维。
进一步:所述抗原垫为玻璃纤维、无纺布或聚酯膜。
上述进两步方案的有益效果是:使样品加入到检测试纸上后,可通过静电作用和疏水相互作用等物理作用与蛋白质结合且能通过毛细管现象展开。
附图说明
图1为本实用新型乙肝疫苗接种效果快速评价试剂盒中的包装盒的爆炸图;
图2为本实用新型中的检测试纸的结构示意图;
图3为本实用新型中的包装盒在揭开第二盖体时的结构示意图;
图4为本实用新型中的活动组件的结构示意图。
具体实施方式
以下结合附图对本实用新型的原理和特征进行描述,所举实例只用于解释本实用新型,并非用于限定本实用新型的范围。
如图1至图4所示,一种乙肝疫苗接种效果快速评价试剂盒包括包装盒1、样品稀释液盛装容器和检测试纸3;所述包装盒1包括盒体12和盖体13,所述盒体12内设有第一隔板11,第一隔板11将所述盒体12分为第一容纳腔111和第二容纳腔112;所述检测试纸3设于所述第一容纳腔111内,所述样品稀释液盛装容器设于所述第二容纳腔112内;所述盖体13包括第一盖体131和第二盖体132,所述第一盖体131设于所述第一容纳腔111的上方,所述第二盖体132设于所述第二容纳腔112的上方;所述第一容纳腔111 内设有若干个第二隔板1115,若干个所述第二隔板1115分别与所述盒体12 的外壁围成第三容纳腔1116,所述第三容纳腔1116内填充有干燥剂;所述第二隔板1115上设有多个直径小于干燥剂粒径的透气孔1117;所述检测试纸3包括包被膜32、标记物结合垫33和抗原垫34;所述抗原垫34上包被有乙肝病毒表面抗原,所述标记物结合垫33上包被有胶体金标记的鼠抗乙肝病毒表面抗原单克隆抗体,所述包被膜32上固定有检测T线321和质控C 线322,所述检测T线321上包被有鼠抗人IgG抗体,所述质控C线322上包被羊抗鼠IgG抗体;所述检测试纸3的最低检测线为10mIU/ml。将样品稀释液盛装容器和检测试纸3均设于包装盒1内,用户在使用时,无需另外准备样品稀释液,使用更加方便,且样品稀释液盛装容器和检测试纸3分别置于试剂盒的两个容纳腔中,且均对应的设置一个盖体13,使试剂盒的尺寸更加紧凑,另用户在使用时只需打开第二盖体132即可取出样品稀释液,不会对检测试纸3造成干扰;另在包装盒1内放有干燥剂,可吸收试剂盒内的湿气、氧气,有效延长试剂瓶储存诊断试剂的保存期限;另将试剂盒的灵敏度设置为10mIU/ml,可实现对乙肝疫苗接种效果的快速评估。
如图1所示,在第二隔板1115上设有多个通气孔1117,可加强干燥剂的吸湿效果。所述第二隔板1115优选为两个,两个所述第二隔板1115分别设于所述第一容纳腔111的前后两端,设于所述第一容纳腔111前方的所述第二隔板1115的两端均向第一容纳腔111的前侧壁延伸形成第三容纳腔1116,设于所述第一容纳腔111后方的所述第二隔板1115的两端均向第一容纳腔111的后侧壁延伸形成另一第三容纳腔1116。
所述第一容纳腔111内还设有用于固定所述检测试纸3的定位装置。通过定位装置可将检测试纸3锁紧在第一容纳腔111中,防止其左右晃动。
如图1所示,所述定位装置包括定位组件1112和活动组件1113,所述定位组件1112和所述活动组件1113分别设于所述第一容纳腔111的左端和右端;所述定位组件1112包括底板11121和U型定位块11122,所述底板 11121固定于所述盒体12上;所述U型定位块11122固定于所述底板11121 的上方,且所述U型定位块11122的开口端朝向所述活动组件1113;所述活动组件1113包括固定板11131、活动板11133和铜片11132,所述固定板 11131固定于所述盒体12上;所述铜片11132的一端嵌设于所述固定板11131 中,所述铜片11132的另一端翘起,翘起的所述铜片11132抵设于所述活动板11133上,所述活动板11133可在所述盒体12内移动。定位组件1112主要用于对检测试纸3的放置位置进行定位,活动组件1113可根据检测试纸3 的具体大小进行调整,使检测试纸3能够卡紧在包装盒1中,避免其左右晃动。
如图1和图4所示,所述活动板11133的底部设有若干个凸起11134,所述盒体12的底部设有若干个与所述凸起11134相匹配的滑槽1118。凸起 11134和滑槽1118的设置可对活动板在盒体12内的移动进行导向,防止活动板11133的偏移。
如图1所示,所述第一容纳腔111内还设有多个交叉型凸筋1114,多个所述交叉型凸筋1114均设于所述定位组件1112与所述活动组件1113之间,所述第一盖体131在与每个所述交叉型凸筋1114相匹配的位置上均设有多个凸条1312。通过设置交叉型凸筋1114和与交叉型凸筋1114相匹配的多个凸条1312,可对检测试纸3起到良好的支撑以及固定的作用。
如图1所示,所述第一盖体131上设有加样口,所述加样口设于所述样品垫35上方的所述第一盖体131上,所述加样口的底部向下延伸形成第三圆筒1313。第三圆筒1313起到导流的作用,可防止添加样品或添加样品稀释液时,液体到处散溅,且能够保证添加的样品稀释液与样品的位置一致,起到良好的稀释作用。
所述第一盖体131上还设有防尘塞,所述防尘塞与所述加样口相匹配。可防止加样口处聚集灰尘、杂质,影响检测试纸3检测结果的准确性。所述第一盖体131上还设有观察窗1314,所述观察窗1314设于所述包被膜32 上方的所述第一盖体131上。便于用户观察检测结果。
如图1和图3所示,所述第一盖体131与所述第二盖体132之间通过铰链133连接,且所述第一盖体131与所述盒体12之间、所述第二盖体132 与所述盒体12之间均通过卡合方式连接。具体的,所述第一容纳腔111内设有多个第一圆筒1111,所述第一盖体131上设有多个与所述第一圆筒1111 相匹配的第一凸起1311。盒体12和盖体13之间可通过所述的第一圆筒1111 和第一凸起1311进行卡合连接,且采用第一圆筒1111和第一凸起1311配合还具有良好的定位效果。所述第二盖体132上设有卡槽1321,所述卡槽 1321设于所述第二盖体132远离所述第一盖体131的一侧的内壁上,所述盒体12上设有与所述卡槽1321相配合的第二凸起121。第二盖体132与盒体 12之间直接采用卡槽1321与第二凸起121进行配合连接,方便开启。
如图1所示,所述第二容纳腔112内设有第二圆筒1121,所述第二圆筒 1121用于放置所述样品稀释液盛装容器。将样品稀释液盛装容器卡设于第二圆筒1121内,使样品稀释液盛装容器的放置更加平稳。所述样品稀释液盛装容器可选为瓶体或包装袋,且瓶体的瓶口或包装袋的开口处设置为锥形,便于样品稀释液的倒出。
本实用新型乙肝疫苗接种效果快速评价试剂盒的组装方法为:首先拨动活动组件1113中的活动板11133,将检测试纸3的底板31放置在交叉型凸筋1114上并使检测试纸3靠近样品垫35的一端卡设于定位组件1112中,松开活动板11133将检测试纸3抵紧;然后将样品稀释液盛装容器卡设于第二圆筒1121中,然后将盒体12和盖体13通过第一圆筒1111和第一凸起1311 进行卡合连接,并将第二凸起121卡合在卡槽1321中。使用时,用户只需揭开第二盖体132,并将样品稀释液取出滴在加样口处即可,操作简单方便。
如图2所示,所述检测试纸3还包括底板31和吸收垫36,所述包被膜32设于所述底板31上;所述标记物结合垫33、所述抗原垫34和所述样品垫35依次搭接在所述包被膜32的一端,所述吸收垫36搭接在所述包被膜 32的另一端。所述抗原垫34为玻璃纤维、无纺布或聚酯膜。所述标记物结合垫33和样品垫35为玻璃纤维,所述吸收垫36为吸水纸。
所述的样品稀释液为:含磷酸氢二钠、磷酸二氢钠、氯化钠的混合水溶液。以下实施例中,样品稀释液的组分为:磷酸氢二钠5.72g,磷酸二氢钠 0.624g,氯化钠8g,超纯水定容至1L。
下面将对乙肝病毒表面IgG抗体检测试纸3的制备、组装、检测原理以及检测效果进行详细的说明:
1、主要材料
抗原:乙肝病毒表面抗原购自厦门波生生物技术有限公司购入,其为粗纯,不具有生物危害,用于制备抗原垫。
鼠抗人IgG单克隆抗体,购自厦门波生生物技术有限公司,用于硝酸纤维素膜T线的包被。
鼠抗乙肝病毒表面抗原单克隆抗体,购自武汉赛欣生物技术有限公司,用于标记胶体金。
羊抗鼠IgG抗体,购自杭州隆基生物技术有限公司,用于硝酸纤维素膜质控C线的包被。
氯金酸:sigma公司产品。
硝酸纤维素膜:millipore公司产品。
牛血清白蛋白(BSA)、酪蛋白:sigma公司产品。
其余化学试剂均为分析纯试剂。
临床实验由公司在武汉市省级以上临床试验机构完成,其中乙肝病毒表面IgG抗体阳性样本217份,阴性样本147份。
乙型肝炎病毒表面抗体检测试剂盒(胶体金法):购自四川迈克生物科技股份有限公司,是有国家局注册证的商用产品。
2、标记物结合垫33的制备
氯金酸-柠檬酸三钠还原法制备直径为40nm的胶体金溶液,制备完成后,取100ml胶体金溶液置于磁力搅拌器上缓慢搅拌,调节pH至8.0,然后按每 100ml胶体金溶液1.0mg抗体加入鼠抗乙肝病毒表面抗原单克隆抗体1.0mg,继续搅拌30min,再加入终浓度为1%的BSA进行封闭,继续搅拌30min。标记结束后,以10000r/min对标记液进行离心,弃上清,然后将沉淀用复溶溶液进行复溶至原体积,所述复溶溶液的配方为:Tris:1.965g,Casein-Na: 2.5g,柠檬酸三钠:2.5g,吐温-20:0.50ml,蔗糖:10.0g,用超纯水定容至1L。将复溶好的金标记溶液按每1ml溶液铺18cm2的比例均匀铺在玻璃纤维上,置于37℃,相对湿度低于20%的环境中,干燥12-18小时,制成标记物结合垫33。
3、抗原垫34的制备
将乙肝病毒表面抗原使用抗原保护液进行稀释到20倍得到抗原液,将稀释好的抗原液按每1ml溶液铺18cm2的比例均匀铺在玻璃纤维、无纺布或聚酯膜上,置于37℃,相对湿度低于40%的环境中,干燥4小时,制成抗原垫34。所述抗原保护液的配方为:Na2HPO4:5.72g,NaH2PO4:0.624g,柠檬酸三钠:8.5g,蔗糖:10g,水定容至1L;所述乙肝病毒表面抗原为粗抗原,其中抗原的含量为45wt%至50wt%。
4、包被膜32的制备
使用0.02M,pH为7.2的磷酸盐缓冲液将鼠抗人IgG单克隆抗体分别稀释成2.0mg/ml(T线溶液),羊抗鼠IgG抗体稀释至110IU/ml(C线溶液)。然后使用划膜仪将检测T线321与质控C线322溶液按1.3ul/cm的出液量均匀地包被于NC膜(硝酸纤维素膜)上,NC膜已事先黏贴于塑料底板上,包被完成后,将NC膜置于37℃,相对湿度低于40%的环境中,干燥3至4 小时,制成包被膜32。
5、乙肝病毒表面IgG抗体检测试纸3的组装
在干燥环境下(温度20至25℃,相对湿度低于30%),将包被膜32置于洁净环境中,在靠近包被膜32的检测T线321的一端紧密压接标记物结合垫33,标记物结合垫33(标记物结合垫33已事先切裁成6mm宽)紧密压接在包被膜32上的长度为2mm左右,抗原垫34(抗原垫已事先切裁成10mm 宽)紧密压接在标记物结合垫33的另一端,抗原垫34(抗原垫34已事先切裁成10mm宽)紧密压接在标记物结合垫33的长度为2mm左右,样品垫35 紧密压接抗原垫34的另一端,样品垫35紧密压接抗原垫34上的长度为4 至5mm,最后用切条机将贴好的底板31切成约4mm宽的检测试纸3。
6、乙肝病毒表面IgG抗体检测试纸3的使用方法
将待检血清或血浆或全血(待检样品)平衡至室温,并将制备好的检测试纸3放入包装盒1中,通过加样口向样品垫35处加入5ul待检样品,再加入2至3滴样品稀释液,若样品中含有乙肝病毒表面IgG抗体,其将和抗原垫34中的乙肝病毒表面抗原形成乙肝病毒表面抗原-乙肝病毒表面IgG抗体复合物,该复合物向前移动,复合物中的乙肝病毒表面抗原再与标记物结合垫33中的胶体金标记的鼠抗乙肝病毒表面抗原单克隆抗体结合,形成乙肝病毒表面IgG抗体-乙肝病毒表面抗原-胶体金标记的鼠抗乙肝病毒表面单克隆抗体免疫复合物,该复合物由于层析作用沿纸条向前移动,至检测T线 321,复合物中的乙肝病毒表面IgG抗体与检测T线321上包被的鼠抗人IgG 单克隆抗体反应形成鼠抗人IgG单克隆抗体-乙肝病毒表面IgG抗体-乙肝病毒表面抗原-胶体金标记的鼠抗乙肝病毒表面抗原单克隆抗体免疫复合物,该复合物可聚集在检测区,当聚集的复合物达到一定的数量时,则形成一条肉眼可见的条带(T线),判断结果为阳性;若样品中不含有或含很少量的乙肝病毒表面IgG抗体,则不能形成免疫复合物,即不能形成肉眼可见的条带,判断结果为阴性;质控C线322作为试剂的质控标准,阳性和阴性检测样品均会产生条带。具体的,在20分钟内可直接用肉眼观察检测T线321 和质控C线322的显色情况:质控C线322不显色,说明本试验失败;质控 C线322显色,检测T线321不显色说明乙肝疫苗接种不成功;质控C线322 和检测T线321均显色说明乙肝疫苗接种成功。
7、根据世界卫生组织规定的乙肝病毒表面IgG抗体的完全保护滴度为 10mIU/ml,当乙肝病毒表面IgG抗体浓度≥10mIU/ml说明人体对乙肝病毒表面具有抵抗性,当乙肝病毒表面IgG抗体浓度<10mIU/ml说明人体对乙肝病毒表面还没有产生抵抗性或者仅有部分保护,因此本检测试纸将检测乙肝病毒表面IgG抗体的检测临界值设置为10mIU/ml,T线显线表明乙肝病毒表面 IgG抗体的浓度≥10mIU/ml,乙肝疫苗接种成功,T线不显线表明乙肝病毒表面IgG抗体的浓度<10mIU/ml,乙肝疫苗接种不成功。因此,本实用新型所述的试剂盒可以实现快速评价乙肝病毒表面的接种效果。
8、临床样品检测结果对照
对公司收集的临床血清样本使用本申请检测试纸及商用胶体金检测试剂盒同时进行检测,再对检测结果进行对照。
四川迈克生物科技股份有限公司的“乙型肝炎病毒表面抗体检测试剂盒 (胶体金法)”是获国家局注册证的产品,使用它作为本公司胶体金试纸条的对照试剂盒。
以胶体金试剂盒为对照,对乙肝病毒表面IgG抗体进行检测,检测出217 份乙肝病毒表面IgG阳性样本,147份乙肝病毒表面IgG阴性样本,而本检测试纸检测出217份乙肝病毒表面IgG阳性样本,147份乙肝病毒表面IgG 阴性样本,总体符合率为99.45%。临床检测结果表明,本试剂盒的性能与已获批的胶体金试剂盒相比无显著差异,说明本实用新型适合用于临床检验,具有实用价值。
以上所述仅为本实用新型的较佳实施例,并不用以限制本实用新型,凡在本实用新型的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本实用新型的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!