可溶性ST2的检测试纸条的制作方法
本实用新型涉及体外诊断
技术领域:
,具体涉及生物检测
技术领域:
,特别涉及一种可溶性ST2的检测试纸条。
背景技术:
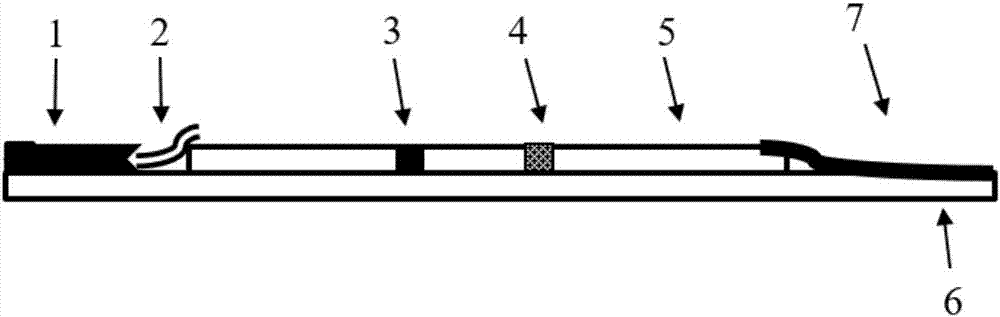
:随着生活方式的改变及人口老龄化程度的增加,我国心脑血管疾病患者的数量日益增加;心力衰竭(简称心衰)是由于心脏结构或功能异常导致心室充盈或射血能力受损的一组复杂临床综合征,其主要临床表现为呼吸困难和乏力,活动耐量受限,以及液体潴留,肺淤血和外周水肿。心衰为各种心脏疾病的严重和终末阶段,发病率和病死率高,其五年存活率与恶性肿瘤相近,是当今最重要的心血管疾病之一。目前临床上对心衰管理存在多种困难,如:早期筛查的检测不普及;病人出院以后难以监控;没有固定的出院指南;无法调整用药的种类以及确定用药的剂量;无法评估再入院的风险;无法鉴别最需要治疗的高风险患者。现代医学研究通过各种生物标志物来实现对心衰的管理;常见的心衰标志物主要包括以下7类:心肌损伤标志物、心肌牵张标志物、心肌纤维化和重构标志物、炎症标志物、氧化应激标志物、神经内分泌激活标志物以及肾功能标志物;其分别反映不同的病理生理过程。作为心肌纤维化和重构标志物,可溶性生长刺激表达因子((GrowthStimμLatingExpressGene2,sST2,或可溶性ST2)在心衰患者管理中的应用越来越受到广泛的关注,《美国心衰指南2013》、《中国心力衰竭诊断和治疗指南2014》中提出可溶性ST2反映心肌纤维化,在急慢性心衰的预测、预后和危险分层中可提供额外信息,是目前临床上最有潜力的、新一代的心衰管理标志物。综上所述,可溶性ST2检测对心衰患者的临床管理具有重要价值。目前对可溶性ST2的检测基本上采用双抗体夹心法的免疫学方法进行检测,包括:酶联免疫吸附法(专利:CN106556705A)、胶体金层析法(专利:CN103487586B)、荧光免疫层析法(专利:CN204287196U)、化学发光法(专利:CN106199002A)、免疫比浊(专利:CN106018789A)等。传统的免疫层析试纸条一般至少由样品垫、结合垫、层析膜、吸水垫组成;由于层析试纸条的结构,导致不同试纸条的差异较大(批内差较大)。而可溶性ST2在临床应用于判断心衰的临界值(>35ng/mL)与正常人群的参考值(8.9~41ng/mL)非常接近,且心衰发病后可溶性ST2浓度升高幅度较小(中位值约45ng/mL);因此,要求可溶性ST2检测试剂盒的准确性较高,尤其是精密性较佳(批内的变异系数小)。造成传统免疫层析试纸条批内变异系数较大的原因较多,如,试纸条使用的环境因素、结合垫上的标记物释放不及时且不充分等原因,其中,尤以结合垫上的标记物释放不及时且不充分为主要原因。究其原因,是因为传统的层析试纸条的结构,是以样品垫压住结合垫、结合垫压住层析膜、吸水纸压住层析膜的结构,而样品垫压住结合垫的部分,由于毛细作用导致被压住的结合垫部分,其上的标记物不会被释放或释放速度较慢;尤其当不同的临床样本,其性质(主要是因血脂等因素导致的样本的粘稠度)差异较大,导致样本滴加到样品垫经毛细作用泳动至结合垫以后,其对结合垫上的标记物的释放程度、速度影响极大;上述原因,是造成可溶性ST2免疫层析检测技术应用与临床诊断受限的主要原因之一。技术实现要素:为了解决上述问题,本实用新型提供一种可溶性ST2的检测试纸条,包括底板,底板上依次分布有加样部、ST2标记抗体结合垫、于捕获的可溶性ST2的抗体的检测部、包被有能够捕获标记可溶性ST2抗体物质的质控部、层析膜和吸水纸,所述的加样部至少由三层样品垫依次叠加而成。较优地,所述的加样部由上层样品垫、中间层样片垫和底层样品垫叠加而成。较优地,所述的中间层样品垫内陷形成“凹”形结构。较优地,所述的结合垫嵌入上层样品垫和底层样品垫之间,并与中间样品垫连接;上下层样品垫和结合垫形成夹心结构。较优地,所述的层析膜由硝酸纤维素、醋酸纤维素膜、尼龙膜、PVDF膜或Fusion5滤纸制成。具体地,以三层的样品垫叠加且中间层的样品内陷形成“凹”状的结构,将结合垫嵌入并与中间层的样品垫连接,形成夹心结构;该试纸条的样品垫、结合垫、层析膜、吸水垫等结构依次连接;其中,将检测用的ST2标记抗体喷点在结合垫上,捕获抗体(检测线)等包被在层析膜上,形成生产工艺较为简单、但检测性能显著改善的可溶性ST2检测试纸条。所述的质控部包被有能够与标记物结合的物质,其中所述的标记物质,包括:胶体金,荧光素(微球)或乳胶微球等。检测时,在样品垫上加入待测的样本,经单层基质泳动至检测线形成夹心结构,对待测样本中的可溶性ST2蛋白进行检测。通过对层析试纸条加样区(样品垫)进行改进,使得试纸条在加样后,其液体(样本或缓冲液)对结合垫上的标记物的释放能力显著提高,速度更快,释放的量更多。该改进的层析试纸条,当待测样本加入后,三层的样品垫从上中下全方位向包裹在内结合垫进行层析泳动,从而加快了结合垫上标记物的释放能力,包括加快了释放的速度,以及提高了释放率。通过结合垫上标记物的充分释放,使得本发明的可溶性ST2检测试纸条的检测性能显著提高,主要表现在精密性(批内变异系数,CV)显著降低,且加快了试纸条的检测速度。本实用新型的有益效果主要有:(1)试纸条的检测性能显著改善,尤其是检测结果的精密性(批内变异系数,CV)显著降低;(2)试纸条的检测速度得以提高。附图说明图1本实用新型的检测试纸条结构的俯视图图2本实用新型的检测试纸条结构的侧视图图3本实用新型的检测试纸条结构中加样部的放大图部分附图标记:1-加样部,11-上层样品垫,12-中间层样品垫,13-底层样品垫,2-结合垫,3-检测部,4-质控部;5-层析膜,6-底板,7-吸水纸具体实施方式为了能够更清楚地理解本实用新型专利的技术内容,特举以下实施例详细说明。本发明专利的可溶性ST2检测方法的试纸条的制备过程简述如下,应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体条件的实验方法,通常按照常规条件,例如Sambrook等人,分子克隆技术实验室操作手册(NewYork:ColdSpringHarborLaboratoryPress,2005)中所述的条件,或按照制造厂商所建议的条件。实施例1可溶性ST2检测试纸条结构一种可溶性ST2的检测试纸条,包括底板6,底板上依次分布有加样部1、ST2标记抗体结合垫2、于捕获的可溶性ST2的抗体的检测部3、包被有能够捕获标记可溶性ST2抗体物质的质控部4、层析膜5和吸水纸7,加样部1至少由三层样品垫依次叠加而成。加样部1由上层样品垫11、中间层样品12和底层样品垫13依次叠加而成;其中,中间层样品垫12内陷形成“凹”形结构,结合垫2嵌入上层样品垫11和底层样品垫13之间,并与中间样品垫12连接;上、下层样品垫和结合垫2形成夹心结构。实施例2荧光标记特异性抗体清洗:取荧光微球(2014年购自BangsLab,货号:11233)至离心管中,加0.1MMES(pH5.0)缓冲液混匀,并以13000rpm,15min,4℃条件离心,弃上清,用0.1MMES(pH5.0)缓冲液重悬待用。活化并清洗:将活化剂EDC、NHS和荧光微球按照质量比比2:1:2的量进行活化,具体操作如下:称取EDC、NHS加入0.1MMES(pH5.0)缓冲液中溶解,迅速取适量至4.3.3.1清洗完毕的荧光微球中,用封口膜封好放置在200rpm摇床上室温摇匀30min,取出后13000rpm,30min,4℃离心除去上清,用等量0.1MMES(pH6.5)缓冲液重悬超声混匀并清洗,重复一次以上操作即清洗两次。离心完成后弃掉上清待用。标记:将活化后的胶乳重悬至0.1MMES(pH6.5)缓冲液中,迅速分别加入特异性结合可溶性ST2的抗体(鼠单抗,2016年购自英国BBISolutions,货号:102321),混匀,放置室温,200rpm摇床上摇匀4小时。封闭:取上述标记好的微球于10000rpm,30min,4℃离心除去上清,立即向微球中加入等量封闭液,超声重悬后再放置室温,200rpm摇床上摇匀1小时。反应完成后10000rpm,20min,4℃离心,取上清待检。检测内容质量标准检测方法包被量包被量≥100μg抗体/mg微球BCA蛋白浓度测定法清洗&重悬:加入重悬液,超声吹打重悬,用高速冷冻离心机10000rpm,20min,4℃离心,弃掉上清;加入重悬液,超声吹打重悬。重悬好的微球溶液做好标记,备用。实施例3结合垫的喷点特异性结合可溶性ST2结合垫滤纸的喷点方法如下:荧光标记溶液稀释:用荧光标记重悬液将上述制备的荧光标记结合物(来自实施例1)稀释2倍;设定点膜仪,开启点膜仪的电源,设定喷点程序,喷点量为8μL/cm;1号管道为喷点通道;点膜仪初始化:将1号管道置于荧光标记重悬溶液中,选择初始化程序,初始化6个循环;喷点:将WhatmanFusion5滤纸按固定位置平放在点膜仪上,按控制面板上“GO”键开始喷点,点完后取下,检查喷点好的结合垫,喷点的荧光标记可溶性ST2特异性抗体带均匀、连续和贯通整个直线为合格喷点品,直线中出现断点为不合格喷点品;每放一片结合垫滤纸,按一次控制面板上的“GO”键为喷点一次(一片);喷点结束,将喷点的结合垫置于室温中自然干燥1小时,膜上应看不到喷点痕迹。实施例4检测线与质控线的制备(特异性抗体)特异性结合可溶性ST2的抗体(鼠单抗,2016年购自英国BBISolutions,货号:102322)从冰箱取出,放置室温,备用。制备方法如下:取鼠抗可溶性ST2的抗体500ug,加到5ml刻度离心管中,抗体稀释液至1ml,容器标记T标志。取羊抗鼠IgG抗体(2016年购自杭州启泰,货号:B103-GMI01)10μL,加到5ml刻度离心管中,抗体稀释液至1ml,容器标记C标志。设定点膜仪,开启点膜仪的电源,设定喷点程序,喷点量为1μL/cm;1号管道为检测线喷点通道,2号管道为质控线喷点通道;点膜仪初始化:将1号管道置于检测线溶液中,将2号管道置于质控线溶液中,选择初始化程序,初始化6个循环;喷点:将硝酸纤维素膜(NC膜)按固定位置平放在点膜仪上,按控制面板上“GO”键开始喷点,点完后取下,检查喷点好的检测线,检测线和质控线为两条均匀、连续和贯通的直线为合格喷点品,两条直线中出现断点为不合格喷点品;每放一片,按一次控制面板上的“GO”键为喷点一次(一片);喷点结束,将喷点的NC膜置于室温中自然干燥1小时,膜上应看不到喷点痕迹。实施例5组装将底板上较宽部分的保护纸除去,沿上面保护纸的下边缘,将喷点好的NC膜(来自实施例3),以质控线在上方的方式贴到底板上,在NC膜的上方贴上吸水滤纸;在底板的最下方贴上样品垫,而后将结合垫贴在样品垫与NC膜之间,且结合垫两端分别压在NC膜与样品垫上(连接部分一般为1~3mm左右);在底层样品垫上涂上亲水的压敏胶水(3M,货号:CA-40H),然后贴上中间层的样品垫,中间层样品垫与结合垫对齐并尽量连接;最后在中间层样品垫上涂上亲水的压敏胶水,再贴上上层样品垫;上层样品垫盖住结合垫约1~3mm。按照上述程序组装成大卡。实施例6切条接通切割机电源,设定切膜程序,设定切割宽度为4mm;将大卡(来自实施例4)平放入切割机平台轨道中,正面朝上,按操作面板上“GO”键,开始切割;每放一片大卡合格品,按操作面板上“GO”键一次,直至切割完所有大卡合格品;切割完成后,将试纸条并列黏贴于底板上,组成检测试纸条。实施例7试纸条组装将上述的试纸条(来自实施例5)装入卡盒中,形成检测卡。取铝箔袋和干燥剂;打开热封机,预热;将待装袋的检测卡、1袋干燥剂装入铝箔袋中;按照规定的长度切断装有检测卡和干燥剂的铝箔袋;用热封机封好铝箔袋;贴上标签。实施例8试纸条检测临床样本中的可溶性ST2将上述的检测卡(来自实施例6),用临床样本进行验证。将待测样本滴加到检测卡的样本孔中,然后置于荧光检测仪中进行读数。检测结果与可溶性ST2检测的金标准(双抗体夹心ELISA法,美国CriticalDiagnostics公司)如下:双抗体夹心法阳性双抗体夹心法阴性合计检测卡检测阳性72173检测卡检测阴性02424合计722597根据上表可得:该试纸条的检测灵敏度为:72/(72+0)×100%=100%;该试纸条的检测特异性为:24/(24+1)=96%。以上检测结果表明,本检测试纸条检测可溶性ST2的准确率较高,能够满足临床应用的要求。实施例9试纸条检测可溶性ST2的精密性将上述的检测卡(来自实施例7),以及加样区未做改进的可溶性ST2检测卡(组件来自实施例1~3,仅组装大卡过程按照传统的方法,以样品垫、结合垫、层析膜和吸水滤纸依次连接的方式),用质控品进行验证。采用可溶性ST2浓度为35ng/mL的质控品,实施例6的检测卡与未做改进的检测卡各检测10次;将待测样本滴加到检测卡的样本孔中,然后置于荧光检测仪中进行读数;检测结果用于计算批内变异系数(CV),结果如下:以上检测结果表明,本发明改进加样区的检测试纸条检测可溶性ST2的精密性显著提高,能够更好地满足临床应用的要求。实施例10试纸条检测可溶性ST2的时间将上述的检测卡(来自实施例6),以及加样区未做改进的可溶性ST2检测卡(组件来自实施例1~3,仅组装大卡过程按照传统的方法,以样品垫、结合垫、层析膜和吸水滤纸依次连接的方式),用质控品进行验证。采用可溶性ST2浓度为35ng/mL的质控品,实施例6的检测卡与未做改进的检测卡各检测10次;将待测样本滴加到检测卡的样本孔中,然后置于荧光检测仪中进行观察计时,以加样开始至检测卡的质控线荧光值不发生变化为止,记为检测卡的检测时间(秒,s);并计算两种卡的平均检测时间,结果如下:以上的检测结果表明,本检测试纸条检测可溶性ST2的速度显著提高(检测时间降低了50%以上),能够更好地满足临床应用的要求。应当说明的是,以上所述仅为本实用新型的较佳实施例而已,并不用于限制本实用新型的范围,凡在本实用新型的精神和原则之内所作出的任何修改、等同的替换和改进等,均应包含在本实用新型的保护范围之内。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1